文档内容
专题63 溶液中粒子浓度大小比较
1.【2022年重庆卷】某小组模拟成垢-除垢过程如图。
100mL0.1mol•L-1CaCl 水溶液 ……
2
忽略体积变化,且步骤②中反应完全。下列说法正确的是
A.经过步骤①,溶液中c(Ca2+)+c(Na+)=c(Cl-)
B.经过步骤②,溶液中c(Na+)=4c(SO )
C.经过步骤②,溶液中c(Cl-)=c(CO )+c(HCO )+c(H CO)
2 3
D.经过步骤③,溶液中c(CHCOOH)+c(CH COO-)=c(Cl-)
3 3
【答案】D
【解析】A.经过步骤①,100mL0.1mol•L-1CaCl 水溶液和0.01molNa SO 反应方程式为CaCl +
2 2 4 2
NaSO =2NaCl+CaSO ↓,生成0.02mol NaCl和0.01molCaSO,CaSO 微溶,则溶液中含有SO 和
2 4 4 4 4
Ca2+,则c(Ca2+)+c(Na+)>c(Cl-),故A错误;B.步骤②中,CaSO(s)+Na CO(aq)=CaCO ↓+NaSO(aq),
4 2 3 3 4
步骤②中反应完全,则反应后的溶质为0.01mol Na SO 、0.01mol Na CO 和0.02molNaCl,则
2 4 2 3
c(Na+)=6c(SO ),故B错误;C.经过步骤②,反应后的溶质为0.01mol Na SO 、0.01mol Na CO 和
2 4 2 3
0.02molNaCl,存在物料守恒:c(Cl-)=2c(CO )+2c(HCO )+2c(H CO),故C错误;D.步骤③中,
2 3
CaCO +2CH COOH=Ca(CH COO) +H O+CO↑,反应后的溶液中含有0.02molNaCl、0.01mol
3 3 3 2 2 2
Ca(CHCOO) ,则c(CHCOOH)+c(CH COO-)=c(Cl-),故D正确;故选D。
3 2 3 3
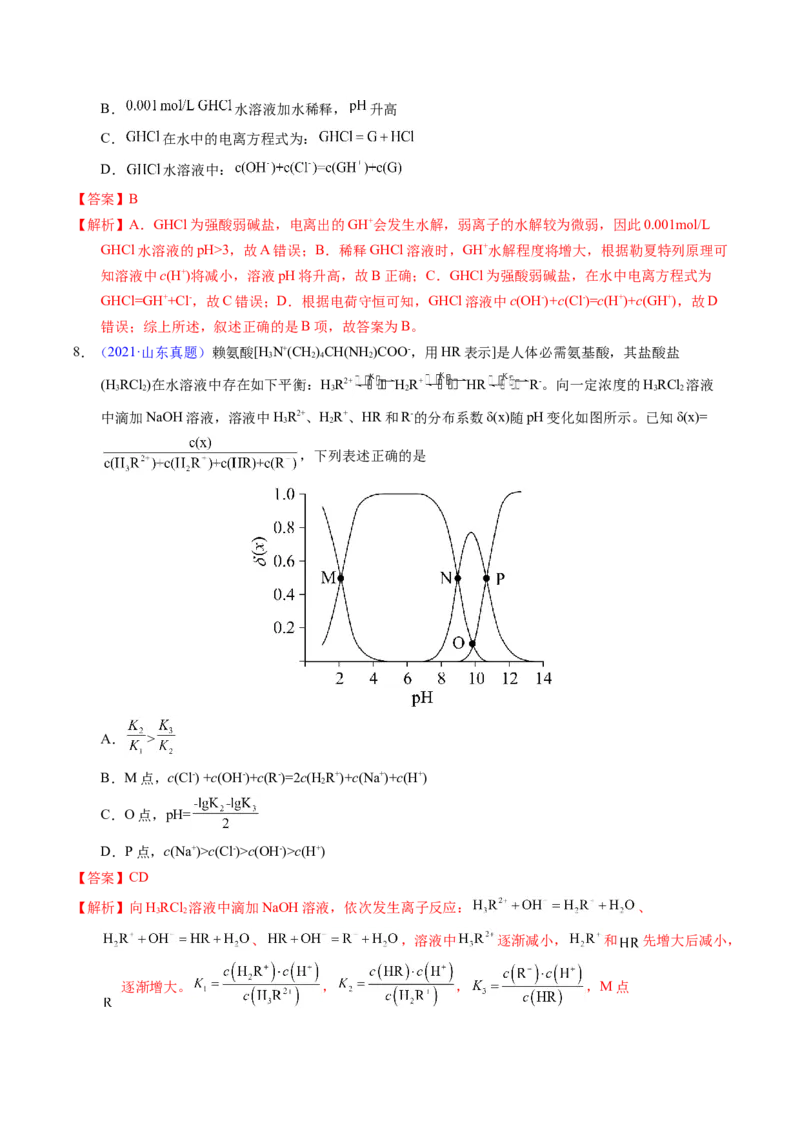
2.(2021·福建真题)如图为某实验测得 溶液在升温过程中(不考虑水挥发)的pH变化曲
线。下列说法正确的是
A.a点溶液的 比c点溶液的小B.a点时,
C.b点溶液中,
D.ab段,pH减小说明升温抑制了 的水解
【答案】A
【解析】A.K =c(H+)c(OH-),随着温度的升高,K 增大;a点、c点的pH相同,即氢离子浓度相同,但
w w
是 不同,c点的K 大,所以a点溶液的 比c点溶液的小,故A正确;B.碳酸氢钠溶
w
液中存在电离平衡和水解平衡,根据图示可知,碳酸氢钠溶液显碱性,水解过程大于电离过程,K=
h
,所以 ,故B错误;C.b点溶液显碱性,溶液中存在电荷守
恒: ,由于c(H+)c(CH COO- )
3
B.向NH Cl溶液中加入少量Al (SO ) 固体、则水的电离程度减小
4 2 4 3
C.向NaCO 溶液中滴加盐酸至c(Na+)=2c(Cl- ),则c(HCO )>c(H CO)
2 3 2 3
D.向0.2 mol·L-1磷酸中加水至原体积的两倍,则c(H+)>0.1 mol·L-1
【答案】C【解析】A.溶液呈酸性则c(H+)>c(OH- ),溶液中存在电荷守恒c(H+)+ c( )=c(CH COO- )+c(OH- ),则
3
c( )c(H CO),C正确;D.磷酸HPO
3 2 3 2 3 3 4
是三元弱酸,部分电离,0.2 mol·L-1磷酸含c(H+)<0.6 mol·L-1,加水至原体积的两倍,越稀弱酸电离程
度越大,则c(H+)>0.3 mol·L-1,D错误;故选:C。
5.【2022年上海卷】向10mL浓度为0.1mol·L 的二元弱酸HA中逐滴加入VmL0.1mol·L 的NaOH溶液。
2
下列离子关系错误的是
A. ,
B. ,
C. ,且测得此时溶液 ,
D.m,
【答案】B
【解析】A.当 时,所得溶液为等物质的量的NaHA和 的混合溶液,存在物料守恒
,A正确;B.当 时,所得溶液为NaHA溶液,存在质子守恒
,B错误;C.当 时,所得溶液为等物质的量的NaHA和 的
混合溶液, ,说明HA-的电离程度大于 的水解程度,则溶液中存在 ,
C正确;D.当 时,所得溶液为 溶液,存在物料守恒 ,
水解生成 , 水解生成 ,且以 的水解为主,所以 ,D
正确;故答案为:B。
6.【2022年辽宁卷】甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液 关系如
图。下列说法错误的是A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
【答案】D
【解析】A. 中存在 和-COOH,所以溶液既有酸性又有碱性,故A正确;B.氨基具
有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离子反应,故曲线a表
示 的分布分数随溶液pH的变化,曲b表示 的分布分数随溶液pH的变
化,曲线c表示 的分布分数随溶液pH的变化,故B正确;C.
的平衡常数 , 时,
根据a,b曲线交点坐标 可知, 时, ,则
,故C正确;D.由C项分析可知, ,根据
b,c曲线交点坐标坐标 分析可得电离平衡 的电离常
数为K= , ,则
1
,即
,故D错误;故答案选D。
7.(2021·广东真题)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
水溶液呈酸性,下列叙述正确的是
A. 水溶液的B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
【答案】B
【解析】A.GHCl为强酸弱碱盐,电离出的GH+会发生水解,弱离子的水解较为微弱,因此0.001mol/L
GHCl水溶液的pH>3,故A错误;B.稀释GHCl溶液时,GH+水解程度将增大,根据勒夏特列原理可
知溶液中c(H+)将减小,溶液pH将升高,故B正确;C.GHCl为强酸弱碱盐,在水中电离方程式为
GHCl=GH++Cl-,故C错误;D.根据电荷守恒可知,GHCl溶液中c(OH-)+c(Cl-)=c(H+)+c(GH+),故D
错误;综上所述,叙述正确的是B项,故答案为B。
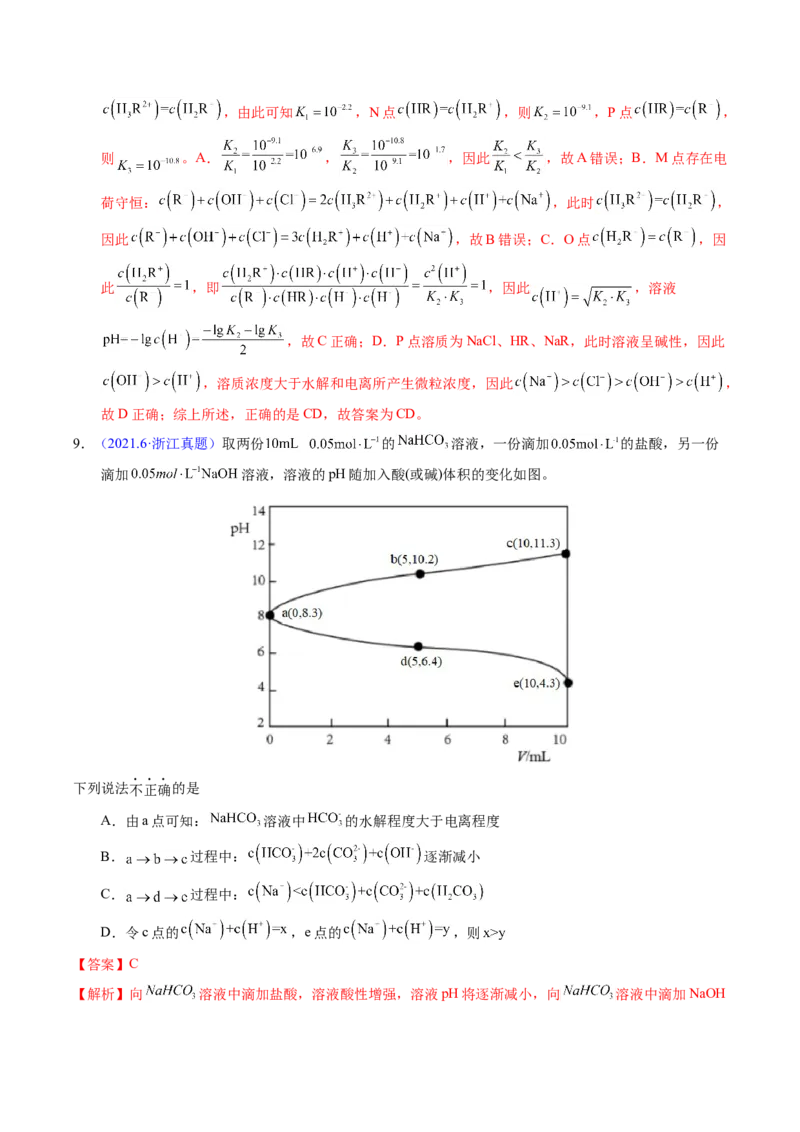
8.(2021·山东真题)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐
3 2 4 2
(H RCl )在水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液
3 2 3 2 3 2
中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
【答案】CD
【解析】向HRCl 溶液中滴加NaOH溶液,依次发生离子反应: 、
3 2
、 ,溶液中 逐渐减小, 和 先增大后减小,
逐渐增大。 , , ,M点,由此可知 ,N点 ,则 ,P点 ,
则 。A. , ,因此 ,故A错误;B.M点存在电
荷守恒: ,此时 ,
因此 ,故B错误;C.O点 ,因
此 ,即 ,因此 ,溶液
,故C正确;D.P点溶质为NaCl、HR、NaR,此时溶液呈碱性,因此
,溶质浓度大于水解和电离所产生微粒浓度,因此 ,
故D正确;综上所述,正确的是CD,故答案为CD。
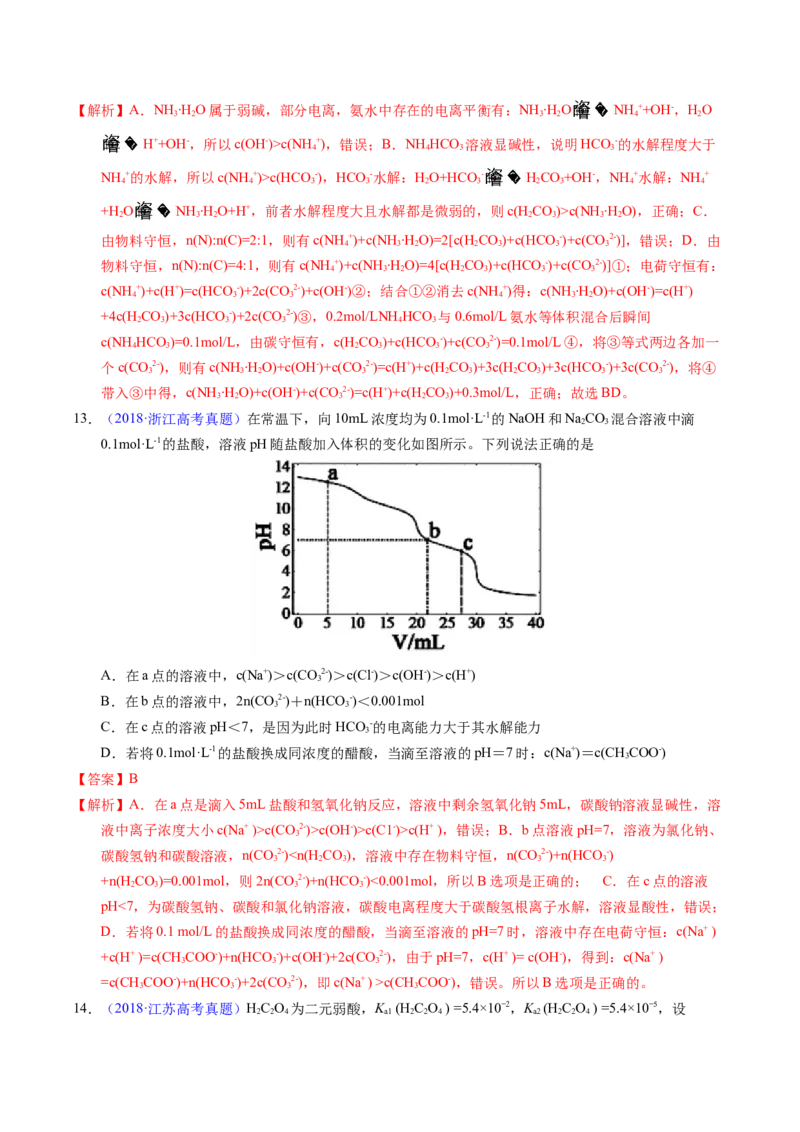
9.(2021.6·浙江真题)取两份 的 溶液,一份滴加 的盐酸,另一份
滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是
A.由a点可知: 溶液中 的水解程度大于电离程度
B. 过程中: 逐渐减小
C. 过程中:
D.令c点的 ,e点的 ,则
【答案】C
【解析】向 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向 溶液中滴加NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向 溶液中滴加NaOH溶液,ade
曲线为向 溶液中滴加盐酸。A.a点溶质为 ,此时溶液呈碱性, 在溶液中电离
使溶液呈酸性, 在溶液中水解使溶液呈碱性,由此可知, 溶液中 的水解程度大
于电离程度,故A正确;B.由电荷守恒可知, 过程溶液中
,滴加NaOH溶液的过程中 保持不变,
逐渐减小,因此 逐渐减小,故B正确;C.由物料守恒可知,a点溶液
中 ,向 溶液中滴加盐酸过程中有CO 逸出,因此
2
过程中 ,故C错误;D.c点溶液中
=(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中 =(0.025+10-
4)mol/L,因此x>y,故D正确;综上所述,说法不正确的是C项,故答案为C。
10.(2020·江苏高考真题)室温下,将两种浓度均为 的溶液等体积混合,若溶液混合引起的
体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
A. 混合溶液(pH=10.30):
B.氨水-NH Cl混合溶液(pH=9.25):
4
C. 混合溶液(pH=4.76):
D. 混合溶液(pH=1.68,HC O 为二元弱酸):
2 2 4
【答案】AD
【解析】A.NaHCO 水溶液呈碱性,说明 的水解程度大于其电离程度,等浓度的NaHCO 和
3 3
NaCO 水解关系为: ,溶液中剩余微粒浓度关系为: ,
2 3
和 水解程度微弱,生成的OH-浓度较低,由NaHCO 和NaCO 化学式可知,该混合溶液中
3 2 3
Na+浓度最大,则混合溶液中微粒浓度大小关系为: ,正确;
B.该混合溶液中电荷守恒为: ,物料守恒为:
,两式联立消去c(Cl-)可得:
,错误;C.若不考虑溶液中相关微粒行为,则c(CHCOOH)=c(CHCOO-)=c(Na+),该溶液呈酸性,说明CHCOOH电离程度大于CHCOONa水解程
3 3 3 3
度,则溶液中微粒浓度关系为:c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+),错误;D.该混合溶液中物
3 3
料守恒为: ,电荷守恒为:
,两式相加可得:
,正确;综上所述,浓度关系正确的是:AD。
11.(2020·浙江高考真题)常温下,用 氨水滴定 浓度均为 的 和
的混合液,下列说法不正确的是( )
A.在氨水滴定前, 和 的混合液中
B.当滴入氨水 时,
C.当滴入氨水 时,
D.当溶液呈中性时,氨水滴入量大于 ,
【答案】C
【解析】A.未滴定时,溶液溶质为HCl和CHCOOH,且浓度均为0.1mol/L,HCl为强电解质,完全电离,
3
CHCOOH为弱电解质,不完全电离,故,c(Cl-)>c(CHCOO-),A正确;B.当滴入氨水10mL时,
3 3
n(NH ·H O)=n(CHCOOH),则在同一溶液中c( )+ c(NH ·H O)=c(CHCOOH)+ c(CH COO-),B正
3 2 3 3 2 3 3
确;C.当滴入氨水20mL时,溶液溶质为NH Cl和CHCOONH,质子守恒为c(CHCOOH)+c(H+)= c(
4 3 4 3
)+c(OH-),C不正确;D.当溶液为中性时,电荷守恒为:c( )+c(H+)= c(CHCOO-)
3
+c(Cl-)+ c(OH-),因为溶液为中性,则c(H+)=c(OH-),( )>c(Cl-),D不正确;故选CD。
12.(2019·江苏高考真题)室温下,反应 +H O HCO+OH−的平衡常数K=2.2×10−8。将
2 2 3
NH HCO 溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,
4 3
室温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.2mol·L−1氨水:c(NH ·H O)>c( )>c(OH−)>c(H+)
3 2
B.0.2mol·L−1NH HCO 溶液(pH>7):c( )>c( )>c(H CO)>c(NH ·H O)
4 3 2 3 3 2
C.0.2mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c( )+c(NH ·H O)=c(H CO)+c( )
4 3 3 2 2 3
+c( )
D.0.6mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c(NH ·H O)+c( )
4 3 3 2
+c(OH−)=0.3mol·L−1+c(H CO)+c(H+)
2 3
【答案】BD【解析】A.NH ∙HO属于弱碱,部分电离,氨水中存在的电离平衡有:NH ∙HO NH ++OH-,HO
3 2 3 2 4 2
H++OH-,所以c(OH-)>c(NH+),错误;B.NH HCO 溶液显碱性,说明HCO -的水解程度大于
4 4 3 3
NH +的水解,所以c(NH +)>c(HCO-),HCO -水解:HO+HCO - HCO+OH-,NH +水解:NH +
4 4 3 3 2 3 2 3 4 4
+H O NH ∙HO+H+,前者水解程度大且水解都是微弱的,则c(HCO)>c(NH∙HO),正确;C.
2 3 2 2 3 3 2
由物料守恒,n(N):n(C)=2:1,则有c(NH +)+c(NH∙HO)=2[c(HCO)+c(HCO-)+c(CO 2-)],错误;D.由
4 3 2 2 3 3 3
物料守恒,n(N):n(C)=4:1,则有c(NH +)+c(NH∙HO)=4[c(HCO)+c(HCO-)+c(CO 2-)]①;电荷守恒有:
4 3 2 2 3 3 3
c(NH +)+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)②;结合①②消去c(NH +)得:c(NH ∙HO)+c(OH-)=c(H+)
4 3 3 4 3 2
+4c(H CO)+3c(HCO-)+2c(CO 2-)③,0.2mol/LNH HCO 与0.6mol/L氨水等体积混合后瞬间
2 3 3 3 4 3
c(NH HCO )=0.1mol/L,由碳守恒有,c(HCO)+c(HCO-)+c(CO 2-)=0.1mol/L④,将③等式两边各加一
4 3 2 3 3 3
个c(CO2-),则有c(NH ∙HO)+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+3c(H CO)+3c(HCO-)+3c(CO 2-),将④
3 3 2 3 2 3 2 3 3 3
带入③中得,c(NH ∙HO)+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+0.3mol/L,正确;故选BD。
3 2 3 2 3
13.(2018·浙江高考真题)在常温下,向10mL浓度均为0.1mol·L-1的NaOH和NaCO 混合溶液中滴
2 3
0.1mol·L-1的盐酸,溶液pH随盐酸加入体积的变化如图所示。下列说法正确的是
A.在a点的溶液中,c(Na+)>c(CO2-)>c(Cl-)>c(OH-)>c(H+)
3
B.在b点的溶液中,2n(CO2-)+n(HCO -)<0.001mol
3 3
C.在c点的溶液pH<7,是因为此时HCO -的电离能力大于其水解能力
3
D.若将0.1mol·L-1的盐酸换成同浓度的醋酸,当滴至溶液的pH=7时:c(Na+)=c(CHCOO-)
3
【答案】B
【解析】A.在a点是滴入5mL盐酸和氢氧化钠反应,溶液中剩余氢氧化钠5mL,碳酸钠溶液显碱性,溶
液中离子浓度大小c(Na+ )>c(CO2-)>c(OH-)>c(C1-)>c(H+ ),错误;B.b点溶液pH=7,溶液为氯化钠、
3
碳酸氢钠和碳酸溶液,n(CO2-)c(CHCOO-),错误。所以B选项是正确的。
3 3 3 3
14.(2018·江苏高考真题)HC O 为二元弱酸,K (H C O ) =5.4×10−2,K (H C O ) =5.4×10−5,设
2 2 4 a1 2 2 4 a2 2 2 4HC O 溶液中c(总)=c(H C O) +c(HC O−) +c(C O2−)。室温下用NaOH溶液滴定25.00 mL 0.1000
2 2 4 2 2 4 2 4 2 4
mol·L−1HC O 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是
2 2 4
A.0.1000 mol·L−1 HC O 溶液:c(H+ ) =0.1000 mol·L−1+c(C O2− )+c(OH−)−c(H C O )
2 2 4 2 4 2 2 4
B.c(Na+ ) =c(总)的溶液:c(Na+ ) >c(H C O ) >c(C O2− ) >c(H+ )
2 2 4 2 4
C.pH = 7的溶液:c(Na+ ) =0.1000 mol·L−1+ c(C O2−) −c(H C O)
2 4 2 2 4
D.c(Na+ ) =2c(总)的溶液:c(OH−) −c(H+) = 2c(H C O) +c(HC O−)
2 2 4 2 4
【答案】AD
【解析】A.HC O 溶液中的电荷守恒为c(H+)=c(HC O-)+2c(C O2-)+c(OH-),0.1000
2 2 4 2 4 2 4
mol·L−1HC O 溶液中0.1000mol/L=c(HC O) + c(HC O-)+ c(C O2-),两式整理得c(H+)
2 2 4 2 2 4 2 4 2 4
=0.1000mol/L-c(HC O)+c(C O2-)+c(OH-),正确;B.c(Na+)=c(总)时溶液中溶质为
2 2 4 2 4
NaHC O,HC O-既存在电离平衡又存在水解平衡,HC O-水解的离子方程式为HC O-+H O
2 4 2 4 2 4 2 4 2
HC O+OH-,HC O-水解常数K= = =
2 2 4 2 4 h
= =1.85 10-13 K (HC O),HC O-的电离程度大于水解程度,则c
a2 2 2 4 2 4
(C O2-) c(HC O),错误;C.滴入NaOH溶液后,溶液中的电荷守恒为c(Na+)+c(H+)=c
2 4 2 2 4
(HC O-)+2c(C O2-)+c(OH-),室温pH=7即c(H+)=c(OH-),则c(Na+)=c(HC O-)+2c
2 4 2 4 2 4
(C O2-)=c(总)+c(C O2-)-c(HC O),由于溶液体积变大,c(总) 0.1000mol/L,c(Na+)
2 4 2 4 2 2 4
0.1000mol/L +c(C O2-)-c(HC O),错误;D.c(Na+)=2c(总)时溶液中溶质为NaC O,溶
2 4 2 2 4 2 2 4
液中的电荷守恒为c(Na+)+c(H+)=c(HC O-)+2c(C O2-)+c(OH-),物料守恒为c(Na+)
2 4 2 4
=2[c(HC O) + c(HC O-)+ c(C O2-)],两式整理得c(OH-)-c(H+)=2c(HC O)+c
2 2 4 2 4 2 4 2 2 4
(HC O-),正确;答案选AD。
2 4
15.(2017·江苏高考真题)常温下,K (HCOOH)=1.77×10-4,K (CH COOH)=1.75×10-5,K (NH·H O)
a a 3 b 3 2
=1.76×10-5,下列说法正确的是
A.浓度均为0.1 mol·L-1的 HCOONa和NH Cl 溶液中阳离子的物质的量浓度之和: 前者大于后者
4
B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CHCOOH溶液至终点,消耗
3
NaOH溶液的体积相等
C.0.2 mol·L-1 HCOOH 与 0.1 mol·L-1 NaOH 等体积混合后的溶液中: c(HCOO-) + c(OH-) =
c(HCOOH) + c(H+)
D.0.2 mol·L-1 CH COONa 与 0.1 mol·L-1盐酸等体积混合后的溶液中(pH<7): c(CHCOO-) > c(Cl- ) >
3 3
c(CHCOOH) > c(H+)
3
【答案】AD
【解析】A.由电荷守恒可知,甲酸钠溶液中存在c(H+)+c(Na+)=c(OH-)+c(HCOO-),氯化铵溶液中存在
c(H+)+c(NH+)=c(OH-)+c(Cl-)。由于在常温下氨水的K 小于甲酸的K、K 不变,铵根的水解程度大于
4 b a W
甲酸根的水解程度,氯化铵溶液中c(OH-)小于甲酸钠溶液中c(H+) ,Cl-和Na+都不水解,
c(Cl-)=c(Na+),所以A正确;由甲酸和乙酸的电离常数可知,甲酸的酸性较强,所以pH为3的两种溶液中,物质的量浓度较大的是乙酸,等体积的两溶液中,乙酸的物质的量较大,用同浓度的氢氧化钠
溶液中和这两种溶液,乙酸消耗的氢氧化钠溶液较多,B错误;C.两溶液等体积混合后得到甲酸和
甲酸钠的混合液,由电荷守恒得c(H+)+c(Na+)=c(OH-)+c(HCOO-),由物料守恒得2c(Na+)=c(HCOOH)
+c(HCOO-),联立两式可得2c(H+)+ c(HCOOH)=2c(OH-)+c(HCOO-),C错误;D.两溶液等体积混合后,
得到物质的量浓度相同的乙酸、乙酸钠和氯化钠的混合液,由于溶液pH<7,所以溶液中乙酸的电离
程度大于乙酸根的水解程度,氯离子不水解,乙酸的电离程度很小,所以
c(CHCOO-)>c(Cl-)>c(CH COOH)>c(H+),D正确。答案选AD。
3 3
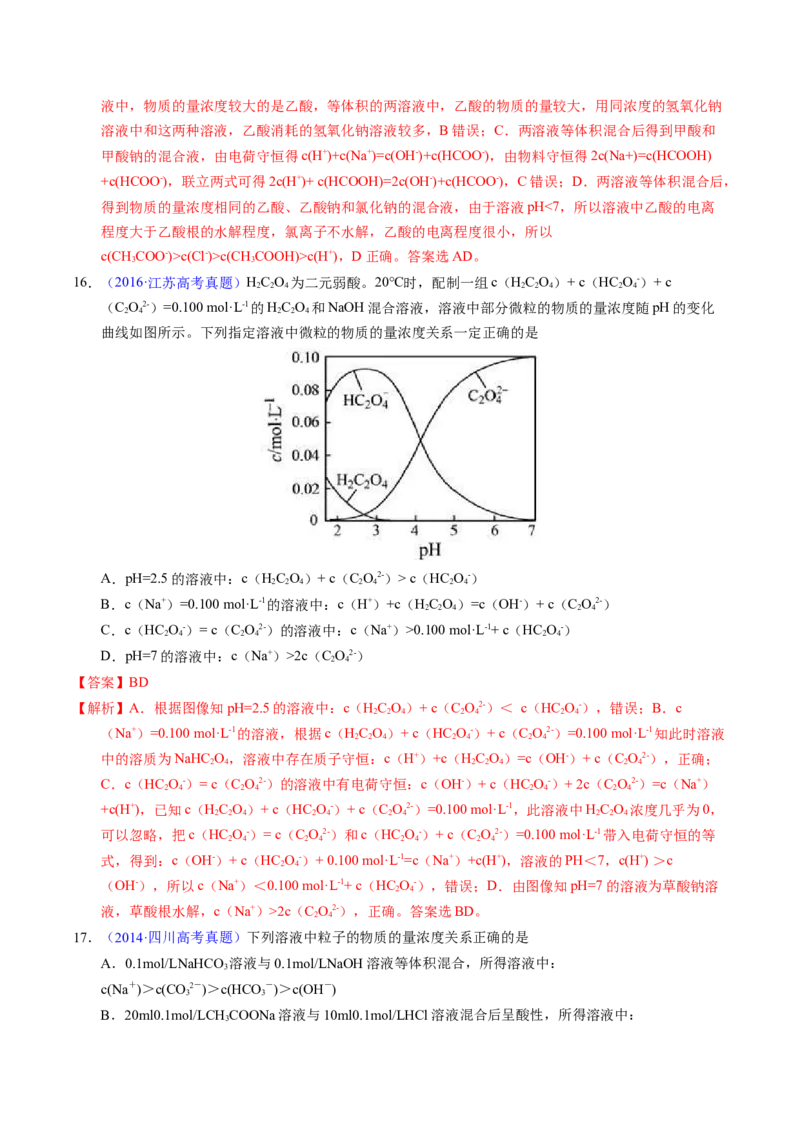
16.(2016·江苏高考真题)HC O 为二元弱酸。20℃时,配制一组c(HC O)+ c(HC O-)+ c
2 2 4 2 2 4 2 4
(C O2-)=0.100 mol·L-1的HC O 和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化
2 4 2 2 4
曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
A.pH=2.5的溶液中:c(HC O)+ c(C O2-)> c(HC O-)
2 2 4 2 4 2 4
B.c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(HC O)=c(OH-)+ c(C O2-)
2 2 4 2 4
C.c(HC O-)= c(C O2-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC O-)
2 4 2 4 2 4
D.pH=7的溶液中:c(Na+)>2c(C O2-)
2 4
【答案】BD
【解析】A.根据图像知pH=2.5的溶液中:c(HC O)+ c(C O2-)< c(HC O-),错误;B.c
2 2 4 2 4 2 4
(Na+)=0.100 mol·L-1的溶液,根据c(HC O)+ c(HC O-)+ c(C O2-)=0.100 mol·L-1知此时溶液
2 2 4 2 4 2 4
中的溶质为NaHC O,溶液中存在质子守恒:c(H+)+c(HC O)=c(OH-)+ c(C O2-),正确;
2 4 2 2 4 2 4
C.c(HC O-)= c(C O2-)的溶液中有电荷守恒:c(OH-)+ c(HC O-)+ 2c(C O2-)=c(Na+)
2 4 2 4 2 4 2 4
+c(H+),已知c(HC O)+ c(HC O-)+ c(C O2-)=0.100 mol·L-1,此溶液中HC O 浓度几乎为0,
2 2 4 2 4 2 4 2 2 4
可以忽略,把c(HC O-)= c(C O2-)和c(HC O-)+ c(C O2-)=0.100 mol·L-1带入电荷守恒的等
2 4 2 4 2 4 2 4
式,得到:c(OH-)+ c(HC O-)+ 0.100 mol·L-1=c(Na+)+c(H+),溶液的PH<7,c(H+) >c
2 4
(OH-),所以c(Na+)<0.100 mol·L-1+ c(HC O-),错误;D.由图像知pH=7的溶液为草酸钠溶
2 4
液,草酸根水解,c(Na+)>2c(C O2-),正确。答案选BD。
2 4
17.(2014·四川高考真题)下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol/LNaHCO 溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
3
c(Na+)>c(CO2-)>c(HCO -)>c(OH-)
3 3
B.20ml0.1mol/LCH COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中:
3c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)>c(H+)>c(NH +)>c(OH-)
4
D.0.1mol/LCH COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
3
c(OH-)>c(H+)+c(CHCOOH)
3
【答案】B
【解析】A、0.1mol/LNaHCO 溶液与0.1mol/LNaOH溶液等体积混合,二者恰好反应生成碳酸钠和水,碳
3
酸根离子水解,溶液显碱性,且碳酸根的水解以第一步水解为主,因此所得溶液中:c(Na+)>c(CO2
3
-)>c(OH-) >c(HCO -),A不正确;B、20ml0.1mol/LCH COONa溶液与10ml0.1mol/LHCl溶液混合
3 3
后反应生成醋酸和氯化钠,反应中醋酸钠过量,所得溶液是醋酸钠、氯化钠和醋酸的混合液,且三种
的浓度相等,呈酸性,说明醋酸的电离程度大于醋酸根的水解程度,因此所得溶液中:c(CHCOO-)
3
>c(Cl-)>c(CHCOOH)>c(H+),B正确;C、氨水是弱碱,盐酸是强碱,因此室温下,pH=2的盐酸
3
与pH=12的氨水等体积混合后生成氯化铵和水,反应中氨水过量,溶液显碱性,因此所得溶液中:
c(NH +)>c(Cl-)>c(OH-) >c(H+),C不正确;D、0.1mol/LCH COOH溶液与0.1mol/LNaOH溶液等体
4 3
积混合,二者恰好反应生成醋酸钠和水,醋酸根水解,溶液显碱性,根据质子守恒可知所得溶液中:
c(OH-)=c(H+)+c(CHCOOH),D不正确,答案选B。
3
18.(2014·江苏高考真题)25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
2c(C O2-)+c(HC O-)+c(OH-)=c(Na+)+c(H+)
2 4 2 4
A.0.1mol/LCH COONa与0.1mol/LHCl溶液等体积混合:c(Na+)>c(Cl-)>cCHCOO-)>c(OH-)
3 3
B.0.1mol/LNH Cl与0.1mol/L氨水等体积混合(pH>7):c(NH ·H O)>c(NH +)>c(Cl-)>c(OH-)
4 3 2 4
C.0.1mol/LNa CO 与0.1mol/L NaHCO 溶液等体积混合: c(Na+)=c(CO2-)+c(HCO -)+c(HCO)
2 3 3 3 3 2 3
D.0.1mol/LNa C O 与0.1mol/LHCl溶液等体积混合(HC O 为二元弱酸):
2 2 4 2 2 4
【答案】C
【解析】A、0.1mol/LCH COONa与0.1mol/LHCl溶液等体积恰好反应混合生成醋酸和氯化钠,醋酸电离溶
3
液显酸性,则c(Na+)=c(Cl-)>cCHCOO-)>c(OH-),A不正确;B、0.1mol/LNH Cl与0.1mol/L氨水
3 4
等体积混合(pH>7),这说明溶液显碱性,因此氨水的电离程度大于铵根的水解程度,则c(NH +)>
4
c(Cl-)>c(NH ·H O)>c(OH-),B不正确;C、0.1mol/LNa CO 与0.1mol/L NaHCO 溶液等体积混合,
3 2 2 3 3
则根据物料守恒可知 c(Na+)=c(CO2-)+c(HCO -)+c(HCO),C正确;D、0.1mol/LNa C O 与
3 3 2 3 2 2 4
0.1mol/LHCl溶液等体积混合(HC O 为二元弱酸),二者恰好反应生成草酸酸氢钠和氯化钠,则根
2 2 4
据电荷守恒可知溶液中2c(C O2-)+c(HC O-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),D不正确,答案选
2 4 2 4
C。
19.(2015·安徽高考真题)25℃时,在10mL浓度均为0.1mol/L NaOH和NH ·H O混合溶液中,滴加
3 2
0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是
A.未加盐酸时:c(OH-)>c(Na+)=c(NH·H O)
3 2B.加入10mL盐酸时:c(NH +)+c(H+)=c(OH-)
4
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20mL盐酸时:c(Cl-)=c(NH+)+c(Na+)
4
【答案】B
【解析】A、混合溶液中,浓度均为0.1mol/L NaOH和NH ·H O,NH ·H O为弱电解质,(Na+)>
3 2 3 2
c(NH ·H O),A错误;B、加入10mL盐酸时,c(Cl-)=c(Na+),又根据电荷守恒得到:c(NH +)+c(H+)
3 2 4
+c(Na+)=c(OH-)+c(Cl-),所以c(NH +)+c(H+)=c(OH-),B正确;C、根据电荷守恒得到:c(NH +)+c(H+)
4 4
+c(Na+)=c(OH-)+c(Cl-),pH=7时,即c(H+)=c(OH-),所以c(NH +)+c(Na+)=c(Cl-),c(Cl-)>c(Na+),C
4
错误;D、加入20mL盐酸时,c(Cl-)=2c(Na+),由于NH +的水解,c(NH +)<c(Na+),所以c(Cl-)>
4 4
c(NH +)+c(Na+),D错误;此题选B。
4
20.(2015·江苏高考真题)室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的
影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
A.向0.10mol·L-1NH HCO 溶液中通入CO:c(NH +)=c(HCO-)+c(CO2-)
4 3 2 4 3 3
B.向0.10mol·L-1NaHSO 溶液中通入NH :c(Na+)>c(NH +)>c(SO 2-)
3 3 4 3
C.0.10mol·L-1NaSO 溶液通入SO :c(Na+)=2[c(SO2-)+c(HSO -)+c(HSO )]
2 3 2 3 3 2 3
D.0.10mol·L-1CHCOONa溶液中通入HCl:c(Na+)>c(CHCOOH)=c(Cl-)
3 3
【答案】D
【解析】A、两者不反应,根据溶液呈现电中性,c(NH +)+c(H+)=c(OH-)+c(HCO -)+2c(CO2-),因为
4 3 3
pH=7,c(H+)=c(OH-),即c(NH +)=c(HCO -)+2c(CO2-),A错误;B、HSO - H++SO 2-,
4 3 3 3 3
NH 和H+反应,生成亚硫酸钠和亚硫酸铵,根据溶液呈现电中性,c(Na+)+c(NH+)+c(H+)=c(OH-)
3 4
+c(HSO -)+2c(SO 2-),pH=7,c(H+)=c(OH-),则c(Na+)+c(NH+)=c(HSO -)+2c(SO 2-);根据物
3 3 4 3 3
料守恒可知,c(Na+)=c(HSO )+c(HSO -)+c(SO 2-),将此式代入上式可得c(NH +)+ c(HSO )=
2 3 3 3 4 2 3
c(SO 2-),则c(SO 2-) >c(NH +),因此,c(Na+) >c(SO 2-) >c(NH +),B错误;C、根据物料守恒可
3 3 4 3 4
知,NaSO 溶液中存在c(Na+)=2[c(SO2-)+c(HSO -)+c(HSO )]。向NaSO 溶液通入SO 后发生
2 3 3 3 2 3 2 3 2
NaSO +SO +HO=2NaHSO,pH=7,反应后溶液的溶质NaSO 、NaHSO,溶液中的硫元素增多
2 3 2 2 3 2 3 3
了,原有的物料守恒被破坏了,(Na+)<2[c(SO 2-)+c(HSO -)+c(HSO )],C错误;D、CHCOONa+
3 3 2 3 3
HCl=CHCOOH+NaCl,溶液pH=7,反应后的溶质:NaCl、CHCOOH、CHCOONa,电离和水解
3 3 3
的程度相同,因此有c(Na+) >c(CHCOOH)=c(Cl-),D正确。答案选D。
3
21.(2014·全国高考真题)一定温度下,下列溶液的离子浓度关系式正确的是
A.pH=5的HS溶液中,c(H+)= c(HS-)=1×10-5mol·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC O-)
2 2 4 2 4
D.pH相同的①CHCOO Na②NaHCO ③NaClO三种溶液的c(Na+):①>②>③
3 3
【答案】D
【解析】A.HS溶液中分步电离,HS H++HS-,HS- H++S2-,根据电荷守恒知c(H+)=c(HS-)
2 2
+2c(S2-)+ c(OH-)=1×10-5mol·L-1,错误;B.加水稀释促进一水合氨的电离,pH=a的氨水,稀释10倍后,其pH=b,则a<b+1,错误;C.pH=2的HC O 溶液与pH=12的NaOH溶液任意比例混合,溶液
2 2 4
中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC O-)+2c(C O2-),错误;D.酸性大小为
2 4 2 4
CHCOOH>HCO>HClO,组成盐的酸根对应的酸越弱,该盐的水解程度越大,相同浓度时溶液的
3 2 3
碱性越强。pH相同的①CHCOONa②NaHCO ③NaClO三种溶液,盐的浓度:①>②>③,c
3 3
(Na+):①>②>③,正确;答案选D。
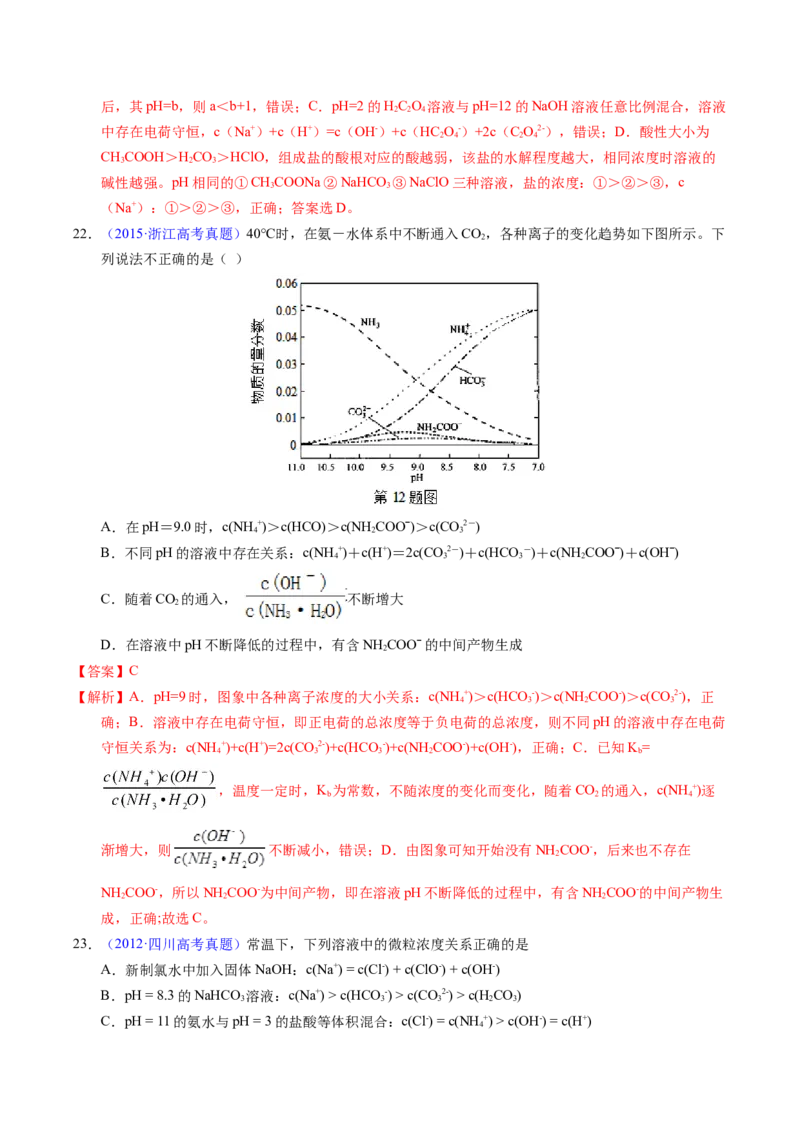
22.(2015·浙江高考真题)40℃时,在氨-水体系中不断通入CO,各种离子的变化趋势如下图所示。下
2
列说法不正确的是( )
A.在pH=9.0时,c(NH +)>c(HCO)>c(NH COOˉ)>c(CO2-)
4 2 3
B.不同pH的溶液中存在关系:c(NH +)+c(H+)=2c(CO2-)+c(HCO -)+c(NH COOˉ)+c(OHˉ)
4 3 3 2
C.随着CO 的通入, 不断增大
2
D.在溶液中pH不断降低的过程中,有含NH COOˉ的中间产物生成
2
【答案】C
【解析】A.pH=9时,图象中各种离子浓度的大小关系:c(NH +)>c(HCO -)>c(NH COO-)>c(CO2-),正
4 3 2 3
确;B.溶液中存在电荷守恒,即正电荷的总浓度等于负电荷的总浓度,则不同pH的溶液中存在电荷
守恒关系为:c(NH +)+c(H+)=2c(CO 2-)+c(HCO-)+c(NHCOO-)+c(OH-),正确;C.已知K=
4 3 3 2 b
,温度一定时,K 为常数,不随浓度的变化而变化,随着CO 的通入,c(NH +)逐
b 2 4
渐增大,则 不断减小,错误;D.由图象可知开始没有NH COO-,后来也不存在
2
NH COO-,所以NH COO-为中间产物,即在溶液pH不断降低的过程中,有含NH COO-的中间产物生
2 2 2
成,正确;故选C。
23.(2012·四川高考真题)常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH:c(Na+) = c(Cl-) + c(ClO-) + c(OH-)
B.pH = 8.3的NaHCO 溶液:c(Na+) > c(HCO -) > c(CO 2-) > c(H CO)
3 3 3 2 3
C.pH = 11的氨水与pH = 3的盐酸等体积混合:c(Cl-) = c(NH +) > c(OH-) = c(H+)
4D.0.2mol/LCH COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+) – 2c(OH-) = c(CH COO-) –
3 3
c(CHCOOH)
3
【答案】D
【解析】A.新制氯水中加入足量固体NaOH存在电荷c(Na+)+c(H+)=c(Cl-)+c(ClO-)+c(OH-),错误;B.pH
= 8.3 的 NaHCO 溶液中HCO -的水解大于其电离,则c(Na+)> c(HCO -) > c(H CO) > c(CO 2-) ,错误;
3 3 3 2 3 3
C.pH=11的氨水与pH=3的盐酸等体积混合后溶液显碱性,错误;D.溶液中存在电荷守恒:
c(CHCOO-)+c(OH-)=c(Na+)+c(H+),物料守恒c(CHCOO-)+c(CH COOH)=2c(Na+),代入计算得到:
3 3 3
2c(OH-)+c(CH COO-)=c(CH COOH)+2c(H+),所以得到:c(H+)-2c(OH-)=c(CH COO-)-c(CHCOOH),正
3 3 3 3
确;答案为D。
24.(2008·上海高考真题)某酸性溶液中只有Na+、CHCOO-、H+、OH-四种离子。则下列描述正确的
3
是( )
A.该溶液由pH=3的CHCOOH与pH=11的NaOH溶液等体积混合而成
3
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CHCOOH溶液混合而成
3
C.加入适量的NaOH,溶液中离子浓度为c(CHCOO-)>c(Na+)>c(OH-)>c(H+)
3
D.加入适量氨水,c(CHCOO-)一定大于c(Na+)、c(NH +)之和
3 4
【答案】A
【解析】A.pH=3的CHCOOH与pH=11的NaOH溶液等体积混合,醋酸过量,溶液呈酸性, 且溶液
3
中存在Na+、CHCOO-、H+、OH-四种离子,正确;B.由等物质的量浓度、等体积的NaOH溶液和
3
CHCOOH溶液混合生成强碱弱酸盐,溶液呈碱性,与溶液的酸性不符,错误; C.根据电荷守恒有
3
c(CHCOO-)+c(OH-)=c(H+)+c(Na+),如果溶液中存在c(CHCOO-)>c(Na+),则c(OH-) c(NH +)> c(HCO -)> c(CO2-)
4 3 3
【答案】C
【解析】A.因为所得滤液pH<7,溶液显酸性,因此有 =c(OH-) <10-7 mol/L,正确;B.因为两者
是等体积等浓度混合,因此NH HCO 和NaCl物质的量相等,即n(Na+)=n(HCO-),根据物料守恒有
4 3 3
c(Na+)= c(HCO -)+ c(CO2-)+ c(HCO),正确;C.发生的反应是NH HCO +NaCl=NaHCO ↓+
3 3 2 3 4 3 3
NH Cl,溶液有NH Cl和一部分NaHCO ,因此依据电荷守恒,有c(H+)+c(Na+)+c(NH +)=c(OH-)+
4 4 3 4
c(HCO -)+c(Cl-)+2c(HCO -),错误;D.根据选项C的分析,离子浓度大小顺序是 c(Cl-)> c(NH
3 3 4
+)> c(HCO -)> c(CO2-),正确;答案选C。
3 3
27.(2013·四川高考真题)室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实
验数据如下表:
起始浓度/(mol·L-1)
实验编号 反应后溶液的pH
c(HA) c(KOH)
① 0.1 0.1 9
② x 0.2 7
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
【答案】B
【解析】A、两者是等体积等浓度混合,应是恰好完全反应,溶质是KA,反应后溶液显碱性,说明HA是
弱酸,A-发生水解,A-+HO HA+OH-,离子浓度大小顺序是c(K+)>c(A-)>c(OH-)>c(H+),
2
正确;B、根据电荷守恒,有c(K+)+c(H+)=c(OH-)+c(A-),则有c(OH-)=c(K+)+c(H+)-c(A-)=Kw/10-9mol·L-1,错误;C、因为HA是弱酸,反应后溶液显中性,溶质为HA和KA,因此HA的
浓度应大于0.2mol,根据物料守恒,c(A-)+c(HA)>0.2/2mol·L-1=0.1mol·L-1,正确;D、根据电中性,
c(K+)+c(H+)=c(OH-)+c(A-),溶液显中性,即c(H+)=c(OH-),c(K+)=c(A-),离子浓度大小顺序是
c(K+)=c(A-)> c(H+)=c(OH-),正确;答案选B。
28.(2016·上海高考真题)随着科学技术的发展和环保要求的不断提高,CO 的捕集利用技术成为研究的
2
重点。
完成下列填空:
(3)碳酸:HCO,K =4.3×10-7,K =5.6×10-11
2 3 i1 i2
草酸:HC O,K =5.9×10-2,K =6.4×10-5
2 2 4 i1 i2
0.1 mol/L Na CO 溶液的pH____________0.1 mol/L Na C O 溶液的pH。(选填“大于”、“小于”或
2 3 2 2 4
“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。
(选填编号)
a.[H+]>[HC O-]>[HCO -]>[CO2-]
2 4 3 3
B.[HCO -]>[HC O-]>[C O2-]>[CO2-]
3 2 4 2 4 3
c.[H+]>[HC O-]>[C O2-]>[CO2-]
2 4 2 4 3
D.[H CO] >[HCO -]>[HC O-]>[CO2-]
2 3 3 2 4 3
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO - H CO,当有少量酸性或碱性物质进入血
3 2 3
液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
____________________________________________________________________________________
【答案】
(3)大于;草酸;ac
(4)当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液的pH基本不变;当少量碱性
物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变。(合理即给分)
【解析】
(3)根据电离常数可知草酸的酸性强于碳酸,则碳酸钠的水解程度大于草酸钠,所以0.1 mol/L Na CO 溶
2 3
液的pH大于0.1 mol/L Na C O 溶液的pH。草酸的酸性强于碳酸,则等浓度草酸溶液和碳酸溶液中,
2 2 4
氢离子浓度较大的是草酸。A.草酸的二级电离常数均大于碳酸的,所以草酸的电离程度大于,因此
溶液中[H+]>[HC O-]>[C O2-]>[HCO -]>[CO2-],a正确;B.根据a中分析可知b错误;c.根据a
2 4 2 4 3 3
中分析可知c正确;d.根据a中分析可知d错误,答案选ac。
(4)根据平衡可知当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不
变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变。
29.(2012·北京高考真题)直接排放含SO 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中
2
的SO 。
2
(1)用化学方程式表示SO 形成硫酸型酸雨的反应:______________。
2
(2)在钠碱循环法中,NaSO 溶液作为吸收液,可由NaOH溶液吸收SO 制得,该反应的离子方程式是
2 3 2________________________
(3)吸收液吸收SO 的过程中,pH随n(SO ²﹣):n(HSO ﹣)变化关系如下表:
2 3 3
n(SO₃²﹣):n(HSO₃﹣) 91:9 1:1 1:91
pH 8.2 7.2 6.2
①上表判断NaHSO 溶液显______性,用化学平衡原理解释:____________
3
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________
a.c(Na+)=2c(SO 2-)+c(HSO -),
3 3
b.c(Na+)> c(HSO -)> c(SO 2-)>c(H+)=c(OH-)
3 3
c.c(Na+)+c(H+)= c(SO 2-)+ c(HSO -)+c(OH-)
3 3
【答案】(1)SO +H O HSO ,2 H SO +O 2HSO (2)SO +2OH- =SO2-+H O (3)①酸
2 2 2 3 2 3 2 2 4 2 3 2
HSO -存在:HSO - SO 2-+H+和HSO -+H O=HSO +OH-,HSO -的电离程度强于水解程度
3 3 3 3 2 2 3 3
②ab
【解析】
(1)SO 形成硫酸型酸雨时,二氧化硫和空气中的水、氧气反应得到硫酸:SO +H O HSO ,2
2 2 2 2 3
HSO +O 2HSO ;
2 3 2 2 4
(2)二氧化硫被氢氧化钠溶液吸收制备亚硫酸钠溶液时:SO +2OH- =SO2-+H O;
2 3 2
(3)根据表中数据,可知,n(SO ²﹣):n(HSO ﹣)=1:91时,溶液的pH值为酸性,故NaHSO 溶液显酸性,
3 3 3
在亚硫酸氢钠溶液中HSO -存在:HSO - SO 2-+H+和HSO -+H O=HSO +OH-,HSO -的电离程
3 3 3 3 2 2 3 3
度强于水解程度,故溶液呈酸性。当吸收液呈中性时,溶液中的c(H+)=c(OH-),由于溶液中存
在着电荷守恒,(Na+)+c(H+)=2c(SO 2-)+ c(HSO -)+c(OH-),可推出:c(Na+)=2c
3 3
(SO 2-)+c(HSO -),a正确;由于n(SO₃²﹣):n(HSO₃﹣)=1:1时,溶液的pH值为7.2,故中性时
3 3
一定有c(HSO -)> c(SO 2-),可推出:c(Na+)> c(HSO -)> c(SO 2-)>c(H+)=c(OH
3 3 3 3
-),b正确;c不符合电荷守恒。故选ab。