文档内容
大庆中学 2024----2025 学年度二模模拟考试 4.在给定条件下,下列选项所示的物质间的转化均能实现的是( )
高三年级化学试题 A.
高 (温 ) ( )
( ) → ( ) →△ ( )
考试时间:75分钟;试卷总分:100分
B.
可能用到的相对原子量 O-16 S-32 Cu-64 Fe-56 ( ) ( )
( ) → ( )葡萄糖→ ( )
C.
第Ⅰ卷(选择题 共45分) ( ) ( )
( ) → ( ) →△ ( )
一、单选题(本题共15个小题,每题3分,共45分) D.
( ) ( )
1. 化学方向的许多新技术、新材料在诸多领域都有巨大的发展前景,下列说法错误的是( ) 5. 代 表( 阿) 伏 → (加 ) 德 罗 ( 常 数) 的→△值。 下 列 说( 法)正确的是( )
A. 环保型量子点InP-HF在X射线衍射仪测试时呈现明锐的衍射峰,说明其具有晶体结构 A. 和 的混合物中含有的铜原子数为
B . 某新型超分子粘合剂,其原料纤维素结构稳定、不能水解 B. 标 .准 状 况 下 溶于足量水,所得溶液中 . 、 、 和 微粒总数为
− −
C. 太阳能电池封装时需要使用PVB树脂,该材料属于有机高分子化合物 C. 常温常压下 . 与 充分反应 后 所得 到产 物 中 含 有 分子数仍为 .
D. 氢能是一种来源广泛、绿色低碳的二次能源,对实现碳达峰的目标具有重要意义 D. 室温下向 . 的 醋 酸 溶. 液 中 加 水 ,所得溶液中 数目小于 .
+
2.下列化学用语或表述正确的是( ) 6.如图实验中 的 仪 器=、 药品的选择或操作均正确且能达 到实验目的的 .是 ( )
A. 基态氧原子的价层轨道表示式:
A. 吸收少量氨气 B. 用 标准溶液滴定锥形瓶中的盐酸
B. 四氯乙烯的空间填充模型: C. 的 模型:
D. 系统命名法名称为: 甲 基 丁 酸
3.下 列 化 学( 用 语 )或 图 示 表 述正确的是( ) −
A. 聚乙炔的链节是: B. 铜氨配离子的结构简式:
— — —
C. 的电子云图为: ,其中的黑点代表核外电子的运动轨迹 C. 探究浓度对反应速率的影响 D. 配制银氨溶液
D. 分子的空间结构为: ,可推测出 为非极性分子
第 1 页 共 6 页
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}7.根据实验操作和现象所得到的结论正确的是( ) 9. 苯环喹溴铵鼻喷雾剂是我国自主研发上市的首个鼻用抗胆碱药物,可有效改善鼻塞、打喷嚏等
选 症状。其结构如图,有关该物质说法正确的是( )
实验操作及现象 对应结论
项 A. 含有4个手性碳
向饱和 溶液中滴加碳酸钠溶液无明显现象 与碳酸钠不反应 B. 原子所有原子均满足8电子结构
C. 可溶于水
将少量 通入 溶液,将所得溶液分两份,一份滴
D. 不能发生消去反应,可在铜催化下和氧气发生氧化反应
加 溶 液变 红 , 另一份加入溶有 的 溶液出 氧化性:
+ −
现白 色 沉淀 > >
10.在 催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列叙述错误的是( )
说明在 溶液中,存在平衡:
取两支试管分别加入 溶液,将其中
一支试管加热,溶液颜 色 呈 .黄 绿 色 / ; 另 一 支试管置于冷
+ −
[ ( ) ] + , 且该⇌反应为放
水中,溶液颜色呈蓝绿色
−
[热 反 应 ] +
在淀粉和 的混合溶液中滴加过量氯水,溶液蓝色褪去 氯水具有漂白性 A. 催化剂可以同时产生多种反应历程 B. 含 微粒参与的反应均有元素化合价变化
C. 增大 量,反应热和平衡产率不变 D. 当主 要发生包含 的历程时,最终生成的水量改变
11.实验 室 将 溶入 冠 结构如图 的乙腈 溶液②中可轻松实现氯的取代,反应过程
8.某化合物结构如图所示,其中 、 、 、 为原子序数依次增大的短周期非金属元素, 是有机
如图 所示, 下 列说法 不−正确−的 (是( ) ) ( )
分子的骨架元素, 位于元素周期 表 区 , 下列说法不正确的是 ( )
第一电离能:
①氢化物沸点: < <
②最高价氧化物对 <应 水<化 酸性:
③该化合物中 均为 杂化 <
④该化合物中, 的化合 价为 价 A. 冠 可循环使用 B. 与 冠 形成的化合物熔点比 低
⑤ 该化合物 中含有的配位+键 数为 C. 与− − 冠 形成化合物的过程体现超分子 自 组 装 的−特征−
⑥A. B. C. D. − −
D. 相同条件下, 比 更易被取代生成相应的氟化物
①②③④ ②③④⑥ ③④⑤⑥ ①③④⑤
第 2 页 共 6 页
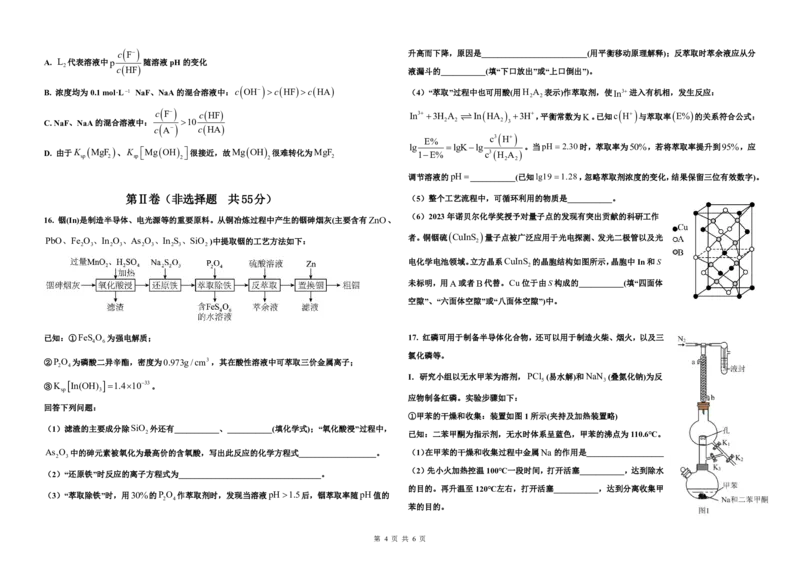
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}12.利用CO 合成甲醇也是有效利用CO 资源的重要途径。将原料气n(CO):n(H )=1:3充入某 14. 某种由Cu、Fe、S三种元素组成的物质具有如图中图1所示的晶胞结构,其中铁原子的投影
2 2 2
一恒容密闭容器中,只发生CO (g)+3H (g) CH OH(g)+H O(g) ΔH,在不同催化剂作用下, 位置如图2,铜原子全部位于楞和面上,设NA为阿伏加德罗常数的值,下列说法正确的是( )
2 2 3 2
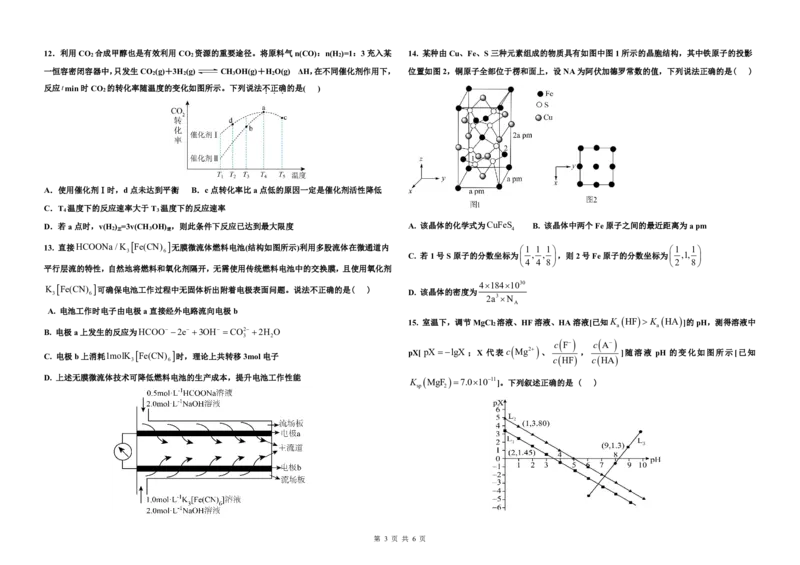
反应tmin时CO 2 的转化率随温度的变化如图所示。下列说法不 . 正 . 确 . 的是( )
A.使用催化剂Ⅰ时,d点未达到平衡 B.c点转化率比a点低的原因一定是催化剂活性降低
C.T 温度下的反应速率大于T 温度下的反应速率
4 3
D.若a点时,v(H ) =3v(CH OH) ,则此条件下反应已达到最大限度 A. 该晶体的化学式为CuFeS B. 该晶体中两个Fe原子之间的最近距离为apm
2 正 3 逆 4
13. 直接HCOONa/K Fe(CN) 无膜微流体燃料电池(结构如图所示)利用多股流体在微通道内 1 1 1 1 1
3 6
C. 若1号S原子的分数坐标为 , , ,则2号Fe原子的分数坐标为 ,1,
4 4 8 2 8
平行层流的特性,自然地将燃料和氧化剂隔开,无需使用传统燃料电池中的交换膜,且使用氧化剂
41841030
K 3 Fe(CN) 6 可确保电池工作过程中无固体析出附着电极表面问题。说法不正确的是( ) D. 该晶体的密度为
2a3N
A
A. 电池工作时电子由电极a直接经外电路流向电极b
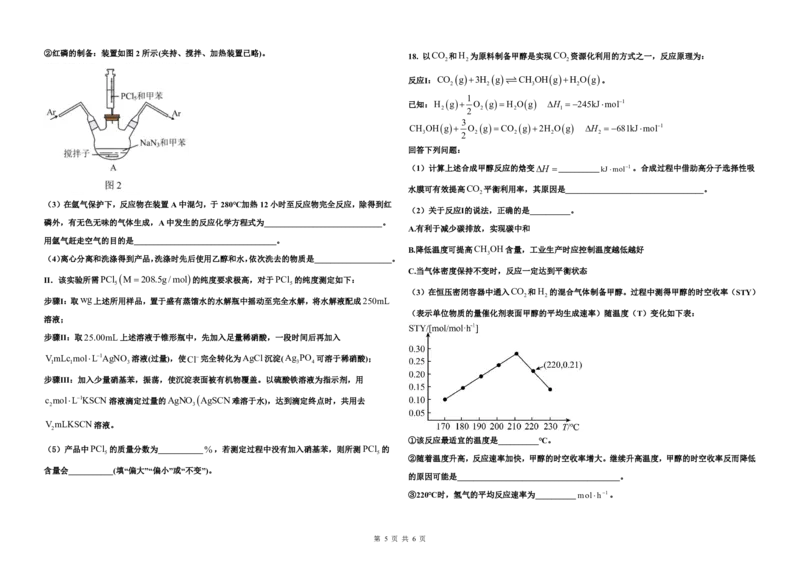
15. 室温下,调节MgCl 溶液、HF溶液、HA溶液[已知K
HF
K
HA
]的pH,测得溶液中
2 a a
B. 电极a上发生的反应为HCOO 2e 3OH CO2 2H O
3 2
c
F
c
A
C. 电极b上消耗1molK Fe(CN) 时,理论上共转移3mol电子 pX[ pXlgX ;X 代表 c
Mg2
、 , ]随溶液 pH 的变化如图所示[已知
3 6 c HF c HA
D. 上述无膜微流体技术可降低燃料电池的生产成本,提升电池工作性能
K
MgF
7.01011
]。下列叙述正确的是 ( )
sp 2
第 3 页 共 6 页
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}c F 升高而下降,原因是__________________________(用平衡移动原理解释);反萃取时萃余液应从分
A. L 代表溶液中p 随溶液pH的变化
2
c HF 液漏斗的___________(填“下口放出”或“上口倒出”)。
B. 浓度均为0.1mol·L1 NaF、NaA的混合溶液中:c OH c HF c HA (4)“萃取”过程中也可用酸(用H A 表示)作萃取剂,使In3进入有机相,发生反应:
2 2
c F c HF In3 3H A In HA 3H,平衡常数为K。已知c H 与萃取率 E% 的关系符合公式:
C.NaF、NaA的混合溶液中: 10 2 2 2 3
c
A
c
HA
E%
c3 H
D. 由于K sp MgF 2 、K sp Mg OH 2 很接近,故Mg OH 2 很难转化为MgF 2 lg 1E% lgKlg c3 H 2 A 2 。当pH 2.30时,萃取率为50%,若将萃取率提升到95%,应
调节溶液的pH ___________(已知lg19 1.28,忽略萃取剂浓度的变化,结果保留三位有效数字)。
第Ⅱ卷(非选择题 共55分) (5)整个工艺流程中,可循环利用的物质是___________。
16. 铟(In)是制造半导体、电光源等的重要原料。从铜冶炼过程中产生的铟砷烟灰(主要含有ZnO、
(6)2023年诺贝尔化学奖授予对量子点的发现有突出贡献的科研工作
PbO、Fe O 、In O 、As O 、In S 、SiO )中提取铟的工艺方法如下: 者。铜铟硫 CuInS 2 量子点被广泛应用于光电探测、发光二极管以及光
2 3 2 3 2 3 2 3 2
电化学电池领域。立方晶系CuInS 的晶胞结构如图所示,晶胞中In和S
2
未标明,用A或者B代替。Cu位于由S构成的___________(填“四面体
空隙”、“六面体空隙”或“八面体空隙”)中。
已知:①FeS O 为强电解质; 17. 红磷可用于制备半导体化合物,还可以用于制造火柴、烟火,以及三
4 6
氯化磷等。
②PO 为磷酸二异辛酯,密度为0.973g/cm3,其在酸性溶液中可萃取三价金属离子;
2 4
Ⅰ.研究小组以无水甲苯为溶剂,PCl (易水解)和NaN (叠氮化钠)为反
③K
In(OH)
1.41033。 5 3
sp 3
应物制备红磷。实验步骤如下:
回答下列问题:
①甲苯的干燥和收集:装置如图1所示(夹持及加热装置略)
(1)滤渣的主要成分除SiO 外还有___________、___________(填化学式);“氧化酸浸”过程中,
2 已知:二苯甲酮为指示剂,无水时体系呈蓝色,甲苯的沸点为110.6℃。
As O 中的砷元素被氧化为最高价的含氧酸,写出此反应的化学方程式___________________。 (1)在甲苯的干燥和收集过程中金属Na 的作用是___________________
2 3
(2)“还原铁”时反应的离子方程式为___________________________________。
(2)先小火加热控温100℃一段时间,打开活塞___________,达到除水
的目的。再升温至120℃左右,打开活塞___________,达到分离收集甲
(3)“萃取除铁”时,用30%的PO 作萃取剂时,发现当溶液pH 1.5后,铟萃取率随pH值的
2 4
苯的目的。
第 4 页 共 6 页
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}②红磷的制备:装置如图2所示(夹持、搅拌、加热装置已略)。
18. 以CO 和H 为原料制备甲醇是实现CO 资源化利用的方式之一,反应原理为:
2 2 2
反应Ⅰ:CO
g
3H
g
CH OH
g
H
O
g
。
2 2 3 2
1
已知:H g O g H O g H 245kJmol1
2 2 2 2 1
3
CH OH g O g CO g 2H O g H 681kJmol1
3 2 2 2 2 2
回答下列问题:
(1)计算上述合成甲醇反应的焓变H __________kJmol1。合成过程中借助高分子选择性吸
水膜可有效提高CO 平衡利用率,其原因是__________________________________。
2
(3)在氩气保护下,反应物在装置A中混匀,于280℃加热12小时至反应物完全反应,除得到红
(2)关于反应Ⅰ的说法,正确的是__________。
磷外,有无色无味的气体生成,A中发生的反应化学方程式为_____________________________。
A.有利于减少碳排放,实现碳中和
用氩气赶走空气的目的是___________________________________。
B.降低温度可提高CH OH含量,工业生产时应控制温度越低越好
3
(4)离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是___________________。
C.当气体密度保持不变时,反应一定达到平衡状态
Ⅱ.该实验所需PCl M208.5g/mol 的纯度要求极高,对于PCl 的纯度测定如下:
5 5
(3)在恒压密闭容器中通入CO 和H 的混合气体制备甲醇。过程中测得甲醇的时空收率(STY)
步骤Ⅰ:取wg上述所用样品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成250mL 2 2
(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
溶液;
步骤Ⅱ:取25.00mL上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入
VmLc molL1AgNO 溶液(过量),使Cl完全转化为AgCl沉淀(Ag PO 可溶于稀硝酸);
1 1 3 3 4
步骤Ⅲ:加入少量硝基苯,振荡,使沉淀表面被有机物覆盖。以硫酸铁溶液为指示剂,用
c molL1KSCN溶液滴定过量的AgNO AgSCN难溶于水),达到滴定终点时,共用去
2 3
V mLKSCN溶液。
2
①该反应最适宜的温度是__________℃。
(5)产品中PCl 的质量分数为___________%,若测定过程中没有加入硝基苯,则所测PCl 的
5 5
②随着温度升高,反应速率加快,甲醇的时空收率增大。继续升高温度,甲醇的时空收率反而降低
含量会___________(填“偏大”“偏小”或“不变”)。
的原因可能是________________________________________。
③220℃时,氢气的平均反应速率为__________molh1。
第 5 页 共 6 页
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}(4)CO 催化加氢制甲醇过程中,存在竞争的副反应主要是:
(1)化合物A的名称为___________________。
2
(2)B→C的反应类型为_____________。
CO
g
H
g
CO
g
H
O
g
H 41kJmol1
2 2 2
(3)C→D过程中实现了由__________到__________的转化(填官能团名称)。
在恒温、压强为p的反应条件中,1mol CO g 和3mol H g 反应并达到平衡状态,CO 平衡
2 2 2 (4)D分子中sp2杂化与sp3杂化的碳原子个数比为________________。
转化率为20%,甲醇选择性为50%,该温度下主反应的平衡常数K
p
__________。(列出计算式
(5)写出G→H的反应的化学方程式___________________________________________。
n
生成CH
OH
(6)试剂X的结构简式为___________________。
即可,用平衡分压代替平衡浓度,分压=总压×物质的量分数,甲醇的选择性 3 100%)
n
消耗CO
2 (7)B的同分异构体中,与B物质类别完全相同的结构有__________种,其中不同化学环境氢原
19. 处方药替米沙坦(化合物K)可用于成人原发性高血压或心血管疾病的治疗。某科研课题组设 子的种类数最少的化合物的结构简式为__________。
计出了一种新的合成路线如下(部分反应条件已省略):已知:
已知:
回答下列问题:
第 6 页 共 6 页
{#{QQABKQaQogCoAAIAABhCQwVgCAKQkhCCASgOwAAIMAIBSAFABAA=}#}高三化学试题参考答案
第Ⅰ卷(选择题 共 45 分)
一、单选题(本题共15小题,每小题3分。每小题只有一个选项符合题意。)
1 2 3 4 5 6 7 8 9 10
B C B D A A B A C D
11 12 13 14 15
C B C D C
第Ⅱ卷(非选择题 共 55 分)
二、非选择题(本题共4小题,总共55分)
16、(14分)
(1)PbSO MnO (2分) As O 2MnO 2H SO H O2H AsO 2MnSO (2分)
4 2 2 3 2 2 4 2 3 4 4
(2)2S O2 2Fe3 S O2 2Fe2 (2分)
2 3 4 6
(3) ln3 3H
2
O
ln(OH)
3
3H pH增大,In3水解生成In(OH)
3
,不利于P
2
O
4
萃取(2分)
上口倒出 (1分)
(4)2.73(2分) (5)萃余液
PO
(1分)
2 4
(6)四面体空隙(2分)
17、(14分)
(1)干燥甲苯(2分) (2) K、K (1分) K、K (1分)
1 3 1 2
280℃
(3) 10NaN 2PCl 2P15N 10NaCl (2分) 防止五氯化磷遇空气中的水蒸气而发生
3 5 2
水解,防止红磷被氧气氧化 (2分)
41.7c V c V
(4)甲苯、氯化钠(2分) (5) 1 1 2 2 (2分) 偏小(2分)
W
𝟏𝟖、(𝟏𝟑分)(1) -54 (2分) 借助高分子选择性吸水膜,分离出水,使得水浓度减小,平衡正向移动 (2分)
(2)A (2分)
(3)① 210 (1分) ②生成甲醇的反应为放热反应,升高温度超过一定程度后,导致平衡逆向移动(2分)
③. 0.63 (2分)
0.2 0.2
p p
3.8 3.8
(4)
3
(2分)
2.6 0.8
p p
3.8 3.8
19(𝟏𝟒分)
(1)邻甲基苯酚 (2分)
(2)取代反应 (1分)
(3) ①酚羟基 (1分) ②醚键 (1分)
(4)7:2 (2分)
(5) +C H COCl +HCl (2分)
3 7
(6) (2分)
(7)① 12 (2分) ② (1分)