文档内容
2023 年高考考前押题密卷(河北卷)
化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 F 19 Na 23 Mg 24 Al 27 P31
S 32 Ca 40 Cr 52
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.(原创)2022年中国科技创新结出累累硕果,加快实现了高水平建设科技强国。下列说法错误的是(
)
A.用于“天和”核心舱推进系统的氮化硼陶瓷是新型无机非金属材料
B.空间站搭载的太阳能电池板的核心材料是二氧化硅
C.“华龙一号”核电项目中核反应堆所用铀棒中含有的 U与 U互为同位素
D.我国新型国产航母福建号正式入列,航母甲板是高强度钢材,钢是一种铁碳合金
2.(原创)设N 表示阿伏加德罗常数的值,下列叙述中正确的是( )
A
A.含4.8g碳元素的石墨晶体中的共价键数是0.8N
A
B.常温下, 溶液中阴离子总数等于
C.标准状况下,甲烷和氧气的混合气体共22.4L,完全燃烧后产物的分子总数可能为N
A
D.常温下,5.6g铁与 的硝酸反应,铁失去的电子数为
3.(原创)化学是实验的科学,下列有关实验设计能达到目的的是( )
A B C D
1
学科网(北京)股份有限公司制备 胶 探究铁与水蒸气的反应,点
分离沸点不同的互溶液体 测定中和热
燃肥皂泡检验氢气
体
4.下列反应的离子方程式不正确的是( )
A.向NH Al(SO ) 中滴加Ba(OH) 使 恰好完全沉淀:
4 4 2 2
B.氯化铝溶液中加过量氨水:Al3++3NH·H O=Al(OH) ↓+3NH
3 2 3
C.向NaClO溶液中通入少量SO :SO +ClO-+H O= +Cl-+2H+
2 2 2
D.用惰性电极电解CuSO 溶液:2Cu2++2H O=======2Cu+O ↑+4H+
4 2 2
5.下列实验中根据现象得出的结论错误的是( )
选项 实验 现象 结论
用手触摸试管外壁 镁条与稀盐酸反应是放热反
A 将打磨后的镁条放盛入有稀盐酸的试管中
感觉变热 应
试管口有红棕色气
B 向某溶液中加铜和稀HSO 原溶液可能含有NO -
2 4 体产生 3
向某钠盐中滴加浓盐酸,将产生的气体通入
C 品红溶液褪色 该钠盐为NaSO 或NaHSO
品红溶液 2 3 3
向浓度均为0.1 mol·L-1的MgCl 、CuCl 混合
D 2 2 先出现蓝色沉淀 K [Mg(OH) ]>K [ Cu(OH) ]
溶液中逐滴加入氨水 sp 2 sp 2
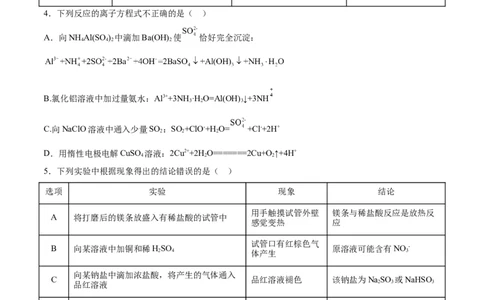
6. 奥司他韦可以用于治疗流行性感冒,其结构如图所示。下列关于奥司他韦的说法正确的是( )
2
学科网(北京)股份有限公司A.分子中至少有7个碳原子共平面
B.存在芳香族化合物的同分异构体
C.1 mol奥司他韦最多能与3 mol H 发生加成反应
2
D.含有4个手性碳原子
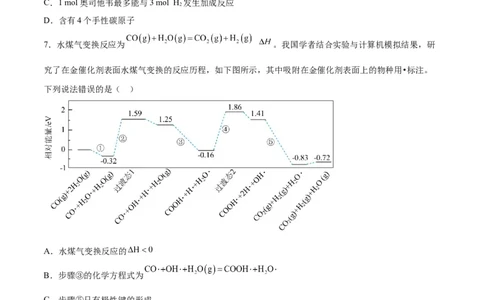
7.水煤气变换反应为 。我国学者结合实验与计算机模拟结果,研
究了在金催化剂表面水煤气变换的反应历程,如下图所示,其中吸附在金催化剂表面上的物种用•标注。
下列说法错误的是( )
A.水煤气变换反应的
B.步骤③的化学方程式为
C.步骤⑤只有极性键的形成
D.该反应中的决速步骤为步骤④
8.2022年诺贝尔化学奖授于了三位科学家,以表彰他们对“点击化学和生物正交化学”的发展做出的贡献。
化合物G是通过“点击化学”合成的产物,其结构如图所示。W、X、Y、Z为原子序数依次增大的短周期
主族元素,W、X、Z位于不同的周期,Y的核外电子数等于Z的最外层电子数。下列有关说法不正确的是
( )
3
学科网(北京)股份有限公司A.W原子核外电子只有一种自旋状态
B.简单氢化物的沸点:
C.X的第一电离能大于Y
D.基态Z原子的价电子排布式为:
9.在体积为1 L的恒容密闭容器中充入1 mol CO 和3 mol H ,一定条件下反应:
2 2
。测得CO 和H 的浓度随时间变化如图所示。下列说法正确的是
2 2
( )
A.平衡时 的转化率为75%
B.平衡后充入惰性气体,平衡向正向移动
C.该条件下,第9 min时 大于第3 min时
D.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
10.氨硼烷可用于制备BN管、制备白色石墨烯等。氨硼烷在催化剂的作用下可以水解释放氢气:
3NH BH+6H O=3NH +B O +9H ↑,的结构如图所示,下列有关说法错误的是( )
3 3 2 3 2
4
学科网(北京)股份有限公司A.氨硼烷和BN中只含有共价键
B.分子间氢键的强度:HO>NH
2 3
C.在反应中硼原子的杂化类型没有发生改变
D.氨硼烷中B、N原子的最外层均满足8电子稳定结构
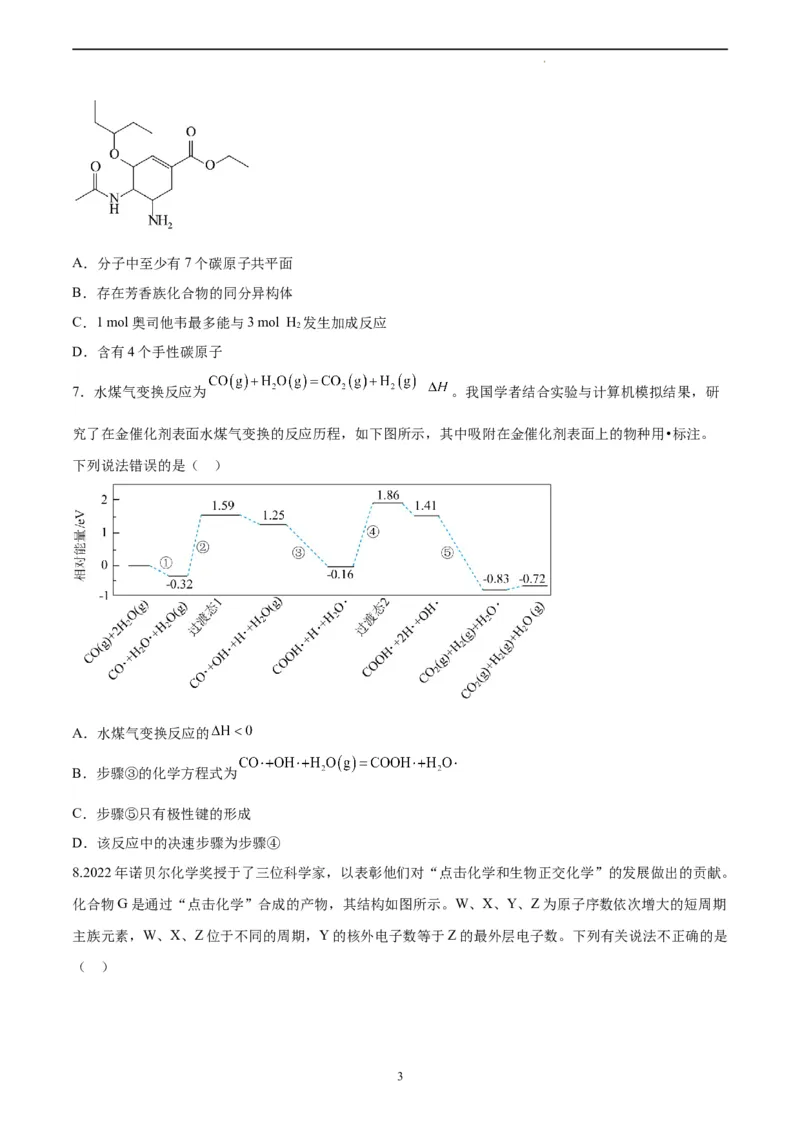
11.工业上利用含铅废渣(主要成分为 )制备碱式硫酸铅( )的简易流程如图所示。下
列说法错误的是( )
A.“转化”过程生成的气体为
B.由流程可推测,
C.该工艺中滤液2可循环利用
D.该流程发生了氧化还原反应
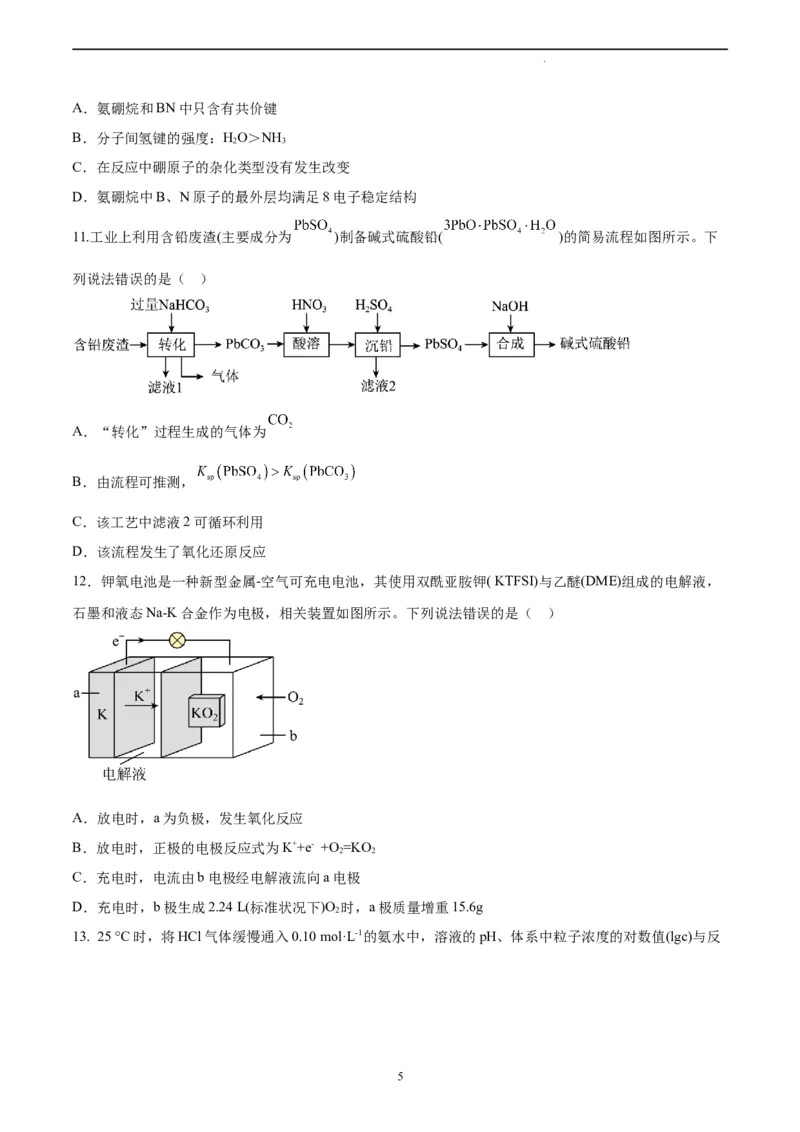
12.钾氧电池是一种新型金属-空气可充电电池,其使用双酰亚胺钾( KTFSI)与乙醚(DME)组成的电解液,
石墨和液态Na-K合金作为电极,相关装置如图所示。下列说法错误的是( )
A.放电时,a为负极,发生氧化反应
B.放电时,正极的电极反应式为K++e- +O =KO
2 2
C.充电时,电流由b电极经电解液流向a电极
D.充电时,b极生成2.24 L(标准状况下)O 时,a极质量增重15.6g
2
13. 25 °C时,将HCl气体缓慢通入0.10 mol·L-1的氨水中,溶液的pH、体系中粒子浓度的对数值(lgc)与反
5
学科网(北京)股份有限公司应物的物质的量之比 的关系如图所示。若忽略溶液体积变化,下列有关说法错误的是(
)
A.25 ° C时, NH ·H O的电离平衡常数为10-4.75
3 2
B.P 所示溶液:c(Cl-) < 0.05 mol·L-1
1
C.P 所示溶液:c( )= 100c( NH·H O )
2 3 2
D.P 所示溶液:c(Cl- )>c( ) >c(H+)>c(OH-)
3
14. 可用于配制无机防锈颜料的复合氧化物的晶胞结构如图,下列说法中不正确的是( )
A.该复合氧化物的化学式为
B.若图中A、B的原子坐标均为(0,0,0),则C的原子坐标为(0,0.5,0.5)
C.若该晶体密度为 ,钙和氧的最近距离为anm,则阿伏加德罗常数
D.由晶胞结构可知,与1个钙原子等距离且最近的氧原子有8个
第Ⅱ卷
二、非选择题:本题共4小题,共58分。微信搜索“高中试卷君”公众号 领取押题卷联考卷
15.(14分)四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);
6
学科网(北京)股份有限公司有关信息如下表:
化学式 SnCl SnCl
2 4
熔点/℃ 246 ﹣33
沸点/℃ 652 144
其他性
无色晶体,易氧化 无色液体,易水解
质
回答下列问题:
(1)甲装置中仪器A的名称为 _____。
(2)用甲装置制氯气,MnO 被还原为Mn2+,该反应的离子方程式为 _____。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到 _____(填现象)后,开始加热丁装置,锡
熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;
②_____。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为 _____;己装置的作用是 _____:
A.除去未反应的氯气,防止污染空气
B.防止空气中CO 气体进入戊装置
2
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O 进入戊装置的试管中使产物氧化
2
(5)某同学认为丁装置中的反应可能产生SnCl 杂质,以下试剂中可用于检测是否产生SnCl 的有 (填标
2 2
号)。
A.HO 溶液
2 2
B.FeCl 溶液(滴有KSCN)
3
C.AgNO 溶液
3
7
学科网(北京)股份有限公司D.溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl ,则SnCl 的产率为 _____。(保留3
4 4
位有效数字)微信搜索“高中试卷君”公众号 领取押题卷联考卷
16.(14分)工业上以工业废渣(主要含CaSO·2H O,还含少量SiO、Al O、 FeO、Fe O)为 原料制取
4 2 2 2 3 2 3
(NH )SO 晶体和轻质CaCO ,其实验流程如下:
4 2 4 3
已知:金属离子形成氢氧化物沉淀的pH范围[ pH =8.5时Al(OH) 开始溶解]
3
金属离子 Al3+ Fe3+ Fe2+ Ca2+
开始沉淀时pH 3.4 2.7 7.6 11.3
完全沉淀时pH 4.7 3.7 9.6
回答下列问题:
(1)提高废渣脱硫速率的方法是_______ (写两点) 。
(2)在“脱硫”中CaSO 可以较完全的转化为CaCO ,用沉淀溶解平衡原理解释选择(NH )CO 的原因_____。
4 3 4 2 3
[K (CaSO)=4.8×10-5,K (CaCO)=3×10-9]
sp 4 sp 3
(3)从滤液1中获取(NH )SO 晶体必要的操作是_______、_______、过滤等。
4 2 4
(4)下列可检验HO 是否过量的试剂是_______ (填字母)
2 2
A.KSCN B.K[Fe(CN) ] C.KMnO
3 6 4
(5)“调pH”除铁和铝时,应调节溶液的pH范围为_______。
(6)利用轻质CaCO 可以按照以下流程制得过氧化钙晶体。步骤②中反应的化学方程式为_______;将步骤
3
③过滤得到的白色晶体依次使用蒸馏水、乙醇洗涤,判断晶体已经洗涤干净的方法是_______; 使用乙醇
洗涤的目的是_______。
17.(15分)国际能源界高端会议“剑桥能源周”于3月 6日至10日在美国“能源之都”休斯敦召开,重
点讨论如何应对能源安全和能源转型的双重挑战。甲烷催化裂解制备乙烯、乙炔时涉及以下反应:
反应I:2CH(g) C H(g)+3H(g) H=+376.4kJ•mol-1
4 2 2 2 1
反应II:C
2
H
2
(g)+H
2
(g) C
2
H
4
(g) △H
2
=-174.4kJ•mol-1
△
8
学科网(北京)股份有限公司反应III:CH(g) C(s)+2H(g) H=+74.8kJ•mol-1
4 2 3
反应IV:2CH
4
(g) C
2
H
4
(g)+2H△2 (g) H
4
(1) H 4 =_______。 △
(2)△甲烷在固体催化剂表面发生反应I的过程如图所示。
①A、B、C中,能量状态最高的是______。
②某温度下,反应I的v =k •p2(CH)、v =k •p(C H)•p3(H ),(k为速率常数),部分数据如表所示。
正 正 4 逆 逆 2 2 2
p(C H)/MPa p(H )/MPa v /(MPa•min-1)
2 2 2 逆
0.05 p 4.8
1
p p 19.2
2 1
p 0.15 8.1
2
表中p=______,该温度下k =______MPa-3•min-1;温度开高,速率常数增大的倍数:k ______k (填
2 逆 正 逆
“>”“<”或“=”)。
(3)某温度下,向恒容密闭容器中充入一定量CH(此时压强为p),仅发生反应IV。
4 0
①测得平衡时p(H ):p(CH)=2:1,CH 的平衡转化率为_______(保留2位有效数字),反应IV的
2 4 4
K=_______。
p
②若升高反应体系温度,在相同时间内测得甲烷的转化率与温度的关系如图所示。T℃之后甲烷转化率减
0
小的原因是_______。
(4)一定条件下,甲烷裂解体系中几种气体的平衡分压的对数与温度的关系如图所示。
9
学科网(北京)股份有限公司①725℃时,反应I、III中,反应倾向较大的是______。
②工业上催化裂解甲烷常通入一定量的H,原因是______。
2
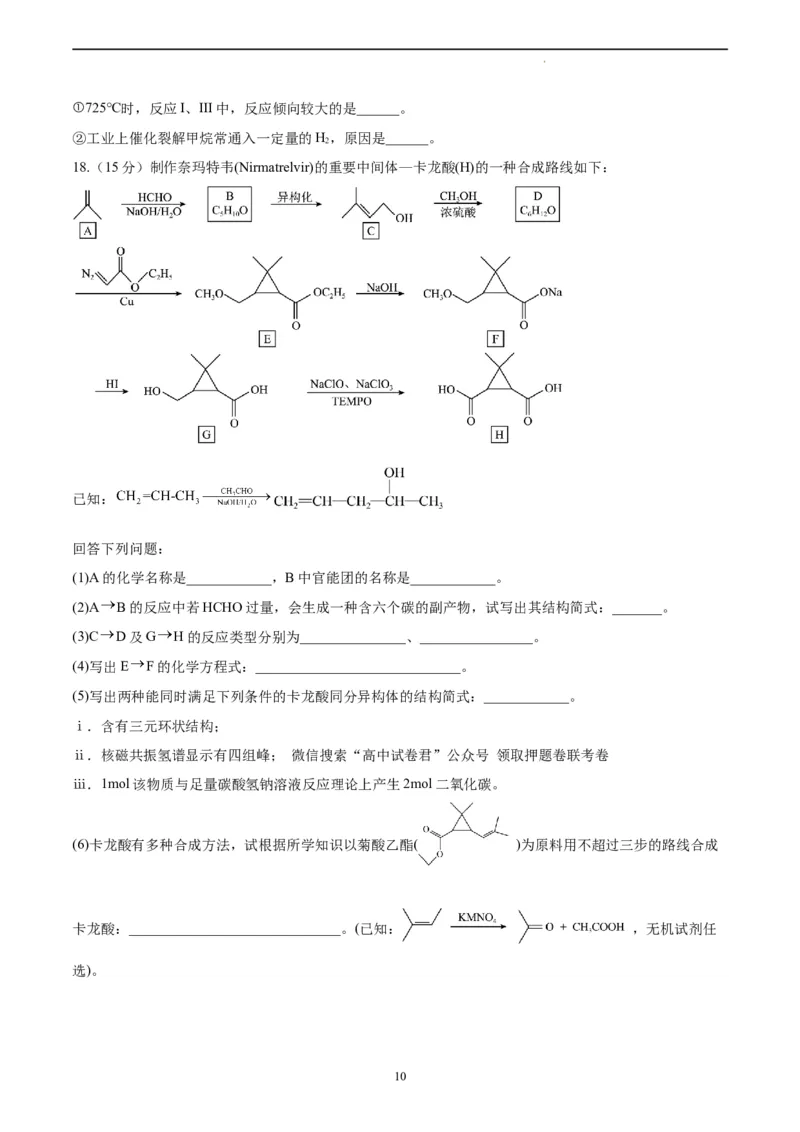
18.(15分)制作奈玛特韦(Nirmatrelvir)的重要中间体—卡龙酸(H)的一种合成路线如下:
已知:
回答下列问题:
(1)A的化学名称是____________,B中官能团的名称是____________。
(2)A B的反应中若HCHO过量,会生成一种含六个碳的副产物,试写出其结构简式:_______。
(3)C D及G H的反应类型分别为_______________、________________。
(4)写出E F的化学方程式:_____________________________。
(5)写出两种能同时满足下列条件的卡龙酸同分异构体的结构简式:____________。
ⅰ.含有三元环状结构;
ⅱ.核磁共振氢谱显示有四组峰; 微信搜索“高中试卷君”公众号 领取押题卷联考卷
ⅲ.1mol该物质与足量碳酸氢钠溶液反应理论上产生2mol二氧化碳。
(6)卡龙酸有多种合成方法,试根据所学知识以菊酸乙酯( )为原料用不超过三步的路线合成
卡龙酸:______________________________。(已知: ,无机试剂任
选)。
10
学科网(北京)股份有限公司11
学科网(北京)股份有限公司