文档内容
2023 年高考考前押题密卷(浙江卷)
化学·参考答案
题号 1 2 3 4 5 6 7 8
答案 D B A C C C A B
题号 9 10 11 12 13 14 15 16
答案 D C B D C D C D
1.D
【解析】A项,NaCl是正盐,故不选A;B项,(NH)CO 是正盐,故不选B;C项,NaHSO 是酸式
4 2 3 4
盐,NaHSO 不易分解,故不选C;D项,NaHCO 是酸式盐,NaHCO 受热分解为碳酸钠、二氧化碳、水,
4 3 3
故选D;故选D。
2.B
【解析】A项,KFeO 中钾、氧元素化合价分别为+1、-2,则铁元素的化合价为+6价,A正确;B项,
2 4
Fe为26号元素,元素位于周期表d区,B错误;C项,强电解质是指在水溶液中或熔融状态下,能够完全
电离的化合物,即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,一般是强酸、强碱和
大部分盐类;高铁酸钾属于强电解质,C正确;D项,用KFeO 对饮用水处理时,六价铁具有强氧化性转
2 4
变为三价铁,能起到消毒杀菌;铁离子水解生成氢氧化铁胶体,具有吸附杂质的作用,D正确;故选B。
3.A
【解析】A项,N的质子数为7,原子核外最外层有5个电子,氨的电子式为: ,A错误;B项,
Cu是29号元素,其核外电子排布式为:[Ar]3d104s1,故Cu位于元素周期表的ds区,B正确;C项,因
HSO 为强酸,故NaHSO 在水中完全电离,电离方程式:NaHSO=Na++H++SO2-,C正确;D项,已知
2 4 4 4 4
SO 中心原子S周围的价层电子对数为:2+ =3,故SO 的VSEPR模型: ,D正确;故选
2 2
A。
4.C
【解析】A项,碳酸钠和碳酸氢钠的溶液均存在水解,使得溶液呈碱性,可用作食用碱或工业用碱,
A正确;B项,不锈钢中的合金元素主要是铬和镍,具有很强抗腐蚀能力,性能优良,可用于医疗器材,
B正确;C项,硅的导电性介于导体与绝缘体之间,可用来生产半导体,C错误;D项,次氯酸的强氧化
1
学科网(北京)股份有限公司性能使某些有机色素褪色,可用作棉麻的漂白剂,D正确;故选C。
5.C
【解析】A项,浓硫酸与蔗糖反应,观察到蔗糖变黑变为碳,体现了浓硫酸的脱水性,A正确;B项,
硝酸见光受热易分解为二氧化氮和氧气,一般保存在棕色试剂瓶中,放置在阴凉处,B正确;C项,
NO 、NO与CO反应需要在催化剂作用下转化为无毒的气体,因此需要催化转化后排放,C错误;D项,
2
铝与酸、碱均会反应,故铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物,D正确;故选C。
6.C
【解析】A项,根据反应方程式,Cu(CHCOO) 中Cu元素化合价由+2价→+1价,化合价降低,
3 2
Cu(CHCOO) 作氧化剂,NH 中N显-2价,N的化合价由-2价→0价,化合价升高,NH 作还原剂,故A
3 2 2 4 2 4
正确;B项,根据A选项分析,Cu(CHCOO) 作氧化剂,Cu O为还原产物,NH 作还原剂,利用还原剂
3 2 2 2 4
的还原性强于还原产物的还原性,即还原性:NH>Cu O,故B正确;C项,Cu O为还原产物,N 为氧
2 4 2 2 2
化产物,氧化产物与还原产物的物质的量之比为1∶2,故C错误;D项,生成0.5molCu O,转移电子物质
2
的量为0.5mol×2×(2-1)=1mol,故D正确;故选C。
7.A
【解析】A项,SO 具有还原性,NaClO具有强氧化性,SO 与NaClO发生氧化还原反应,该反应的离
2 2
子方程式应该为2ClO-+SO+H O=SO 2-+Cl-+2HClO,A错误;B项,由于K (H CO)>K(HClO)>
2 2 4 a1 2 3 a
K (H CO),NaCO 溶液吸收少量Cl,碳酸根转化为碳酸氢根,方程式为:2CO2-+Cl+H O=2HCO -+ClO-
a2 2 3 2 3 2 3 2 2 3
+Cl-,B正确;C项,乙酰水杨酸( )与过量NaOH溶液共热,羧基显酸性且酯基是酚羟基与羧基
形成的酯基,即 +3OH- +CH COO-+2H O,C正确;D项,氯化铜浓溶液常呈绿
3 2
色,是棕黄色([CuCl]2-)与蓝色([Cu(HO)]2+)的互补色,可知[CuCl]2-和[Cu(HO)]2+在溶液中共存,两者之间
4 2 4 4 2 4
存在动态平衡,可表示为:[CuCl]2-+4H O [Cu(HO)]2++4Cl-,D正确;故选A。
4 2 2 4
8.B 微信搜索“高中试卷君”公众号 领取押题卷联考卷
【解析】A项,苯酚和甲醛在催化剂条件发生缩聚反应生成酚醛树脂,酸催化生成线型结构树脂,碱
催化得到体型结构树脂,故A正确;B项,木材、秸秆都含有大量的纤维素,加工后可以提取纤维素,得
不到合成纤维,故B错误;C项,乙烯在较高压力、较高温度并在引发剂的作用下,发生加聚反应得到的
是低密度聚乙烯,故C正确;D项,氨基酸残基在蛋白质肽链中的排列顺序称为蛋白质的一级结构,一级
2
学科网(北京)股份有限公司结构是形成二级、三级等其他高级结构的基础,故D正确;故选B。
9.D
【解析】A项,化合物Ⅰ的分子式为C HO,化合物Ⅱ的分子式为C HO,可推断出该反应的原子利
3 6 4 6 3
用率为100%,A正确;B项,化合物Ⅰ分子中含有亚甲基结构,不可能所有原子共平面,B正确;C项,
根据化合物Ⅱ的分子结构可知,碳原子的杂化方式有sp2、sp3两种,C正确;D项,如图所示 、
,化合物Ⅰ和化合物Ⅱ分子的一氯代物数目均为2,D错误;故选D。
10.C
【解析】W、X、Y、Z为原子序数依次增大的短周期主族元素,X与Y、Z均相邻,则X为第二周期
元素,根据题给化合物的结构,W元素形成1个共价键,W为H,X与H形成XH + ,X为-3价,则X为
4
N,Y是O,Z是P。A项,同周期主族元素,原子序数越大,半径越小,同主族元素,电子层数越多,原
子半径越大,则原子半径大小关系为P>N>O,故A正确;B项,NH 和PH 的中心原子杂化方式均为sp3,
3 3
且均有一个孤电子对,键长:P—H键>N—H键,导致PH 中成键电子对之间斥力比NH 小,故键角:
3 3
NH>PH ,故B正确;C项,该化合物的阴离子中P原子形成5个共价键,形成最外层有10个电子的结构,
3 3
故C错误;D项,H、N、O三种元素形成的化合物NH NO 中既含离子键又含共价键,故D正确;故选
4 3
C。
11.B
【解析】从总反应分析, LiC 变为C和Li+为氧化反应,该极为原电池的负极。而Li FePO 变为
x 6 1-x 4
LiFePO 发生还原反应,它为原电池的正极。A项,放电的负极为 LiC - xe- = xLi++6C,A项正确;B项,
4 x 6
a过程由于Fe2+化合价升高为Fe3+,为了平衡电荷Li+脱嵌减少。从图看晶胞中减少了棱上1个和面心的一
个Li+总共减少 ,所以1mol晶体中转移 N 电子,B项错误;C项,放电时,该材料在正极发生
A
还原反应,即Fe由+2变为+3为b过程,Li+嵌入正极,C项正确;D项,充电时的总反应为 6C+LiFePO =
4
LiC +Li FePO ,阳极发生氧化反应为 LiFePO - xe-= Li FePO +xLi+,D项正确;故选B。
x 6 1-x 4 4 1-x 4
12.D
3
学科网(北京)股份有限公司【解析】A项,HO 的结构: ,正负电荷中心不能重合,为极性分子,故A错误;
2 2
B项,电负性:N<O,NH 分子中的氮原子更容易给出孤电子对,所以NH 、HO与Co3+形成配离子的稳
3 3 2
定性:NH >HO,故B错误;C项,[Co(NH )]Cl 中含有NH 与Co3+形成6个配位键,6个的NH 中有
3 2 3 6 3 3 3
6×3=18个N-H键,所以1 mol [Co(NH )]Cl 含有σ键的数目为(18+6=24)N ,故C错误;D项,根据结构
3 6 3 A
图可知,若[Co(NH )]3+中两个NH 被Cl-替代,可能取代的邻近的或者相对位置的两个NH ,得到的
3 6 3 3
[Co(NH ) Cl]-有2种结构,故D正确;故选D。
3 4 2
13.C
【解析】已知:CHNH ·H O为一元弱碱,性质与NH ·H O类似,则会发生部分电离, CHNH ·H O
3 2 2 3 2 3 2 2
CHNH ++OH-;随着pH值变大,CHNH +含量变小、CHNH ·H O含量变大,结合图像可知,图
3 3 3 3 3 2 2
中实曲线为混合溶液中pH与CHNH +浓度的对数值(lgc)的关系、虚线为混合溶液中pH与CHNH ·H O浓
3 3 3 2 2
度的对数值(lgc)的关系;两条对角斜线分别为氢离子、氢氧根离子对应曲线,斜率为正的代表氢离子、斜
率为负的代表氢氧根离子。A项,CHNH ·H O的水溶液中存在:CHNH ·H O CHNH ++OH-,A正确;
3 2 2 3 2 2 3 3
⇌
B项,由点Q可知,pH=9.5,pOH=4.5,则 ,故其数量级为
10-5,B正确;C项,P点无法计算氯离子的浓度,故不能计算c(Cl-)+c(CHNH +)+c(CH NH ·H O)的值,C
3 3 3 2 2
错误; D项,P点之后根据电荷守恒可知,溶液中存在c(Cl-)+c(OH-)=c(CHNH +)+c(H+),D正确;故选
3 3
C。
14.D 微信搜索“高中试卷君”公众号 领取押题卷联考卷
【解析】A项,由题干可知,反应为(CH)CBr+H O (CH)COH+HBr,HBr = H++Br-,酸性增强
3 3 2 3 3
导致反应(CH)CBr+H O (CH)COH+HBr逆向进行,使得(CH)CBr→(CH)COH转化率降低,A错
3 3 2 3 3 3 3 3 3
误; B项,反应物能量大于生成物能量,为放热反应,升高温度,平衡逆向移动,导致原料平衡转化率下
降,B错误;C项,过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,
峰值越小则活化能越小,活化能越小反应越快,活化能越大反应越慢;由图可知,分子中碳溴键断裂所需
活化能更大,故分子中碳溴键断裂的速率比(CH)C+与HO结合速率慢,C错误;D项,碘原子半径大于
3 3 2
溴原子大于氯原子,则C-I键能更小,利于C-I断裂发生反应,故推测(CH)C-X水解生成(CH)COH的速
3 3 3 3
率:(CH)C-I>(CH)C-Br>(CH)C-Cl,D正确;故选D。
3 3 3 3 3 3
15.C
4
学科网(北京)股份有限公司【解析】A项,醋酸电离平衡常数小于磷酸电离平衡常数,则醋酸酸性小于磷酸,根据强酸制取弱酸
原理知,醋酸不能制取磷酸,A错误;B项,牙膏中经常添加碳酸钙,主要是碳酸钙难溶于水,用作为摩
擦剂,而不是增加Ca2+浓度,抑制牙齿腐蚀,B错误;C项,存在沉淀溶解平衡Ca (PO )OH(s)+F-(aq)
5 4 3
Ca (PO )F(s)+OH-(aq),K= =2.0×1030,当
5 4 3
时, Q= < <2.0×1030=K,沉淀溶解平衡正向移动,所以Ca (PO )OH
c 5 4 3
与F-反应生成Ca (PO )F, C正确; D项,向牙膏中添加NaF可增强护齿效果,是由于Ca (PO )F的溶解
5 4 3 5 4 3
度小于Ca (PO )(OH),羟基磷酸钙在水中存在溶解平衡:Ca (PO )(OH) 5Ca2++3 PO 3-+OH-,当F-与
5 4 3 5 4 3 4
Ca2+、PO 3-结合生成了更难溶于水的Ca (PO )F时,起到保护牙齿的作用,而NaHCO 是可将口腔内的细
4 5 4 3 3
菌发酵产生的酸性物质逐渐地减少,有助于保护牙齿,减少对牙釉质的损伤,两者原理不相同,D错误;
故选C。
16.D
【解析】A项,因醛基与新制Cu(OH) 悬浊液反应时应在碱性条件下进行,题中蔗糖水解后,没有加
2
NaOH中和稀硫酸,就加入新制的Cu(OH) 悬浊液,不能检验葡萄糖,不能证明蔗糖未水解,A不合题意;
2
B项,挥发的盐酸与苯酚钠也会发生反应,由操作和现象不能比较碳酸、苯酚的酸性强弱,B不合题意;C
项,将铁锈溶于浓盐酸,滴入KMnO 溶液,由于盐酸或者Cl-也能使酸性高锰酸钾溶液褪色,故紫色褪去
4
不能说明铁锈中含有二价铁,C不合题意;D项,向1mL0.1 mol·L-1MgSO 溶液中滴入2滴0.1
4
mol·L-1NaOH溶液,则MgSO 过量,再滴入2滴0.1 mol·L-1CuSO 溶液,先产生白色沉淀,滴入CuSO 溶
4 4 4
液后白色沉淀逐渐变为蓝色,说明存在Mg(OH) 转化为Cu(OH) 的沉淀转化,故能说明K [Cu(OH) ]<
2 2 sp 2
K [Mg(OH) ],D符合题意;故选D。
sp 2
17.(1) 1s22s22p63s23p63d64s2 或 [Ar]3d64s2(1分) d(1分)
(2)Fe3+的3d5半满状态更稳定(1分)微信搜索“高中试卷君”公众号 领取押题卷联考卷
(3) FeCl 为分子晶体,熔点受分子间作用力影响,FeF 是离子晶体,熔点受离子键强弱的影响,离子
3 3
键强度比分子间作用力大得多(2分) H O和OH-中的O原子提供孤电子对,Fe3+有空轨道能接受孤电子
2
对,形成配位键(2分)
(4) 1:3(1分) N ·a3·10-6(2分)
A
【解析】(1)基态Fe原子核外电子排布式为1s22s22p63s23p63d64S2 或 [Ar]3d64S2;Ni是28号元素,其价
5
学科网(北京)股份有限公司电子排布式为3d84s2,其位于元素周期表的d区;(2)从结构角度分析,Fe2+ 易被氧化成Fe3+的原因是
Fe3+的3d5半满状态更稳定;(3)①FeCl 的熔点(306℃)显著低于FeF 的熔点(1000℃)的原因是FeCl 为分子
3 3 3
晶体,熔点受分子间作用力影响,FeF 是离子晶体,熔点受离子键强弱的影响,离子键强度比分子间作用
3
力大得多;②形成双核阳离子的原因HO和OH- 中的O原子提供孤电子对,Fe3+ 有空轨道能接受孤电子
2
对,形成配位键;(4)①由晶胞图可知,Cu原子位于顶点,其个数为8× =1,Ni原子位于面心,其个数为
6× =3,则晶胞中铜原子与镍原子的原子个数比为1:3;②由①可知,该晶胞中含有1个Cu原子,含有
3个Ni原子,则1个晶胞含有1个CuNi ,其物质的量为 mol,1个晶胞的体积为 ,则该晶
3
体的摩尔体积为N ·a3·10-6 m3·mol-1。
A
18.(1) 铁、钠、氧(2分) NaFe (OH) (SO ) 或NaFe (OH) (SO )(2分)
3 6 4 2 2 6 12 4 4
(2) Na SO 、HSO (2分)
2 4 2 4
(3)2NaFeO+4H SO = Na SO +Fe (SO )+4H O(2分)
2 2 4 2 4 2 4 3 2
(4)先将混合气体通过品红溶液,如溶液褪色,说明有SO ,再将气体通过酸性高锰酸钾溶液除去
2
SO ,剩余气体用带火星的木条检验,如木条复燃,说明有O(2分)
2 2
【解析】从流程图可知,X+HO→A+B,A为碱性溶液且焰色试验呈黄色,且能与HCl发生中和反应,
2
则A为NaOH,恰好中和A溶液消耗0.06mol HCl,n(NaOH)=0.06mol,n(Na+)=0.06mol,m(Na+)=1.38g;B
为红褐色沉淀,则B为Fe(OH) ,n[Fe(OH) ]=0.06mol,n(Fe3+)=0.06mol,m(Fe3+)=3.36g;化合物X由3种元
3 3
素组成,则组成X的元素为Fe、Na和O, ,n(Na):n(Fe):n(O)=1:1:
2,X的化学式为NaFeO。NaFeO 与过量稀硫酸反应,化学方程式为2NaFeO+4H SO =
2 2 2 2 4
NaSO +Fe (SO )+4H O,得到无色溶液C和浅黄色沉淀D。溶液C无色,则所含溶质为NaSO 和过量的
2 4 2 4 3 2 2 4
HSO 。溶液C中不含铁元素,则浅黄色沉淀D含n(Fe3+)=0.06mol,D隔绝空气加热得到气体F和固体E,
2 4
气体F中含有水蒸气1.08 g,则n(H O)=0.06mol,说明D中含n(OH-)=0.12mol,n(Fe3+):n(OH-)=1:2,固
2
体E和水反应生成红色沉淀Fe(OH) 和无色溶液,往无色溶液中加足量氯化钡溶液得到白色沉淀,此沉淀
3
为BaSO 沉淀,说明D中含SO 2-,由此可得D的化学式为NaFe (OH) (SO ) 或NaFe (OH) (SO )。(1)组成
4 4 3 6 4 2 2 6 12 4 4
X的元素为铁、钠和氧;根据分析浅黄色沉淀D含n(Fe3+)=0.06mol,含n(OH-)=0.12mol,n(Fe3+):
6
学科网(北京)股份有限公司n(OH-)=1:2,且含SO 2-,由此可得D的化学式为NaFe (OH) (SO ) 或NaFe (OH) (SO );(2)根据分析,
4 3 6 4 2 2 6 12 4 4
溶液C无色,则所含溶质为NaSO 和过量的HSO ;(3)X的化学式为NaFeO,NaFeO 与过量稀硫酸反应,
2 4 2 4 2 2
化学方程式为2NaFeO+4H SO = Na SO +Fe (SO )+4H O;(4)根据分析,D为NaFe (OH) (SO ) 或
2 2 4 2 4 2 4 3 2 3 6 4 2
NaFe (OH) (SO ),D隔绝空气加热得到的气体F中除水蒸气外,另2种气体应为SO 和O,检验这两种
2 6 12 4 4 2 2
气体,可以先将混合气体通过品红溶液,如溶液褪色,说明有SO ,再将气体通过酸性高锰酸钾溶液除去
2
SO ,剩余气体用带火星的木条检验,如木条复燃,说明有O。
2 2
19.(1) A(1分) 622.7~913.3K(2分)
(2) K= (1分) 保持O 的浓度,降低CO 的浓度,使平衡正向移动,提高二氧化锰的产率(2分)
2 2
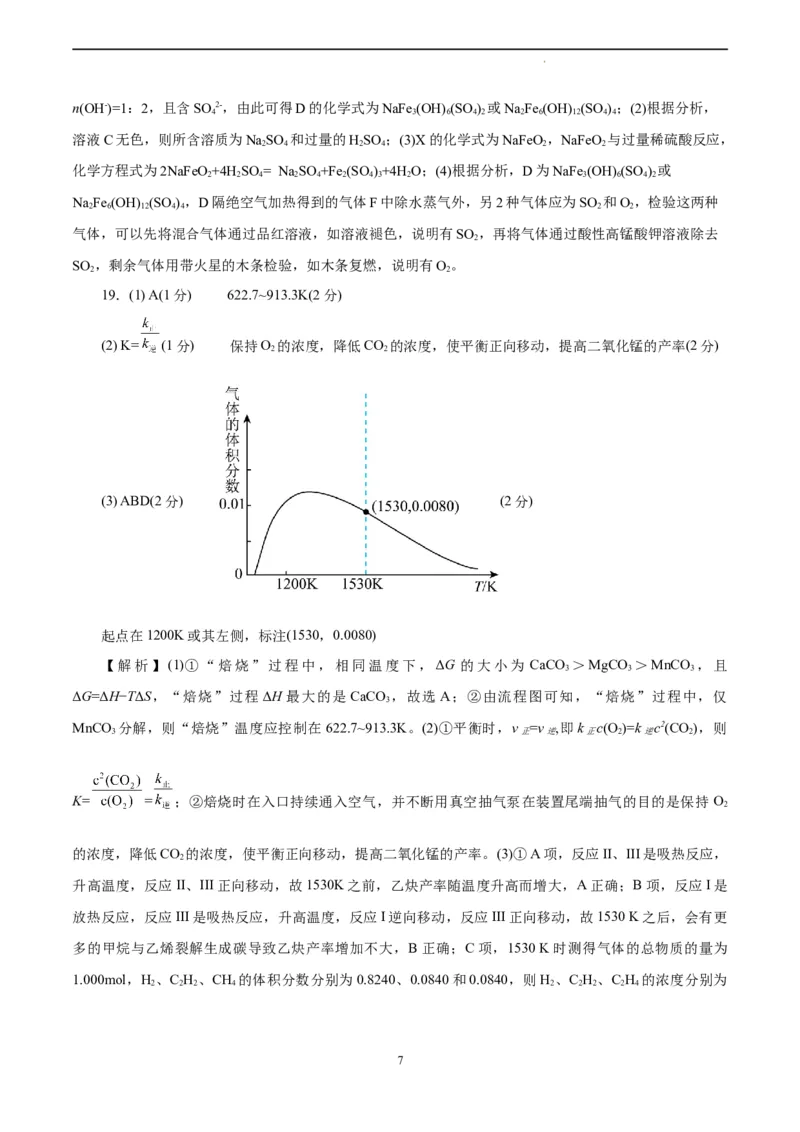
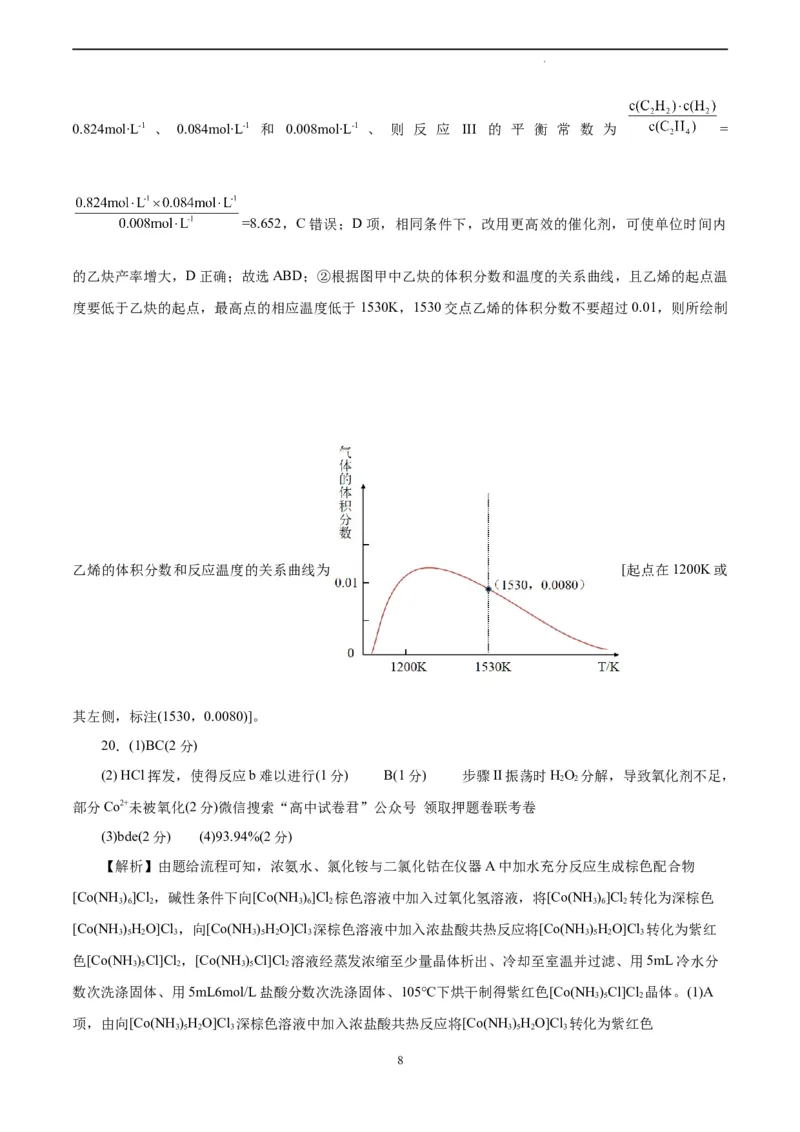
(3) ABD(2分) (2分)
起点在1200K或其左侧,标注(1530,0.0080)
【解析】(1)①“焙烧”过程中,相同温度下,ΔG 的大小为 CaCO >MgCO >MnCO ,且
3 3 3
ΔG=ΔH−TΔS,“焙烧”过程 ΔH 最大的是 CaCO ,故选 A;②由流程图可知,“焙烧”过程中,仅
3
MnCO 分解,则“焙烧”温度应控制在 622.7~913.3K。(2)①平衡时,v =v ,即k c(O )=k c2(CO),则
3 正 逆 正 2 逆 2
K= = ;②焙烧时在入口持续通入空气,并不断用真空抽气泵在装置尾端抽气的目的是保持 O
2
的浓度,降低CO 的浓度,使平衡正向移动,提高二氧化锰的产率。(3)①A项,反应II、III是吸热反应,
2
升高温度,反应II、III正向移动,故1530K之前,乙炔产率随温度升高而增大,A正确;B项,反应I是
放热反应,反应III是吸热反应,升高温度,反应I逆向移动,反应III正向移动,故1530 K之后,会有更
多的甲烷与乙烯裂解生成碳导致乙炔产率增加不大,B正确;C项,1530 K时测得气体的总物质的量为
1.000mol,H 、C H 、CH 的体积分数分别为0.8240、0.0840和0.0840,则H 、C H 、C H 的浓度分别为
2 2 2 4 2 2 2 2 4
7
学科网(北京)股份有限公司0.824mol∙L-1 、 0.084mol∙L-1 和 0.008mol∙L-1 、 则 反 应 III 的 平 衡 常 数 为 =
=8.652,C错误;D项,相同条件下,改用更高效的催化剂,可使单位时间内
的乙炔产率增大,D正确;故选ABD;②根据图甲中乙炔的体积分数和温度的关系曲线,且乙烯的起点温
度要低于乙炔的起点,最高点的相应温度低于 1530K,1530交点乙烯的体积分数不要超过0.01,则所绘制
乙烯的体积分数和反应温度的关系曲线为 [起点在1200K或
其左侧,标注(1530,0.0080)]。
20.(1)BC(2分)
(2) HCl挥发,使得反应b难以进行(1分) B(1分) 步骤II振荡时HO 分解,导致氧化剂不足,
2 2
部分Co2+未被氧化(2分)微信搜索“高中试卷君”公众号 领取押题卷联考卷
(3)bde(2分) (4)93.94%(2分)
【解析】由题给流程可知,浓氨水、氯化铵与二氯化钴在仪器A中加水充分反应生成棕色配合物
[Co(NH )]Cl ,碱性条件下向[Co(NH )]Cl 棕色溶液中加入过氧化氢溶液,将[Co(NH )]Cl 转化为深棕色
3 6 2 3 6 2 3 6 2
[Co(NH )HO]Cl ,向[Co(NH )HO]Cl 深棕色溶液中加入浓盐酸共热反应将[Co(NH )HO]Cl 转化为紫红
3 5 2 3 3 5 2 3 3 5 2 3
色[Co(NH )Cl]Cl ,[Co(NH )Cl]Cl 溶液经蒸发浓缩至少量晶体析出、冷却至室温并过滤、用5mL冷水分
3 5 2 3 5 2
数次洗涤固体、用5mL6mol/L盐酸分数次洗涤固体、105℃下烘干制得紫红色[Co(NH )Cl]Cl 晶体。(1)A
3 5 2
项,由向[Co(NH )HO]Cl 深棕色溶液中加入浓盐酸共热反应将[Co(NH )HO]Cl 转化为紫红色
3 5 2 3 3 5 2 3
8
学科网(北京)股份有限公司[Co(NH )Cl]Cl 可知,与钴离子形成配位键的能力由强到弱为:NH >Cl−>H O,故正确;B项,一水合氨
3 5 2 3 2
在溶液中存在电离平衡,制备[Co(NH )Cl]Cl 时,氯化铵除提供氯离子外,还可以增大一水合氨的浓度,
3 5 2
有利于[Co(NH )Cl]Cl 的生成,故错误;C项,将步骤III中的浓盐酸改为硫酸溶液不可能增大溶液中的氯
3 5 2
离子浓度,不能将[Co(NH )HO]Cl 转化为紫红色[Co(NH )Cl]Cl ,故错误;D项,若步骤II的溶液pH过
3 5 2 3 3 5 2
低,溶液中的氢离子会使氨分子转化为铵根离子,不利于[Co(NH )Cl]Cl 的生成会导致产率降低,故正确;
3 5 2
故选BD;(2)①步骤III振荡仪器A时,可能导致氯化氢挥发使得盐酸浓度减小,不利于反应b进行,使得
产物中混有大量粉红色的副产物[Co(NH )HO]Cl ;②用密封的仪器B代替敞口的仪器A可以减少氯化氢
3 5 2 3
挥发使得盐酸浓度减小,有利于反应b进行,从而提高产品的纯度和产率,故选B,③步骤II振荡时HO
2 2
发生分解反应,导致过氧化氢溶液的浓度减小,使得部分Co2+未被氧化,发生副反应生成碱式氯化亚钴,
所以不管有无改进装置,产物中都会混杂有少量蓝色碱式氯化亚钴晶体;(3)由分析可知,[Co(NH )Cl]Cl
3 5 2
溶液经蒸发浓缩至少量晶体析出、冷却至室温并过滤、用5mL冷水分数次洗涤固体、用5mL6mol/L盐酸
分数次洗涤固体、105℃下烘干制得紫红色[Co(NH )Cl]Cl 晶体,故答案为:b、d、e;(4)设样品中
3 5 2
[Co(NH )Cl]Cl 和氯化铵的物质的量分别为amol、bmol,由步骤I可得:5a+b=0.008,由步骤II可得:
3 5 2
3a+b=0.005,解得a=0.0015mol,则样品的纯度为 ×100%=93.94%。
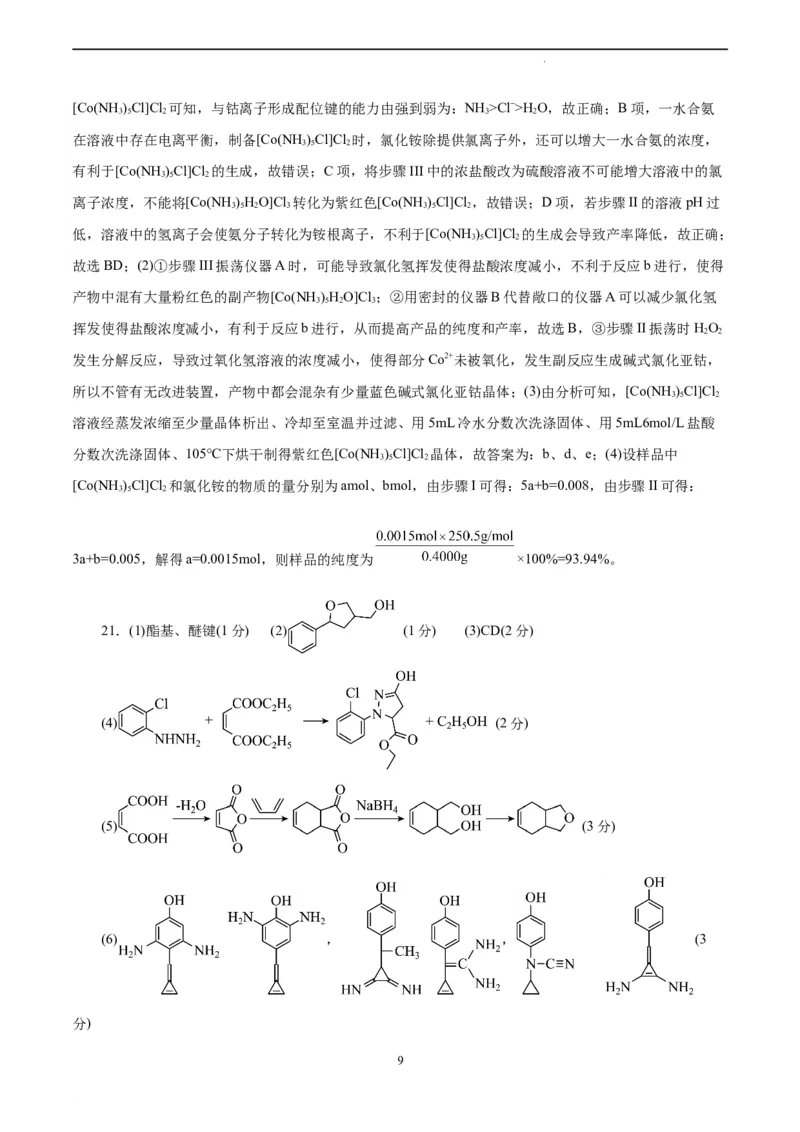
21.(1)酯基、醚键(1分) (2) (1分) (3)CD(2分)
(4) (2分)
(5) (3分)
(6) , , (3
分)
9
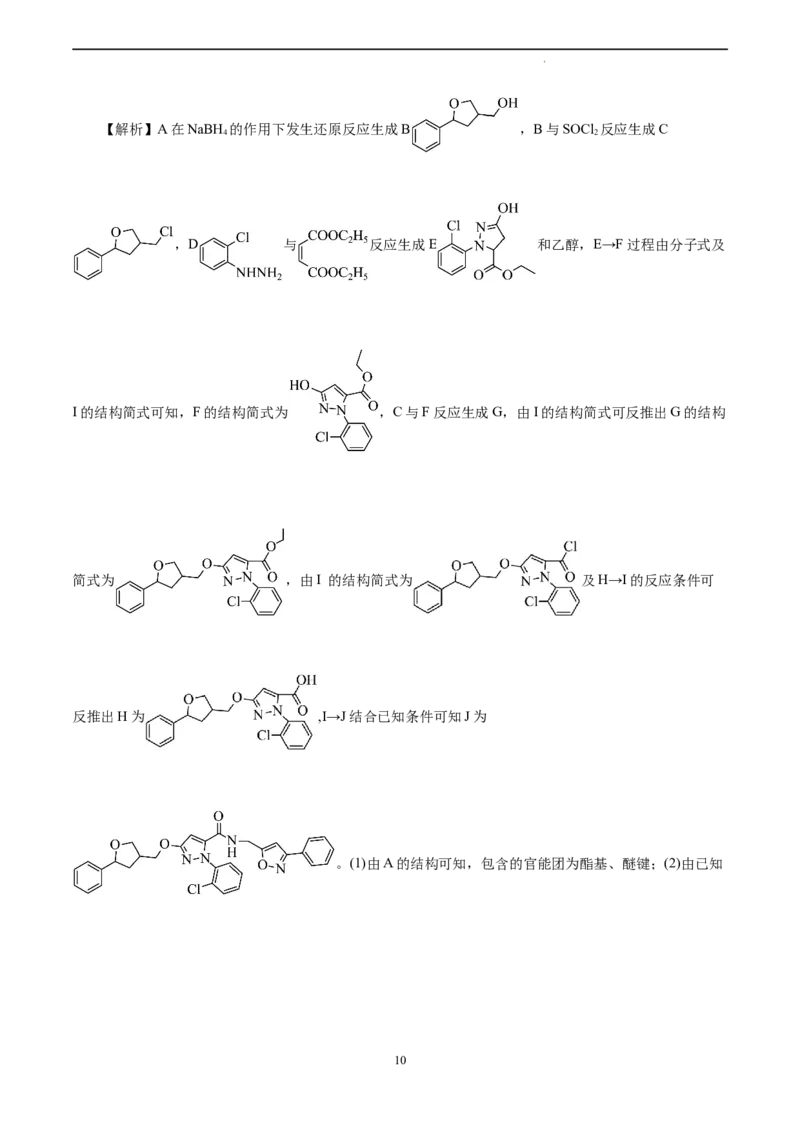
学科网(北京)股份有限公司【解析】A在NaBH 的作用下发生还原反应生成B ,B与SOCl 反应生成C
4 2
,D 与 反应生成E 和乙醇,E→F过程由分子式及
I的结构简式可知,F的结构简式为 ,C与F反应生成G,由I的结构简式可反推出G的结构
简式为 ,由I 的结构简式为 及H→I的反应条件可
反推出H为 ,I→J结合已知条件可知J为
。(1)由A的结构可知,包含的官能团为酯基、醚键;(2)由已知
10
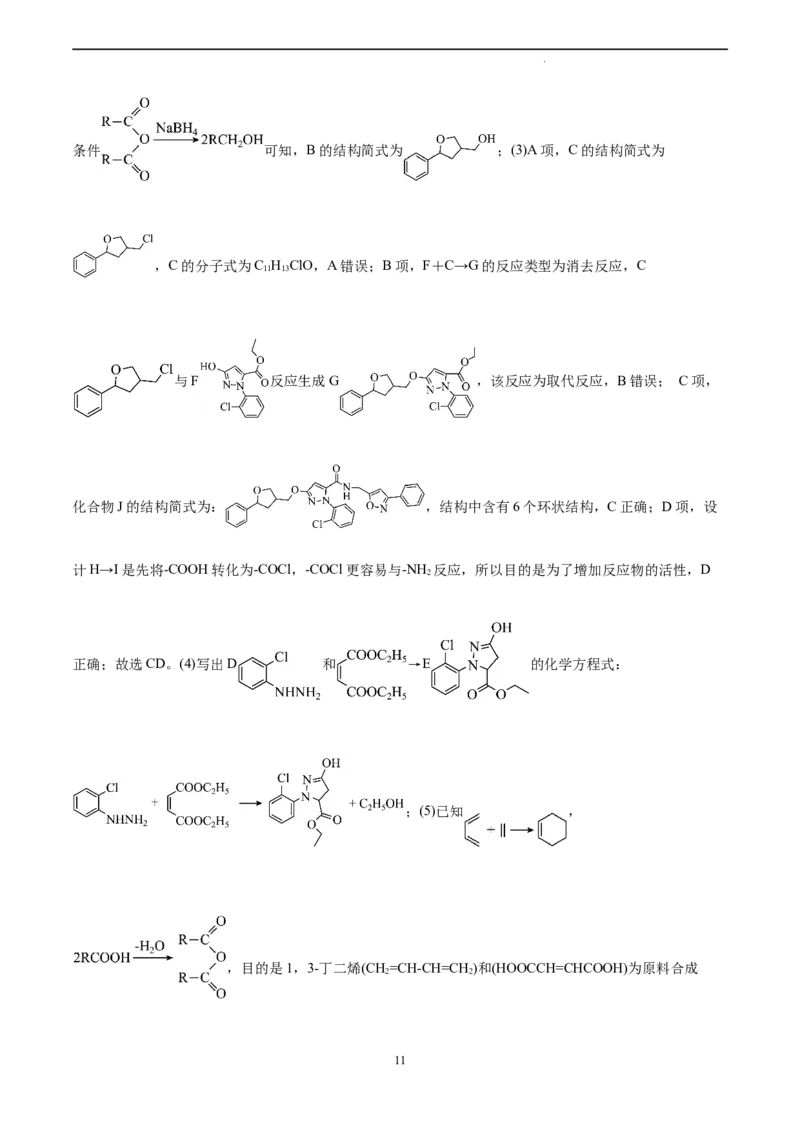
学科网(北京)股份有限公司条件 可知,B的结构简式为 ;(3)A项,C的结构简式为
,C的分子式为C H ClO,A错误;B项,F+C→G的反应类型为消去反应,C
11 13
与F 反应生成G ,该反应为取代反应,B错误; C项,
化合物J的结构简式为: ,结构中含有6个环状结构,C正确;D项,设
计H→I是先将-COOH转化为-COCl,-COCl更容易与-NH 反应,所以目的是为了增加反应物的活性,D
2
正确;故选CD。(4)写出D 和 →E 的化学方程式:
;(5)已知 ,
,目的是1,3-丁二烯(CH=CH-CH=CH )和(HOOCCH=CHCOOH)为原料合成
2 2
11
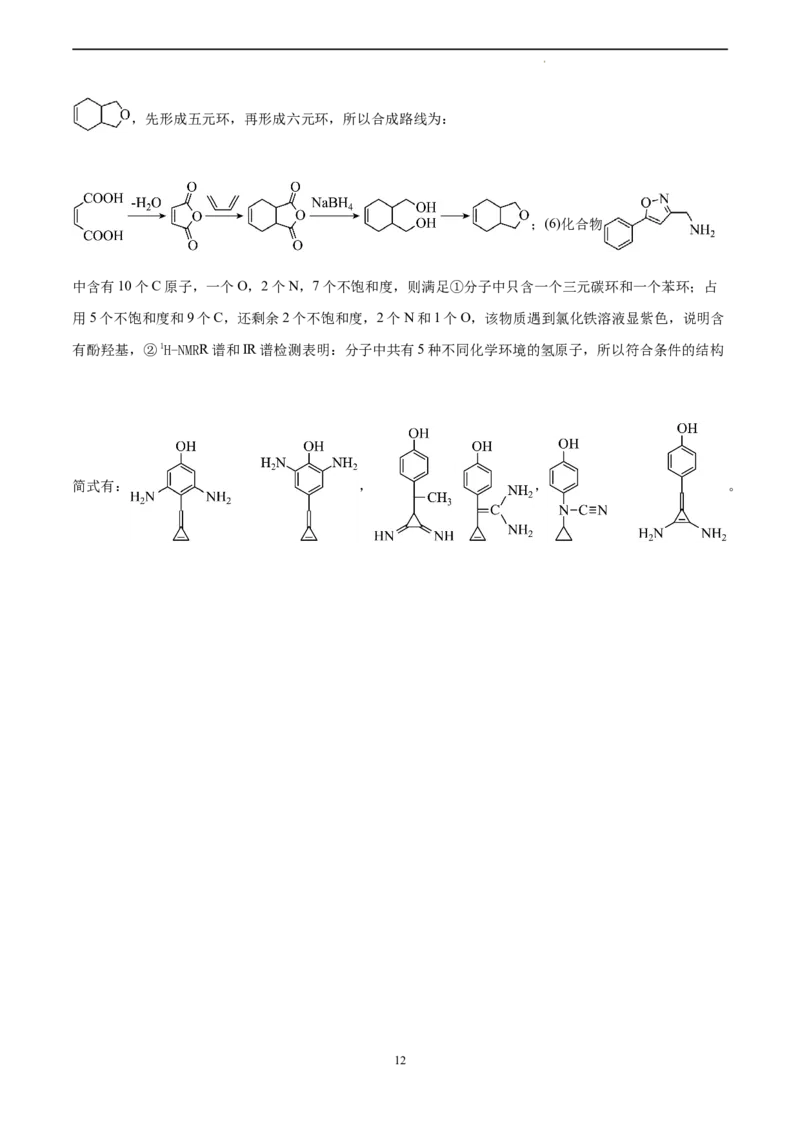
学科网(北京)股份有限公司,先形成五元环,再形成六元环,所以合成路线为:
;(6)化合物
中含有10个C原子,一个O,2个N,7个不饱和度,则满足①分子中只含一个三元碳环和一个苯环;占
用5个不饱和度和9个C,还剩余2个不饱和度,2个N和1个O,该物质遇到氯化铁溶液显紫色,说明含
有酚羟基,②1H-NMRR谱和IR谱检测表明:分子中共有5种不同化学环境的氢原子,所以符合条件的结构
简式有: , , 。
12
学科网(北京)股份有限公司13
学科网(北京)股份有限公司