文档内容
专题82 实验操作与目的一致性
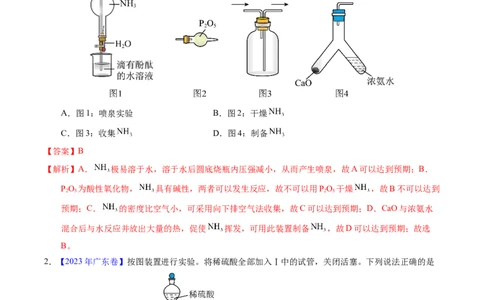
1.【2023年广东卷】1827年,英国科学家法拉第进行了 喷泉实验。在此启发下,兴趣小组利用以下
装置,进行如下实验。其中,难以达到预期目的的是
A.图1:喷泉实验 B.图2:干燥
C.图3:收集 D.图4:制备
【答案】B
【解析】A. 极易溶于水,溶于水后圆底烧瓶内压强减小,从而产生喷泉,故A可以达到预期;B.
PO 为酸性氧化物, 具有碱性,两者可以发生反应,故不可以用PO 干燥 ,故B不可以达到
2 5 2 5
预期;C. 的密度比空气小,可采用向下排空气法收集,故C可以达到预期;D.CaO与浓氨水
混合后与水反应并放出大量的热,促使 挥发,可用此装置制备 ,故D可以达到预期;故选
B。
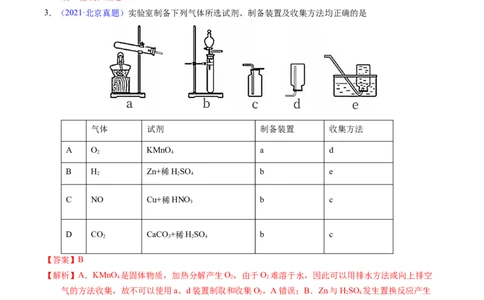
2.【2023年广东卷】按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是
A.Ⅰ中试管内的反应,体现 的氧化性 B.Ⅱ中品红溶液褪色,体现 的还原性
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象 D.撤掉水浴,重做实验,Ⅳ中红色更快褪去【答案】C
【解析】Ⅰ中发生反应 ,二氧化硫进入Ⅱ中使品红溶液褪色,二氧化硫进
入Ⅲ中与硫化钠反应生成S沉淀,二氧化硫进入Ⅳ中与氢氧化钠反应使溶液碱性减弱,酚酞褪色。
A.Ⅰ中试管内发生反应 ,氢元素化合价不变, 不体现氧化性,
故A错误;B.Ⅱ中品红溶液褪色,体现 的漂白性,故B错误;C.Ⅰ试管内发生反应
,Ⅲ试管内发生反应 ,Ⅰ和Ⅲ的试管中
都出现了浑浊现象,故C正确;D.撤掉水浴,重做实验,反应速率减慢,Ⅳ中红色褪去的速率减慢,
故D错误;故选C。
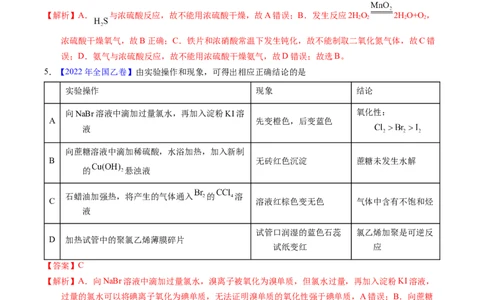
3.(2021·北京真题)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法
A O KMnO a d
2 4
B H Zn+稀HSO b e
2 2 4
C NO Cu+稀HNO b c
3
D CO CaCO +稀HSO b c
2 3 2 4
【答案】B
【解析】A.KMnO 是固体物质,加热分解产生O,由于O 难溶于水,因此可以用排水方法或向上排空
4 2 2
气的方法收集,故不可以使用a、d装置制取和收集O,A错误;B.Zn与HSO 发生置换反应产生
2 2 4
H,块状固体与液体反应制取气体,产生的H 难溶于水,因此可以用排水方法收集,故可以使用装置
2 2
b、e制取H,B正确;C.Cu与稀HNO 反应产生NO气体,NO能够与O 发生反应产生NO 气体,
2 3 2 2
因此不能使用排空气的方法收集,C错误;D.CaCO 与稀硫酸反应产生的CaSO、CO 气体,CaSO
3 4 2 4
微溶于水,使制取CO 气体不能持续发生,因此不能使用该方法制取CO 气体,D错误;故合理选项
2 2
是B。
4.(2021·海南真题)用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是
选项 气体 a bA 稀
B 溶液
C 浓 铁片
D 浓氨水
【答案】B
【解析】A. 与浓硫酸反应,故不能用浓硫酸干燥,故A错误;B.发生反应2HO 2HO+O,
2 2 2 2
浓硫酸干燥氧气,故B正确;C.铁片和浓硝酸常温下发生钝化,故不能制取二氧化氮气体,故C错
误;D.氨气与浓硫酸反应,故不能用浓硫酸干燥氨气,故D错误;故选B。
5.【2022年全国乙卷】由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
向NaBr溶液中滴加过量氯水,再加入淀粉KI溶 氧化性:
A 先变橙色,后变蓝色
液
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制
B 无砖红色沉淀 蔗糖未发生水解
的 悬浊液
石蜡油加强热,将产生的气体通入 的 溶
C 溶液红棕色变无色 气体中含有不饱和烃
液
试管口润湿的蓝色石蕊 氯乙烯加聚是可逆反
D 加热试管中的聚氯乙烯薄膜碎片
试纸变红 应
【答案】C
【解析】A.向NaBr溶液中滴加过量氯水,溴离子被氧化为溴单质,但氯水过量,再加入淀粉KI溶液,
过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错误;B.向蔗糖
溶液中滴加稀硫酸,水浴加热后,应加入氢氧化钠溶液使体系呈碱性,若不加氢氧化钠,未反应的稀
硫酸会和新制氢氧化铜反应,则不会产生砖红色沉淀,不能说明蔗糖没有发生水解,B错误;C.石
蜡油加强热,产生的气体能使溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,与溴发生加成反应
使溴的四氯化碳溶液褪色,C正确;D.聚氯乙烯加强热产生能使湿润蓝色湿润试纸变红的气体,说
明产生了氯化氢,不能说明氯乙烯加聚是可逆反应,可逆反应是指在同一条件下,既能向正反应方向
进行,同时又能向逆反应的方向进行的反应,而氯乙烯加聚和聚氯乙烯加强热分解条件不同,D错误;
答案选C。
6.【2022年山东卷】某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合要求的是
气体 液体 固体粉末
A 饱和 溶液
B 溶液
C
溶液
D
【答案】A
【解析】A.通入CO 气体依次发生反应CO+Na CO+H O=2NaHCO 、CaCO +H O+CO=Ca(HCO ),由
2 2 2 3 2 3 3 2 2 3 2
于在相同温度下NaHCO 的溶解度小于NaCO,最终瓶中仍有白色晶体析出,不会得到澄清溶液,A
3 2 3
项选;B.通入Cl,发生反应Cl+2FeCl =2FeCl 、2FeCl +Fe=3FeCl ,最终Fe消失得到澄清溶液,B
2 2 2 3 3 2
项不选;C.通入HCl, 在酸性条件下会表现强氧化性,发生离子反应:3Cu+8H++2 =3Cu2+
+2NO↑+4H
2
O,最终Cu消失得到澄清溶液,C项不选;D.AgCl在水中存在溶解平衡AgCl(s)⇌Ag+
(aq)+Cl-(aq),通入NH 后,Ag+与NH 结合成[Ag(NH)]+,使溶解平衡正向移动,最终AgCl消失得到
3 3 3 2
澄清溶液,D项不选;答案选A。
7.(2021·全国甲卷真题)实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
【答案】D
【解析】A.氯化铵不稳定,加热易分解生成氨气和氯化氢,但两者遇冷又会化合生成氯化铵固体,所以
不能用于制备氨气,A不可行;B.将铝片加到冷浓硝酸中会发生钝化现象,不能用于制备二氧化氮,
B不可行;C.硫化氢为还原性气体,浓硫酸具有强氧化性,不能用浓硫酸与硫化钠固体反应制备该
硫化氢气体,因为该气体会与浓硫酸发生氧化还原反应,C不可行;D.实验室加热氯酸钾和二氧化
锰的混合物,生成氯化钾和氧气,二氧化锰作催化剂,可用此方法制备氧气,D可行;故选D。
8.(2021·广东真题)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
选项 操作或做法 目的
A 将铜丝插入浓硝酸中 制备B 将密闭烧瓶中的 降温 探究温度对平衡移动的影响
C 将溴水滴入 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余 固体放回原试剂瓶 节约试剂
【答案】B
【解析】A.将铜丝插入浓硝酸中开始会产生二氧化氮,不能达到实验目的,A不符合题意;B.二氧化氮
气体在一定条件下存在平衡: ,正反应为放热反应,NO 为红棕色气体,将密闭烧瓶
2
中NO 降温,会使该平衡向正反应方向移动,气体颜色变浅,因此可达到实验目的,B符合题意;
2
C.乙醇与水互溶,不能作碘单质的萃取剂,做法不正确,C不符合题意;D.一般情况下,剩余试剂
需放到指定的容器中,不能放回原试剂瓶,以防污染原试剂,操作错误,D不符合题意;故选B。
9.(2020·山东高考真题)下列操作不能达到实验目的的是
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的气体直接通入苯酚钠
3
B 证明酸性:碳酸>苯酚
溶液
C 除去碱式滴定管胶管内的气泡 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
配制用于检验醛基的氢氧化铜 向试管中加入2mL10%NaOH溶液,再滴加数滴
D
悬浊液 2%CuSO 溶液,振荡
4
【答案】BC
【解析】A.苯酚可与氢氧化钠溶液反应生成可溶于水的苯酚钠,最后与苯混合后互不相溶,分层,该操
作能达到实验目的,正确;B.盐酸易挥发,若将盐酸与碳酸氢钠溶液混合产生的气体直接通入苯酚
钠,可能挥发的HCl会与苯酚钠反应生成常温下难溶于水的苯酚,不能证明是二氧化碳与其发生的反
应,达不到实验目的,应该先除去二氧化碳中可能挥发的HCl再进行实验操作,错误;C.除去碱式
滴定管胶管内气泡时,尖嘴不应该垂直向下,应向上挤压橡胶管,利用空气排出,该实验操作达不到
实验目的,错误;D.为检验醛基,配制氢氧化铜悬浊液时,碱需过量,保证醛基是在碱性条件下发
生反应,该操作可达到实验目的,正确;答案选BC。
10.(2017·全国高考真题)下列实验操作规范且能达到目的的是
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读数为
A 取20.00 mL盐酸
30.00 mL后,将剩余盐酸放入锥形瓶
B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上配制浓度为0.010 mol·L-1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量瓶中,
4 4
D
溶液 加水溶解并稀释至刻度
【答案】B
【解析】A.50 mL酸式滴定管的50.00 mL刻度下方没有刻度,但仍有盐酸,所以调整初始读数为30.00
mL后,放入锥形瓶中盐酸的体积大于20.00 mL,错误;B.碘易溶于酒精,清洗试管中附着的碘可以
先用酒精清洗,再用水清洗,正确;C.醋酸钠溶液呈碱性,测定醋酸钠溶液的pH时,pH试纸不能
预先湿润(湿润相当于将溶液稀释),否则测定的pH会偏小,错误;D.不能在容量瓶中直接配制溶液,
错误。故答案选B。
11.(2016·全国高考真题)下列实验操作能达到实验目的的是
实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和的FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
D 比较水和乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
【答案】D
【解析】A.将NaOH浓溶液滴加到饱和的FeCl 溶液中生成的是Fe(OH) 沉淀,不能制备Fe(OH) 胶体;
3 3 3
B.将MgCl 溶液加热蒸干时,由于发生生水解且水解产物易挥发或易分解,故不能由MgCl 溶液制
2 2
备无水MgCl ,B不能达到;C.加入稀硝酸溶液, Cu粉及其中混有的CuO全部溶解,不能达到;
2
D.分别将少量钠投入到盛有水和乙醇的烧杯中,可以根据反应的剧烈程度比较水和乙醇中羟基氢的
活泼性,D能达到。故选D。
12.(2016·全国高考真题)下列有关实验的操作正确的是
实验 操作
A 配制稀硫酸 先将浓硫酸加入烧杯中,后倒入蒸馏水
B 排水法收集KMnO 分解产生的O 先熄灭酒精灯,后移出导管
4 2
C 浓盐酸与MnO 反应制备纯净Cl 气体产物先通过浓硫酸,后通过饱和食盐水
2 2
D CCl 萃取碘水中的I 先从分液漏斗下口放出有机层,后从上口倒出水层
4 2
【答案】D
【解析】A、因浓硫酸稀释会发出大量的热,且浓硫酸密度大于水,所以配制稀硫酸时要酸入水,错误;
B、为防止倒吸,排水法收集KMnO 分解产生的O 时,先移出导管,后熄灭酒精灯,错误;C、浓盐
4 2酸与MnO 反应制备纯净Cl,气体产物先通过饱和食盐水,后通过浓硫酸,错误;D、CCl 密度大于
2 2 4
水,CCl 萃取碘水中的I 时,先从分液漏斗下口放出有机层,后从上口倒出水层,正确,答案选D。
4 2
13.(2015·福建高考真题)下列实验操作正确且能达到相应实验目的的是
实验目的 实验操作
先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘
A 称取2.0gNaOH固体
上添加NaOH固体
B 配制FeCl 溶液 将FeCl 固体溶解于适量蒸馏水
3 3
取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色
C 检验溶液中是否含有NH +
4
石蕊试纸检验产生的气体
D 验证铁的吸氧腐蚀 将铁钉放入试管中,用盐酸浸没
【答案】C
【解析】A.氢氧化钠易潮解且具有腐蚀性,不能用滤纸称量,A错误;B.氯化铁易水解而使溶液变浑浊,
应将氯化铁溶于少量盐酸中,再稀释,B错误;C、加热时铵离子与氢氧根反应产生氨气,湿润的红
色石蕊试纸遇氨气变蓝,能达到相应实验目的,C正确;D、在盐酸作用下,铁发生析氢腐蚀,D错
误;故选C。
14.(2016·江苏高考真题)根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
A 室温下,向苯酚钠溶液中通入足量CO,溶液变浑浊。 碳酸的酸性比苯酚的强
2
室温下,向浓度均为0.1 mol·L–1的BaCl 和CaCl 混合溶液中 K (BaSO)<K
2 2 sp 4 sp
B
滴加NaSO 溶液,出现白色沉淀。 (CaSO)
2 4 4
室温下,向FeCl 溶液中滴加少量KI溶液,再滴加几滴淀粉
3
C Fe3+的氧化性比I 的强
2
溶液,溶液变蓝色。
室温下,用pH试纸测得:0.1mol·L–1NaSO 溶液的pH约为 HSO –结合H+的能力比SO 2–
2 3 3 3
D
10;0.1mol·L–1NaHSO 溶液的pH约为5。 的强
3
【答案】AC
【解析】A.室温下,向苯酚钠溶液中通入足量CO,发生反应: + CO+ H O
2 2 2
+ NaHCO ,说明碳酸的酸性比苯酚的强,A正确;B.硫酸钙为微溶物、硫酸钡为难溶物,均能形成
3
白色沉淀,但题给实验无法判断二者的K 大小,B错误;C.室温下,向FeCl 溶液中滴加少量KI溶
sp 3
液,发生反应:2Fe3++2I–=2Fe2++I ,Fe3+的氧化性比I 的强,C正确;D.亚硫酸氢钠溶液显酸性,这
2 2
说明亚硫酸氢根离子的电离程度大于其水解程度,因此题给实验说明HSO –结合H+的能力比SO 2–的
3 3
弱,D错误;答案选AC。15.(2016·全国高考真题)下列实验操作能达到实验目的的是
实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和的FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
D 比较水和乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
【答案】D
【解析】A.将NaOH浓溶液滴加到饱和的FeCl 溶液中生成的是Fe(OH) 沉淀,不能制备Fe(OH) 胶体;
3 3 3
B.将MgCl 溶液加热蒸干时,由于发生生水解且水解产物易挥发或易分解,故不能由MgCl 溶液制
2 2
备无水MgCl ,B不能达到;C.加入稀硝酸溶液, Cu粉及其中混有的CuO全部溶解,不能达到;
2
D.分别将少量钠投入到盛有水和乙醇的烧杯中,可以根据反应的剧烈程度比较水和乙醇中羟基氢的
活泼性,D能达到。故选D。
16.(2020·江苏高考真题)根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加NaOH
2 4
A 淀粉未水解
溶液至中性,再滴加少量碘水,溶液变蓝
室温下,向 HCl溶液中加入少量镁粉,产生大量气
B 镁与盐酸反应放热
泡,测得溶液温度上升
室温下,向浓度均为 的BaCl 和CaCl 混合溶液中
2 2
C 白色沉淀是BaCO
3
加入NaCO 溶液,出现白色沉淀
2 3
向 HO 溶液中滴加 KMnO 溶液,溶液
2 2 4
D HO 具有氧化性
2 2
褪色
【答案】B
【解析】A.加入碘水后,溶液呈蓝色,只能说明溶液中含有淀粉,并不能说明淀粉是否发生了水解反应,
错误;B.加入盐酸后,产生大量气泡,说明镁与盐酸发生化学反应,此时溶液温度上升,可证明镁
与盐酸反应放热,正确;C.BaCl 、CaCl 均能与NaCO 反应,反应产生了白色沉淀,沉淀可能为
2 2 2 3
BaCO 或CaCO 或二者混合物,错误;D.向HO 溶液中加入高锰酸钾后,发生化学反应
3 3 2 2
2KMnO +3H O=2MnO+2KOH+2H O+3O↑等(中性条件),该反应中HO 被氧化,体现出还原性,错
4 2 2 2 2 2 2 2
误;综上所述,故答案为:B。
17.(2020·山东高考真题)下列操作不能达到实验目的的是
目的 操作A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的气体直接通入苯酚钠
3
B 证明酸性:碳酸>苯酚
溶液
C 除去碱式滴定管胶管内的气泡 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
配制用于检验醛基的氢氧化铜 向试管中加入2mL10%NaOH溶液,再滴加数滴
D
悬浊液 2%CuSO 溶液,振荡
4
【答案】BC
【解析】A.苯酚可与氢氧化钠溶液反应生成可溶于水的苯酚钠,最后与苯混合后互不相溶,分层,该操
作能达到实验目的,正确;B.盐酸易挥发,若将盐酸与碳酸氢钠溶液混合产生的气体直接通入苯酚
钠,可能挥发的HCl会与苯酚钠反应生成常温下难溶于水的苯酚,不能证明是二氧化碳与其发生的反
应,达不到实验目的,应该先除去二氧化碳中可能挥发的HCl再进行实验操作,错误;C.除去碱式
滴定管胶管内气泡时,尖嘴不应该垂直向下,应向上挤压橡胶管,利用空气排出,该实验操作达不到
实验目的,错误;D.为检验醛基,配制氢氧化铜悬浊液时,碱需过量,保证醛基是在碱性条件下发
生反应,该操作可达到实验目的,正确;答案选BC。
18.(2019·江苏高考真题)室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向X溶液中滴加几滴新制氯水,振荡,再加入少量
A X溶液中一定含有Fe2+
KSCN溶液,溶液变为红色
向浓度均为0.05 mol·L−1的NaI、NaCl混合溶液中滴
B K (AgI)> K (AgCl)
sp sp
加少量AgNO 溶液,有黄色沉淀生成
3
向3 mL KI溶液中滴加几滴溴水,振荡,再滴加
C Br 的氧化性比I 的强
2 2
1mL淀粉溶液,溶液显蓝色
用pH试纸测得:CHCOONa溶液的pH约为 HNO 电离出H+的能力比
3 2
D
9,NaNO 溶液的pH约为8 CHCOOH的强
2 3
【答案】C
【解析】A.先滴加氯水,再加入KSCN溶液,溶液变红,说明加入KSCN溶液前溶液中存在Fe3+,而此
时的Fe3+是否由Fe2+氧化而来是不能确定的,所以结论中一定含有Fe2+是错误的,错误;B.黄色沉淀
为AgI,说明加入AgNO 溶液优先形成AgI沉淀,AgI比AgCl更难溶,AgI与AgCl属于同种类型,
3
则说明K (AgI)K (AgI)
sp sp
液,有黄色沉淀生成
【答案】B
【解析】A.向苯酚浊液中加入NaCO 溶液,浊液变清,发生反应 +Na CO→ +NaHCO,酸性:
2 3 2 3 3
HCO HCO -,错误;B.向碘水中加入等体积CCl ,振荡后静置,上层接近无色,下层显紫
2 3 3 4
红色,说明CCl 将I 从碘水中萃取出来,I 在CCl 中的溶解度大于在水中的溶解度,正确;C.,向
4 2 2 4
CuSO 溶液中加入铁粉,有红色固体析出,发生的反应为Fe+Cu2+=Fe2++Cu,根据同一反应中氧化性:
4
氧化剂 氧化产物,氧化性Cu2+ Fe2+,错误;D.向NaCl、NaI的混合稀溶液中滴入少量稀AgNO
3
溶液,有黄色沉淀生成,说明先达到AgI的溶度积,但由于NaCl、NaI的浓度未知,不能说明AgCl、
AgI溶度积的大小,错误;答案选B。
20.(2018·全国高考真题)下列实验过程可以达到实验目的的是
编号 实验目的 实验过程
配制0.4000 mol·L−1的 称取4.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,立即转
A
NaOH溶液 移至250 mL容量瓶中定容
向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,
B 探究维生素C的还原性
观察颜色变化
向稀盐酸中加入锌粒,将生成的气体依次通过NaOH溶液、浓硫
C 制取纯净氢气
酸和KMnO 溶液
4
探究浓度对反应速率的影 向2支盛有5 mL不同浓度NaHSO 溶液的试管中同时加入2 mL
3
D
响 5%H O 溶液,观察实验现象
2 2
【答案】B
【解析】A.氢氧化钠溶于水放热,因此溶解后需要冷却到室温下再转移至容量瓶中,A错误;B.氯化铁
具有氧化性,能被维生素C还原为氯化亚铁,从而使溶液颜色发生变化,所以向盛有2 mL黄色氯化
铁溶液的试管中滴加浓的维生素C溶液,通过观察颜色变化可以探究维生素C的还原性,B正确;C.向稀盐酸中加入锌粒,生成氢气,由于生成的氢气中含有氯化氢和水蒸气,因此将生成的气体依
次通过NaOH溶液、浓硫酸即可,不需要通过KMnO 溶液,或者直接通过碱石灰,C错误;D.反应
4
的方程式为HSO -+H O=SO 2-+H++H O,这说明反应过程中没有明显的实验现象,因此无法探究浓
3 2 2 4 2
度对反应速率的影响,D错误。答案选B。
21.(2013·全国高考真题)下列操作不能达到目的的是
选项 目的 操作
A. 配制100 mL 1.0 mol/L CuSO 溶液 将25 g CuSO ·5H O溶于100 mL蒸馏水中
4 4 2
B. 除去KNO 中少量NaCl 将混合物制成热的饱和溶液,冷却结晶,过滤
3
C. 在溶液中将MnO -完全转化为Mn2+ 向酸性KMnO 溶液中滴加HO 溶液至紫色消失
4 4 2 2
D. 确定NaCl溶液中是否混有NaCO 取少量溶液滴加CaCl 溶液,观察是否出现白色浑浊
2 3 2
【答案】A
【解析】A、将25gCuSO ·5H O溶于100 mL蒸馏水中所得溶液的体积不是0.1L,所以不能实现目的,A
4 2
错误;B、硝酸钾和氯化钠的溶解度受温度影响相差大,因此将混合物制成热的饱和溶液,冷却结晶,
过滤即可除去KNO 中少量NaCl,B正确;C、高锰酸钾具有强氧化性,能把双氧水氧化为氧气,而
3
高锰酸钾被还原为锰离子,导致溶液紫色消失,所以能实现目的,C正确;D、NaCl和CaCl 不反应,
2
NaCO 和CaCl 反应生成碳酸钙沉淀,所以可以检验是否含有NaCO,则可以实现目的,D正确;答
2 3 2 2 3
案选A。
22.(2016·全国高考真题)下列实验操作能达到实验目的的是
实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和的FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
D 比较水和乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
【答案】D
【解析】A.将NaOH浓溶液滴加到饱和的FeCl 溶液中生成的是Fe(OH) 沉淀,不能制备Fe(OH) 胶体;
3 3 3
B.将MgCl 溶液加热蒸干时,由于发生生水解且水解产物易挥发或易分解,故不能由MgCl 溶液制
2 2
备无水MgCl ,B不能达到;C.加入稀硝酸溶液, Cu粉及其中混有的CuO全部溶解,不能达到;
2
D.分别将少量钠投入到盛有水和乙醇的烧杯中,可以根据反应的剧烈程度比较水和乙醇中羟基氢的
活泼性,D能达到。故选D。
23.(2014·安徽高考真题)为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
选项 实验目的 主要仪器 试剂A 分离Br 和CCl 混合物 分液漏斗、烧杯 Br 和CCl 混合物、蒸馏水
2 4 2 4
B 鉴别葡萄糖和蔗糖 试管、烧杯、酒精灯 葡萄糖溶液、蔗糖溶液、银氨溶液
C 实验室制取H 试管、带导管的橡皮塞 锌粒、稀HNO
2 3
D 测定NaOH溶液浓度 滴定管、锥形瓶、烧杯 NaOH溶液,0.1000mol/L盐酸
【答案】B
【解析】A、溴易溶于四氯化碳,无法用分液的方法分离,应该用蒸馏的方法,错误;B、葡萄糖中含醛基,
而蔗糖中没有,所以可以用银氨溶液检验醛基的存在,正确;C、硝酸具有强氧化性,和锌反应不生
成氢气,错误;D、滴定实验中需要指示剂,而所给的试剂中没有,错误。答案选B。
24.(2010·江苏高考真题)下列实验操作与预期实验目的或所得实验结论一致的是
选项 实验操作 实验目的或结论
某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色
A 说明该钾盐是KCO
2 3
无味气体
向含有少量FeCl 的MgCl 溶液中加入足量Mg(OH)
3 2 2
B 除去MgCl 溶液中少量FeCl
2 3
粉末,搅拌一段时间后过滤
常温下,向饱和NaCO 溶液中加少量BaSO 粉末, 说明常温下,K (BaCO)<
2 3 4 sp 3
C
过滤,向洗净的沉淀中加稀盐酸,有气泡产生 K (BaSO)
sp 4
C HOH与浓硫酸170℃共热,制得的气体通入酸性
2 5
D 检验制得的气体是否含有乙烯
KMnO 溶液
4
【答案】B
【解析】A.向某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水,石灰水变浑浊,气体
为二氧化碳,则为碳酸盐或碳酸氢盐溶液,错误;B.向含有少量FeCl 的MgCl 溶液中加入足量Mg
3 2
(OH) 粉末,搅拌一段时间后过滤,促进铁离子的水解,使其转化为沉淀,达到除杂的目的,正确;
2
C.洗净的沉淀中加稀盐酸,有气泡产生,不一定能说明Ksp(BaCO )<Ksp(BaSO),能否形成
3 4
沉淀与溶液中的离子浓度有关,当c(Ba2+)×c(CO2-)>Ksp(BaCO )就能析出沉淀,错误;D.
3 3
C2H5OH与浓硫酸170℃共热,发生消去反应生成乙烯,但乙醇易挥发,也具有还原性,均使高锰酸
钾褪色,应利用溴水检验产物,错误。答案选B。
25.(2016·江苏高考真题)根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
A 室温下,向苯酚钠溶液中通入足量CO,溶液变浑浊。 碳酸的酸性比苯酚的强
2
室温下,向浓度均为0.1 mol·L–1的BaCl 和CaCl 混合溶液中 K (BaSO)<K
2 2 sp 4 sp
B
滴加NaSO 溶液,出现白色沉淀。 (CaSO)
2 4 4室温下,向FeCl 溶液中滴加少量KI溶液,再滴加几滴淀粉
3
C Fe3+的氧化性比I 的强
2
溶液,溶液变蓝色。
室温下,用pH试纸测得:0.1mol·L–1NaSO 溶液的pH约为 HSO –结合H+的能力比SO 2–
2 3 3 3
D
10;0.1mol·L–1NaHSO 溶液的pH约为5。 的强
3
【答案】AC
【解析】A.室温下,向苯酚钠溶液中通入足量CO,发生反应: + CO+ H O
2 2 2
+ NaHCO ,说明碳酸的酸性比苯酚的强,A正确;B.硫酸钙为微溶物、硫酸钡为难溶物,均能形成
3
白色沉淀,但题给实验无法判断二者的K 大小,B错误;C.室温下,向FeCl 溶液中滴加少量KI溶
sp 3
液,发生反应:2Fe3++2I–=2Fe2++I ,Fe3+的氧化性比I 的强,C正确;D.亚硫酸氢钠溶液显酸性,这
2 2
说明亚硫酸氢根离子的电离程度大于其水解程度,因此题给实验说明HSO –结合H+的能力比SO 2–的
3 3
弱,D错误;答案选AC。
26.(2007·广东高考真题)下述实验能达到预期目的的是
编号 实验内容 实验目的
A 将SO 通入酸性KMnO 溶液中 证明SO 具有氧化性
2 4 2
B 将Cl 通入NaBr溶液中 比较氯与溴的氧化性强弱
2
将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却
C 研究温度对化学平衡的影响
降温
分别向2支试管中加入相同体积不同浓度的HO 溶液,
2 2
D 研究催化剂对HO 分解速率的影响
2 2
再向其中1支加入少量MnO
2
【答案】BC
【解析】A.KMnO 具有强氧化性,SO 通入酸性KMnO 溶液中,紫色褪去,说明SO 具有还原性,A错
4 2 4 2
误;B.Cl 通入NaBr溶液中,溶液显橙色,说明生成了Br ,说明Cl 的氧化性大于Br 的,B正确;
2 2 2 2
C.铜与浓硝酸反应生成的气体为NO ,因为2NO (g,红棕色) NO(g,无色) ΔH<0,改
2 2 2 4
变温度,平衡移动,混合气体的颜色改变,C正确;D.研究外界因素对反应速率的影响时,必须只
改变一个变量,保持其他条件不变,选项中有两个变量:浓度和催化剂,故无法研究催化剂对速率的
影响,D错误;答案选BC。