文档内容
专题92 定量分析综合实验
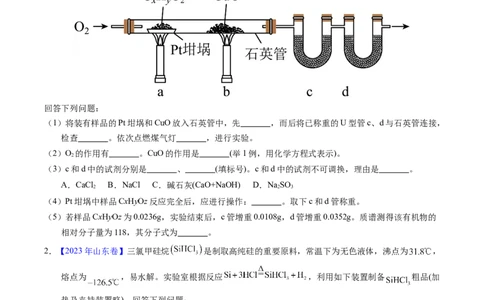
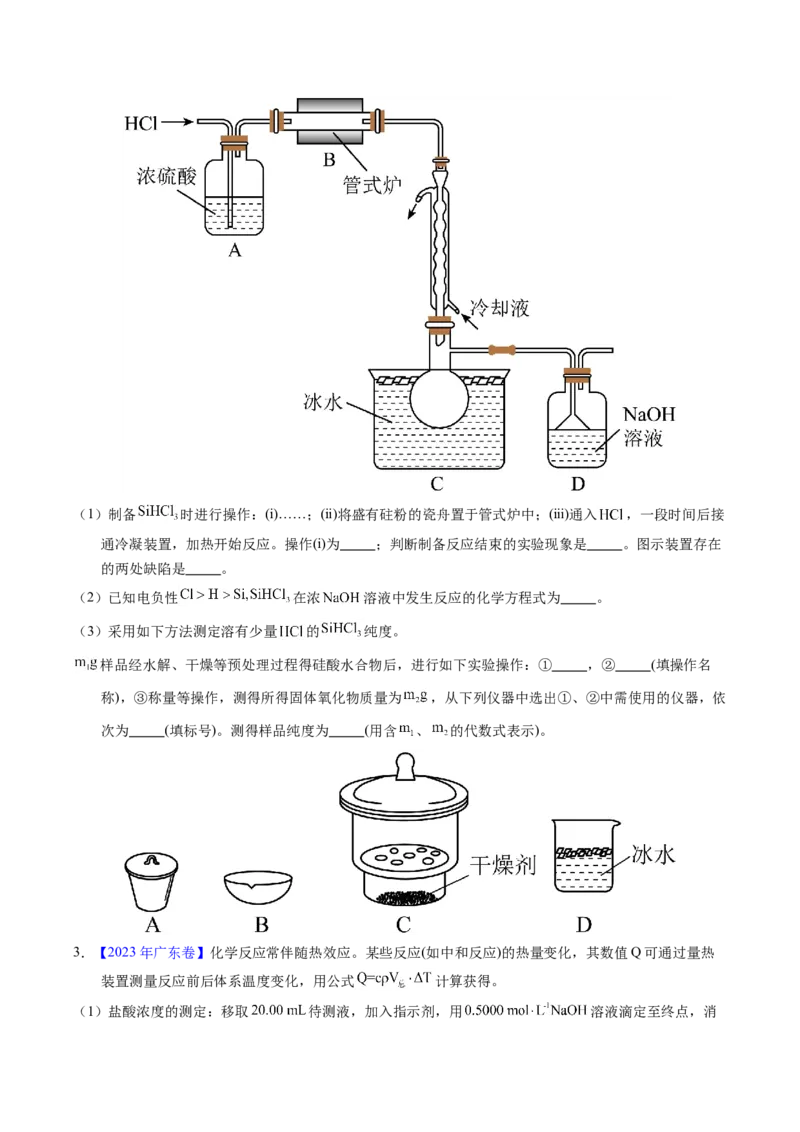
1.【2023年全国乙卷】元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化合
物进行C、H元素分析。
回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先 ,而后将已称重的U型管c、d与石英管连接,
检查 。依次点燃煤气灯 ,进行实验。
(2)O 的作用有 。CuO的作用是 (举1例,用化学方程式表示)。
2
(3)c和d中的试剂分别是 、 (填标号)。c和d中的试剂不可调换,理由是 。
A.CaCl B.NaCl C.碱石灰(CaO+NaOH) D.NaSO
2 2 3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作: 。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的
相对分子量为118,其分子式为 。
2.【2023年山东卷】三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,
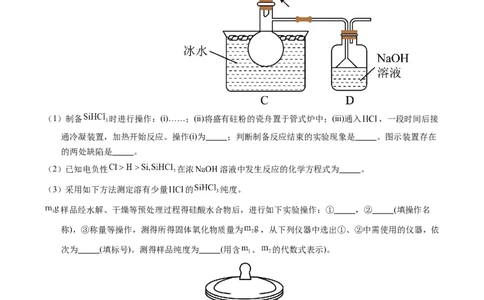
熔点为 ,易水解。实验室根据反应 ,利用如下装置制备 粗品(加
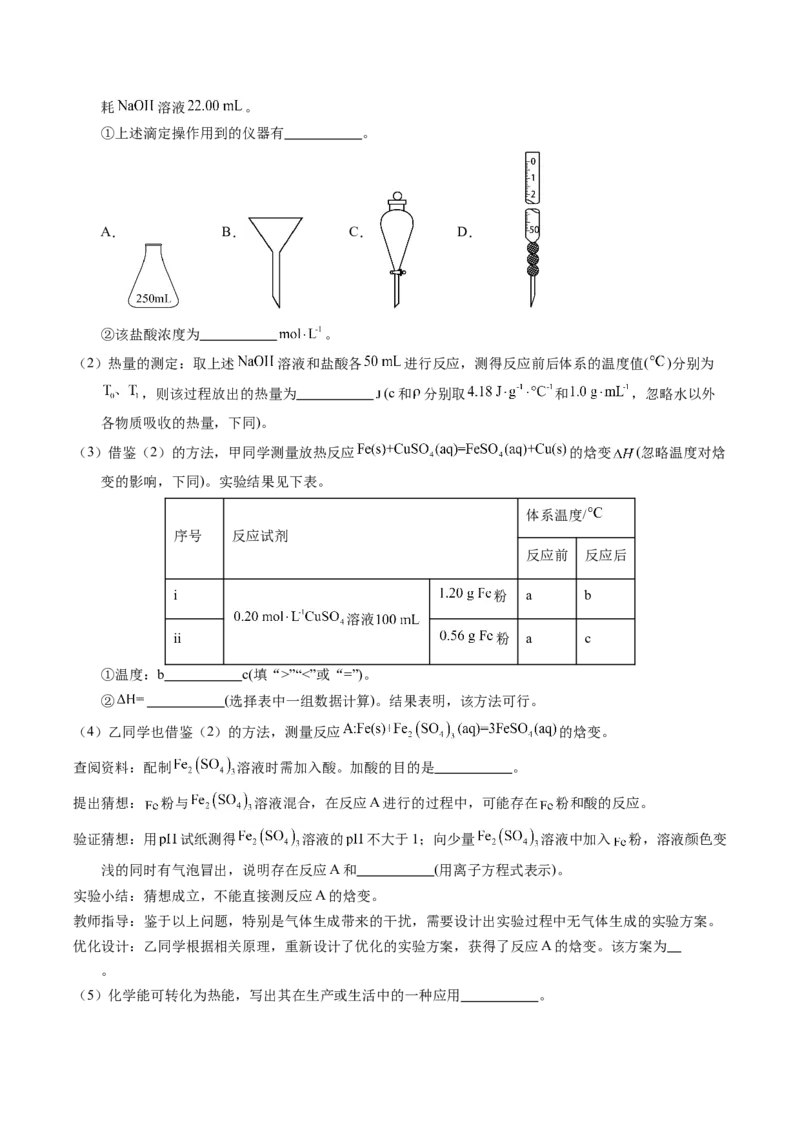
热及夹持装置略)。回答下列问题:(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接
通冷凝装置,加热开始反应。操作(ⅰ)为 ;判断制备反应结束的实验现象是 。图示装置存在
的两处缺陷是 。
(2)已知电负性 在浓 溶液中发生反应的化学方程式为 。
(3)采用如下方法测定溶有少量 的 纯度。
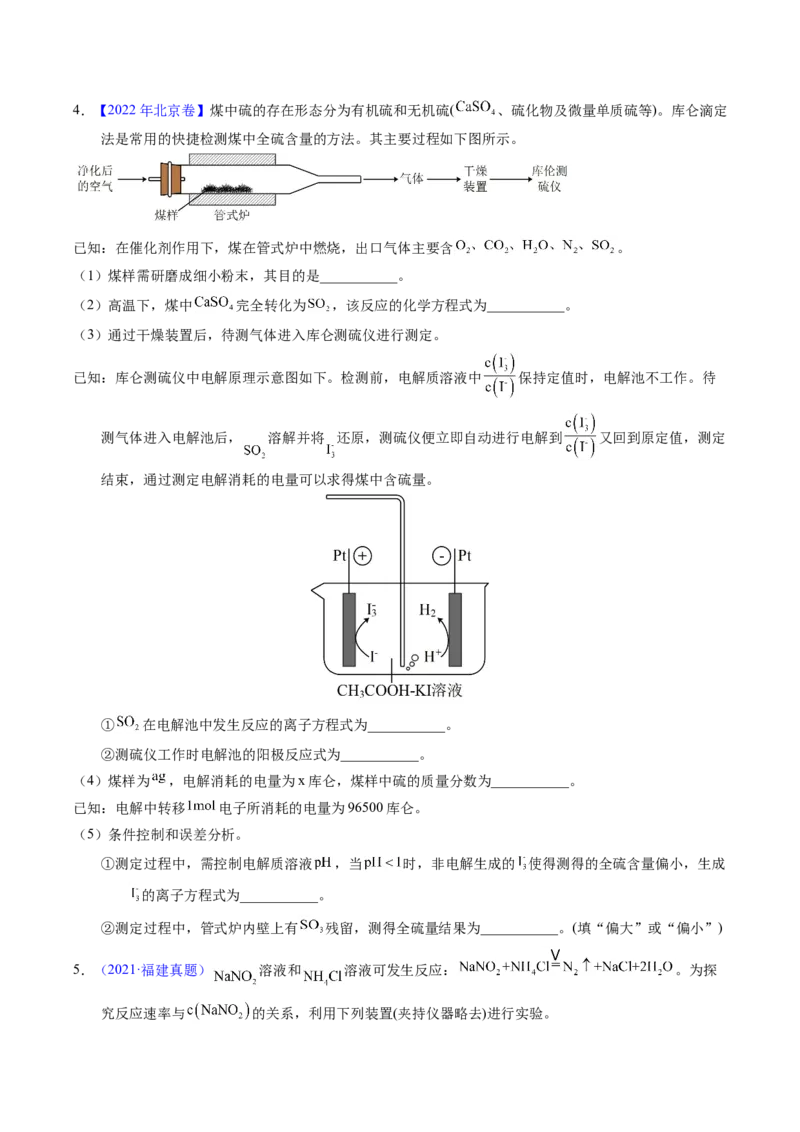
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,② (填操作名
称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依
次为 (填标号)。测得样品纯度为 (用含 、 的代数式表示)。
3.【2023年广东卷】化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热
装置测量反应前后体系温度变化,用公式 计算获得。
(1)盐酸浓度的测定:移取 待测液,加入指示剂,用 溶液滴定至终点,消耗 溶液 。
①上述滴定操作用到的仪器有 。
A. B. C. D.
②该盐酸浓度为 。
(2)热量的测定:取上述 溶液和盐酸各 进行反应,测得反应前后体系的温度值( )分别为
,则该过程放出的热量为 (c和 分别取 和 ,忽略水以外
各物质吸收的热量,下同)。
(3)借鉴(2)的方法,甲同学测量放热反应 的焓变 (忽略温度对焓
变的影响,下同)。实验结果见下表。
体系温度/
序号 反应试剂
反应前 反应后
i 粉 a b
溶液
ii 粉 a c
①温度:b c(填“>”“<”或“=”)。
② (选择表中一组数据计算)。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应 的焓变。
查阅资料:配制 溶液时需加入酸。加酸的目的是 。
提出猜想: 粉与 溶液混合,在反应A进行的过程中,可能存在 粉和酸的反应。
验证猜想:用 试纸测得 溶液的 不大于1;向少量 溶液中加入 粉,溶液颜色变
浅的同时有气泡冒出,说明存在反应A和 (用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为
。
(5)化学能可转化为热能,写出其在生产或生活中的一种应用 。4.【2022年北京卷】煤中硫的存在形态分为有机硫和无机硫( 、硫化物及微量单质硫等)。库仑滴定
法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。
已知:在催化剂作用下,煤在管式炉中燃烧,出口气体主要含 。
(1)煤样需研磨成细小粉末,其目的是___________。
(2)高温下,煤中 完全转化为 ,该反应的化学方程式为___________。
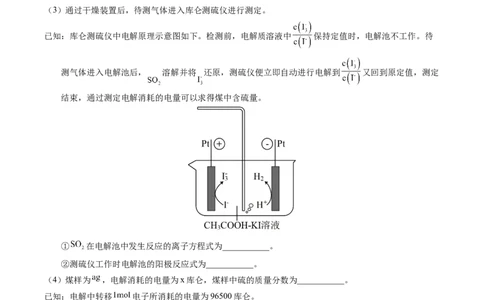
(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。待
测气体进入电解池后, 溶解并将 还原,测硫仪便立即自动进行电解到 又回到原定值,测定
结束,通过测定电解消耗的电量可以求得煤中含硫量。
① 在电解池中发生反应的离子方程式为___________。
②测硫仪工作时电解池的阳极反应式为___________。
(4)煤样为 ,电解消耗的电量为x库仑,煤样中硫的质量分数为___________。
已知:电解中转移 电子所消耗的电量为96500库仑。
(5)条件控制和误差分析。
①测定过程中,需控制电解质溶液 ,当 时,非电解生成的 使得测得的全硫含量偏小,生成
的离子方程式为___________。
②测定过程中,管式炉内壁上有 残留,测得全硫量结果为___________。(填“偏大”或“偏小”)
5.(2021·福建真题) 溶液和 溶液可发生反应: 。为探
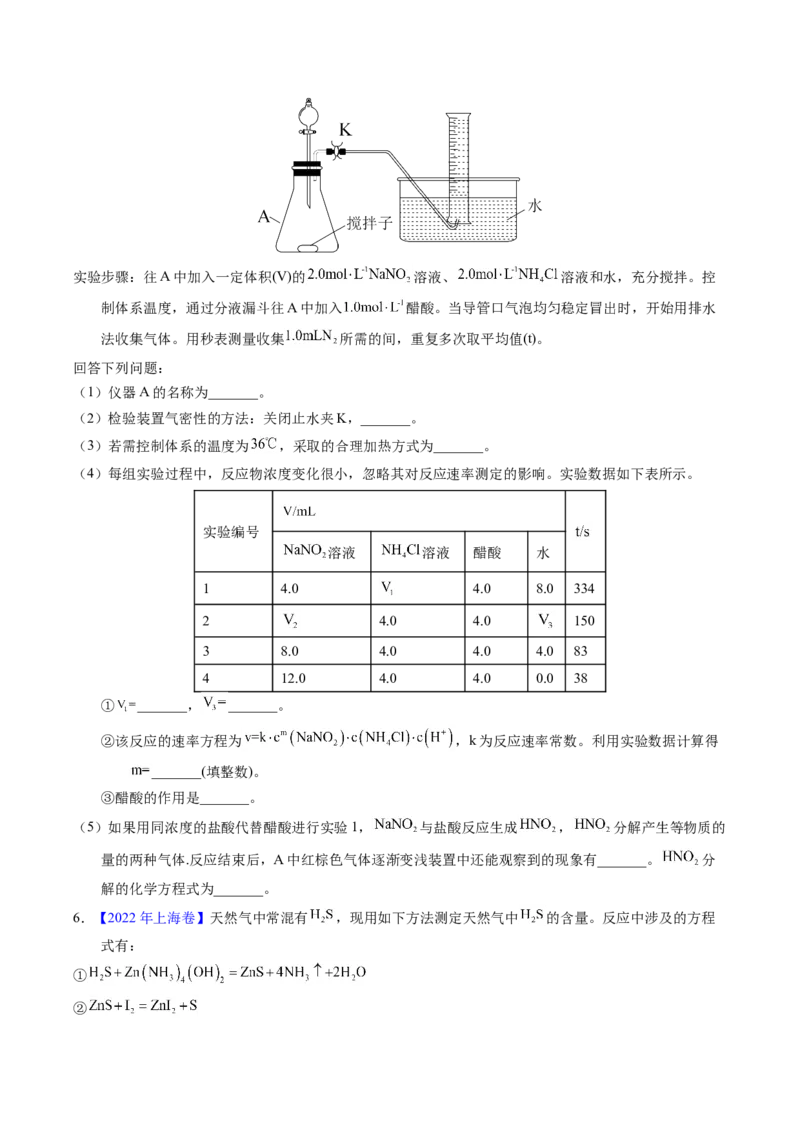
究反应速率与 的关系,利用下列装置(夹持仪器略去)进行实验。实验步骤:往A中加入一定体积(V)的 溶液、 溶液和水,充分搅拌。控
制体系温度,通过分液漏斗往A中加入 醋酸。当导管口气泡均匀稳定冒出时,开始用排水
法收集气体。用秒表测量收集 所需的间,重复多次取平均值(t)。
回答下列问题:
(1)仪器A的名称为_______。
(2)检验装置气密性的方法:关闭止水夹K,_______。
(3)若需控制体系的温度为 ,采取的合理加热方式为_______。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
实验编号
溶液 溶液 醋酸 水
1 4.0 4.0 8.0 334
2 4.0 4.0 150
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
① _______, _______。
②该反应的速率方程为 ,k为反应速率常数。利用实验数据计算得
_______(填整数)。
③醋酸的作用是_______。
(5)如果用同浓度的盐酸代替醋酸进行实验1, 与盐酸反应生成 , 分解产生等物质的
量的两种气体.反应结束后,A中红棕色气体逐渐变浅装置中还能观察到的现象有_______。 分
解的化学方程式为_______。
6.【2022年上海卷】天然气中常混有 ,现用如下方法测定天然气中 的含量。反应中涉及的方程
式有:
①
②③
(1)反应①中, 体现_______(选填“酸性”“氧化性”或“还原性”)。
采用以下方法测定 的含量。
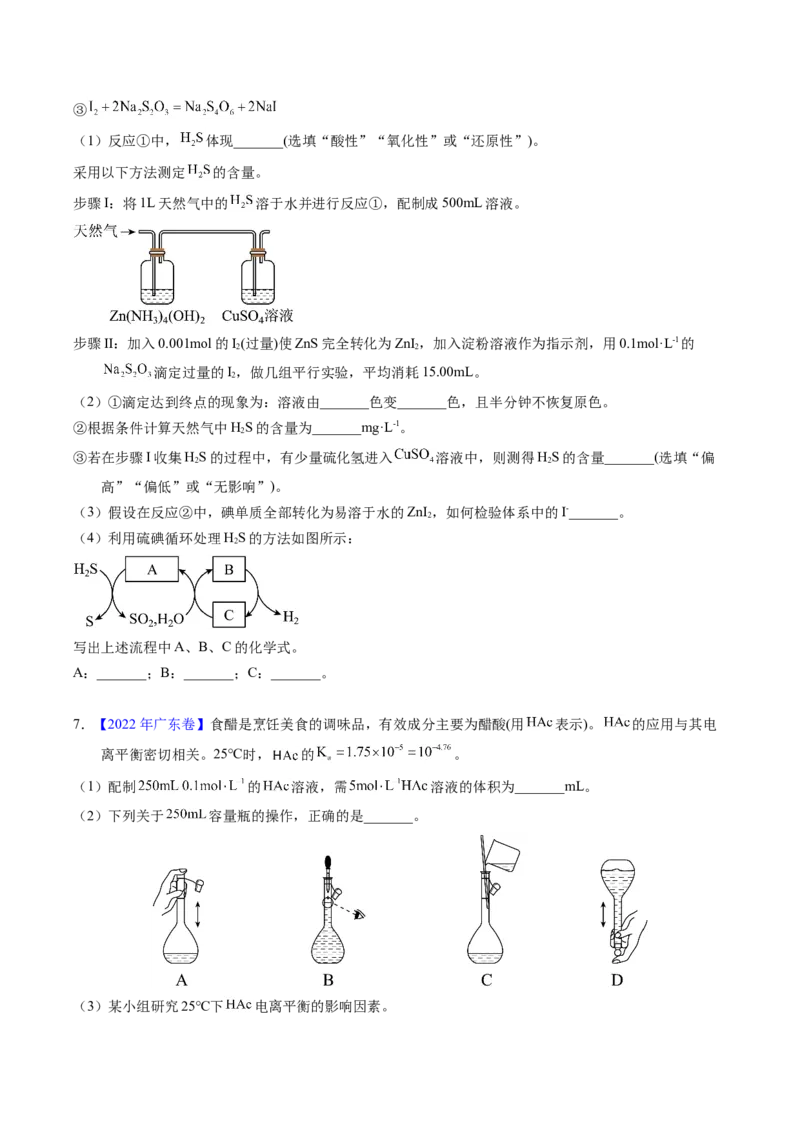
步骤I:将1L天然气中的 溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I(过量)使ZnS完全转化为ZnI,加入淀粉溶液作为指示剂,用0.1mol·L-1的
2 2
滴定过量的I,做几组平行实验,平均消耗15.00mL。
2
(2)①滴定达到终点的现象为:溶液由_______色变_______色,且半分钟不恢复原色。
②根据条件计算天然气中HS的含量为_______mg·L-1。
2
③若在步骤I收集HS的过程中,有少量硫化氢进入 溶液中,则测得HS的含量_______(选填“偏
2 2
高”“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI,如何检验体系中的I-_______。
2
(4)利用硫碘循环处理HS的方法如图所示:
2
写出上述流程中A、B、C的化学式。
A:_______;B:_______;C:_______。
7.【2022年广东卷】食醋是烹饪美食的调味品,有效成分主要为醋酸(用 表示)。 的应用与其电
离平衡密切相关。25℃时, 的 。
(1)配制 的 溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。
(3)某小组研究25℃下 电离平衡的影响因素。提出假设。稀释 溶液或改变 浓度, 电离平衡会发生移动。设计方案并完成实验用浓度均为
的 和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序号
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
①根据表中信息,补充数据: _______, _______。
②由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
③由实验Ⅱ~VIII可知,增大 浓度, 电离平衡逆向移动。
实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加, 的值逐渐接近 的 。
查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于 的 。
对比数据发现,实验VIII中 与资料数据 存在一定差异;推测可能由物质浓度准确程度
不够引起,故先准确测定 溶液的浓度再验证。
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
,则该 溶液的浓度为_______ 。在答题卡虚线框中,画出上述过程的滴定曲线示
意图并标注滴定终点_______。
②用上述 溶液和 溶液,配制等物质的量的 与 混合溶液,测定pH,结果
与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的 ?
小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
Ⅰ 移取 溶液,用 溶液滴定至终点,消耗 溶液
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。(6)根据 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
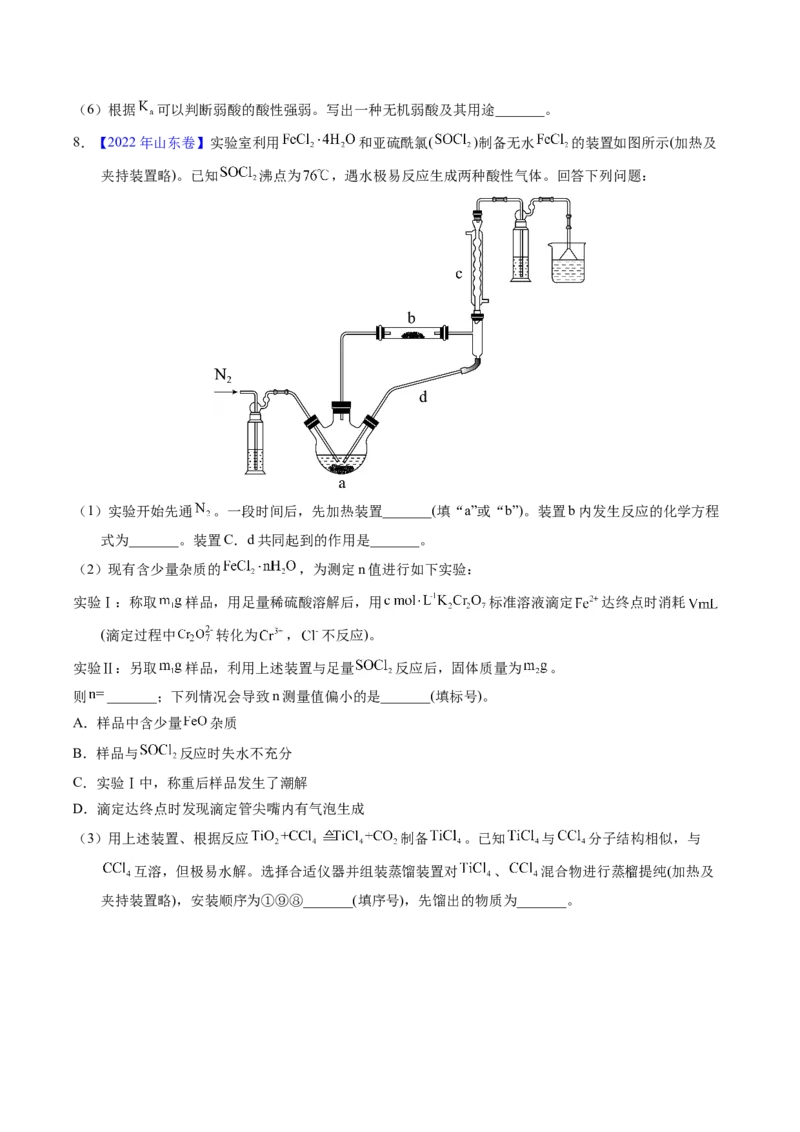
8.【2022年山东卷】实验室利用 和亚硫酰氯( )制备无水 的装置如图所示(加热及
夹持装置略)。已知 沸点为 ,遇水极易反应生成两种酸性气体。回答下列问题:
(1)实验开始先通 。一段时间后,先加热装置_______(填“a”或“b”)。装置b内发生反应的化学方程
式为_______。装置C.d共同起到的作用是_______。
(2)现有含少量杂质的 ,为测定n值进行如下实验:
实验Ⅰ:称取 样品,用足量稀硫酸溶解后,用 标准溶液滴定 达终点时消耗
(滴定过程中 转化为 , 不反应)。
实验Ⅱ:另取 样品,利用上述装置与足量 反应后,固体质量为 。
则 _______;下列情况会导致n测量值偏小的是_______(填标号)。
A.样品中含少量 杂质
B.样品与 反应时失水不充分
C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
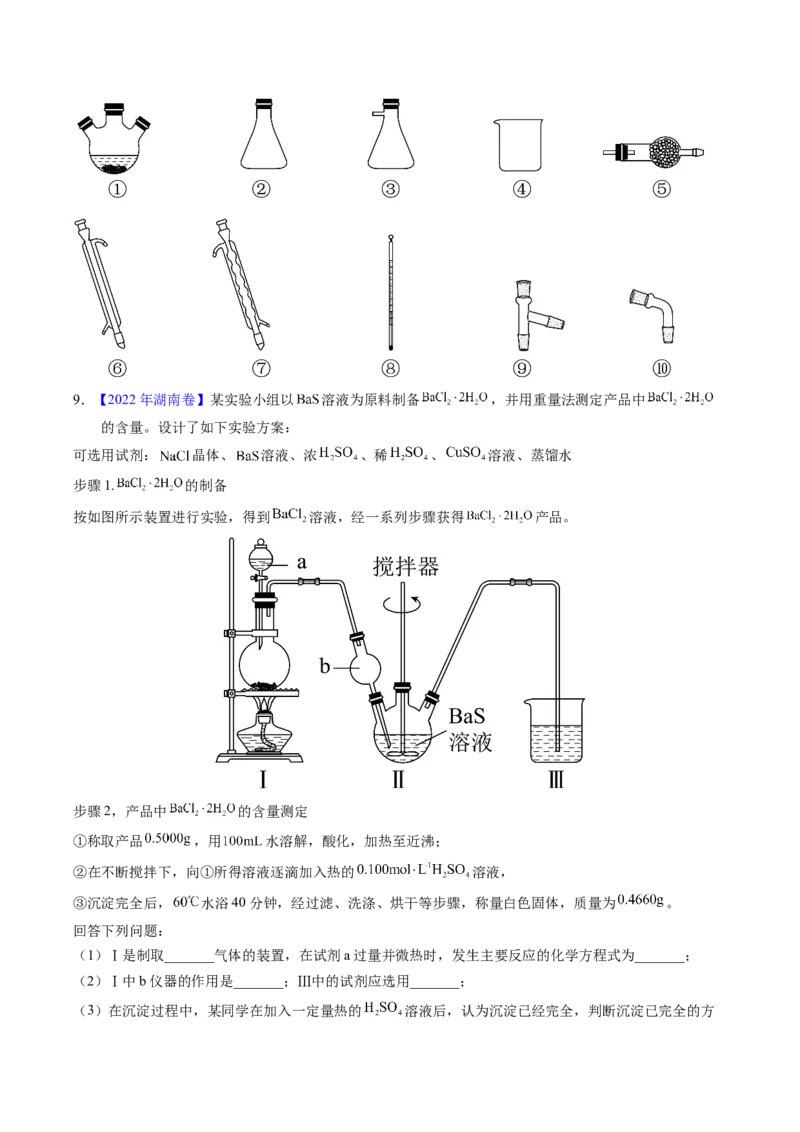
(3)用上述装置、根据反应 制备 。已知 与 分子结构相似,与
互溶,但极易水解。选择合适仪器并组装蒸馏装置对 、 混合物进行蒸榴提纯(加热及
夹持装置略),安装顺序为①⑨⑧_______(填序号),先馏出的物质为_______。9.【2022年湖南卷】某实验小组以 溶液为原料制备 ,并用重量法测定产品中
的含量。设计了如下实验方案:
可选用试剂: 晶体、 溶液、浓 、稀 、 溶液、蒸馏水
步骤1. 的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得 产品。
步骤2,产品中 的含量测定
①称取产品 ,用 水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的 溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为 。
回答下列问题:
(1)Ⅰ是制取_______气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为_______;
(2)Ⅰ中b仪器的作用是_______;Ⅲ中的试剂应选用_______;
(3)在沉淀过程中,某同学在加入一定量热的 溶液后,认为沉淀已经完全,判断沉淀已完全的方法是_______;
(4)沉淀过程中需加入过量的 溶液,原因是_______;
(5)在过滤操作中,下列仪器不需要用到的是_______(填名称);
(6)产品中 的质量分数为_______(保留三位有效数字)。
10.【2022年河北卷】某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下:
①三颈烧瓶中加入 香菇样品和 水;锥形瓶中加入 水、 淀粉溶液,并预加
的碘标准溶液,搅拌。
②以 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时
滴定消耗了 碘标准溶液。
③做空白实验,消耗了 碘标准溶液。
④用适量 替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
已知: ,
回答下列问题:
(1)装置图中仪器A.b的名称分别为_______、_______。
(2)三颈烧瓶适宜的规格为_______(填标号)。
A. B. C.
(3)解释加入 ,能够生成 的原因:_______。
(4)滴定管在使用前需要_______、洗涤、润洗;滴定终点时溶液的颜色为_______;滴定反应的离子方
程式为_______。
(5)若先加磷酸再通氮气,会使测定结果_______(填“偏高”“偏低”或“无影响”)。
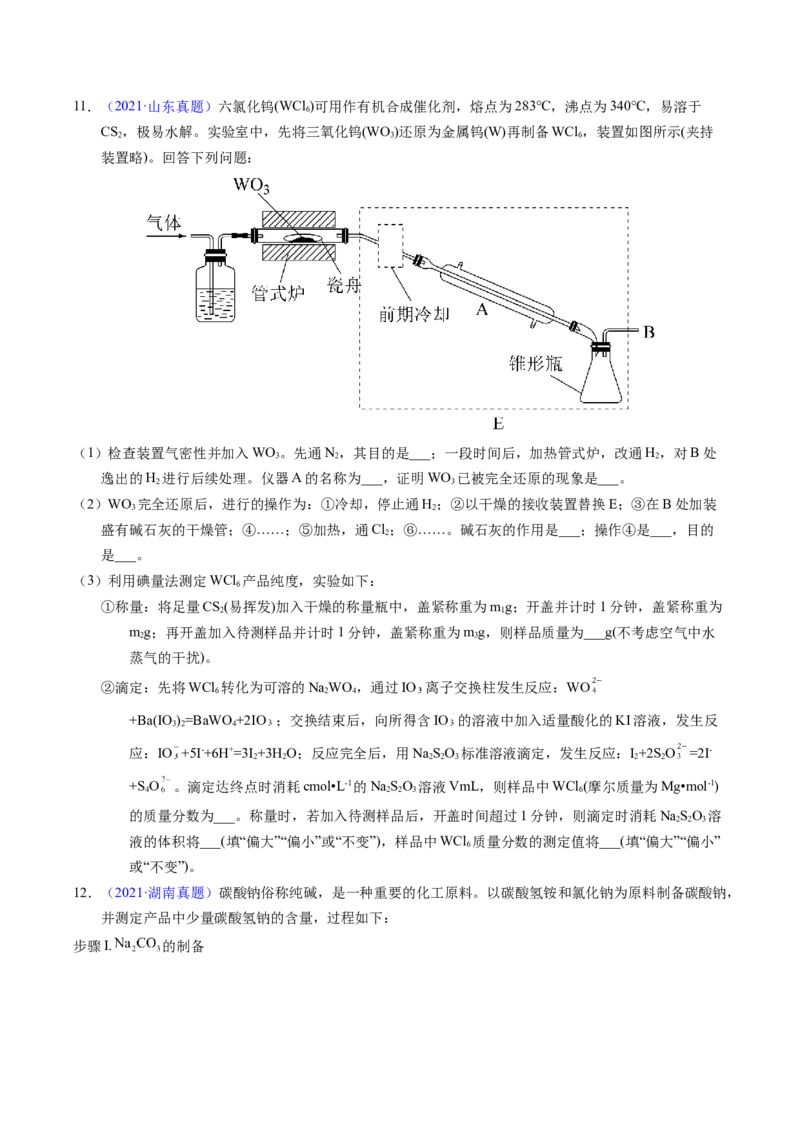
(6)该样品中亚硫酸盐含量为_______ (以 计,结果保留三位有效数字)。11.(2021·山东真题)六氯化钨(WCl )可用作有机合成催化剂,熔点为283℃,沸点为340℃,易溶于
6
CS,极易水解。实验室中,先将三氧化钨(WO)还原为金属钨(W)再制备WCl,装置如图所示(夹持
2 3 6
装置略)。回答下列问题:
(1)检查装置气密性并加入WO。先通N,其目的是___;一段时间后,加热管式炉,改通H,对B处
3 2 2
逸出的H 进行后续处理。仪器A的名称为___,证明WO 已被完全还原的现象是___。
2 3
(2)WO 完全还原后,进行的操作为:①冷却,停止通H;②以干燥的接收装置替换E;③在B处加装
3 2
盛有碱石灰的干燥管;④……;⑤加热,通Cl;⑥……。碱石灰的作用是___;操作④是___,目的
2
是___。
(3)利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为mg;开盖并计时1分钟,盖紧称重为
2 1
mg;再开盖加入待测样品并计时1分钟,盖紧称重为mg,则样品质量为___g(不考虑空气中水
2 3
蒸气的干扰)。
②滴定:先将WCl 转化为可溶的NaWO,通过IO 离子交换柱发生反应:WO
6 2 4
+Ba(IO )=BaWO +2IO ;交换结束后,向所得含IO 的溶液中加入适量酸化的KI溶液,发生反
3 2 4
应:IO +5I-+6H+=3I +3H O;反应完全后,用NaSO 标准溶液滴定,发生反应:I+2S O =2I-
2 2 2 2 3 2 2
+S O 。滴定达终点时消耗cmol•L-1的NaSO 溶液VmL,则样品中WCl(摩尔质量为Mg•mol-1)
4 2 2 3 6
的质量分数为___。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗NaSO 溶
2 2 3
液的体积将___(填“偏大”“偏小”或“不变”),样品中WCl 质量分数的测定值将___(填“偏大”“偏小”
6
或“不变”)。
12.(2021·湖南真题)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,
并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. 的制备步骤Ⅱ.产品中 含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液由红色
变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸 ;
④平行测定三次, 平均值为22.45, 平均值为23.51。
已知:(i)当温度超过35℃时, 开始分解。
(ii)相关盐在不同温度下的溶解度表
温度/ 0 10 20 30 40 50 60
35.7 35.8 36.0 36.3 36.6 37.0 37.3
11.9 15.8 21.0 27.0
6.9 8.2 9.6 11.1 12.7 14.5 16.4
29.4 33.3 37.2 41.4 45.8 50.4 55.2
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是_______;
(2)步骤I中“300℃加热”所选用的仪器是_______(填标号);
A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化_______;
(4)产品中 的质量分数为_______(保留三位有效数字);
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 质量分数的计算结果_______(填
“偏大”“偏小”或“无影响”)。
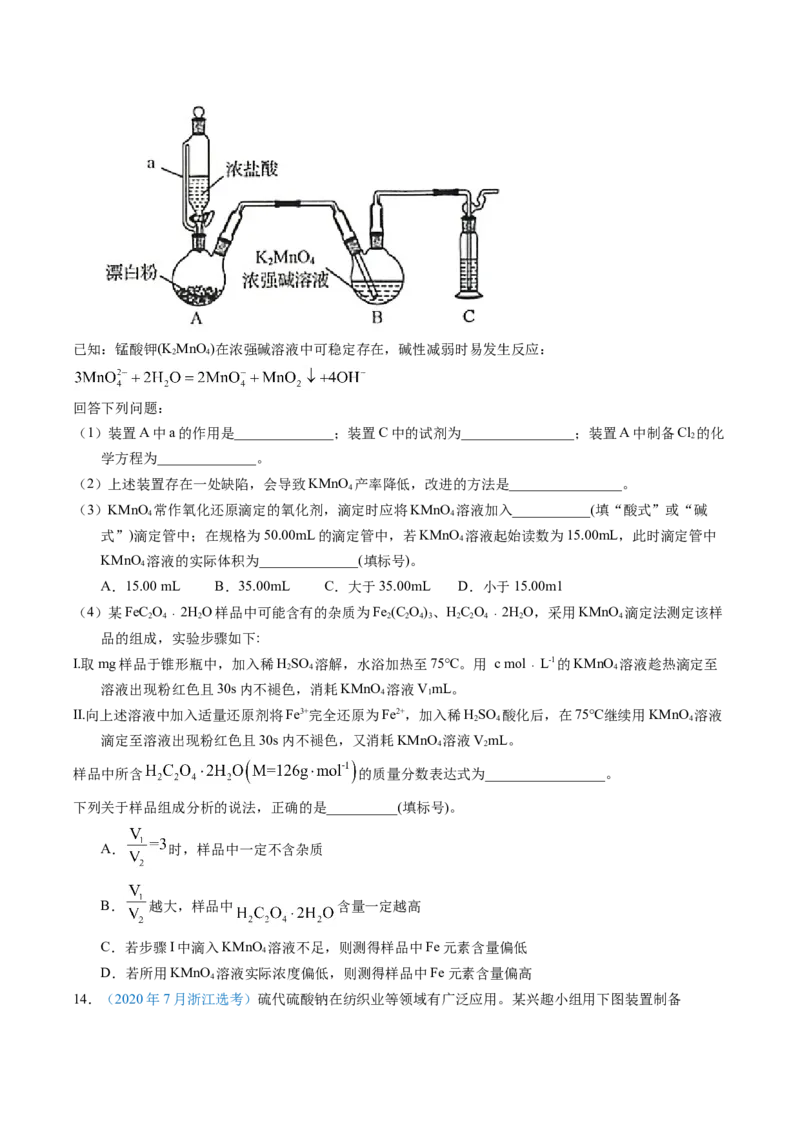
13.(2020年山东新高考)某同学利用Cl 氧化KMnO 制备KMnO 的装置如下图所示(夹持装置略):
2 2 4 4已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
回答下列问题:
(1)装置A中a的作用是______________;装置C中的试剂为________________;装置A中制备Cl 的化
2
学方程为______________。
(2)上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是________________。
4
(3)KMnO 常作氧化还原滴定的氧化剂,滴定时应将KMnO 溶液加入___________(填“酸式”或“碱
4 4
式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO 溶液起始读数为15.00mL,此时滴定管中
4
KMnO 溶液的实际体积为______________(填标号)。
4
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00m1
(4)某FeC O﹒2HO样品中可能含有的杂质为Fe (C O)、HC O﹒2HO,采用KMnO 滴定法测定该样
2 4 2 2 2 4 3 2 2 4 2 4
品的组成,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀HSO 溶解,水浴加热至75℃。用 c mol﹒L-1的KMnO 溶液趁热滴定至
2 4 4
溶液出现粉红色且30s内不褪色,消耗KMnO 溶液VmL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀HSO 酸化后,在75℃继续用KMnO 溶液
2 4 4
滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO 溶液VmL。
4 2
样品中所含 的质量分数表达式为_________________。
下列关于样品组成分析的说法,正确的是__________(填标号)。
A. 时,样品中一定不含杂质
B. 越大,样品中 含量一定越高
C.若步骤I中滴入KMnO 溶液不足,则测得样品中Fe元素含量偏低
4
D.若所用KMnO 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
4
14.(2020年7月浙江选考)硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备。
合成反应:
滴定反应:
已知: 易溶于水,难溶于乙醇, 开始失结晶水。
实验步骤:
Ⅰ. 制备:装置A制备的 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液 约为
7时,停止通入 气体,得产品混合溶液。
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到 产品。
Ⅲ.产品纯度测定:以淀粉作指示剂,用 产品配制的溶液滴定碘标准溶液至滴定终点,计
算 含量。
请回答:
(1)步骤Ⅰ:单向阀的作用是______;装置C中的反应混合溶液 过高或过低将导致产率降低,原因是
_______。
(2)步骤Ⅱ:下列说法正确的是_____。
A 快速蒸发溶液中水分,可得较大晶体颗粒
B 蒸发浓缩至溶液表面出现品晶膜时,停止加热
C 冷却结晶后的固液混合物中加入乙醇可提高产率
D 可选用冷的 溶液作洗涤剂
(3)步骤Ⅲ
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→(______)→(______)→(______)→(______)→(______)→开始滴定。
A 烘干 B 装入滴定液至零刻度以上 C 调整滴定液液面至零刻度或零刻度以下D 用洗耳球吹出润
洗液 E 排除气泡 F 用滴定液润洗2至3次 G 记录起始读数
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是______。
③滴定法测得产品中 含量为 ,则 产品中可能混有的物质是________。
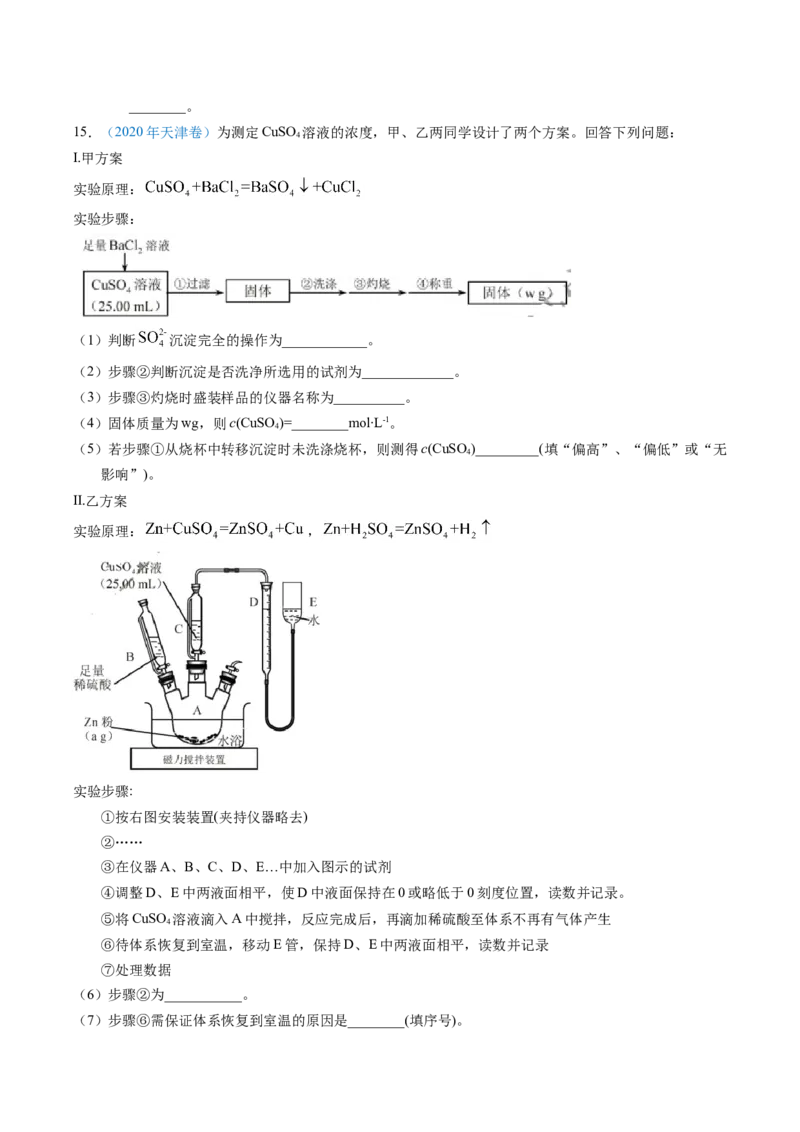
15.(2020年天津卷)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ.甲方案
实验原理:
实验步骤:
(1)判断 沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO )=________mol‧L-1。
4
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_________(填“偏高”、“偏低”或“无
4
影响”)。
Ⅱ.乙方案
实验原理: ,
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。A.反应热受温度影响 B.气体密度受温度影响 C.反应速率受温度影响
(8)Zn粉质量为ag,若测得H 体积为bmL,已知实验条件下 ,则c(CuSO )______mol‧
2 4
L-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )________(填“偏高”、“偏低”或
4
“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:_________(填“是”或“否”)。
4
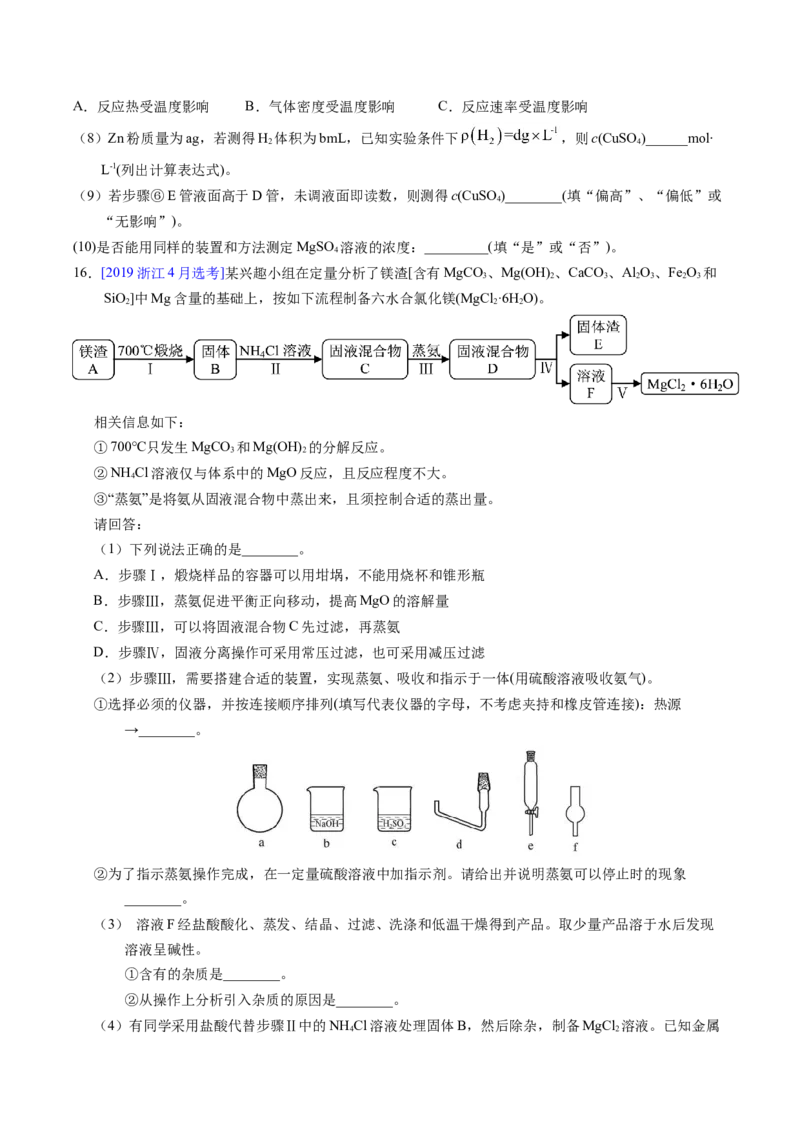
16.[2019浙江4月选考]某兴趣小组在定量分析了镁渣[含有MgCO 、Mg(OH) 、CaCO 、Al O、Fe O 和
3 2 3 2 3 2 3
SiO]中Mg含量的基础上,按如下流程制备六水合氯化镁(MgCl ·6H O)。
2 2 2
相关信息如下:
①700℃只发生MgCO 和Mg(OH) 的分解反应。
3 2
②NH Cl溶液仅与体系中的MgO反应,且反应程度不大。
4
③“蒸氨”是将氨从固液混合物中蒸出来,且须控制合适的蒸出量。
请回答:
(1)下列说法正确的是________。
A.步骤Ⅰ,煅烧样品的容器可以用坩埚,不能用烧杯和锥形瓶
B.步骤Ⅲ,蒸氨促进平衡正向移动,提高MgO的溶解量
C.步骤Ⅲ,可以将固液混合物C先过滤,再蒸氨
D.步骤Ⅳ,固液分离操作可采用常压过滤,也可采用减压过滤
(2)步骤Ⅲ,需要搭建合适的装置,实现蒸氨、吸收和指示于一体(用硫酸溶液吸收氨气)。
①选择必须的仪器,并按连接顺序排列(填写代表仪器的字母,不考虑夹持和橡皮管连接):热源
→________。
②为了指示蒸氨操作完成,在一定量硫酸溶液中加指示剂。请给出并说明蒸氨可以停止时的现象
________。
(3) 溶液F经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。取少量产品溶于水后发现
溶液呈碱性。
①含有的杂质是________。
②从操作上分析引入杂质的原因是________。
(4)有同学采用盐酸代替步骤Ⅱ中的NH Cl溶液处理固体B,然后除杂,制备MgCl 溶液。已知金属
4 2离子形成氢氧化物沉淀的pH范围:
pH[来源:学&科&网Z&X&X&K][来源:学|科|
金属离子[来源:学科
网]
网ZXXK]
开始沉淀 完全沉淀
Al3+ 3.0 4.7
Fe3+ 1.1 2.8
Ca2+ 11.3 -
Mg2+ 8.4 10.9
请给出合理的操作排序(从下列操作中选取,按先后次序列出字母,操作可重复使用):固体B→a→(
)→( )→( )→( )→( )→( )→MgCl 溶液→产品。
2
a.用盐酸溶解 b.调pH=3.0 c.调pH=5.0 d.调pH=8.5
e.调pH=11.0 f.过滤 g.洗涤
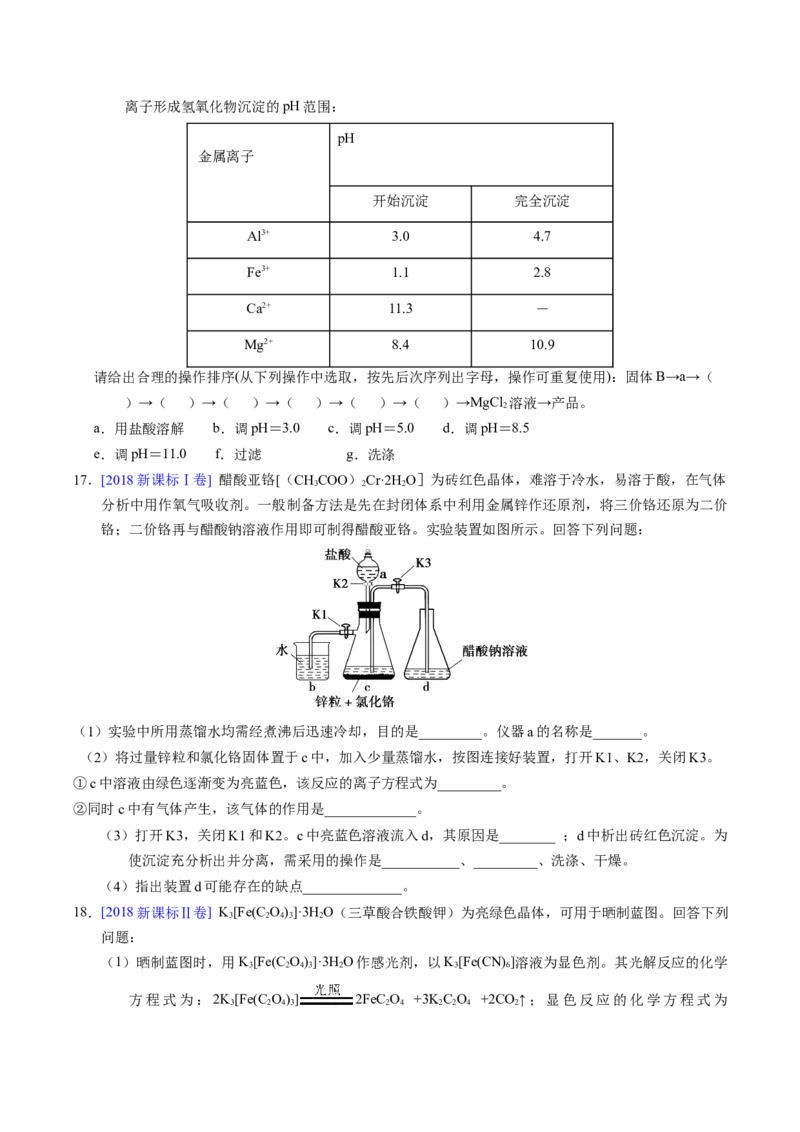
17.[2018新课标Ⅰ卷] 醋酸亚铬[(CHCOO)Cr·2H O]为砖红色晶体,难溶于冷水,易溶于酸,在气体
3 2 2
分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价
铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_________。仪器a的名称是_______。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________。
②同时c中有气体产生,该气体的作用是_____________。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是________ ;d中析出砖红色沉淀。为
使沉淀充分析出并分离,需采用的操作是___________、_________、洗涤、干燥。
(4)指出装置d可能存在的缺点______________。
18.[2018新课标Ⅱ卷] K[Fe(C O)]·3H O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列
3 2 4 3 2
问题:
(1)晒制蓝图时,用K[Fe(C O)]·3H O作感光剂,以K[Fe(CN) ]溶液为显色剂。其光解反应的化学
3 2 4 3 2 3 6
方程式为:2K[Fe(C O)] 2FeC O +3K C O +2CO ↑;显色反应的化学方程式为
3 2 4 3 2 4 2 2 4 2______________。
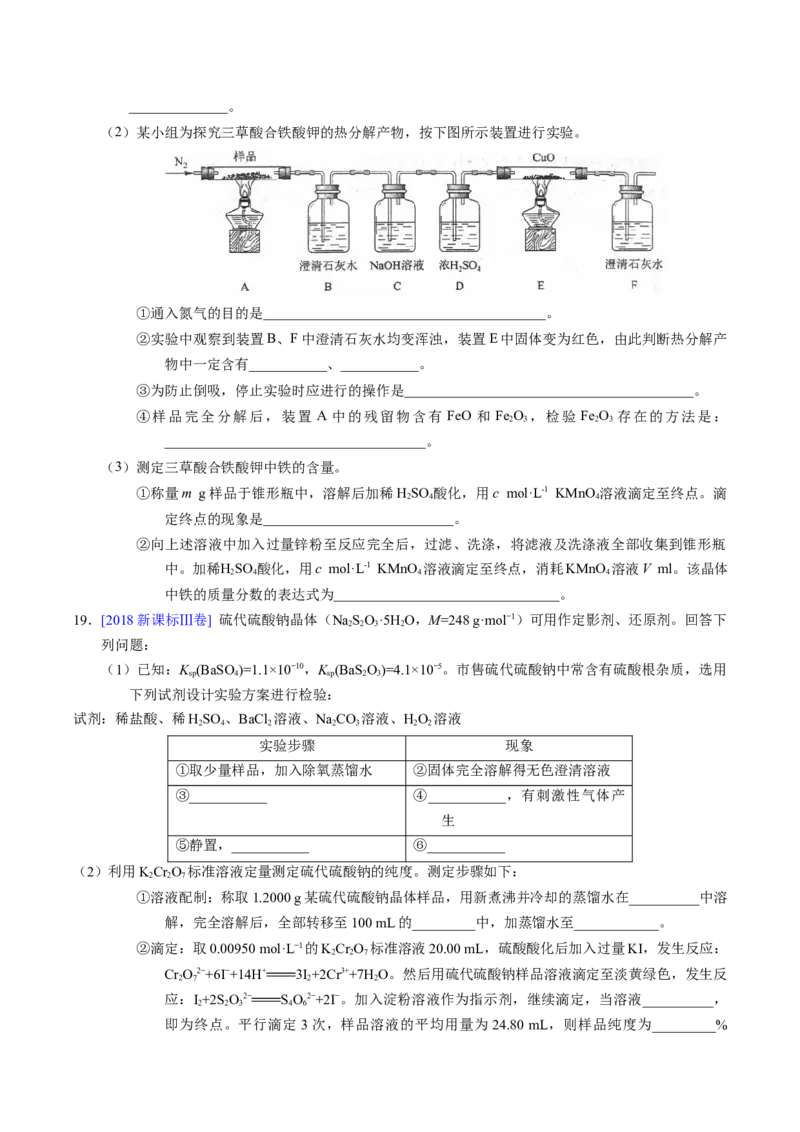
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产
物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_________________________________________。
④样品完全分解后,装置 A 中的残留物含有 FeO 和 Fe O ,检验 Fe O 存在的方法是:
2 3 2 3
_____________________________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀HSO 酸化,用c mol·L-1 KMnO 溶液滴定至终点。滴
2 4 4
定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶
中。加稀HSO酸化,用c mol·L-1 KMnO 溶液滴定至终点,消耗KMnO 溶液V ml。该晶体
2 4 4 4
中铁的质量分数的表达式为________________________________。
19.[2018新课标Ⅲ卷] 硫代硫酸钠晶体(NaSO·5H O,M=248 g·mol−1)可用作定影剂、还原剂。回答下
2 2 3 2
列问题:
(1)已知:K (BaSO)=1.1×10−10,K (BaS O)=4.1×10−5。市售硫代硫酸钠中常含有硫酸根杂质,选用
sp 4 sp 2 3
下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀HSO 、BaCl 溶液、NaCO 溶液、HO 溶液
2 4 2 2 3 2 2
实验步骤 现象
①取少量样品,加入除氧蒸馏水 ②固体完全溶解得无色澄清溶液
③___________ ④___________,有刺激性气体产
生
⑤静置,___________ ⑥___________
(2)利用KCr O 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
2 2 7
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶
解,完全溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
②滴定:取0.00950 mol·L−1的KCr O 标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:
2 2 7
Cr O2−+6I−+14H+ 3I+2Cr3++7H O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反
2 7 2 2
应:I+2S O2− SO2−+2I−。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,
2 2 3 4 6
即为终点。平行滴定3次,样品溶液的平均用量为 24.80 mL,则样品纯度为_________%(保留1位小数)。
20.[2018天津卷] 烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。
x
回答下列问题:
Ⅰ.采样
采样步骤:
①检验系统气密性;②加热器将烟道气加热至140℃;③打开抽气泵置换系统内空气;④采集无尘、
干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用是___________。
(2)C中填充的干燥剂是(填序号)___________。
a.碱石灰 b.无水CuSO c.P O
4 2 5
(3)用实验室常用仪器组装一套装置,其作用是与 D(装有碱液)相同,在虚线框中画出该装置的
示意图,标明气体的流向及试剂。
(4)采样步骤②加热烟道气的目的是___________。
Ⅱ.NO 含量的测定
x
将v L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO −,加水稀释至100.00 mL。量取
2 2 x 3
20.00 mL该溶液,加入v mL c mol·L−1 FeSO 标准溶液(过量),充分反应后,用c mol·L−1
1 1 4 2
KCr O 标准溶液滴定剩余的Fe2+,终点时消耗v mL。
2 2 7 2
(5)NO被HO 氧化为NO −的离子方程式是___________。
2 2 3
(6)滴定操作使用的玻璃仪器主要有___________。
(7)滴定过程中发生下列反应:
3Fe2++NO−+4H+ NO↑+3Fe3++2H O
3 2
Cr O2− + 6Fe2+ +14H+ 2Cr3+ +6Fe3++7H O
2 7 2
则气样中NO 折合成NO 的含量为_________mg·m−3。
x 2
(8)判断下列情况对NO 含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)
x
若缺少采样步骤③,会使测试结果___________。
若FeSO 标准溶液部分变质,会使测定结果___________。
4
21.[2017天津]用沉淀滴定法快速测定NaI等碘化物溶液中c(I−),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO 基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避
3
光保存,备用。
b.配制并标定100 mL 0.1000 mol·L−1 NH SCN标准溶液,备用。
4
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L−1 AgNO 溶液(过量),使I−完全转化为AgI沉淀。
3
c.加入NH Fe(SO ) 溶液作指示剂。
4 4 2
d.用0.1000 mol·L−1 NH SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡
4
红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗NH SCN标准溶液体积/mL 10.24 10.02 9.98
4
f.数据处理。
回答下列问题:
(1)将称得的AgNO 配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有__________。
3
(2)AgNO 标准溶液放在棕色试剂瓶中避光保存的原因是___________________________。
3
(3)滴定应在pH<0.5的条件下进行,其原因是___________________________________。
(4)b和c两步操作是否可以颠倒________________,说明理由________________________。
(5)所消耗的NH SCN标准溶液平均体积为_____mL,测得c(I−)=_________________ mol·L−1。
4
(6)在滴定管中装入NH SCN标准溶液的前一步,应进行的操作为________________________。
4
(7)判断下列操作对c(I−)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,则测定结果_______________。
3
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果____________________。
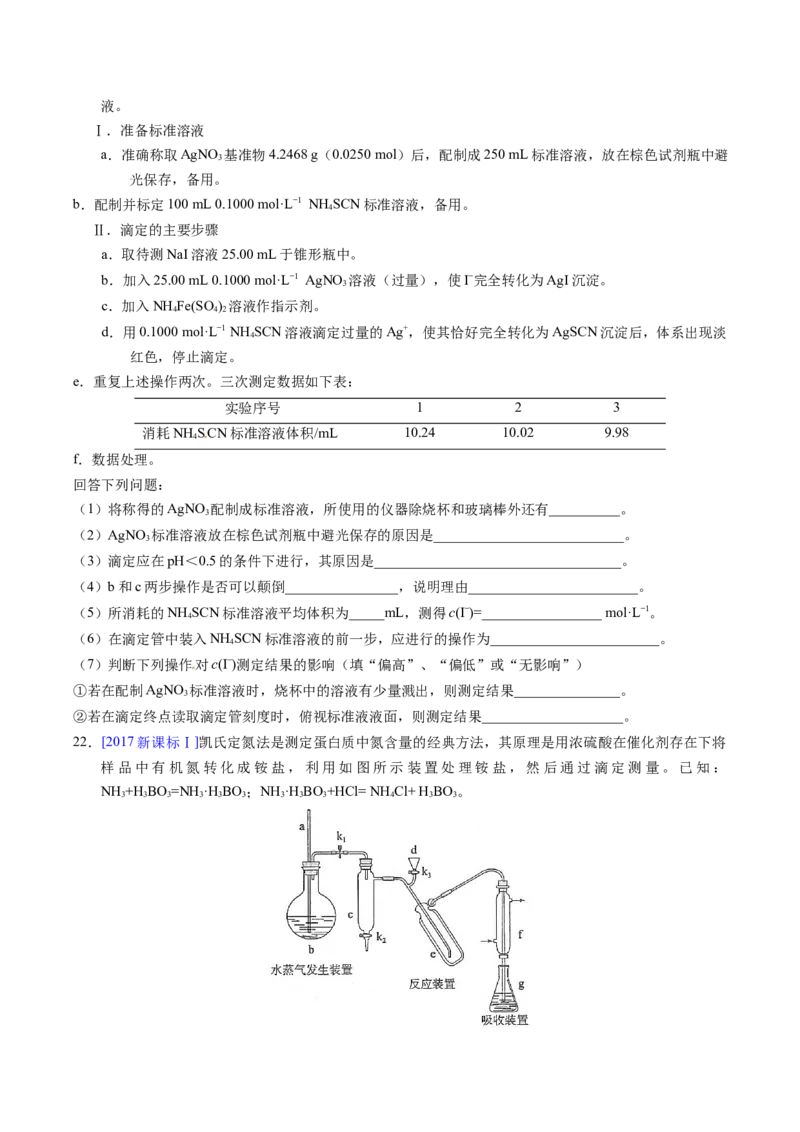
22.[2017新课标Ⅰ]凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将
样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:
NH +H BO=NH·H BO;NH ·H BO+HCl= NH Cl+ H BO。
3 3 3 3 3 3 3 3 3 4 3 3回答下列问题:
(1)a的作用是_______________。
(2)b中放入少量碎瓷片的目的是____________。f的名称是__________________。
(3)清洗仪器:g中加蒸馏水;打开k ,关闭k 、k ,加热b,蒸气充满管路;停止加热,关闭k ,g
1 2 3 1
中蒸馏水倒吸进入c,原因是____________;打开k 放掉水,重复操作2~3次。
2
(4)仪器清洗后,g中加入硼酸(HBO )和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,
3 3
用蒸馏水冲洗d,关闭k,d中保留少量水。打开k,加热b,使水蒸气进入e。
3 1
①d中保留少量水的目的是___________________。
②e中主要反应的离子方程式为________________,e采用中空双层玻璃瓶的作用是________。
(5)取某甘氨酸(C HNO )样品m 克进行测定,滴定g中吸收液时消耗浓度为c mol·L–1的盐酸V
2 5 2
mL,则样品中氮的质量分数为_________%,样品的纯度≤_______%。
23.[2017新课标Ⅱ]水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边
河水中的溶解氧。实验步骤及测定原理如下:Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH) 碱性悬浊液(含有KI)混合,反应
2
生成MnO(OH) ,实现氧的固定。
2
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH) 被I−还原为Mn2+,在暗处静置5 min,然后用标准NaSO 溶液滴定
2 2 2 3
生成的I(2 +I =2I−+ )。
2 2
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____________。
(2)“氧的固定”中发生反应的化学方程式为_______________。
(3)NaSO 溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和
2 2 3
____________;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除____及二氧化碳。
(4)取100.00 mL水样经固氧、酸化后,用a mol·L−1NaSO 溶液滴定,以淀粉溶液作指示剂,终点
2 2 3
现象为________________;若消耗 NaSO 溶液的体积为 b mL,则水样中溶解氧的含量为
2 2 3
_________mg·L−1。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测量结果偏___________。(填“高”或“低”)
24.【2016年高考天津卷】(18分)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解
氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于
5mg/L。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。1、测定原理:
碱性体积下,O 将Mn2+氧化为MnO(OH) ①2Mn2++O +4OH-=2 MnO(OH) ↓,酸性条件下,MnO(OH)
2 2: 2 2 2
将I-氧化为 I ②MnO(OH) +I-+H+→Mn2++I +H O(未配平),用NaSO 标准溶液滴定生成的 I ,
2: 2 2 2 2 2 3 2
③2SO2-+I =S O2-+2I-
2 3 2 4 6
2、测定步骤
a.安装装置,检验气密性,充N 排尽空气后,停止充N。
2 2
b.向烧瓶中加入200ml水样
c.向烧瓶中依次迅速加入1mlMnSO 无氧溶液(过量)2ml碱性KI无氧溶液(过量),开启搅拌器,至
4
反应①完全。
d搅拌并向烧瓶中加入2ml硫酸无氧溶液至反应②完全,溶液为中性或若酸性。
e.从烧瓶中取出40.00ml溶液,以淀粉作指示剂,用0.001000mol/L Na SO 溶液进行滴定,记录
2 2 3
数据。
f.……
g.处理数据(忽略氧气从水样中的溢出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为__________。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为__________。
①滴定管②注射器③量筒
(3)搅拌的作用是__________。
(4)配平反应②的方程式,其化学计量数依次为__________。
(5)步骤f为__________。
(6)步骤 e中达到滴定终点的标志为__________。若某次滴定消耗 NaSO 溶液 4.50ml,水样的
2 2 3
DO=__________mg/L(保留一位小数)。作为饮用水源,此次测得DO是否达标:__________(填是
或否)
(7)步骤d中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的
原因(用离子方程式表示,至少写出2个)__________。
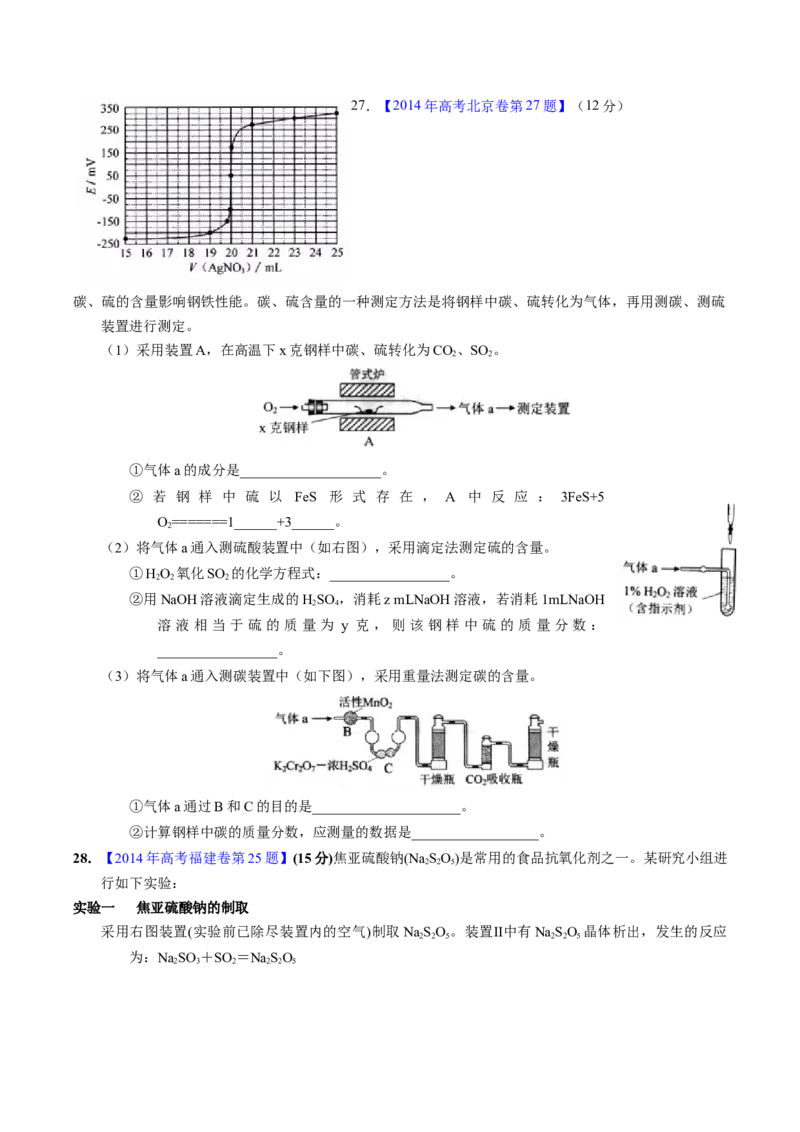
25.【2016年高考浙江卷】(15分)无水MgBr 可用作催化剂。实验室采用镁屑与液溴为原料制备无水
2
MgBr ,装置如图1,主要步骤如下:
2
步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得
三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160 ℃分解
得无水MgBr 产品。
2
已知:①Mg和Br 反应剧烈放热;MgBr 具有强吸水性。
2 2
②MgBr +3C HOC H MgBr 3C HOC H
2 2 5 2 5 2· 2 5 2 5
请回答:
(1)仪器A的名称是____________。
实验中不能用干燥空气代替干燥N2,原因是___________。
(2)如将装置B改为装置C(图2),可能会导致的后果是___________。
(3)步骤3中,第一次过滤除去的物质是___________。
(4)有关步骤4的说法,正确的是___________。
A.可用95%的乙醇代替苯溶解粗品 B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯 D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++ Y4-====Mg Y2-
①滴定前润洗滴定管的操作方法是__________。
②测定前,先称取0.2500g无水MgBr 产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至
2
终 点 , 消 耗 EDTA 标 准 溶 液 26.50 mL , 则 测 得 无 水 MgBr 产 品 的 纯 度 是
2
________________________(以质量分数表示)。
26.【2015浙江理综化学】(15分)某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
取0.0100 mol·Lˉ1的AgNO 标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定
3
法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
V(AgNO)/mL 15.00 19.00 19.80 19.98 20.00 20.02 21.00 23.00 25.00
3
E/mV -225 -200 -150 -100 50.0 175 275 300 325
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:已知:3I+6NaOH=5NaI+NaIO +3HO。
2 3 2
请回答:
(1)实验(一) 中的仪器名称:仪器A , 仪器 B 。
(2)①根据表中数据绘制滴定曲线:
②该次滴定终点时用去AgNO 溶液的体积为 mL,计算得海带中碘的百分含量为 %。
3
(3)①分液漏斗使用前须检漏,检漏方法为 。
②步骤X中,萃取后分液漏斗内观察到的现象是 。
③下列有关步骤Y的说法,正确的是 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
④实验(二) 中操作Z的名称是 。
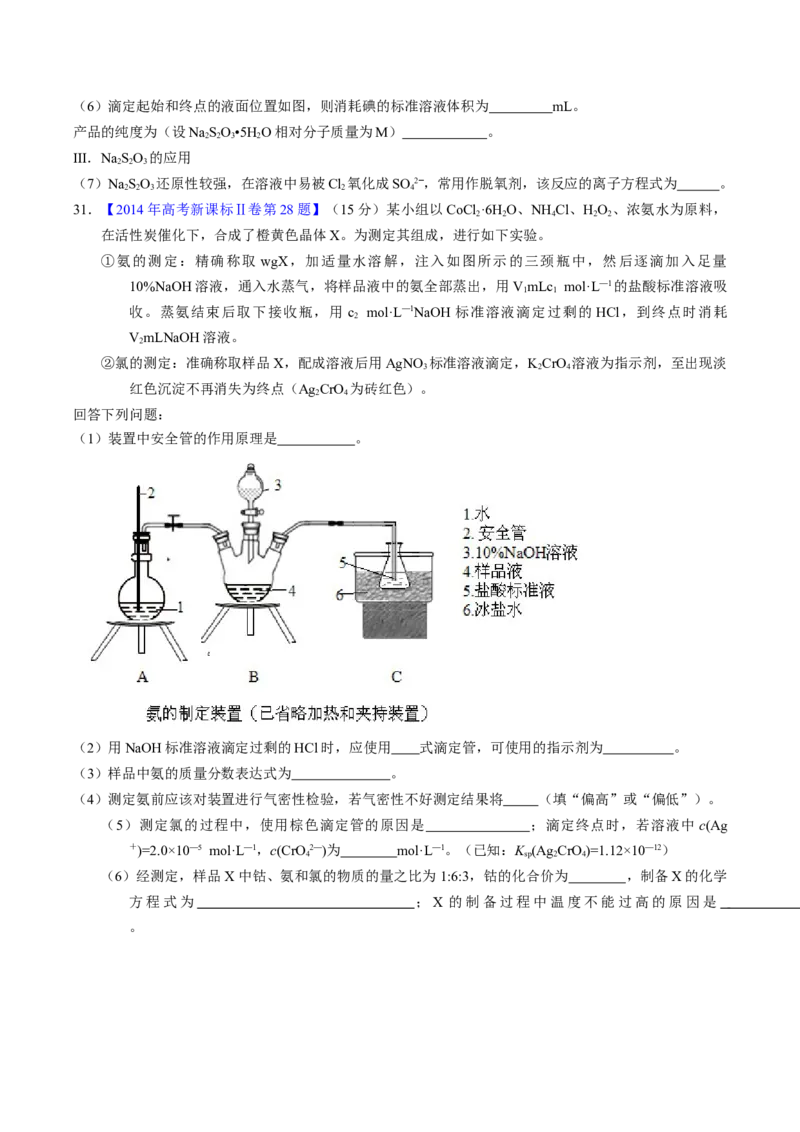
(4)方案甲中采用蒸馏不合理,理由是 。27.【2014年高考北京卷第27题】(12分)
碳、硫的含量影响钢铁性能。碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫
装置进行测定。
(1)采用装置A,在高温下x克钢样中碳、硫转化为CO、SO 。
2 2
①气体a的成分是____________________。
② 若 钢 样 中 硫 以 FeS 形 式 存 在 , A 中 反 应 : 3FeS+5
O=======1______+3______。
2
(2)将气体a通入测硫酸装置中(如右图),采用滴定法测定硫的含量。
①HO 氧化SO 的化学方程式:_________________。
2 2 2
②用NaOH溶液滴定生成的HSO ,消耗z mLNaOH溶液,若消耗1mLNaOH
2 4
溶液相当于硫的质量为 y 克,则该钢样中硫的质量分数:
_________________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。
①气体a通过B和C的目的是_____________________。
②计算钢样中碳的质量分数,应测量的数据是__________________。
28.【2014年高考福建卷第25题】(15分)焦亚硫酸钠(Na SO)是常用的食品抗氧化剂之一。某研究小组进
2 2 5
行如下实验:
实验一 焦亚硫酸钠的制取
采用右图装置(实验前已除尽装置内的空气)制取NaSO 。装置II中有NaSO 晶体析出,发生的反应
2 2 5 2 2 5
为:NaSO +SO =NaSO
2 3 2 2 2 5(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。
实验二 焦亚硫酸钠的性质
NaSO 溶于水即生成NaHSO。
2 2 5 3
(4)证明NaHSO 溶液中HSO - 的电离程度大于水解程度,可采用的实验方法是 (填序号)。
3 3
a.测定溶液的pH b.加入Ba(OH) 溶液 c.加入盐酸
2
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验NaSO 晶体在空气中已被氧化的实验方案是 。
2 2 5
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用NaSO 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO 计算)的方案如
2 2 5 2
下:
(已知:滴定时反应的化学方程式为SO +I+2HO=HSO +2HI)
2 2 2 2 4
①按上述方案实验,消耗标准I 溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离
2
SO 计算)为 g·L-1。
2
②在上述实验过程中,若有部分 HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不
变”)。
29.【2014年高考江苏卷第21B题】[实验化学]
磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生成药物、食品添加剂和锂离子电池的正极材料,
实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,
反应加热的目的是 。(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定
滤液中的Fe2+,离子方程式如下:
①在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、 和 。
②若滴定xmL滤液中的Fe2+,消耗amol·L—1 K2Cr2O7标准溶液bmL,则滤液中
c(Fe2+)= mol·L—1
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是 (填序号)。
A.加入适当过量的H2O2溶液 B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行 D.用氨水调节pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干
燥得到FePO4·2H2O 。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为
。
30.【2014年高考天津卷第9题】(18分)NaSO 是重要的化工原料,易溶于水。在中性或碱性环境中
2 2 3
稳定。
I.制备NaSO•5H O
2 2 3 2
反应原理:NaSO (aq)+S(s) NaSO(aq)
2 3 2 2 3
实验步骤:
①称取15g Na SO 加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研
2 3
细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。
③趁热过滤,将滤液水浴加热浓缩,冷却析出NaSO•5H O,经过滤,洗涤,干燥,
2 2 3 2
得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的名称是 ,其作用是
。
( 3 ) 产 品 中 除 了 有 未 反 应 的 NaSO 外 , 最 可 能 存 在 的 无 机 杂 质 是
2 3
, 检 验 是 否 存 在 该 杂 质 的 方 法 是
。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。
反应原理为:2SO2‾+I =S4O62-+2I‾
2 3 2
(5)滴定至终点时,溶液颜色的变化: 。(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。
产品的纯度为(设NaSO•5H O相对分子质量为M) 。
2 2 3 2
III.NaSO 的应用
2 2 3
(7)NaSO 还原性较强,在溶液中易被Cl 氧化成SO 2‾,常用作脱氧剂,该反应的离子方程式为 。
2 2 3 2 4
31.【2014年高考新课标Ⅱ卷第28题】(15分)某小组以CoCl ·6H O、NH Cl、HO 、浓氨水为原料,
2 2 4 2 2
在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。
①氨的测定:精确称取 wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用VmLc mol·L—1的盐酸标准溶液吸
1 1
收。蒸氨结束后取下接收瓶,用 c mol·L—1NaOH 标准溶液滴定过剩的 HCl,到终点时消耗
2
VmLNaOH溶液。
2
②氯的测定:准确称取样品X,配成溶液后用AgNO 标准溶液滴定,KCrO 溶液为指示剂,至出现淡
3 2 4
红色沉淀不再消失为终点(Ag CrO 为砖红色)。
2 4
回答下列问题:
(1)装置中安全管的作用原理是 。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用 式滴定管,可使用的指示剂为 。
(3)样品中氨的质量分数表达式为 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将 (填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是 ;滴定终点时,若溶液中 c(Ag
+)=2.0×10—5 mol·L—1,c(CrO 2—)为 mol·L—1。(已知:K (Ag CrO)=1.12×10—12)
4 sp 2 4
(6)经测定,样品X中钴、氨和氯的物质的量之比为1:6:3,钴的化合价为 ,制备X的化学
方程式为 ;X 的制备过程中温度不能过高的原因是
。