文档内容
辽宁省大连市滨城高中联盟2025-2026学年高三上学期10月月考 化学试
卷
一、单选题
1.闵恩泽院士在炼油催化应用科学领域做出卓越贡献,被称为“中国催化剂之父”。催化剂是化学反应
的重要工具,下列物质类别中原则上一般不常作为催化剂的是
A.非金属单质 B.手性有机小分子 C.金属配合物 D.过渡元素的金属单质
2.化学品在衣食住行中应用广泛。下列说法错误的是
A.合成纤维可制作衣帽鞋袜 B.不锈钢防盗网为合金
C.甲醛水溶液可用于海鲜保存 D.碳纤维复合材料可用于自行车架
3.下列图示或化学用语正确的是
A.NH 分子的VSEPR模型为
3
B. 的系统命名:1,3,4-三甲苯
C.CaC 的电子式
2
D.基态Cr原子的价层电子轨道表示式为
4.类比是学习化学的重要方法。下列“类比”说法中正确的是
A. 在 中燃烧生成 ,则 在 中燃烧生成
B. 与 反应生成 ,则 与 反应生成
C. 可与 反应生成 ,则 可与 反应生成
D. 与烧碱溶液反应生成 ,则 与氨水反应生成
5.下列对应离子方程式正确的是
A 向饱和 溶液中通入过量B 溶液中加入过量的 溶液
C 溶液与过量石灰水反应
D 溶液中通入少量 气体
A.A B.B C.C D.D
6.已知过二硫酸钾( )和水的反应: 及过二硫酸根( )的结构如
图所示。设 为阿伏加德罗常数的值,下列说法正确
A.标准状况下, 中电子数目为
B. 是还原剂
C. 固体中阴阳离子总数目为
D.标准状况下,生成 ,转移电子数目为
7.下列实验装置或操作不能达到实验目的的是
A.熔融纯碱 B.制备Fe(OH)
2C.验证金属锌保护铁 D.向容量瓶转移溶液
A.A B.B C.C D.D
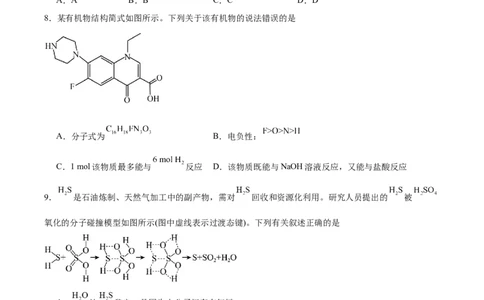
8.某有机物结构简式如图所示。下列关于该有机物的说法错误的是
A.分子式为 B.电负性:
C.1 mol该物质最多能与 反应 D.该物质既能与NaOH溶液反应,又能与盐酸反应
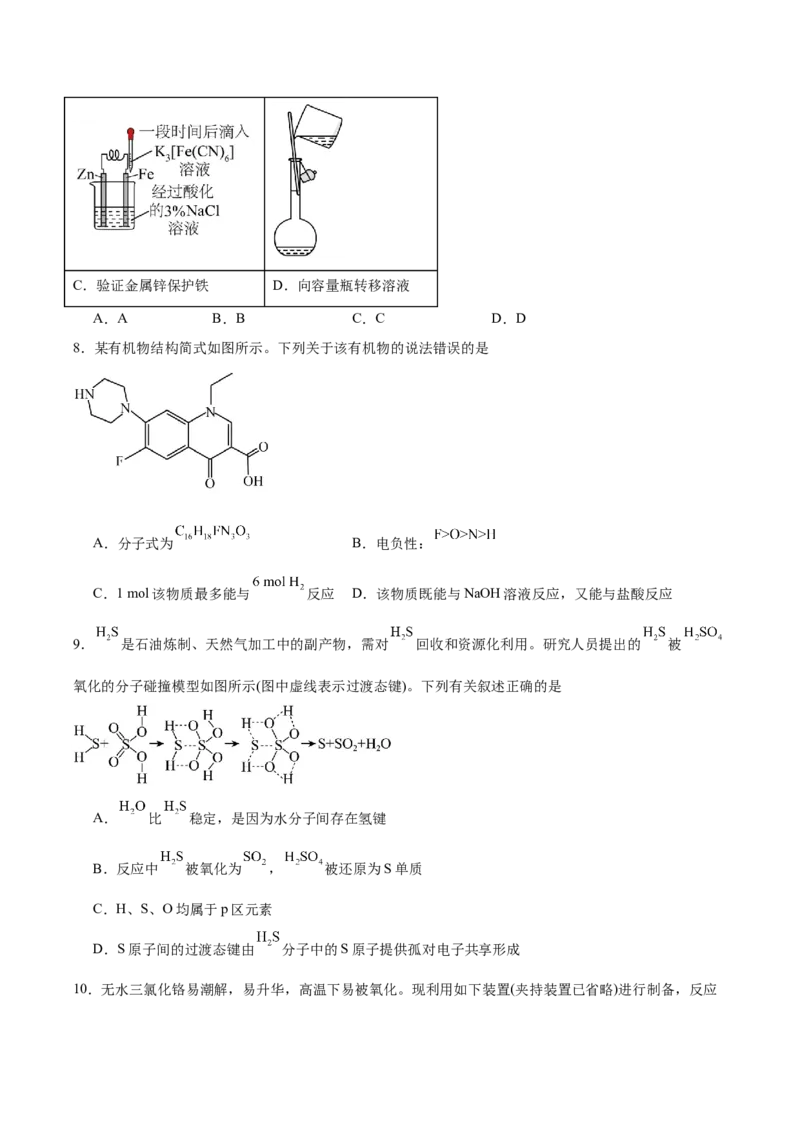
9. 是石油炼制、天然气加工中的副产物,需对 回收和资源化利用。研究人员提出的 被
氧化的分子碰撞模型如图所示(图中虚线表示过渡态键)。下列有关叙述正确的是
A. 比 稳定,是因为水分子间存在氢键
B.反应中 被氧化为 , 被还原为S单质
C.H、S、O均属于p区元素
D.S原子间的过渡态键由 分子中的S原子提供孤对电子共享形成
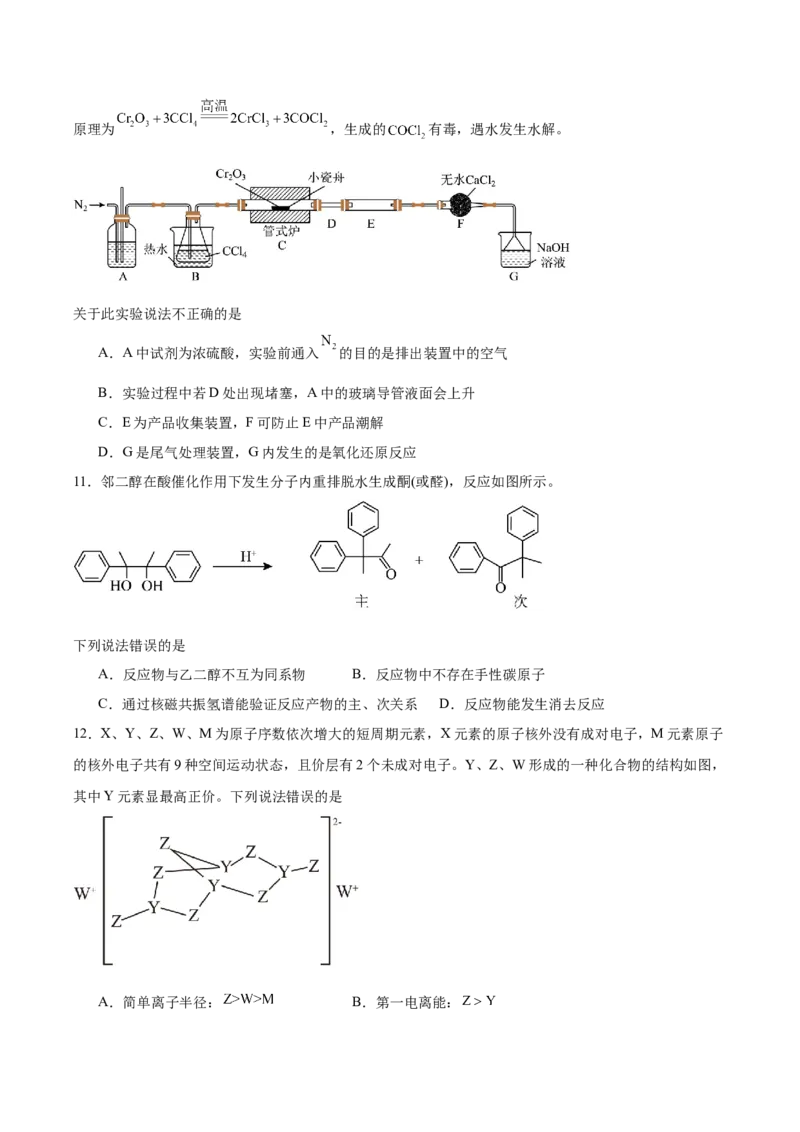
10.无水三氯化铬易潮解,易升华,高温下易被氧化。现利用如下装置(夹持装置已省略)进行制备,反应原理为 ,生成的 有毒,遇水发生水解。
关于此实验说法不正确的是
A.A中试剂为浓硫酸,实验前通入 的目的是排出装置中的空气
B.实验过程中若D处出现堵塞,A中的玻璃导管液面会上升
C.E为产品收集装置,F可防止E中产品潮解
D.G是尾气处理装置,G内发生的是氧化还原反应
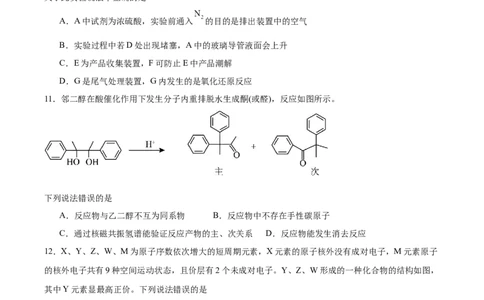
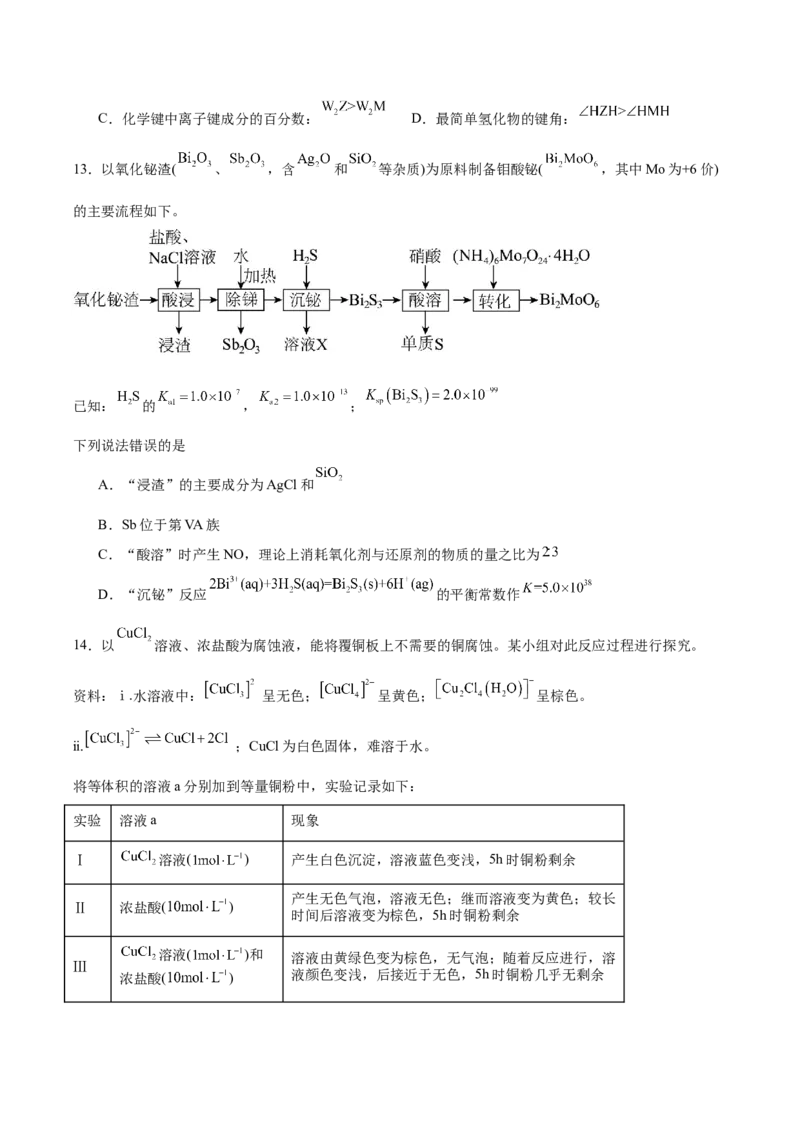
11.邻二醇在酸催化作用下发生分子内重排脱水生成酮(或醛),反应如图所示。
下列说法错误的是
A.反应物与乙二醇不互为同系物 B.反应物中不存在手性碳原子
C.通过核磁共振氢谱能验证反应产物的主、次关系 D.反应物能发生消去反应
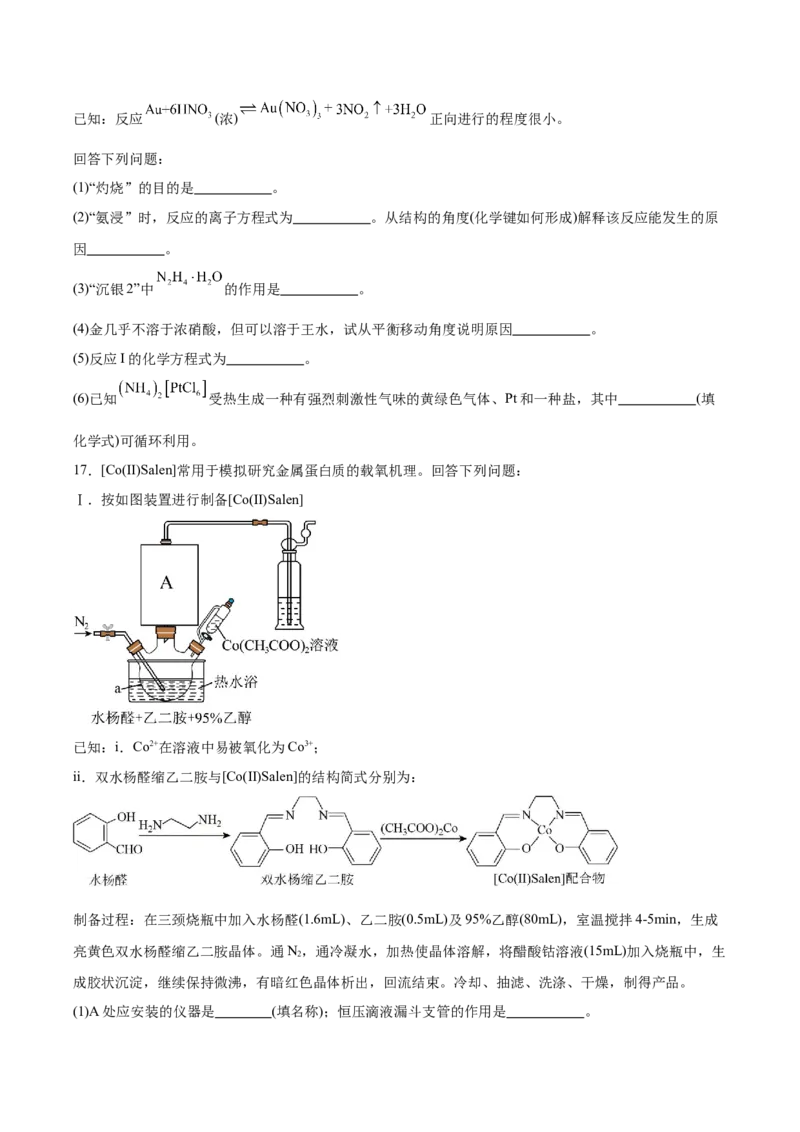
12.X、Y、Z、W、M为原子序数依次增大的短周期元素,X元素的原子核外没有成对电子,M元素原子
的核外电子共有9种空间运动状态,且价层有2个未成对电子。Y、Z、W形成的一种化合物的结构如图,
其中Y元素显最高正价。下列说法错误的是
A.简单离子半径: B.第一电离能:C.化学键中离子键成分的百分数: D.最简单氢化物的键角:
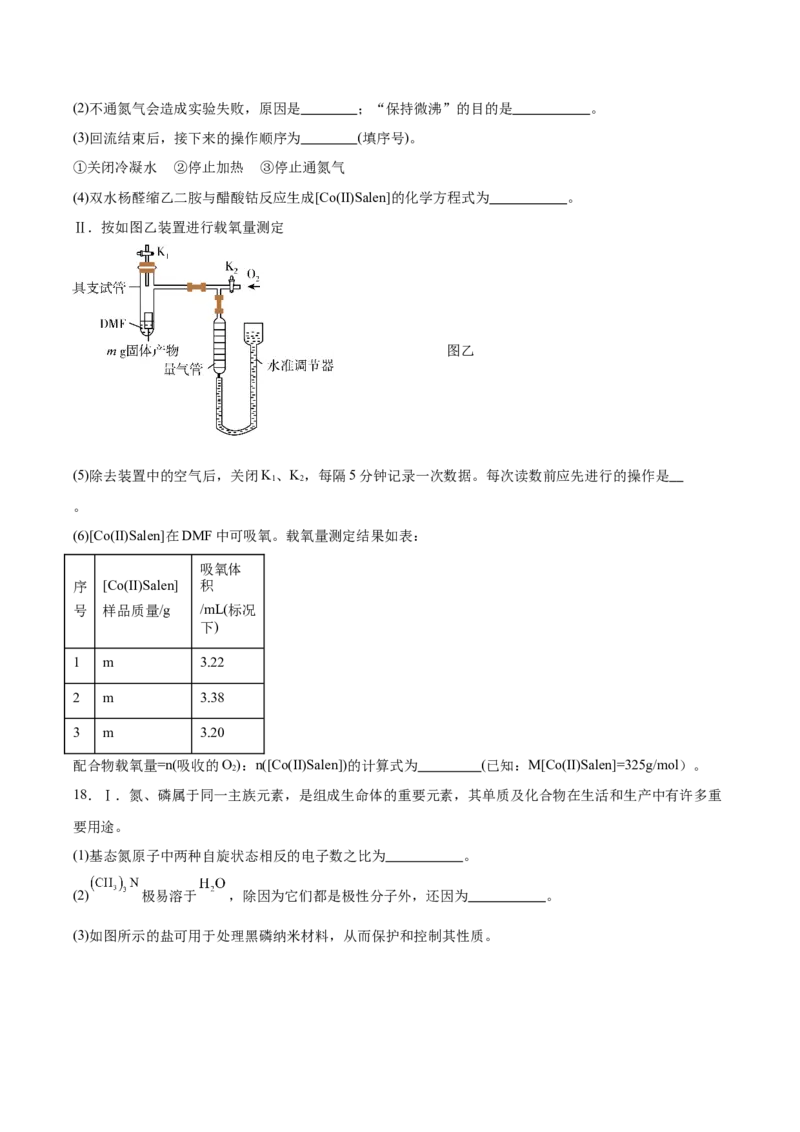
13.以氧化铋渣( 、 ,含 和 等杂质)为原料制备钼酸铋( ,其中Mo为+6价)
的主要流程如下。
已知: 的 , ;
下列说法错误的是
A.“浸渣”的主要成分为AgCl和
B.Sb位于第VA族
C.“酸溶”时产生NO,理论上消耗氧化剂与还原剂的物质的量之比为
D.“沉铋”反应 的平衡常数作
14.以 溶液、浓盐酸为腐蚀液,能将覆铜板上不需要的铜腐蚀。某小组对此反应过程进行探究。
资料:ⅰ.水溶液中: 呈无色; 呈黄色; 呈棕色。
ⅱ. ;CuCl为白色固体,难溶于水。
将等体积的溶液a分别加到等量铜粉中,实验记录如下:
实验 溶液a 现象
Ⅰ 溶液( ) 产生白色沉淀,溶液蓝色变浅,5h时铜粉剩余
产生无色气泡,溶液无色;继而溶液变为黄色;较长
Ⅱ 浓盐酸( )
时间后溶液变为棕色,5h时铜粉剩余
溶液( )和 溶液由黄绿色变为棕色,无气泡;随着反应进行,溶
Ⅲ
浓盐酸( ) 液颜色变浅,后接近于无色,5h时铜粉几乎无剩余经检验,Ⅱ中产生的气体为 ,下列有关说法中不正确的是
A.Ⅰ中产生白色沉淀的过程可以描述为
B.将 加到铜粉中,溶液变蓝,未检测到 。证明 的产生与 、 结合成
,提高了Cu的还原性有关
C.对比实验Ⅰ、Ⅲ,分析实验Ⅲ中将溶液a加到铜粉中未产生白色沉淀的原因可能是Ⅲ中溶液的酸性
太强,白色沉淀被溶解
D.实验Ⅱ、Ⅲ对比,实验Ⅱ中产生气泡,实验Ⅲ中无气泡,可能是在此条件下 或 的氧
化性强于
二、多选题
15.由下列事实或现象能得出相应结论的是
事实或现象 结论
A 向苯酚浊液中加入足量NaCO 溶液,溶液变澄清 Ka(C HOH)>Ka (H CO)
2 3 6 6 2 2 3
向两份5mL 0.1mol·L-1HO 溶液中分别加入 KMnO 的催化效果比FeCl
B 2 2 4 3
1mL0.1mol·L-1KMnO 和FeCl ,前者产生气泡速率快 好
4 3
C 常温下,用pH计测定0.1mol·L-1NaH PO 溶液的pH>7 HPO 为三元弱酸
2 2 3 2
分别向丙烯酸乙酯和α-氰基丙烯酸乙酯中滴入水,前 氰基能活化双键,使其更
D
者无明显现象,后者快速固化 易发生加聚反应
A.A B.B C.C D.D
三、解答题
16.贵金属(主要指金、银、铂等8种金属)是国家战略资源之一。一种从制作首饰的废料(主要成分为金、
银、铂、蜡和纤维等)中提取金、银、铂的工艺流程如图所示。已知:反应 (浓) 正向进行的程度很小。
回答下列问题:
(1)“灼烧”的目的是 。
(2)“氨浸”时,反应的离子方程式为 。从结构的角度(化学键如何形成)解释该反应能发生的原
因 。
(3)“沉银2”中 的作用是 。
(4)金几乎不溶于浓硝酸,但可以溶于王水,试从平衡移动角度说明原因 。
(5)反应I的化学方程式为 。
(6)已知 受热生成一种有强烈刺激性气味的黄绿色气体、Pt和一种盐,其中 (填
化学式)可循环利用。
17.[Co(Ⅱ)Salen]常用于模拟研究金属蛋白质的载氧机理。回答下列问题:
Ⅰ.按如图装置进行制备[Co(Ⅱ)Salen]
已知:i.Co2+在溶液中易被氧化为Co3+;
ii.双水杨醛缩乙二胺与[Co(Ⅱ)Salen]的结构简式分别为:
制备过程:在三颈烧瓶中加入水杨醛(1.6mL)、乙二胺(0.5mL)及95%乙醇(80mL),室温搅拌4-5min,生成
亮黄色双水杨醛缩乙二胺晶体。通N,通冷凝水,加热使晶体溶解,将醋酸钴溶液(15mL)加入烧瓶中,生
2
成胶状沉淀,继续保持微沸,有暗红色晶体析出,回流结束。冷却、抽滤、洗涤、干燥,制得产品。
(1)A处应安装的仪器是 (填名称);恒压滴液漏斗支管的作用是 。(2)不通氮气会造成实验失败,原因是 ;“保持微沸”的目的是 。
(3)回流结束后,接下来的操作顺序为 (填序号)。
①关闭冷凝水 ②停止加热 ③停止通氮气
(4)双水杨醛缩乙二胺与醋酸钴反应生成[Co(Ⅱ)Salen]的化学方程式为 。
Ⅱ.按如图乙装置进行载氧量测定
图乙
(5)除去装置中的空气后,关闭K、K,每隔5分钟记录一次数据。每次读数前应先进行的操作是
1 2
。
(6)[Co(Ⅱ)Salen]在DMF中可吸氧。载氧量测定结果如表:
吸氧体
序 [Co(Ⅱ)Salen] 积
号 样品质量/g /mL(标况
下)
1 m 3.22
2 m 3.38
3 m 3.20
配合物载氧量=n(吸收的O):n([Co(Ⅱ)Salen])的计算式为 (已知:M[Co(Ⅱ)Salen]=325g/mol)。
2
18.Ⅰ.氮、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物在生活和生产中有许多重
要用途。
(1)基态氮原子中两种自旋状态相反的电子数之比为 。
(2) 极易溶于 ,除因为它们都是极性分子外,还因为 。
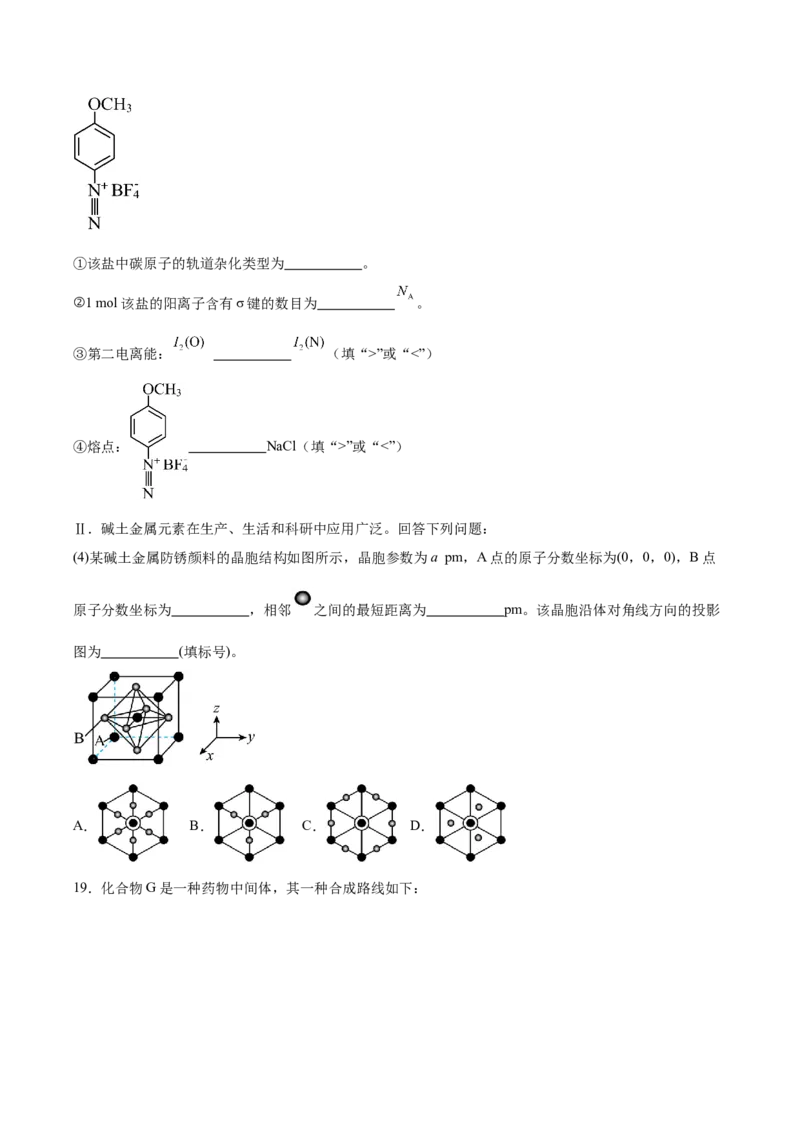
(3)如图所示的盐可用于处理黑磷纳米材料,从而保护和控制其性质。①该盐中碳原子的轨道杂化类型为 。
②1 mol该盐的阳离子含有σ键的数目为 。
③第二电离能: (填“>”或“<”)
④熔点: NaCl(填“>”或“<”)
Ⅱ.碱土金属元素在生产、生活和科研中应用广泛。回答下列问题:
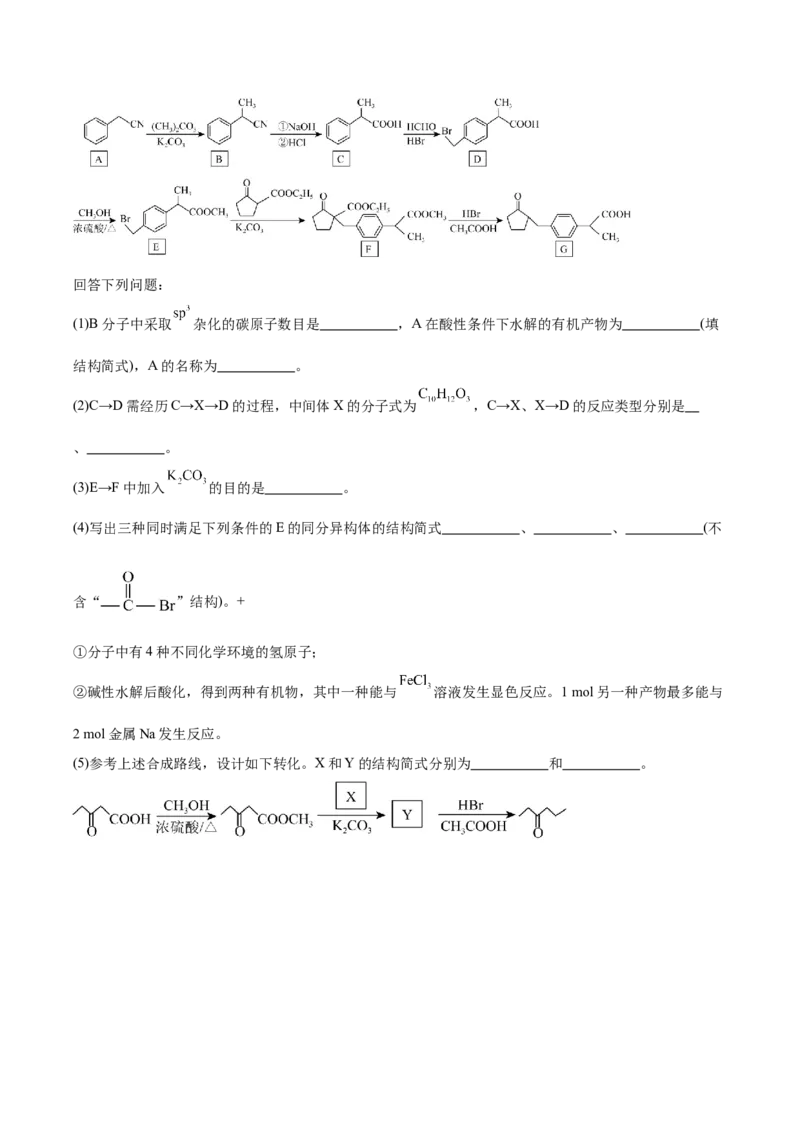
(4)某碱土金属防锈颜料的晶胞结构如图所示,晶胞参数为a pm,A点的原子分数坐标为(0,0,0),B点
原子分数坐标为 ,相邻 之间的最短距离为 pm。该晶胞沿体对角线方向的投影
图为 (填标号)。
A. B. C. D.
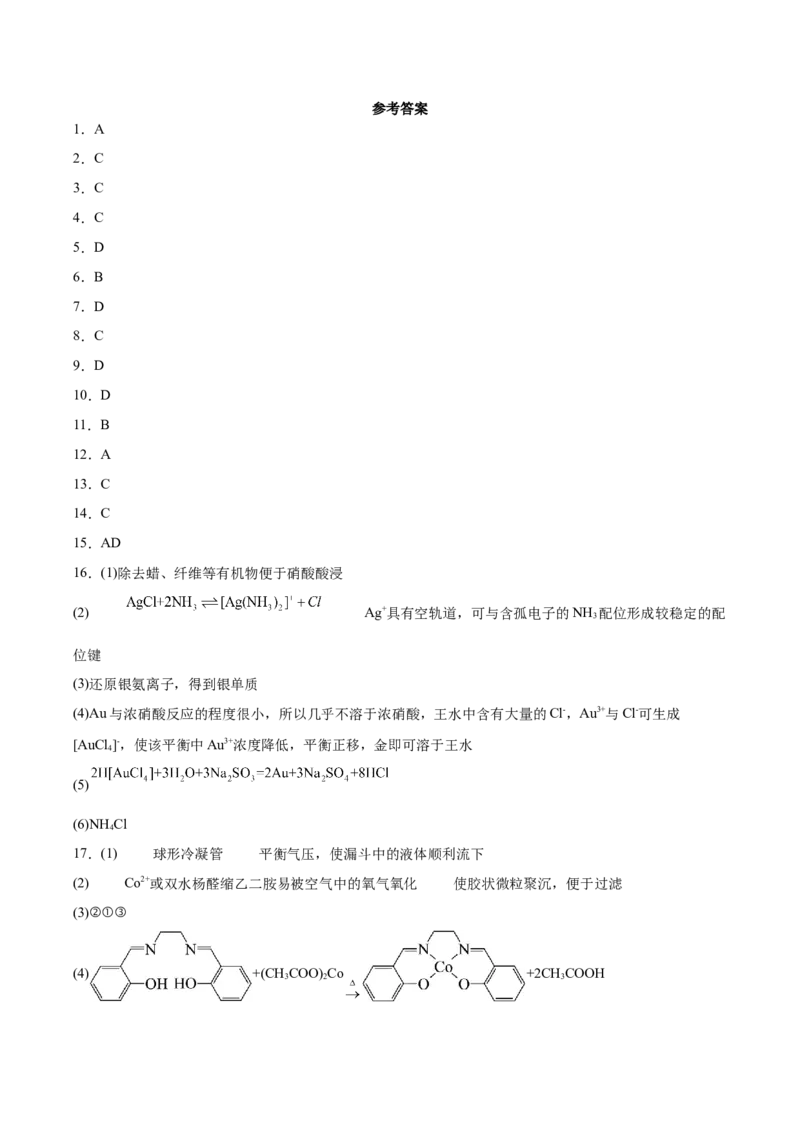
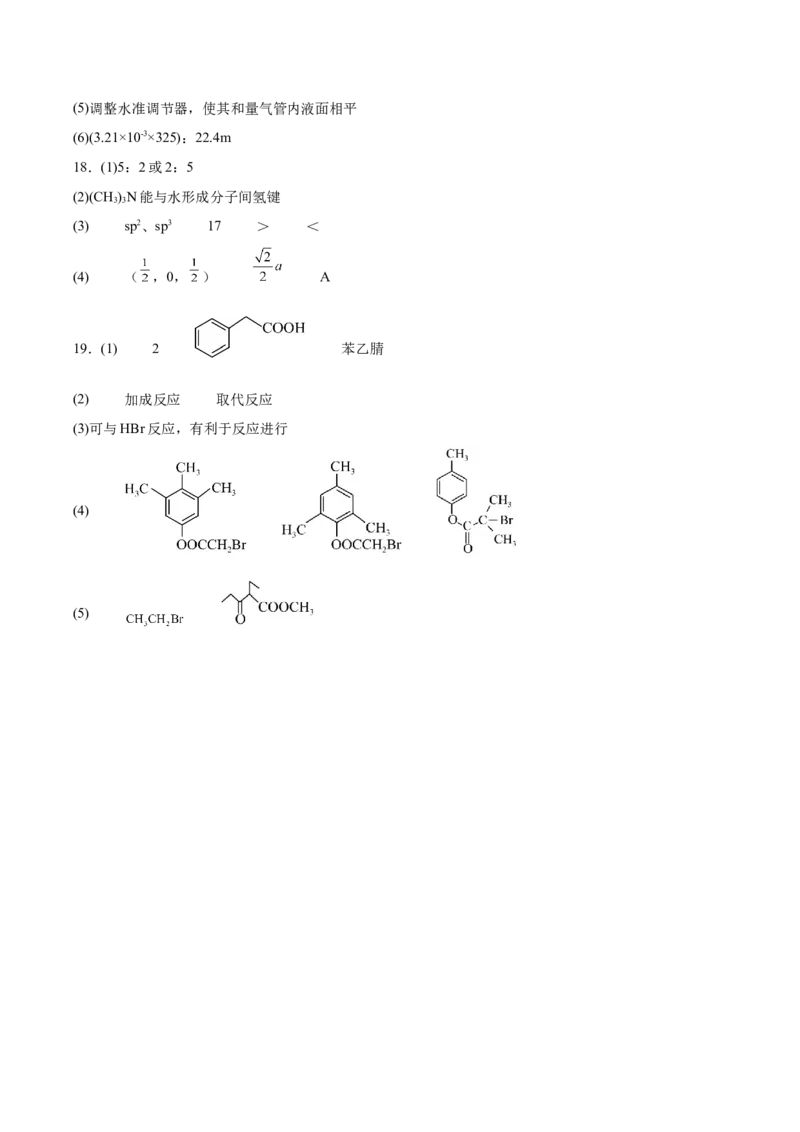
19.化合物G是一种药物中间体,其一种合成路线如下:回答下列问题:
(1)B分子中采取 杂化的碳原子数目是 ,A在酸性条件下水解的有机产物为 (填
结构简式),A的名称为 。
(2)C→D需经历C→X→D的过程,中间体X的分子式为 ,C→X、X→D的反应类型分别是
、 。
(3)E→F中加入 的目的是 。
(4)写出三种同时满足下列条件的E的同分异构体的结构简式 、 、 (不
含“ ”结构)。+
①分子中有4种不同化学环境的氢原子;
②碱性水解后酸化,得到两种有机物,其中一种能与 溶液发生显色反应。1 mol另一种产物最多能与
2 mol金属Na发生反应。
(5)参考上述合成路线,设计如下转化。X和Y的结构简式分别为 和 。参考答案
1.A
2.C
3.C
4.C
5.D
6.B
7.D
8.C
9.D
10.D
11.B
12.A
13.C
14.C
15.AD
16.(1)除去蜡、纤维等有机物便于硝酸酸浸
(2) Ag+具有空轨道,可与含孤电子的NH 配位形成较稳定的配
3
位键
(3)还原银氨离子,得到银单质
(4)Au与浓硝酸反应的程度很小,所以几乎不溶于浓硝酸,王水中含有大量的Cl-,Au3+与Cl-可生成
[AuCl ]-,使该平衡中Au3+浓度降低,平衡正移,金即可溶于王水
4
(5)
(6)NH Cl
4
17.(1) 球形冷凝管 平衡气压,使漏斗中的液体顺利流下
(2) Co2+或双水杨醛缩乙二胺易被空气中的氧气氧化 使胶状微粒聚沉,便于过滤
(3)②①③
(4) +(CH COO) Co +2CH COOH
3 2 3(5)调整水准调节器,使其和量气管内液面相平
(6)(3.21×10-3×325):22.4m
18.(1)5:2或2:5
(2)(CH )N能与水形成分子间氢键
3 3
(3) sp2、sp3 17 > <
(4) ( ,0, ) A
19.(1) 2 苯乙腈
(2) 加成反应 取代反应
(3)可与HBr反应,有利于反应进行
(4)
(5)