文档内容
2024 年高考江苏卷化学试题
一、单选题
1.我国探月工程取得重大进展。月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元素周期表第二周期的是
A.O B.P C.Ca D.Fe
2.反应PbS+4H O =PbSO +4H O可用于壁画修复。下列说法正确的是
2 2 4 2
A.S2-的结构示意图为 B.H O 中既含离子键又含共价键
2 2
C.SO2−中S元素的化合价为+6 D.H O的空间构型为直线形
4 2
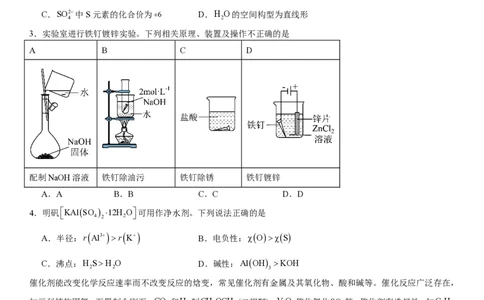
3.实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是
A B C D
配制NaOH溶液 铁钉除油污 铁钉除锈 铁钉镀锌
A.A B.B C.C D.D
4.明矾
KAl(SO
4
)
2
⋅12H
2
O
可用作净水剂。下列说法正确的是
A.半径:r ( Al3+) >r ( K+) B.电负性:χ(O)>χ(S)
C.沸点:H S>H O D.碱性:Al(OH) >KOH
2 2 3
催化剂能改变化学反应速率而不改变反应的焓变,常见催化剂有金属及其氧化物、酸和碱等。催化反应广泛存在,
如豆科植物固氮、石墨制金刚石、CO 和H 制CH OCH (二甲醚)、VO 催化氧化SO 等。催化剂有选择性,如C H
2 2 3 3 2 5 2 2 4
与O 反应用Ag催化生成 (环氧乙烷)、用CuCl /PdCl 催化生成CH CHO。催化作用能消除污染和影
2 2 2 3
响环境,如汽车尾气处理、废水中NO−电催化生成N 、氯自由基催化O 分解形成臭氧空洞。我国在石油催化领域
3 2 3
领先世界,高效、经济、绿色是未来催化剂研究的发展方向。完成下列小题。
5.下列说法正确的是
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能
B.C H 与O 反应中,Ag催化能提高生成CH CHO的选择性
2 4 2 3
C.H O 制O 反应中,MnO 能加快化学反应速率
2 2 2 2D.SO 与O 反应中,VO 能减小该反应的焓变
2 2 2 5
6.下列化学反应表示正确的是
催化剂
A.汽车尾气处理:2NO+4CO N +4CO
2 2
B.NO−电催化为N 的阳极反应:2NO−+12H+ +10e− =N ↑+6H O
3 2 3 2 2
催化剂
C.硝酸工业中NH 的氧化反应:4NH +3O 2N +6H O
3 3 2 2 2
Δ
D.CO 和H 催化制二甲醚:2CO +6H 催化剂→CH OCH +3H O
2 2 2 2 高温、高压 3 3 2
7.下列有关反应描述正确的是
A.CH CH OH催化氧化为CH CHO,CH CH OH断裂C-O键
3 2 3 3 2
B.氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变O 分解的历程
3
C.丁烷催化裂化为乙烷和乙烯,丁烷断裂σ键和π键
D.石墨转化为金刚石,碳原子轨道的杂化类型由sp3转变为sp2
8.碱性锌锰电池的总反应为Zn+2MnO +H O=ZnO+2MnOOH,电池构造示意图如图所示。下列有关说法正确
2 2
的是
A.电池工作时,MnO 发生氧化反应
2
B.电池工作时,OH−通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成1mol MnOOH,转移电子数为2×6.02×1023
9.化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是
A.X分子中所有碳原子共平面 B.1mol Y最多能与1mol H 发生加成反应
2
C.Z不能与Br 的CCl 溶液反应 D.Y、Z均能使酸性KMnO 溶液褪色
2 4 4
10.在给定条件下,下列制备过程涉及的物质转化均可实现的是A.HCl制备:NaCl溶液电解→H 和Cl 点燃→HCl
2 2
B.金属Mg制备:Mg(OH)
2
盐酸→MgCl
2
溶液 电
→
解
Mg
C.纯碱工业:NaCl溶液CO2→NaHCO △→Na CO
3 2 3
D.硫酸工业:FeS O2→SO H2O→H SO
2 高温 2 2 4
11.室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项 实验过程及现象 实验结论
用0.1mol⋅L−1 NaOH溶液分别中和等体积的0.1mol⋅L−1 H SO 溶液和 酸性:
2 4
A
H SO >CH COOH
0.1mol⋅L−1 CH COOH溶液,H SO 消耗的NaOH溶液多 2 4 3
3 2 4
B 向2mL 0.1mol⋅L−1 Na S溶液中滴加几滴溴水,振荡,产生淡黄色沉淀 氧化性:Br >S
2 2
向2mL浓度均为0.1mol⋅L−1的CaCl 和BaCl 混合溶液中滴加少量 溶度积常数:
2 2
C
CaCO >BaCO
0.1mol⋅L−1 Na CO 溶液,振荡,产生白色沉淀 3 3
2 3
结合H+能力:
D 用pH试纸分别测定CH COONa溶液和NaNO 溶液pH,CH COONa溶液pH大
3 2 3 CH COO− >NO−
3 2
A.A B.B C.C D.D
12.室温下,通过下列实验探究SO 的性质。已知K (H SO )=1.3×10−2,K (H SO )=6.2×10−8。
2 a1 2 3 a2 2 3
实验1:将SO 气体通入水中,测得溶液pH=3。
2
实验2:将SO 气体通入0.1mol⋅L−1 NaOH溶液中,当溶液pH=4时停止通气。
2
实验3:将SO 气体通入0.1mol⋅L−1酸性KMnO 溶液中,当溶液恰好褪色时停止通气。
2 4
下列说法正确的是
A.实验1所得溶液中:c
( HSO−)
+c
( SO2−)
>c
( H+)
3 3
B.实验2所得溶液中:c
( SO2−)
>c
( HSO−)
3 3
C.实验2所得溶液经蒸干、灼烧制得NaHSO 固体
3
D.实验3所得溶液中:c
( SO2−)
>c
( Mn2+)
4
13.二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①CO (g)+H (g)=CO(g)+H O(g) ∆H =41.2kJ⋅mol−1
2 2 2 1
②CO(g)+2H (g)=CH OH(g) ∆H
2 3 2
225℃、8×106Pa下,将一定比例CO
2
、H
2
混合气匀速通过装有催化剂的绝热反应管。装置及L
1
、L
2
、L
3
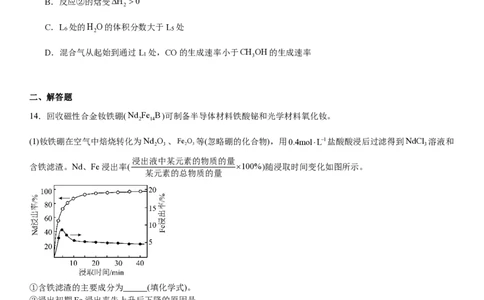
…位点处(相邻位点距离相同)的气体温度、CO和CH OH的体积分数如图所示。下列说法正确的是
3
A.L 处与L 处反应①的平衡常数K相等
4 5
B.反应②的焓变∆H >0
2
C.L 处的H O的体积分数大于L 处
6 2 5
D.混合气从起始到通过L 处,CO的生成速率小于CH OH的生成速率
1 3
二、解答题
14.回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
(1)钕铁硼在空气中焙烧转化为Nd O 、Fe O 等(忽略硼的化合物),用0.4mol⋅L−1盐酸酸浸后过滤得到NdCl 溶液和
2 3 2 3 3
浸出液中某元素的物质的量
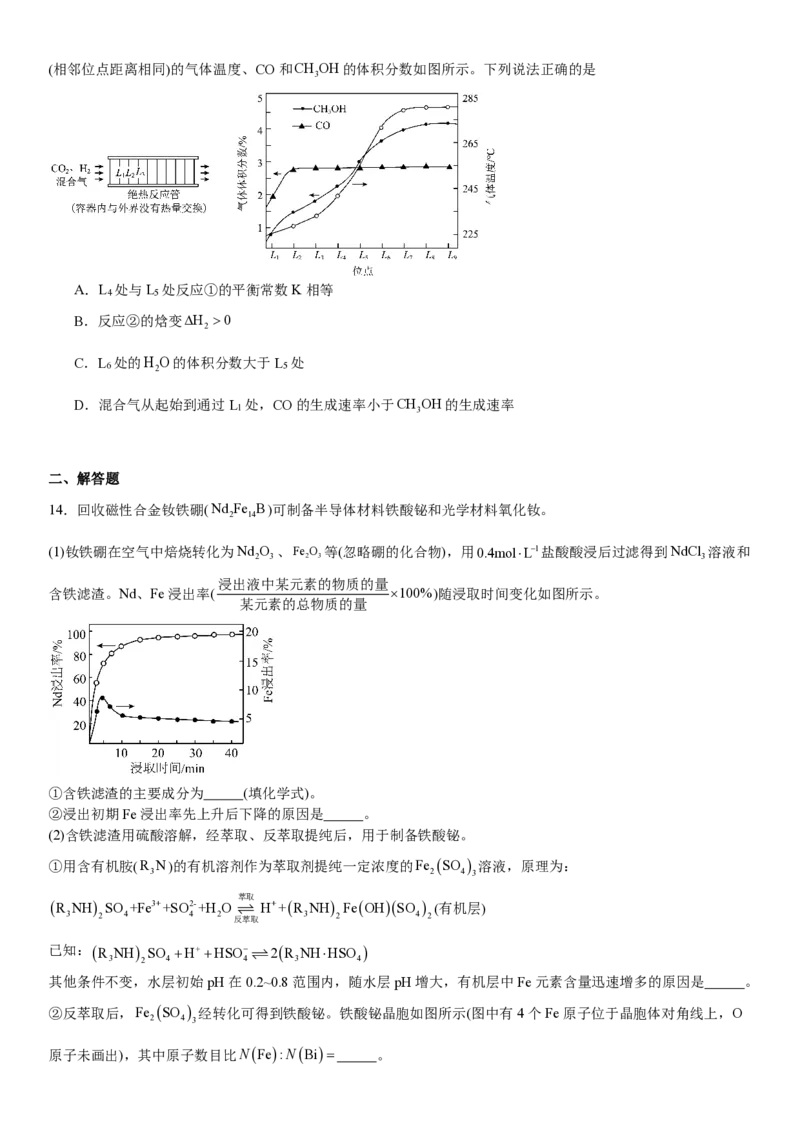
含铁滤渣。Nd、Fe浸出率( ×100%)随浸取时间变化如图所示。
某元素的总物质的量
①含铁滤渣的主要成分为 (填化学式)。
②浸出初期Fe浸出率先上升后下降的原因是 。
(2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
①用含有机胺(R N)的有机溶剂作为萃取剂提纯一定浓度的Fe (SO ) 溶液,原理为:
3 2 4 3
萃取
(R NH) SO +Fe3++SO2-+H O H++(R NH) Fe(OH)(SO ) (有机层)
3 2 4 4 2 反萃取 3 2 4 2
已知:(R NH) SO +H+ +HSO−2(R NH⋅HSO )
3 2 4 4 3 4
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多的原因是 。
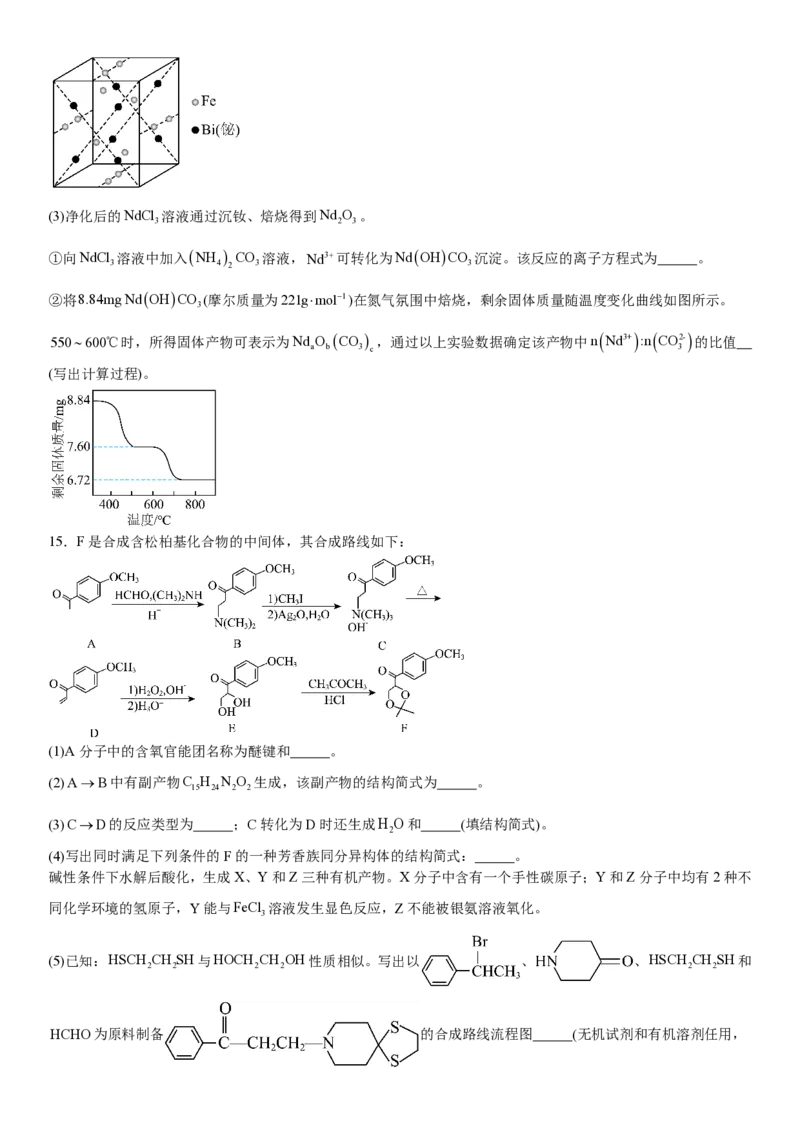
②反萃取后,Fe (SO ) 经转化可得到铁酸铋。铁酸铋晶胞如图所示(图中有4个Fe原子位于晶胞体对角线上,O
2 4 3
原子未画出),其中原子数目比N(Fe):N(Bi)= 。(3)净化后的NdCl 溶液通过沉钕、焙烧得到Nd O 。
3 2 3
①向NdCl 溶液中加入(NH ) CO 溶液,Nd3+可转化为Nd(OH)CO 沉淀。该反应的离子方程式为 。
3 4 2 3 3
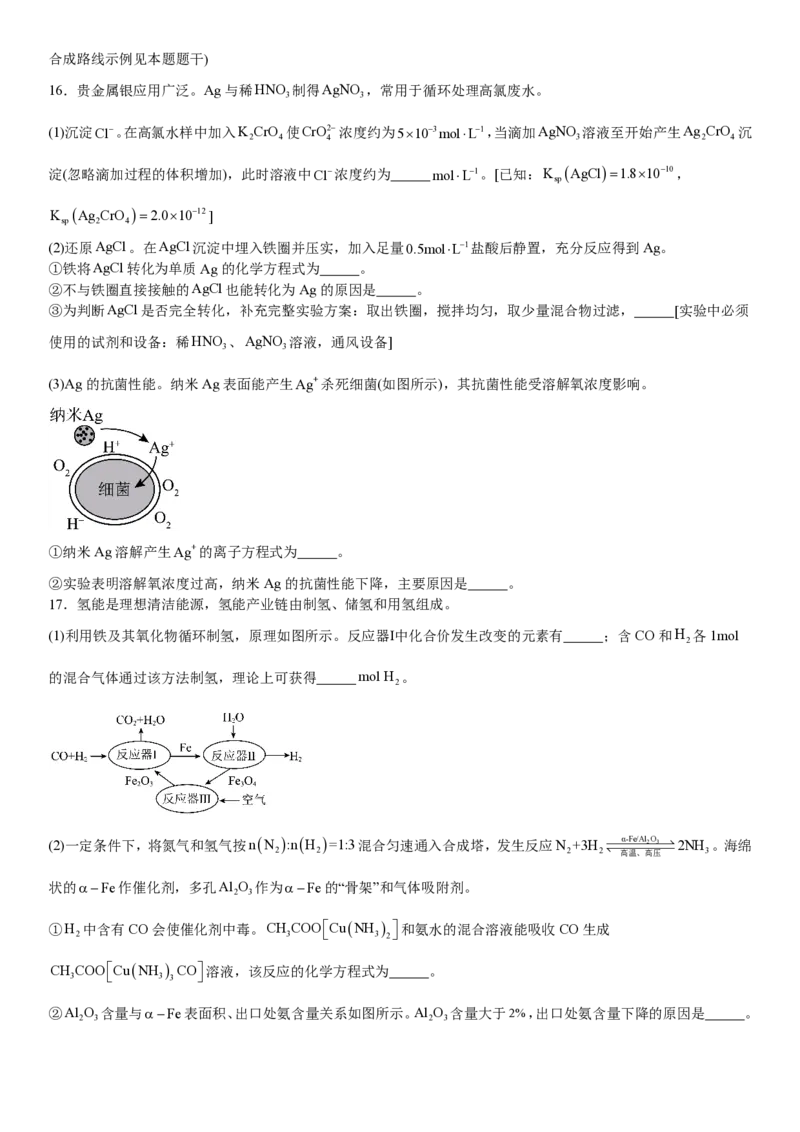
②将8.84mg Nd(OH)CO (摩尔质量为221g⋅mol−1)在氮气氛围中焙烧,剩余固体质量随温度变化曲线如图所示。
3
550∼600℃时,所得固体产物可表示为Nd O (CO ) ,通过以上实验数据确定该产物中n ( Nd3+) :n ( CO2-) 的比值
a b 3 c 3
(写出计算过程)。
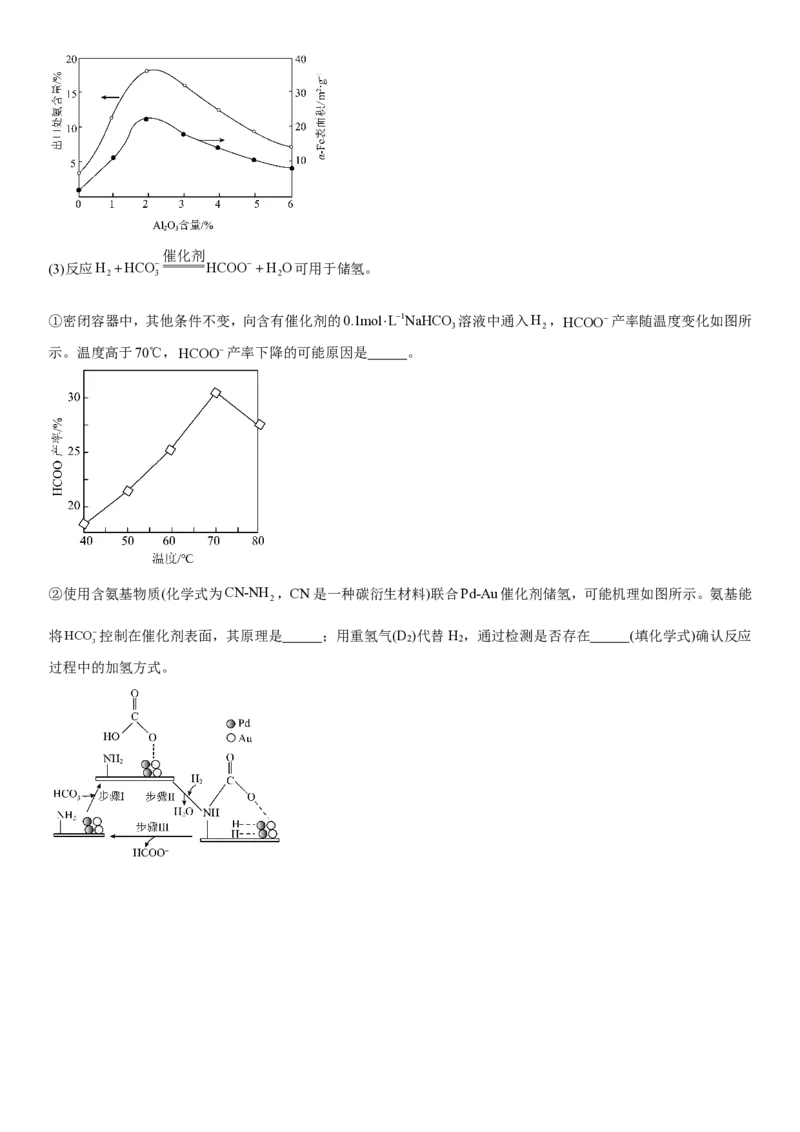
15.F是合成含松柏基化合物的中间体,其合成路线如下:
(1)A分子中的含氧官能团名称为醚键和 。
(2)A→B中有副产物C H N O 生成,该副产物的结构简式为 。
15 24 2 2
(3)C→D的反应类型为 ;C转化为D时还生成H O和 (填结构简式)。
2
(4)写出同时满足下列条件的F的一种芳香族同分异构体的结构简式: 。
碱性条件下水解后酸化,生成X、Y和Z三种有机产物。X分子中含有一个手性碳原子;Y和Z分子中均有2种不
同化学环境的氢原子,Y能与FeCl 溶液发生显色反应,Z不能被银氨溶液氧化。
3
(5)已知:HSCH CH SH与HOCH CH OH性质相似。写出以 、 、HSCH CH SH和
2 2 2 2 2 2
HCHO为原料制备 的合成路线流程图 (无机试剂和有机溶剂任用,合成路线示例见本题题干)
16.贵金属银应用广泛。Ag与稀HNO 制得AgNO ,常用于循环处理高氯废水。
3 3
(1)沉淀Cl−。在高氯水样中加入K CrO 使CrO2−浓度约为5×10−3mol⋅L−1,当滴加AgNO 溶液至开始产生Ag CrO 沉
2 4 4 3 2 4
淀(忽略滴加过程的体积增加),此时溶液中Cl−浓度约为 mol⋅L−1。[已知:K (AgCl)=1.8×10−10,
sp
K (Ag CrO )=2.0×10−12]
sp 2 4
(2)还原AgCl。在AgCl沉淀中埋入铁圈并压实,加入足量0.5mol⋅L−1盐酸后静置,充分反应得到Ag。
①铁将AgCl转化为单质Ag的化学方程式为 。
②不与铁圈直接接触的AgCl也能转化为Ag的原因是 。
③为判断AgCl是否完全转化,补充完整实验方案:取出铁圈,搅拌均匀,取少量混合物过滤, [实验中必须
使用的试剂和设备:稀HNO 、AgNO 溶液,通风设备]
3 3
(3)Ag的抗菌性能。纳米Ag表面能产生Ag+杀死细菌(如图所示),其抗菌性能受溶解氧浓度影响。
①纳米Ag溶解产生Ag+的离子方程式为 。
②实验表明溶解氧浓度过高,纳米Ag的抗菌性能下降,主要原因是 。
17.氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
(1)利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有 ;含CO和H 各1mol
2
的混合气体通过该方法制氢,理论上可获得 mol H 。
2
(2)一定条件下,将氮气和氢气按n(N ):n(H )=1:3混合匀速通入合成塔,发生反应N +3H α-F e/A l2 O32NH 。海绵
2 2 2 2 高温、高压 3
状的α−Fe作催化剂,多孔Al O 作为α−Fe的“骨架”和气体吸附剂。
2 3
①H
2
中含有CO会使催化剂中毒。CH
3
COO
Cu(NH
3
)
2
和氨水的混合溶液能吸收CO生成
CH
3
COO
Cu(NH
3
)
3
CO
溶液,该反应的化学方程式为 。
②Al O 含量与α−Fe表面积、出口处氨含量关系如图所示。Al O 含量大于2%,出口处氨含量下降的原因是 。
2 3 2 3催化剂
(3)反应H +HCO− HCOO−+H O可用于储氢。
2 3 2
①密闭容器中,其他条件不变,向含有催化剂的0.1mol⋅L−1NaHCO 溶液中通入H ,HCOO−产率随温度变化如图所
3 2
示。温度高于70℃,HCOO−产率下降的可能原因是 。
②使用含氨基物质(化学式为CN-NH ,CN是一种碳衍生材料)联合Pd-Au催化剂储氢,可能机理如图所示。氨基能
2
将HCO
3
−控制在催化剂表面,其原理是 ;用重氢气(D
2
)代替H
2
,通过检测是否存在 (填化学式)确认反应
过程中的加氢方式。