文档内容
2024年高考河北卷化学试题
一、单选题
1.燕赵大地历史悠久,文化灿烂。对下列河北博物院馆藏文物的说法错误的是
A.青铜铺首主要成分是铜锡合金 B.透雕白玉璧主要成分是硅酸盐
C.石质浮雕主要成分是碳酸钙 D.青花釉里红瓷盖罐主要成分是硫酸钙
【答案】D
【详解】A.青铜铺首是青铜器,青铜的主要成分是铜锡合金,A正确;
B.透雕白玉璧是玉石,玉石的主要成分是硅酸盐,B正确;
C.石质浮雕是汉白玉,汉白玉的主要成分是碳酸钙,C正确;
D.青花釉里红瓷盖罐是陶瓷,陶瓷的主要成分是硅酸盐,D错误;
故选D。
2.关于实验室安全,下列表述错误的是
A.BaSO 等钡的化合物均有毒,相关废弃物应进行无害化处理
4
B.观察烧杯中钠与水反应的实验现象时,不能近距离俯视
C.具有 标识的化学品为易燃类物质,应注意防火
D.硝酸具有腐蚀性和挥发性,使用时应注意防护和通风
【答案】A
【详解】A.BaSO 性质稳定,不溶于水和酸,可用作“钡餐”说明对人体无害,无毒性,A错误;
4
B.钠与水反应剧烈且放热,观察烧杯中钠与水反应的实验现象时,不能近距离俯视,B正确;
C. 为易燃类物质的标识,使用该类化学品时应注意防火,以免发生火灾,C正确;
D.硝酸具有腐蚀性和挥发性,使用时应注意防护和通风,D正确;
故选A。
3.高分子材料在生产、生活中得到广泛应用。下列说法错误的是
A.线型聚乙烯塑料为长链高分子,受热易软化
B.聚四氟乙烯由四氟乙烯加聚合成,受热易分解
C.尼龙66由己二酸和己二胺缩聚合成,强度高、韧性好
D.聚甲基丙烯酸酯(有机玻璃)由甲基丙烯酸酯加聚合成,透明度高
【答案】B
【详解】A.线型聚乙烯塑料具有热塑性,受热易软化,A正确;
B.聚四氟乙烯由四氟乙烯加聚合成,具有一定的热稳定性,受热不易分解,B错误;
C.尼龙66即聚己二酰己二胺,由己二酸和己二胺缩聚合成,强度高、韧性好,C正确;
D.聚甲基丙烯酸酯由甲基丙烯酸酯加聚合成,又名有机玻璃,说明其透明度高,D正确;
故选B。
4.超氧化钾(KO )可用作潜水或宇航装置的CO 吸收剂和供氧剂,反应为4KO +2CO =2K CO +3O ,N 为阿伏加德
2 2 2 2 2 3 2 A
罗常数的值。下列说法正确的是
A.44gCO 中σ键的数目为2N
2 AB.1molKO 晶体中离子的数目为3N
2 A
C. 溶液中 的数目为
1L1mol⋅L-1K CO CO2- N
2 3 3 A
D.该反应中每转移1mol电子生成O 的数目为1.5N
2 A
【答案】A
【详解】A.44g(即1mol)CO 中σ键的数目为2N ,A正确;
2 A
B. 由 和 构成, 晶体中离子的数目为 ,B错误;
KO K+ O- 1mol KO 2N
2 2 2 A
C. 在水溶液中会发生水解: ,故 溶液中 的数目小于 ,C错
CO
3
2- CO
3
2-+H
2
O
⇌
HCO
3
-+OH- 1L1mol⋅L-1K
2
CO
3
CO
3
2- N
A
误;
D.该反应中部分氧元素化合价由-0.5价升至0价,部分氧元素化合价由-0.5价降至-2价,则每4mol KO 参加
2
反应转移3mol电子,每转移1mol电子生成O 的数目为N ,D错误;
2 A
故选A。
5.化合物X是由细菌与真菌共培养得到的一种天然产物,结构简式如图。下列相关表述错误的是
A.可与Br 发生加成反应和取代反应 B.可与FeCl 溶液发生显色反应
2 3
C.含有4种含氧官能团 D.存在顺反异构
【答案】D
【详解】A.化合物X中存在碳碳双键,能和Br 发生加成反应,苯环连有酚羟基,下方苯环上酚羟基邻位有氢原
2
子,可以与Br 发生取代反应,A正确;
2
B.化合物X中有酚羟基,遇FeCl 溶液会发生显色反应,B正确;
3
C.化合物X中含有酚羟基、醛基、酮羰基、醚键4种含氧官能团,C正确;
D.该化合物中只有一个碳碳双键,其中一个双键碳原子连接的2个原子团都是甲基,所以不存在顺反异构,D错
误;
故选D。
6.下列实验操作及现象能得出相应结论的是
选
实验操作及现象 结论
项
A 还原铁粉与水蒸气反应生成的气体点燃后有爆鸣声 H O具有还原性
2
B 待测液中滴加BaCl 溶液,生成白色沉淀 待测液含有SO2-
2 4
Mg(OH) 和Al(OH) 中均分别加入NaOH溶液和盐酸,Mg(OH) 只溶于
C 2 3 2 Mg(OH) 比Al(OH) 碱性强
盐酸,Al(OH) 都能溶 2 3
3
增大生成物的浓度,平衡向逆反应
D K Cr O 溶液中滴加NaOH溶液,溶液由橙色变为黄色
2 2 7 方向移动
A.A B.B C.C D.D
【答案】C
【详解】A.铁与水蒸气反应生成的气体是H ,该反应中H由+1价变成0价,被还原,体现了H O的氧化性,A错
2 2误;
B.如果待测液中含有 , 与 反应也能产生白色沉淀,或者 、 也会与Ba2+产生白色沉淀,所以
Ag+ Ag+ Cl- CO2- SO2-
3 3
通过该实验不能得出待测液中含有 的结论,B错误;
SO2-
4
C.Mg(OH) 溶液能与盐酸反应,不能与NaOH溶液反应,Al(OH) 与NaOH溶液和盐酸都能反应,说明Mg(OH) 的
2 3 2
碱性比Al(OH) 的强,C正确;
3
D. 溶液中存在平衡 (橙色) (黄色) ,加入 溶液后, 与 反应,生成物浓
K
2
Cr
2
O
7
Cr
2
O
7
2- +H
2
O
⇌
2CrO2
4
- +2H+ NaOH OH- H+
度减小,使平衡正向移动,导致溶液由橙色变为黄色,题给结论错误,D错误;
故选C。
7.侯氏制碱法工艺流程中的主反应为QR+YW +XZ +W Z=QWXZ +YW R,其中W、X、Y、Z、Q、R分别代表相关
3 2 2 3 4
化学元素。下列说法正确的是
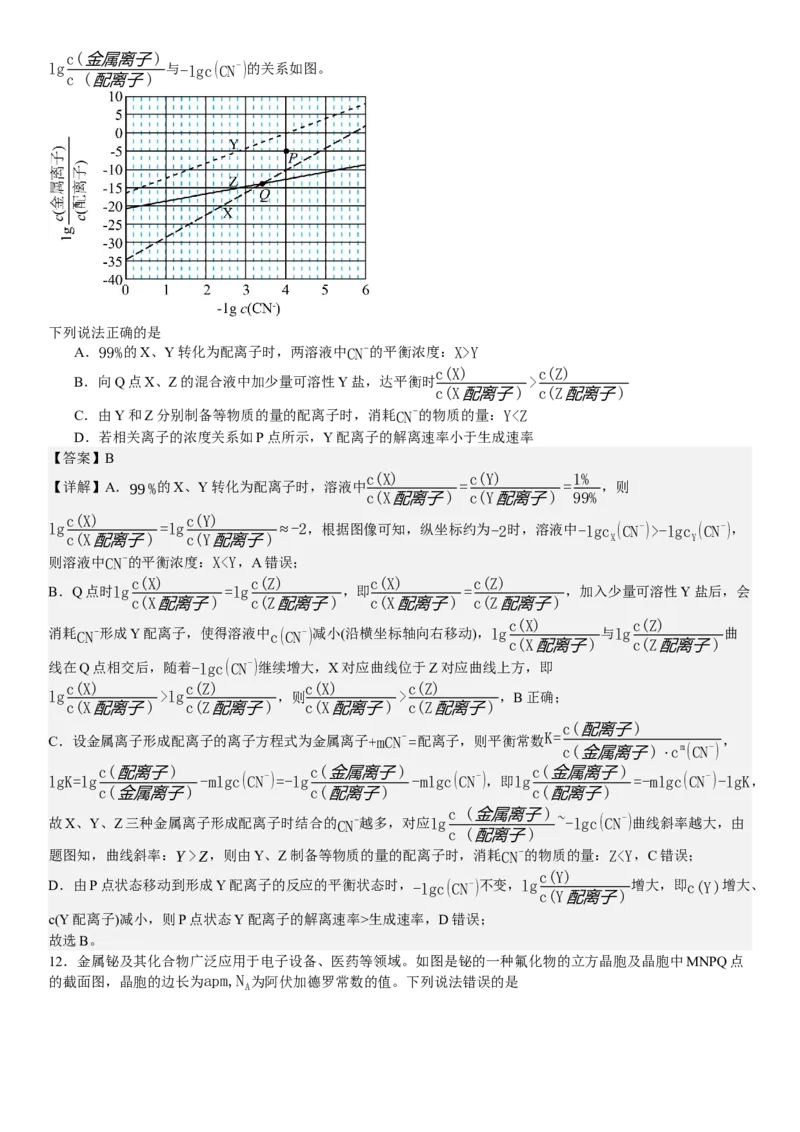
A.原子半径:WY
c(X) c(Z)
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时 >
c(X配离子) c(Z配离子)
C.由Y和Z分别制备等物质的量的配离子时,消耗CN-的物质的量:Y-lgc (CN-),
c(X配离子) c(Y配离子) X Y
则溶液中CN-的平衡浓度:Xlg ,则 > ,B正确;
c(X配离子) c(Z配离子) c(X配离子) c(Z配离子)
c(配离子)
C.设金属离子形成配离子的离子方程式为金属离子+mCN-=配离子,则平衡常数K= ,
c(金属离子)⋅cm(CN-)
c(配离子) c(金属离子) c(金属离子)
lgK=lg -mlgc(CN-)=-lg -mlgc(CN-),即lg =-mlgc(CN-)-lgK,
c(金属离子) c(配离子) c(配离子)
c (金属离子)
故X、Y、Z三种金属离子形成配离子时结合的CN-越多,对应lg ~-lgc(CN-)曲线斜率越大,由
c (配离子)
题图知,曲线斜率:Y>Z,则由Y、Z制备等物质的量的配离子时,消耗CN-的物质的量:Z生成速率,D错误;
故选B。
12.金属铋及其化合物广泛应用于电子设备、医药等领域。如图是铋的一种氟化物的立方晶胞及晶胞中MNPQ点
的截面图,晶胞的边长为apm,N 为阿伏加德罗常数的值。下列说法错误的是
AA.该铋氟化物的化学式为BiF
3
√11
B.粒子S、T之间的距离为 apm
4
1064
C.该晶体的密度为
g⋅cm-3
N ×a3×10-30
A
D.晶体中与铋离子最近且等距的氟离子有6个
【答案】D
1 1 1
【详解】A.根据题给晶胞结构,由均摊法可知,每个晶胞中含有1+12× =4个Bi3+,含有8+8× +6× =12个
4 8 2
F-,故该铋氟化物的化学式为BiF ,A正确;
3
B.将晶胞均分为8个小立方体,由晶胞中MNPQ点的截面图可知,晶胞体内的8个F-位于8个小立方体的体心,
以M为原点建立坐标系,令N的原子分数坐标为(0,0,1),与Q、M均在同一条棱上的F-的原子分数坐标为
1 1 1 1 3
(1,0,0),则T的原子分数坐标为(1, , ), S的原子分数坐标为( , , ),所以粒子S、T之间的距离为
2 2 4 4 4
√
(1-
1
)
2
+(
1
-
1
)
2
+(
1
-
3
)
2
×apm=
√11
apm
,B正确;
4 2 4 2 4 4
m
C.由A项分析可知,每个晶胞中有4个Bi3+、12个F-,晶胞体积为(apm)3=a3×10-30cm3,则晶体密度为ρ= =
V
4×(209+19×3)
g⋅cm-3=
1064
g⋅cm-3
,C正确;
N ×a3×10-30 N ×a3×10-30
A A
D.以晶胞体心处铋离子为分析对象,距离其最近且等距的氟离子位于晶胞体内,为将晶胞均分为8个小立方体后,
每个小立方体的体心的F-,即有8个,D错误;
故选D。
我国科技工作者设计了如图所示的可充电Mg-CO 电池,以Mg(TFSI) 为电解质,电解液中加入1,3-丙二胺(PDA)
2 2
以捕获CO ,使放电时CO 还原产物为MgC O 。该设计克服了MgCO 导电性差和释放CO 能力差的障碍,同时改善了
2 2 2 4 3 2
Mg2+的溶剂化环境,提高了电池充放电循环性能。
回答下列问题。
13.下列说法错误的是
A.放电时,电池总反应为2CO +Mg=MgC O
2 2 4
B.充电时,多孔碳纳米管电极与电源正极连接C.充电时,电子由Mg电极流向阳极,Mg2+向阴极迁移
D.放电时,每转移1mol电子,理论上可转化1molCO
2
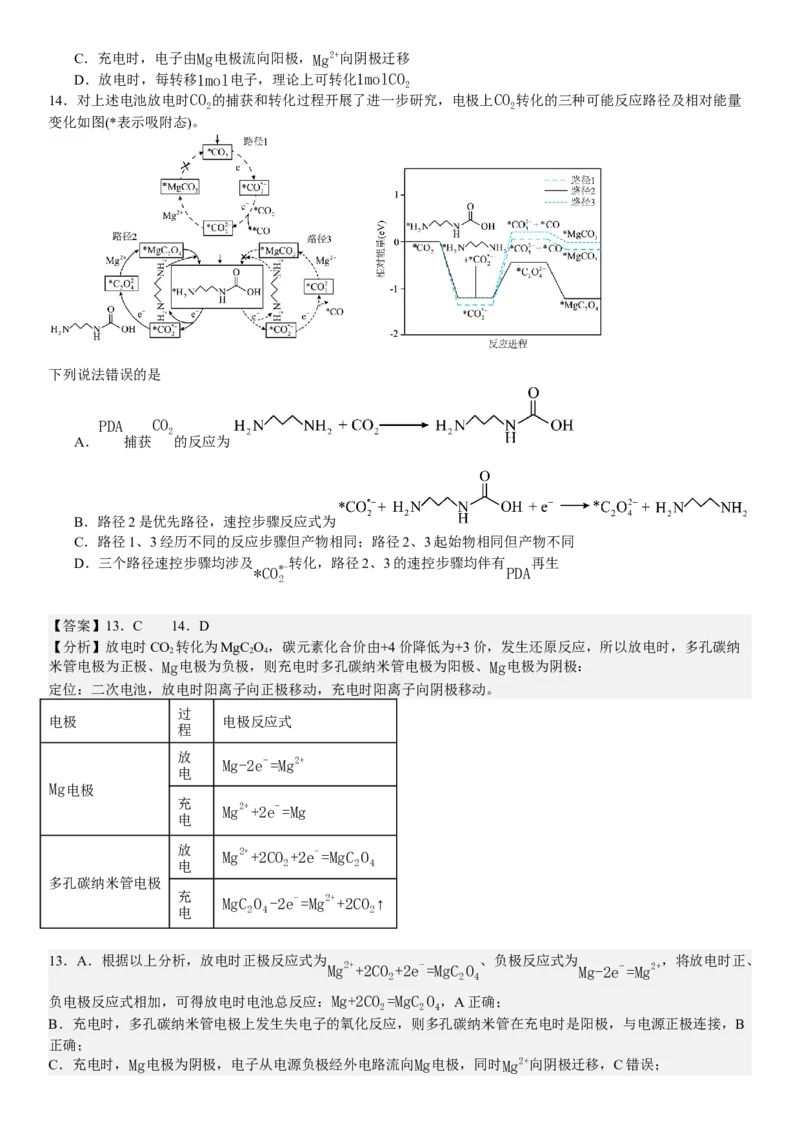
14.对上述电池放电时CO 的捕获和转化过程开展了进一步研究,电极上CO 转化的三种可能反应路径及相对能量
2 2
变化如图(*表示吸附态)。
下列说法错误的是
PDA CO
2
A. 捕获 的反应为
B.路径2是优先路径,速控步骤反应式为
C.路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D.三个路径速控步骤均涉及 转化,路径2、3的速控步骤均伴有 再生
*CO*- PDA
2
【答案】13.C 14.D
【分析】放电时CO 转化为MgC O,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,多孔碳纳
2 2 4
米管电极为正极、Mg电极为负极,则充电时多孔碳纳米管电极为阳极、Mg电极为阴极:
定位:二次电池,放电时阳离子向正极移动,充电时阳离子向阴极移动。
过
电极 电极反应式
程
放
Mg-2e-=Mg2+
电
Mg电极
充
Mg2++2e-=Mg
电
放 Mg2++2CO +2e-=MgC O
电 2 2 4
多孔碳纳米管电极
充 MgC O -2e-=Mg2++2CO ↑
电 2 4 2
13.A.根据以上分析,放电时正极反应式为 、负极反应式为 ,将放电时正、
Mg2++2CO +2e-=MgC O Mg-2e-=Mg2+
2 2 4
负电极反应式相加,可得放电时电池总反应:Mg+2CO =MgC O ,A正确;
2 2 4
B.充电时,多孔碳纳米管电极上发生失电子的氧化反应,则多孔碳纳米管在充电时是阳极,与电源正极连接,B
正确;
C.充电时,Mg电极为阴极,电子从电源负极经外电路流向Mg电极,同时Mg2+向阴极迁移,C错误;D.根据放电时的电极反应式 可知,每转移 电子,有 参与反应,因此每转
Mg2++2CO +2e-=MgC O 2mol 2mol CO
2 2 4 2
移1mol电子,理论上可转化1molCO ,D正确;
2
故选C。
PDA CO PDA CO
2 2
14.A.根据题给反应路径图可知, (1,3-丙二胺)捕获 的产物为 ,因此 捕获 的反
应为 ,A正确;
B.由反应进程-相对能量图可知,路径2的最大能垒最小,因此与路径1和路径3相比,路径2是优先路径,且
*CO*-→*C O2-
2 2 4
路径2的最大能垒为 的步骤,据反应路径2的图示可知,该步骤有 参与反应,
因此速控步骤反应式为 ,B正确;
C.根据反应路径图可知,路径1、3的中间产物不同,即经历了不同的反应步骤,但产物均为*MgCO ,而路径
3
*MgC O *MgCO
2 4 3
2、3的起始物均为 ,产物分别为 和 ,C正确;
D.根据反应路径与相对能量的图像可知,三个路径的速控步骤中 都参与了反应,且由B项分析可知,路径
*CO*-
2
2的速控步骤伴有 再生,但路径3的速控步骤为 得电子转化为 和 ,没有 的生成,D错误;
PDA *CO*- *CO *CO2- PDA
2 3
故选D。
二、解答题
15.市售的溴(纯度99%)中含有少量的Cl 和I ,某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的
2 2
溴。回答下列问题:
(1)装置如图(夹持装置等略),将市售的溴滴入盛有浓CaBr 溶液的B中,水浴加热至不再有红棕色液体馏出。仪器
2
C的名称为 ;CaBr 溶液的作用为 ;D中发生的主要反应的化学方程式为 。
2
(2)将D中溶液转移至 (填仪器名称)中,边加热边向其中滴加酸化的KMnO 溶液至出现红棕色气体,继续加
4
热将溶液蒸干得固体R。该过程中生成I 的离子方程式为 。
2
(3)利用图示相同装置,将R和K Cr O 固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓
2 2 7
H SO ,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为 和
2 4
。
3
(4)为保证溴的纯度,步骤(3)中K Cr O 固体的用量按理论所需量的 计算,若固体R质量为m克(以KBr计),则需
2 2 7 4称取 (用含m的代数式表示)。
gK Cr O (M=294g⋅mol-1)
2 2 7
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内壁,转移溶
液时用 ,滤液沿烧杯壁流下。
Δ
【答案】(1) 直形冷凝管 除去市售的溴中少量的Cl
2
Br
2
+K
2
C
2
O 4¿2KBr+2CO
2
↑
¿
Δ
(2) 蒸发皿 2MnO
4
-+10I-+16H+ ¿2Mn2++5I +8H O
2 2
¿
(3) 液封 降低温度
(4)0.31m
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处
【分析】市售的溴(纯度99%)中含有少量的Cl 和I,实验利用氧化还原反应原理制备高纯度的溴,市售的溴滴入
2 2
盛有浓CaBr 溶液中,Cl 可与CaBr 发生氧化还原反应而除去,I 与Br 一起蒸馏入草酸钾溶液中,并被草酸钾还
2 2 2 2 2
原为I-、Br-,并向溶液中滴加高锰酸钾溶液氧化I-,加热蒸干得KBr固体,将KBr固体和KCr O 固体混合均匀加
2 2 7
入冷的蒸馏水,同时滴加适量浓HSO ,水浴加热蒸馏,得到的液体分液、干燥、蒸馏,可得高纯度的溴。
2 4
【详解】(1)仪器C为直形冷凝管,用于冷凝蒸气;市售的溴中含有少量的Cl ,Cl 可与CaBr 发生氧化还原反
2 2 2
应而除去;水浴加热时,Br 、I 蒸发进入装置D中,分别与K C O 发生氧化还原反应,
2 2 2 2 4
Δ Δ
Br
2
+K
2
C
2
O 4¿2KBr+2CO
2
↑ 、I
2
+K
2
C
2
O 4¿2KI+2CO
2
↑ ,由于Br 2 为进入D的主要物质,故主要反应的化学方程
¿ ¿
Δ
式为Br
2
+K
2
C
2
O 4¿2KBr+2CO
2
↑ ;
¿
(2)将D中溶液转移至蒸发皿中,边加热边向其中滴加酸化的KMnO 溶液至出现红棕色气体(Br ),即说明KMnO
4 2 4
Δ
已将KI全部氧化,发生反应的离子方程式为2MnO
4
-+10I-+16H+ ¿2Mn2++5I +8H O ;KBr几乎未被氧化,继续加热
2 2
¿
将溶液蒸干所得固体R的主要成分为KBr;
(3)密度Br >H O,D中冷的蒸馏水起到液封的作用,同时冷的蒸馏水温度较低,均可减少溴的挥发;
2 2
m
(4)m克KBr固体的物质的量为 mol,根据转移电子相等可得关系式6KBr~6e-~K Cr O ,则理论上需要
119 2 2 7
1 m 1 m 3
K Cr O 的物质的量为 × mol,实际所需称取K Cr O 的质量为 × mol× ×294g⋅mol-1≈0.31mg;
2 2 7 6 119 2 2 7 6 119 4
(5)趁热过滤的具体操作:漏斗下端管口紧靠烧杯内壁,转移溶液时用玻璃棒引流,玻璃棒下端靠在三层滤纸处,
滤液沿烧杯壁流下。
16.V O 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂从石煤中提取V O 的工艺,
2 5 2 5
具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程如下。已知:i石煤是一种含V O 的矿物,杂质为大量Al O 和少量CaO等;苛化泥的主要成分为
2 3 2 3
CaCO 、NaOH、Na CO 等。
3 2 3
ⅱ高温下,苛化泥的主要成分可与 反应生成偏铝酸盐;室温下,偏钒酸钙 和偏铝酸钙均难溶于水。
Al O [Ca(VO ) ]
2 3 3 2
回答下列问题:
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生的气体①为
(填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为 (填化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为 ;CO 加压导入盐浸工序可提高
2
浸出率的原因为 ;浸取后低浓度的滤液①进入 (填工序名称),可实现钒元素的充分利用。
(4)洗脱工序中洗脱液的主要成分为 (填化学式)。
(5)下列不利于沉钒过程的两种操作为 (填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低NH Cl溶液的浓度
4
【答案】(1) 3d34s2 +5 CO
2
(2)NaAlO
2
65~70℃
(3) HCO
3
-+OH-+Ca(VO
3
) 2¿CaCO
3
+H
2
O+2VO
3
- 提高溶液中HCO
3
-浓度,促使偏钒酸钙转化为碳酸钙,释放
¿
离子交换
VO-
3
(4)NaCl
(5)bd
【分析】石煤和苛化泥通入空气进行焙烧,反应生成NaVO 、Ca(VO ) 、NaAlO 、Ca(AlO ) 、CaO和CO 等,水浸
3 3 2 2 2 2 2
可分离焙烧后的可溶性物质(如NaVO )和不溶性物质[Ca(VO ) 、Ca(AlO ) 等],过滤后滤液进行离子交换、洗脱,
3 3 2 2 2
用于富集和提纯 ,加入氯化铵溶液沉钒,生成 ,经一系列处理后得到VO;滤渣①在 ,
VO- NH VO 2 3 pH≈8
3 4 3
65∼70℃的条件下加入3%NH HCO 溶液进行盐浸,滤渣①中含有钒元素,通过盐浸,使滤渣①中的钒元素进
4 3
入滤液①中,再将滤液①回流到离子交换工序,进行 的富集。
VO-
3
【详解】(1)钒是23号元素,其价层电子排布式为 ;焙烧过程中,氧气被还原, 被氧化生成 ,偏
3d34s2 V O VO-
2 3 3
钒酸盐中钒的化合价为+5价;CaCO 在800°C以上开始分解,生成的气体①为CO 。
3 2
(2)高温下,苛化泥的主要成分与Al O 反应生成偏铝酸钠和偏铝酸钙,偏铝酸钠溶于水,偏铝酸钙难溶于水,
2 3
所以滤液中杂质的主要成分是NaAlO 。
2(3)在弱碱性环境下, 与 和 反应生成 、 和 ,离子方程式为:
Ca(VO ) HCO- OH- CaCO VO- H O
3 2 3 3 3 2
65~70℃
HCO 3 -+OH-+Ca(VO 3 ) 2¿CaCO 3 +H 2 O+2VO 3 -; CO 2 加压导入盐浸工序可提高浸出率,因为C可提高溶液中HCO 3 -浓度,
¿
促使偏钒酸钙转化为碳酸钙,释放 ;滤液①中含有 、 等,且浓度较低,若要利用其中的钒元素,需要通
VO- VO- NH+
3 3 4
过离子交换进行分离、富集,故滤液①应进入离子交换工序。
(4)由离子交换工序中树脂的组成可知,洗脱液中应含有Cl-,考虑到水浸所得溶液中含有Na+,为避免引人其他
杂质离子,且NaCl廉价易得,故洗脱液的主要成分应为NaCl。
(5)a.延长沉钒时间,能使反应更加完全,有利于沉钒,a错误;
b. 呈弱酸性,如果将溶液调至碱性, 与 反应,不利于生成 ,b正确;
NH Cl OH- NH+ NH VO
4 4 4 3
c.搅拌能使反应物更好的接触,提高反应速率,使反应更加充分,有利于沉钒,c错误;
d.降低NH Cl溶液的浓度,不利于生成NH VO ,d正确;
4 4 3
故选bd。
17.氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯
化反应制备。
(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
。
SO (g)+Cl (g)
⇌
SO Cl (g) ΔH=-67.59kJ⋅mol-1
2 2 2 2
①若正反应的活化能为
E kJ⋅mol-1
,则逆反应的活化能
E = kJ⋅mol-1
(用含
E
正的代数式表示)。
正 逆 正
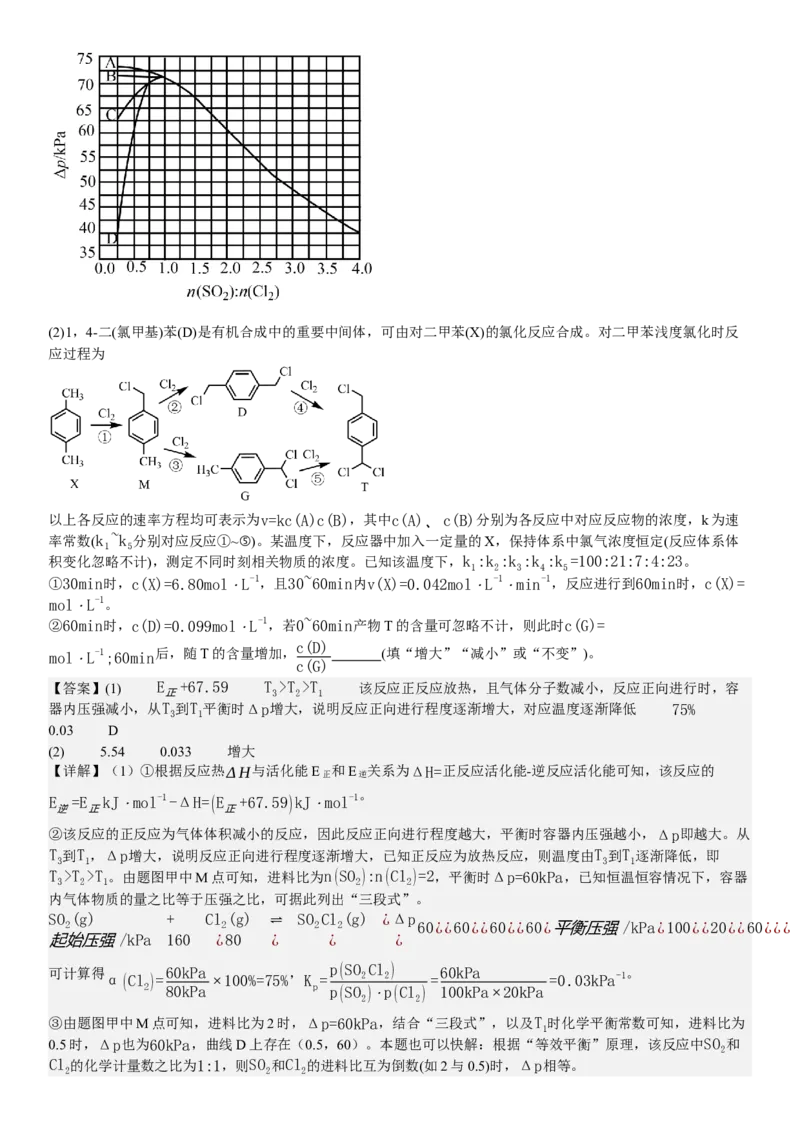
②恒容密闭容器中按不同进料比充入SO (g)和其Cl (g),测定T 、T 、T 温度下体系达平衡时的Δp(
2 2 1 2 3
Δp=p -p,p 为体系初始压强,p =240kPa,P为体系平衡压强),结果如图。
0 0 0
上图中温度由高到低的顺序为 ,判断依据为 。M点Cl 的转化率为 ,T 温度下用分压表示
2 1
的平衡常数K = kPa-1。
p
③下图曲线中能准确表示T 温度下Δp随进料比变化的是 (填序号)。
1(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅度氯化时反
应过程为
以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对应反应物的浓度,k为速
率常数(k ~k 分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度恒定(反应体系体
1 5
积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下,k :k :k :k :k =100:21:7:4:23。
1 2 3 4 5
①30min时,c(X)=6.80mol⋅L-1,且30~60min内v(X)=0.042mol⋅L-1 ⋅min-1,反应进行到60min时,c(X)=
mol⋅L-1。
②60min时,c(D)=0.099mol⋅L-1,若0~60min产物T的含量可忽略不计,则此时c(G)=
c(D)
mol⋅L-1;60min后,随T的含量增加, (填“增大”“减小”或“不变”)。
c(G)
【答案】(1) E +67.59 T >T >T 该反应正反应放热,且气体分子数减小,反应正向进行时,容
正 3 2 1
器内压强减小,从T 到T 平衡时Δp增大,说明反应正向进行程度逐渐增大,对应温度逐渐降低 75%
3 1
0.03 D
(2) 5.54 0.033 增大
【详解】(1)①根据反应热ΔH与活化能E 和E 关系为ΔH=正反应活化能-逆反应活化能可知,该反应的
正 逆
E =E kJ⋅mol-1-ΔH=(E +67.59)kJ⋅mol-1。
逆 正 正
②该反应的正反应为气体体积减小的反应,因此反应正向进行程度越大,平衡时容器内压强越小,Δp即越大。从
T 到T ,Δp增大,说明反应正向进行程度逐渐增大,已知正反应为放热反应,则温度由T 到T 逐渐降低,即
3 1 3 1
T >T >T 。由题图甲中M点可知,进料比为n(SO ):n(Cl )=2,平衡时Δp=60kPa,已知恒温恒容情况下,容器
3 2 1 2 2
内气体物质的量之比等于压强之比,可据此列出“三段式”。
SO
2
(g) + Cl
2
(g)
⇌
SO
2
Cl
2
(g) ¿Δp
60¿¿60¿¿60¿¿60¿平衡压强/kPa¿100¿¿20¿¿60¿¿¿
起始压强/kPa 160 ¿80 ¿ ¿ ¿
可计算得 α(Cl )= 60kPa ×100%=75% , K = p(SO 2 Cl 2 ) = 60kPa =0.03kPa-1。
2 80kPa p p(SO )⋅p(Cl ) 100kPa×20kPa
2 2
③由题图甲中M点可知,进料比为2时,Δp=60kPa,结合“三段式”,以及T 时化学平衡常数可知,进料比为
1
0.5时,Δp也为60kPa,曲线D上存在(0.5,60)。本题也可以快解:根据“等效平衡”原理,该反应中SO 和
2
Cl 的化学计量数之比为1:1,则SO 和Cl 的进料比互为倒数(如2与0.5)时,Δp相等。
2 2 2Δc(X)
(2)①根据化学反应速率的计算公式时,v(X)= ,60min时,
Δt
c(X)=6.80mol⋅L-1-v(X)⋅Δt=6.80mol⋅L-1-0.042mol⋅L-1 ⋅min-1×30min=5.54mol⋅L-1。
Δc(D)
v(D) t Δc(D) v(D) k ⋅c(M) k
②已知 = = ,又由题给反应速率方程推知, = 2 = 2 =3,则
v(G) Δc(G) Δc(G) v(G) k ⋅c(M) k
3 3
t
1
Δc(G)= ×Δc(D)=0.033mol⋅L-1,即60min后c(G)=0.033mol⋅L-1。60min后,D和G转化为T的速率比
3
k ⋅c(D) 4⋅0.099 c(D)
为 4 = ,G消耗得更快,则 增大。
k ⋅c(G) 23⋅0.033 c(G)
5
18.甲磺司特(M)是一种在临床上治疗支气管哮喘、特应性皮炎和过敏性鼻炎等疾病的药物。M的一种合成路线如
下(部分试剂和条件省略)。
回答下列问题:
(1)A的化学名称为 。
(2)B→C的反应类型为 。
(3)D的结构简式为 。
(4)由F生成G的化学方程式为 。
(5)G和H相比,H的熔、沸点更高,原因为 。
(6)K与E反应生成L,新构筑官能团的名称为 。
(7)同时满足下列条件的I的同分异构体共有 种。
(a)核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:2;
C=O
(b)红外光谱中存在 和硝基苯基( )吸收峰。
其中,可以通过水解反应得到化合物H的同分异构体的结构简式为 。
【答案】(1)丙烯酸
(2)加成反应
(3)浓硫酸
→
(4) +HO-NO +H O
2 2
Δ
(5)H分子中存在羟基,能形成分子间氢键
(6)酰胺基
(7) 6
【分析】由流程图可知,A与甲醇发生酯化反应生成B,则A的结构简式为 ;B与CHSH发生加成反
3
应生成C;C在碱性条件下发生酯的水解反应,酸化后生成D,则D的结构简式为 ;D与SOCl
2
发生取代反应生成E;由F的分子式可知,F的结构简式为 ;F发生硝化反应生成G,G的结构简式为 ;
G在一定条件下发生水解反应生成H,H的结构简式为 ;H与 发生取代反应生成I;I与乙醇钠
发生反应生成J;J发生硝基的还原生成K,K的结构简式为 ;K与E发生取代反应生成L;L
与 反应生成M。
【详解】(1)由A→B的反应条件和B的结构简式可知该步骤为酯化反应,因此A为 ,其名称为丙烯
酸。
(2)B与CH SH发生加成反应,—H和—SCH 分别加到双键碳原子上生成C。
3 3
(3)结合C和E的结构简式以及C→D和D→E的反应条件,可知C→D为C先在碱性条件下发生水解反应后酸
化,D为 ,D与亚硫酰氯发生取代反应生成E。
(4)F→G的反应中,结合I的结构可知,苯环上碳氯键的对位引入硝基,浓硫酸作催化剂和吸水剂,吸收反应产
浓硫酸
物中的水,硝化反应的条件为加热,反应的化学方程式是: +HO-NO → +H O。
2 2
Δ
(5)由分析可知,G的结构简式为 ,H的结构简式为 ,H分子中存在羟基,能形成分子间氢键,G分子
不能形成分子间氢键,分子间氢键会使物质的熔、沸点显著升高。
(6)根据分析可知,K与E反应生成L为取代反应,反应中新构筑的官能团为酰胺基。
(7)I的分子式为C H NO ,其不饱和度为6,其中苯环占4个不饱和度,C=O和硝基各占1个不饱和度,因此满
9 9 4
足条件的同分异构体中除了苯环、C=O和硝基之外没有其他不饱和结构。由题给信息,结构中存在“
”,根据核磁共振氢谱中峰面积之比为3:2:2:2可知,结构中不存在羟基、存在甲基,结构高
度对称,硝基苯基和C=O共占用3个O原子,还剩余1个O原子,因此剩余的O原子只能插入两个相邻的C原子
之间。不考虑该O原子,碳骨架的异构有2种,且每种都有3个位置可以插入该O原子,如图:
, (序号表示插入O原子的位置),故符合题意的同
分异构体共有6种。其中,能够水解生成H( )的结构为 。