文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(浙江专用)
黄金卷 02
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35.5 K
39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Br 80 Ag 108 I 127 Ba 137 Pb 207
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列含有离子键的食品添加剂是( )
A.CH COOH B.ZnSO C.SO D.C H O (葡萄糖)
3 4 2 6 12 6
2.下列符号表征或说法不正确的是( )
A.氨的电子式:
B.Cu位于元素周期表的ds区
C.NaHSO 在水中的电离方程式:NaHSO =Na++H++SO 2-
4 4 4
D.SO 的VSEPR模型:
2
3.氯化钠应用广泛,下列说法正确的是( )
A.侯氏制碱法是将足量CO 通入氨化的氯化钠饱和溶液中,析出Na CO 晶体
2 2 3
B.氯碱工业采用阴离子交换膜电解槽电解饱和食盐水获得氯气和氢氧化钠
C.用洗净的铂丝蘸取某样品在酒精灯上灼烧,火焰呈黄色,该样品一定是氯化钠
D.饱和氯化钠溶液能使蛋白质盐析
4.下列有关物质用途的说法正确的是( )
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.葡萄酒中加入二氧化硫,可抗氧化、抑制细菌生长
B.生石灰、铁粉、硅胶是食品行业中常用的干燥剂
C.碳酸氢铵、碳酸氢钠可做食品凝固剂
D.工业上用氢气高温还原二氧化硅制取粗硅
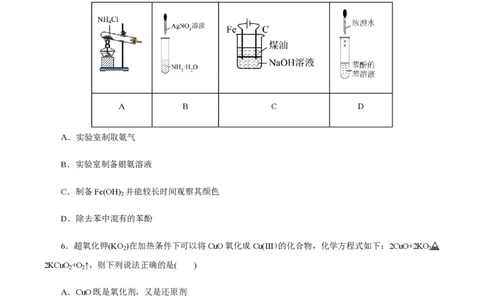
5.下列实验装置能达到实验目的的是( )
A B C D
A.实验室制取氨气
B.实验室制备银氨溶液
C.制备Fe(OH) 并能较长时间观察其颜色
2
D.除去苯中混有的苯酚
6.超氧化钾(KO )在加热条件下可以将CuO氧化成Cu(Ⅲ)的化合物,化学方程式如下:2CuO+2KO
2 2
2KCuO+O↑,则下列说法正确的是( )
2 2
A.CuO既是氧化剂,又是还原剂
B.KCuO 只是氧化产物
2
C.当反应中转移的电子数为0.3N 时,则有0.2 molCuO被氧化
A
D.标准状况下,生成2.24LO 时,被还原的超氧化钾(KO )为0.2mol
2 2
7.N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.0.5mol异丁烷分子中共价键的数目为6.5N
A
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.0.9g水中含有的孤电子对数为0.2N
A
C.2L 1.0mol⋅L−1 AlCl 溶液中,Al3+的数目为2N
3 A
D.标准状况下,2.24L CCl 中的原子总数为0.5N
4 A
8.下化学与生活、生产、科技等息息相关,下列有关说法正确的是( )
A.制造蛟龙号潜艇载人舱的钛合金中的钛属于稀土金属
B.食盐、白糖是常见的食品调味剂,没有防腐作用
C.笔墨纸砚中的“纸”特指宣纸,宣纸的主要成分是蛋白质
D.《本草纲目》记载“凡酸坏之酒,皆可蒸烧”,所用的分离方法是蒸馏
9.下列反应的离子方程式正确的是( )
A.NaHCO 溶液中滴加少量的Ca(OH) 溶液:2HCO -+2OH−+Ca2+=CaCO ↓+CO 2-+2H O
3 2 3 3 3 2
B.向酸性高锰酸钾溶液加入草酸:5C O 2-+2MnO -+16H+=10CO ↑+2Mn2++8H O
2 4 4 2 2
C.CH BrCO18OCH CH 与足量NaOH溶液共热:CH BrCO18OCH CH +OH-
2 2 3 2 2 3
CH BrCOO-+H18OCH CH
2 2 3
D.Ba(NO ) 溶液中通入过量SO :3SO +3Ba2++2NO -+2H O=3BaSO ↓+2NO↑+4H+
3 2 2 2 3 2 4
10.乙醛可发生如下转化,下列说法不正确的是( )
A.乙醛分子中最多5个原子共面
B.X与NaOH的乙醇溶液共热可生成HOCH CHO
2
C.乙醛→Y的反应类型为氧化反应
D.Z的结构简式为CH CH(OH)CH CHO
3 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00211.中国地质科学院地质研究所对嫦娥五号月球玄武岩开展了分析,证明月球在19.6亿年前仍存在岩
浆活动。X、Y、Z、V、W是月核中含有的五种原子序数依次增大的前20号元素,X原子的s能级电子数
量和p能级电子数量相等,V的单质常在地球火山口附近沉积,Y的氧化物常用作耐高温材料。Y、W原子
的最外层电子数相等,且之和等于Z原子的最外层电子数。下列说法正确的是( )
A.Y的氧化物是两性氧化物 B.简单氢化物的稳定性:XZV
C.简单离子半径:WVY D.第一电离能WYZVX
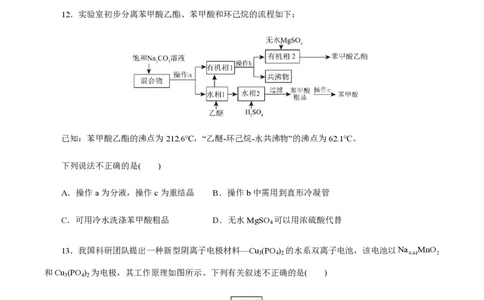
12.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为212.6℃,“乙醚-环己烷-水共沸物”的沸点为62.1℃。
下列说法不正确的是( )
A.操作a为分液,操作c为重结晶 B.操作b中需用到直形冷凝管
C.可用冷水洗涤苯甲酸粗品 D.无水MgSO 可以用浓硫酸代替
4
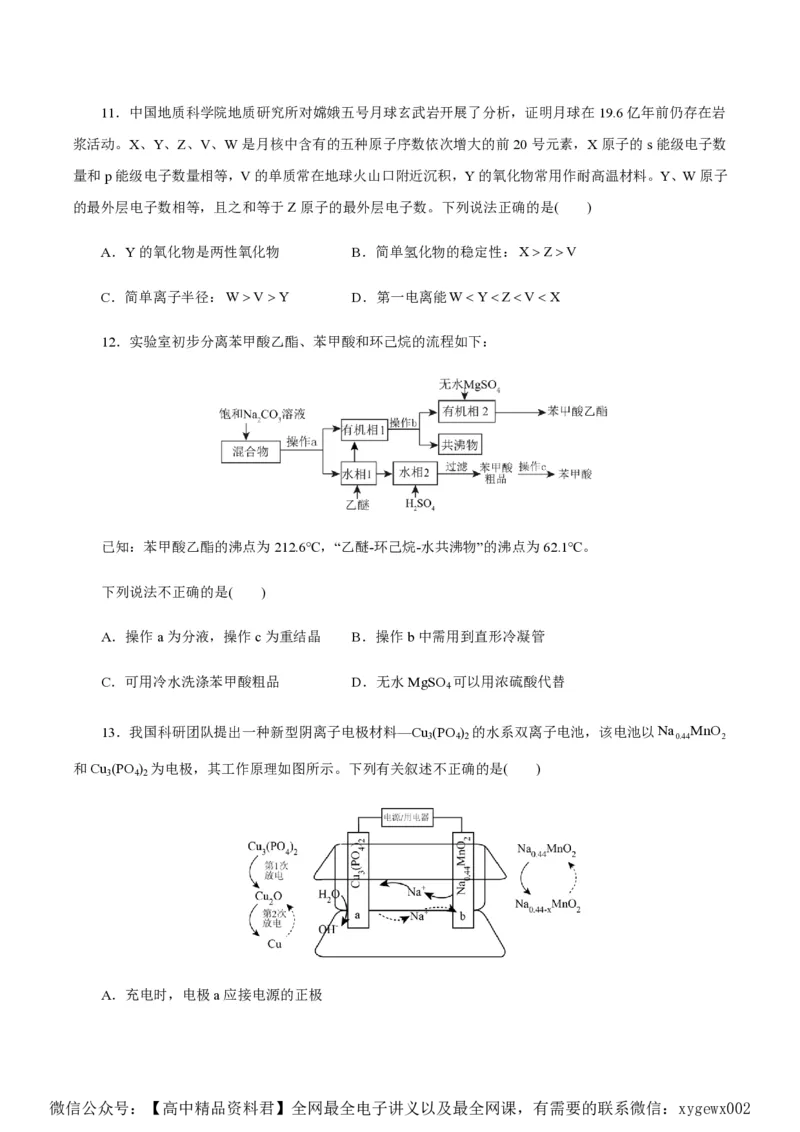
13.我国科研团队提出一种新型阴离子电极材料—Cu (PO ) 的水系双离子电池,该电池以Na MnO
3 4 2 0.44 2
和Cu (PO ) 为电极,其工作原理如图所示。下列有关叙述不正确的是( )
3 4 2
A.充电时,电极a应接电源的正极
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.放电时,若电极a得到6.4g Cu和1.44g Cu O,则电路中转移0.22mol电子
2
C.充电时,电极b的电极反应式为Na MnO +xNa+-xe-=Na MnO
0.44-x 2 0.44 2
D.第2次放电时,溶液碱性逐渐增强
14.25℃时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图
所示:
下列说法不正确的是( )
A.乙醇通过氢键吸附于固体酸分子筛表面并放出热量
B.生成产物2的决速步活化能为60.1 kcal·mol−1
C.生成产物1的热化学方程式为:CH CH OH (l)→CH =CH (g) +H O(l) ΔH=13.8kcal·mol−1
3 2 2 2 2
D.升高温度、延长反应时间及选择合适催化剂均可提高产物1的产率
15.草酸钙是常见的难溶物。将过量草酸钙粉末置于水中达到溶解平衡:CaC O (s) Ca2+ (aq)+
2 4
C O 2- (aq)[已知 K (CaC O )=2.3×10-9,K (CH COOH)=1.75×10-5,H C O 的电离常数 K =5.6×10-2,
2 4 sp 2 4 a 3 2 2 4 a1
K =1.5×10-4,下列有关说法不正确的是( )
a2
A.上层清液中含碳微粒最主要以C O 2-形式存在
2 4
B.上层清液中存在:c(Ca2+)=c(C O 2-)+c(HC O -)+c(H C O )
2 4 2 4 2 2 4
C.H C O 加入CaCl 溶液时,加入适量醋酸钠粉末,有利于生成CaC O 沉淀
2 2 4 2 2 4
D.向上层清液中通入HCl至pH=1,则:2c(Ca2+)-2c(C O 2-)-c(HC O -)- c(OH―)= 0.1mol·L-1
2 4 2 4
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00216.探究铁单质及其化合物的性质,由操作、现象能得出正确结论的是( )
选
操作 现象 结论
项
向2mL 0.1mol·L⁻¹FeCl 溶液加入 2mL
3
A. 出现黄色浑浊 证明 FeCl 和 KI反应存在限度
3
0.01mol·L⁻¹KI溶液,再滴入数滴AgNO 溶液
3
得到黑色固体,该固
将Fe粉与S粉混合在惰性气体中加热,再将
B. 体溶于稀硫酸后得 证明Fe与S生成了FeS
反应后的产物溶于稀硫酸
浅绿色溶液
证明Fe 粉与Fe3⁺反应,降低
向2mL 0.01mol·L⁻¹Fe(SCN) 溶液加入少量
3
C. 溶液的血红色变浅 Fe3⁺浓度,使生成Fe(SCN) 平衡
3
Fe粉,振荡后静置
逆向移动
将SO 气体通入 Fe(NO ) 和BaCl 的混合溶 溶液的棕黄色变浅、
2 3 3 2
D. 白色沉淀为 BaSO
3
液 产生白色沉淀
第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)卤化物、氢化物在科研和生活中占有重要地位。回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s22p5 D.1s22s22p6
(2)OF 的VSEPR模型名称为____________。
2
(3)二氟氮烯(N F )分子中,每个原子均满足八电子稳定结构,则N F 的结构式为____________。
2 2 2 2
(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键
的键能(kJmol1)如下表:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002H C-CH H N-NH HO-OH
3 3 2 2
346 247 207
A-A键的键能依次降低的原因是_______________________________________。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(CH NH PbI )半导体作为吸光材料。CH NH PbI
3 3 3 3 3 3
的晶胞如图所示,其中CH NH +位于顶点(大空心球)位置。已知CH NH PbI 晶体的晶胞参数为a nm,阿佛
3 3 3 3 3
加德罗常数的值为N ,则晶体的密度为____________ g·c m -3。(用最简式表达)
A
18.(10分)烟道气中含有SO ,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质
2
量为184)。
(1)写出NH 的电子式 ;
3
(2)下列叙述正确的是 ;
A.烟道气中的SO 含量可用一定体积、浓度的酸性高锰酸钾溶液测定
2
B.S Cl 是橡胶硫化剂,橡胶硫化程度越高,弹性越好
2 2
C.SOCl 可与H O发生反应,能作为AlCl ·6H O的脱水剂
2 2 3 2
D.PCl 固体中含阳离子PCl +和阴离子PCl -,PCl +空间构型为正四面体
5 4 6 4
E.S Cl 易溶于CCl ,则S Cl 为非极性分子
2 2 4 2 2
(3) SOCl 与过量NH 反应的化学方程式 ;
2 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(4) S Cl 与 NH 反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为 ;
2 2 3
(5)设计实验检验SOCl 与足量NaOH溶液反应生成的阴离子 。
2
19.(10分)低碳烯烃(乙烯、丙烯等)作为化学工业重要基本有机化工原料,在现代石油和化学工业中起
着举足轻重的作用。碘甲烷(CH I)热裂解制低碳烯烃的主要反应有:
3
反应Ⅰ 2 CH I (g) C H (g)+ 2HI(g) ΔH
3 2 4 1
反应Ⅱ 3C H (g) 2C H (g) ΔH
2 4 3 6 2
反应Ⅲ 2C H (g) C H (g) ΔH
2 4 4 8 3
(1)反应Ⅰ、Ⅱ、Ⅲ的H随温度的变化如图1所示。298K下,ΔH = kJ·mol-1。
1
(2)针对反应Ⅰ,利于提高碘甲烷的平衡转化率的条件有 。
A.低温 B.高温 C.低压 D.高压 E.催化剂
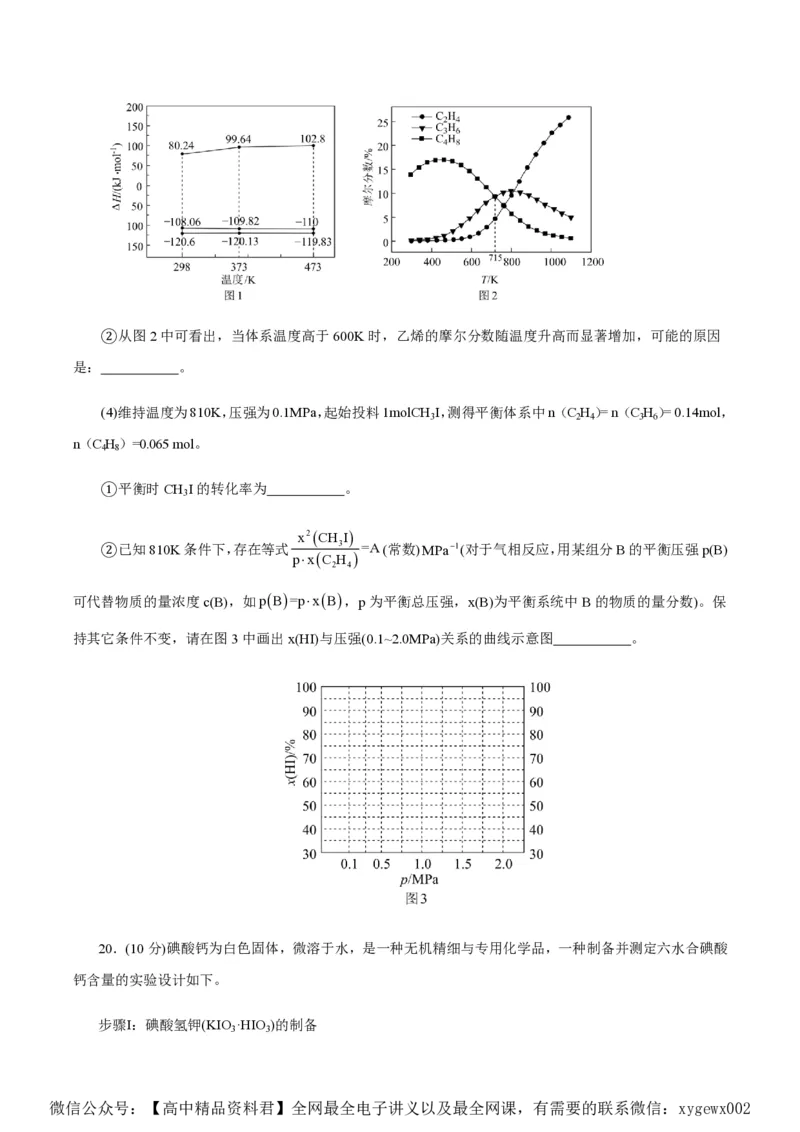
(3)利用计算机模拟反应过程。一定压强条件下,测定反应温度对碘甲烷热裂解制低碳烯烃平衡体系中
乙烯、丙烯和丁烯组成的影响如图2所示。结合图1、图2,回答下列问题:
①下列有关说法正确的是 。
A.因为反应Ⅱ、Ⅲ自发,且为熵减小反应,所以ΔH <0、ΔH <0
2 3
B.若H随温度的上升而增大,则ΔH>0
C.随温度升高,反应Ⅱ、Ⅲ的化学平衡先正向移动后逆向移动
D.当温度范围:T≤715K时,相同条件下的反应Ⅱ的平衡常数小于反应Ⅲ
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002②从图2中可看出,当体系温度高于600K时,乙烯的摩尔分数随温度升高而显著增加,可能的原因
是: 。
(4)维持温度为810K,压强为0.1MPa,起始投料1molCH I,测得平衡体系中n(CH)= n(CH)= 0.14mol,
3 2 4 3 6
n(CH)=0.065 mol。
4 8
①平衡时CH I的转化率为 。
3
x2CH I
②已知810K条件下,存在等式 3 =A(常数)MPa1(对于气相反应,用某组分B的平衡压强p(B)
pxC H
2 4
可代替物质的量浓度c(B),如pB=pxB,p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。保
持其它条件不变,请在图3中画出x(HI)与压强(0.1~2.0MPa)关系的曲线示意图 。
20.(10分)碘酸钙为白色固体,微溶于水,是一种无机精细与专用化学品,一种制备并测定六水合碘酸
钙含量的实验设计如下。
步骤Ⅰ:碘酸氢钾(KIO ·HIO )的制备
3 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002在三颈烧瓶中加入2.54g I 、2.60g氯酸钾和50mL水,滴加6mol/L的盐酸至pH=1,控制温度85℃左右,
2
装置如图。
步骤Ⅱ:碘酸钙晶体[Ca(IO ) ·6H O]的制备
3 2 2
将步骤Ⅰ反应后的溶液转入烧杯中,加入KOH溶液调节pH10;继续滴加11mL1mol/LCaCl 溶液,充
2
分反应后用冰水冷却,抽滤、用少量冰水洗涤、再用少量无水乙醇洗涤,干燥,得粗产品碘酸钙晶体
4.50g。
步骤Ⅲ:产品中碘酸钙晶体含量测定
① 准确称取1.200g粗产品,置于烧杯中,加入20mLHClO 溶解样品,转移到250mL容量瓶中定容。
4
量取25.00mL溶液于碘量瓶中,加入稍过量的KI,然后用0.1000mol/L Na S O 标准溶液滴定至浅黄色,加
2 2 3
入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去25.24mL标准溶液。
②空白实验:不取产品,其余试剂用量和步骤相同,消耗0.04mL Na S O 标准溶液。
2 2 3
已知:Ca(IO ) +2 HClO =2HIO + Ca (ClO ) ,IO -+5I-+6H+=3I +3H O,I +2S O 2-=2I-+S O 2-
3 2 4 3 4 2 3 2 2 2 2 3 4 6
请回答下列问题:
(1)仪器c与普通漏斗相比的优点为 。
(2)步骤1中有黄绿色气体产生,则制备KIO ·HIO ;反应的化学方程式为 ,d中盛放的药品
3 3
是 。(写化学式)
(3)步骤Ⅰ中控制温度85℃左右的原因是 。
(4)步骤Ⅱ中用少量无水乙醇洗涤的目的是 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(5)下列关于滴定分析的操作,不正确的是 。
A.用量筒量取25.00待测液转移至碘量瓶中
B.滴定过程中用少量蒸馏水将锥形瓶内壁附着的溶液冲下
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“零刻度”以下
(6)碘酸钙晶体中Ca(IO ) ·6H O (相对分子质量为498)的纯度为 (计算结果保留两位小数)。
3 2 2
21.(12分)化合物 G是一种生物拮抗剂的前体,它的合成路线如下所示:
请回答:
(1)A的官能团名称是 。
(2)下列说法正确的是___________。
A.化合物B、C 都具有碱性
B.C→D 的反应类型是还原反应
C.已知用甲酸乙酯代替HC(OC H ) 和D反应生成E,推测其限度相对较小
2 5 3
D.化合物G 的分子式是C H ClN
9 8 4
(3)化合物 F的结构简式是 。
(4)已知D→E的反应生成三个相同的小分子,写出化学方程式 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(5)写出同时符合下列条件E的同分异构的结构简式 。
①分子中只含一个苯环、不含其它环
②可以发生银镜反应
③核磁共振氢谱表明分子中有3 种不同化学环境的氢原子
(6)完成以F为原料合成G的路线(用流程图表示,无机试剂任选) 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002