文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(黑龙江、甘肃、吉林、
安徽、江西、贵州、广西)
黄金卷 03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Zn 65 Cu 64 Co 59
第Ⅰ卷
一、单项选择题:共15题,每题3分,共45分。每题只有一个选项最符合题意。
1.化学与科学、技术、社会、生活等密切相关。下列有关说法正确的是
A.用于清洗伤口、杀菌、消毒的医用酒精有强氧化性
B.我国“神舟十二号”飞船返回舱的舱体外壳部件材料是由金属复合材料——专业的铝合金材料制成的,
主要是利用了其硬度大的特性
C.食品袋中放置的CaO可直接防止食品氧化变质
D.客家围屋建造过程中用作黏稠剂的糯米和鸡蛋清都属于混合物
一定条件
2.镁粉在火星上可以扮演地球上煤的角色,反应Mg+CO MgO+CO可以为火星上的采矿
2
车、电站等提供热能。下列关于该反应的说法中,不正确的是
A.属于放热反应 B.反应物的总能量低于生成物的总能量
C.属于氧化还原反应 D.能量变化与化学键的断裂和形成有关
3.下列有关化学用语的叙述错误的是
A.NH 的结构式为 B.CS 的电子式为
3 2
C.简单硫离子的结构示意图为 D.基态N原子的价层电子排布图为
4.下列各组离子在指定溶液中能大量共存的是
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.0.1molL1的NaHCO 溶液中:Al3、K、Cl、SO2
3 4
B.使pH试纸显红色的溶液中:Na、NO、CO2、SO2
3 3 4
C.含有KSCN的溶液中:Fe3、Na、SO2、Cl
4
c
OH
D. 1012的溶液中:Na、K、SO2、ClO
c H 4
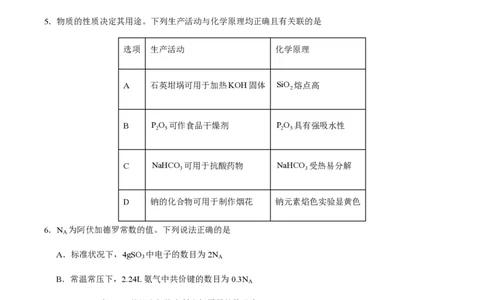
5.物质的性质决定其用途。下列生产活动与化学原理均正确且有关联的是
选项 生产活动 化学原理
A 石英坩埚可用于加热KOH固体 SiO 熔点高
2
B PO 可作食品干燥剂 PO 具有强吸水性
2 5 2 5
C NaHCO 可用于抗酸药物 NaHCO 受热易分解
3 3
D 钠的化合物可用于制作烟花 钠元素焰色实验显黄色
6.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,4gSO 中电子的数目为2N
3 A
B.常温常压下,2.24L氨气中共价键的数目为0.3N
A
C.46gNO 和N O 的混合气体中所含氮原子的数目为1.5N
2 2 4 A
D.常温下,1.0LpH=12的Ba(OH) 溶液中OH-的数目是0.02N
2 A
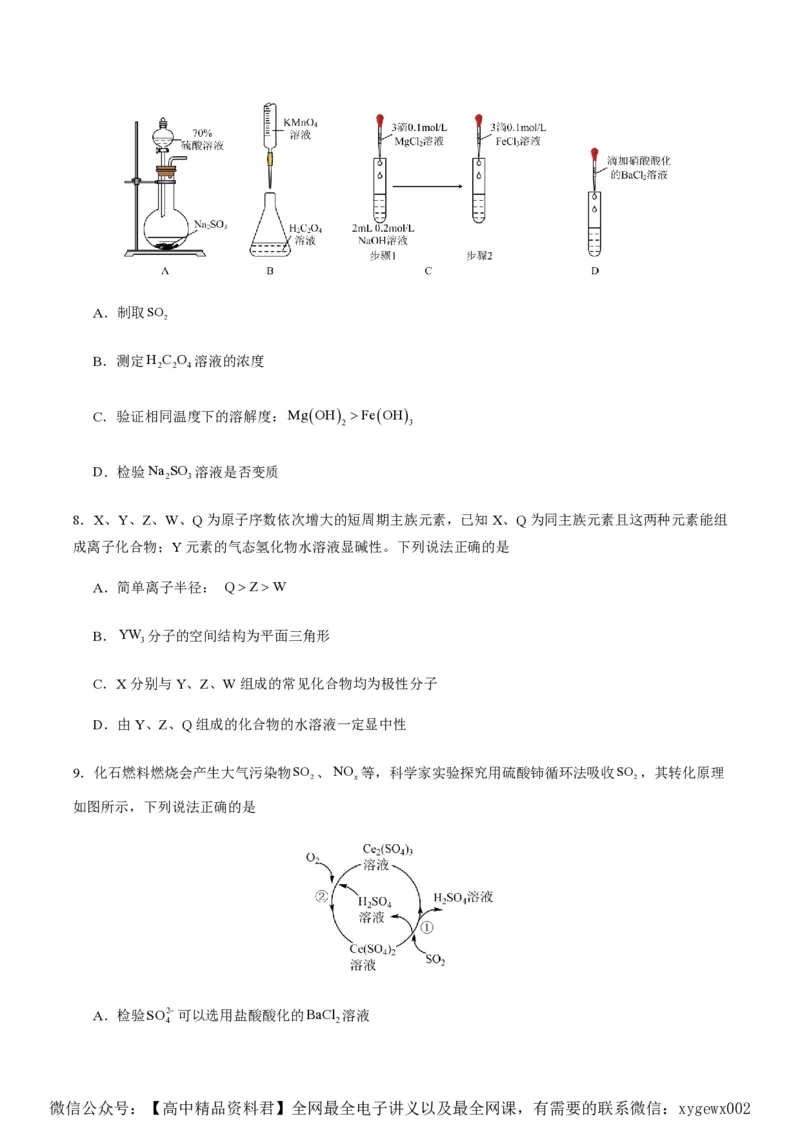
7.下列实验能达到实验目的的是
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.制取SO
2
B.测定H C O 溶液的浓度
2 2 4
C.验证相同温度下的溶解度:MgOH FeOH
2 3
D.检验Na SO 溶液是否变质
2 3
8.X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,已知X、Q为同主族元素且这两种元素能组
成离子化合物;Y元素的气态氢化物水溶液显碱性。下列说法正确的是
A.简单离子半径: QZW
B.YW 分子的空间结构为平面三角形
3
C.X分别与Y、Z、W组成的常见化合物均为极性分子
D.由Y、Z、Q组成的化合物的水溶液一定显中性
9.化石燃料燃烧会产生大气污染物SO 、NO 等,科学家实验探究用硫酸铈循环法吸收SO ,其转化原理
2 x 2
如图所示,下列说法正确的是
A.检验SO2可以选用盐酸酸化的BaCl 溶液
4 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.反应①的离子方程式为2Ce4 SO 2H O2Ce3 SO24H
2 2 4
C.反应②中氧化剂与氧化产物的物质的量之比为1:2
D.理论上每吸收标准状况下224mLSO ,一定消耗0.32gO
2 2
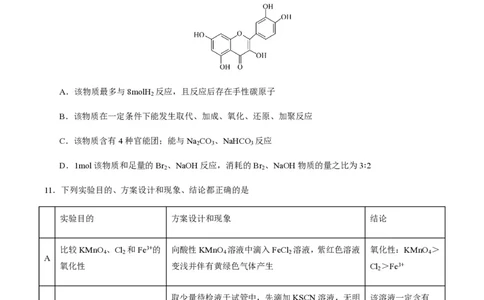
10.槲皮素是植物界广泛分布,具有多种类生物活性的化合物,结构如下图;下列有关该物质的说法不正
确的是
A.该物质最多与8molH 反应,且反应后存在手性碳原子
2
B.该物质在一定条件下能发生取代、加成、氧化、还原、加聚反应
C.该物质含有4种官能团;能与Na CO 、NaHCO 反应
2 3 3
D.1mol该物质和足量的Br 、NaOH反应,消耗的Br 、NaOH物质的量之比为3∶2
2 2
11.下列实验目的、方案设计和现象、结论都正确的是
实验目的 方案设计和现象 结论
比较KMnO 、Cl 和Fe3+的 向酸性KMnO 溶液中滴入FeCl 溶液,紫红色溶液 氧化性:KMnO >
4 2 4 2 4
A
氧化性 变浅并伴有黄绿色气体产生 Cl >Fe3+
2
取少量待检液于试管中,先滴加KSCN溶液,无明 该溶液一定含有
B 检验某溶液中是否含有Fe2+
显变化,再滴加新制氯水,变为红色溶液 Fe2+
比较K (AgCl)、K (AgI)的 向NaCl、NaI混合溶液中滴入少量AgNO 溶液,有 K (AgCl)大于
sp sp 3 sp
C
大小 黄色沉淀生成 K (AgI)
sp
检验某有机物(如图)中含有 取少量待检液于试管中,滴加酸性KMnO 溶液,紫 该有机物中含有醛
4
D
醛基 红色褪去 基
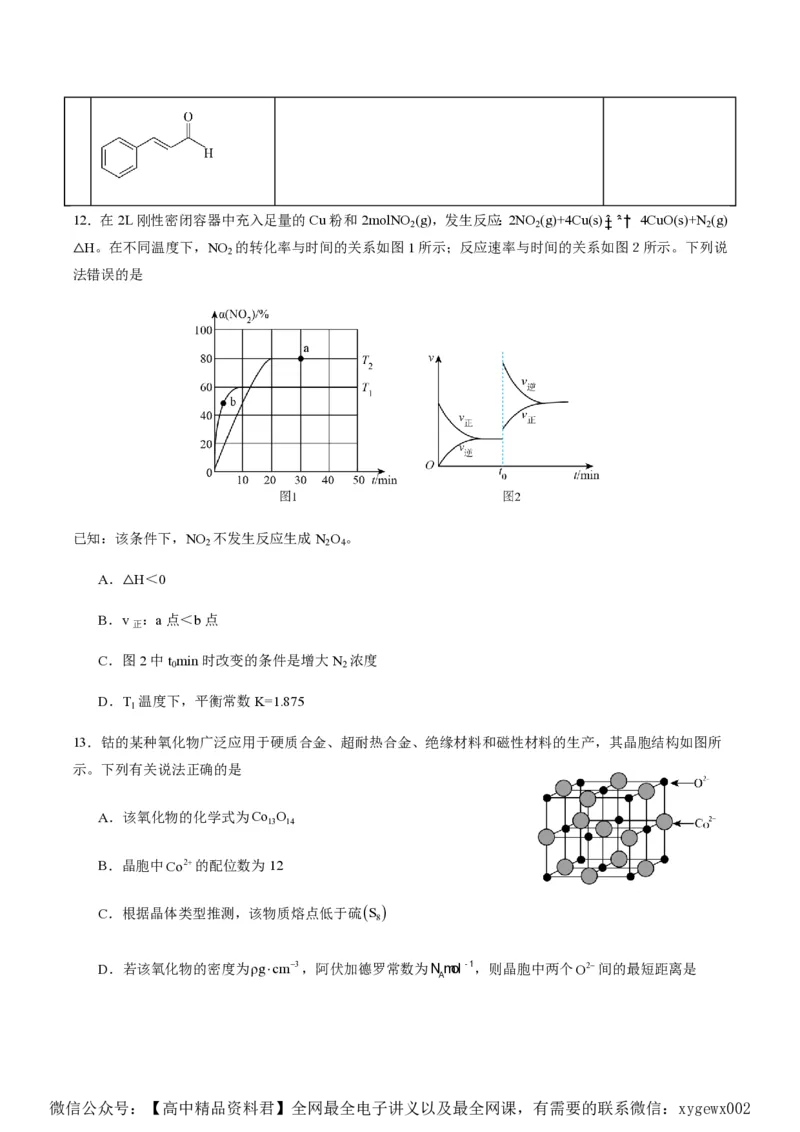
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00212.在2L刚性密闭容器中充入足量的Cu粉和2molNO
2
(g),发生反应:2NO
2
(g)+4Cu(s)‡ˆ ˆˆ†ˆ 4CuO(s)+N
2
(g)
△H。在不同温度下,NO 的转化率与时间的关系如图1所示;反应速率与时间的关系如图2所示。下列说
2
法错误的是
已知:该条件下,NO 不发生反应生成N O 。
2 2 4
A.△H<0
B.v :a点<b点
正
C.图2中t min时改变的条件是增大N 浓度
0 2
D.T 温度下,平衡常数K=1.875
1
13.钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其晶胞结构如图所
示。下列有关说法正确的是
A.该氧化物的化学式为Co O
13 14
B.晶胞中Co2的配位数为12
C.根据晶体类型推测,该物质熔点低于硫S
8
D.若该氧化物的密度为ρgcm3,阿伏加德罗常数为Nmol-1,则晶胞中两个O2间的最短距离是
A
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx0022 300
cm
3
2 ρN
A
14.双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层为水层,装置工作时水层中的H O解离
2
成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇的电解原理如图所示。该装置工作时,下
2
列说法正确的是
A.H+穿过b膜进入右室溶液 B.石墨电极区溶液pH不变
C.催化电极上发生氧化反应 D.电解一段时间后,右室HCO的物质的量减少
15.室温下,将0.1 mol·L1 NaOH溶液滴入10 mL 0.1 mol·L1 HCl和0.1 mol·L1 HA(K 103)的混合溶
a
液,测得混合溶液的pH随滴加的VNaOH的变化关系如图所示。下列说法正确的是
A.a点时,c Cl c A cHA B.b点时,c Cl 0.05 mol·L1
C.c点时,c Na c A cHA D.a→d过程中,水的电离程度大小关系为:c>b>a>d
第Ⅱ卷
二、非选择题:共4题,共55分。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00216.(13分)二氧化氯(ClO )是一种优良的消毒剂,熔点为-59℃,沸点为11℃,浓度过高时易发生分解,
2
甚至爆炸。
Ⅰ.某课外兴趣小组通过氯气与NaClO 溶液反应来制取少量ClO ,装置如图所示:
2 2
(1)丙装置中发生反应的化学方程式为 。
(2)Cl-存在时会催化ClO 的生成,若无乙装置,则丙装置内产生ClO 的速率明显加快。乙装置中试剂瓶
2 2
内的液体是 。实验过程中常需通入适量的N 稀释ClO ,其目的是 。
2 2
(3)戊装置烧杯中NaOH溶液吸收ClO 后,生成了ClO、ClO,该反应的离子方程式是 。
2 2 3
Ⅱ.用右图装置可以测定混合气中ClO 的含量:
2
①在锥形瓶中加入足量的碘化钾-淀粉溶液,用50mL水溶解后,再加入3mL稀硫酸:
②在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
③将一定量的混合气体通入锥形瓶中吸收;
④将玻璃液封装置中的水倒入锥形瓶中:
⑤用0.1000molL1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I 2S O2 2IS O2),指示剂显示终点时
2 2 3 4 6
共用去20.00mL硫代硫酸钠溶液。在此过程中:
(4)玻璃液封装置的作用是 , 。
(5)滴定至终点的现象是 。
(6)测得混合气中ClO 的质量为 g。
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00217.(14分)活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上
用菱锌矿(主要成分为ZnCO ,还含有Ni、Cd、Fe、Cu等元素及少量不溶于成的杂质)制备ZnO,工艺流程
3
图所示:
(1)为了提高“溶浸”效果,可采取的措施有 。(任写一点)
(2)“除铁”时,加入H O 发生反应的离子方程式为 。如果用NaClO 代替H O ,恰好完全反应时,
2 2 3 2 2
理论上消耗n(NaClO ):n(H O )= 。
3 2 2
(3)常温下,“调pH=5”时,Fe3+的浓度降到了8×10-11mol/L,此时Fe(OH) 的溶度积常数的数值
3
为 。
(4)已知三种硫化物的K 如表。当溶液中某离子物质的量浓度≤10-5mol/L时视为沉淀完全。假设原溶液
sp
中Cu2+、Cd2+、Ni2+的物质的量浓度均为0.1mol/L,则在加Na S使Cu2+在溶液中的残留浓度为6.3×10-11mol/L
2
离子的减少量
时,此时Cd2+的去除率为 (去除率= ×100%,不考虑溶液的体积变化)
离子的初始量
物质 CdS CuS NiS
8.0×10-2 6.3×10-3 1.0×10-2
K
sp
7 6 6
(5)“沉锌”时,在近中性条件下加入Na CO 可得碱式碳酸锌[ZnCO •2Zn(OH) •H O]固体,同时产生大量
2 3 3 2 2
的气体。该反应的离子方程式为 。
(6)用锌与铜侧得的高纯铜锌合金滤料被广泛应用于各种水处理设备。一种铜锌合金
的晶胞结构如图,已知:晶胞参数为anm。
①与Zn原子等距离且最近的Zn原子有 个。
②该铜锌合金晶体密度为 g•cm-3(设N 为阿伏加德罗常数的值)
A
18.(14分)甲烷、甲醇(CH OH)、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物, 广泛应用
3
于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(1)已知: HCHO(g )+H (g)=CH OH(g) △H = - 84kJ/mol
2 3 1
CO (g)+ 3H (g)=CH OH(g)+H O(g) △H = - 49.5 kJ/mol
2 2 3 2 2
则反应CO (g)+ 2H (g)=HCHO(g)+H O(g) △H = kJ/mol
2 2 2 3
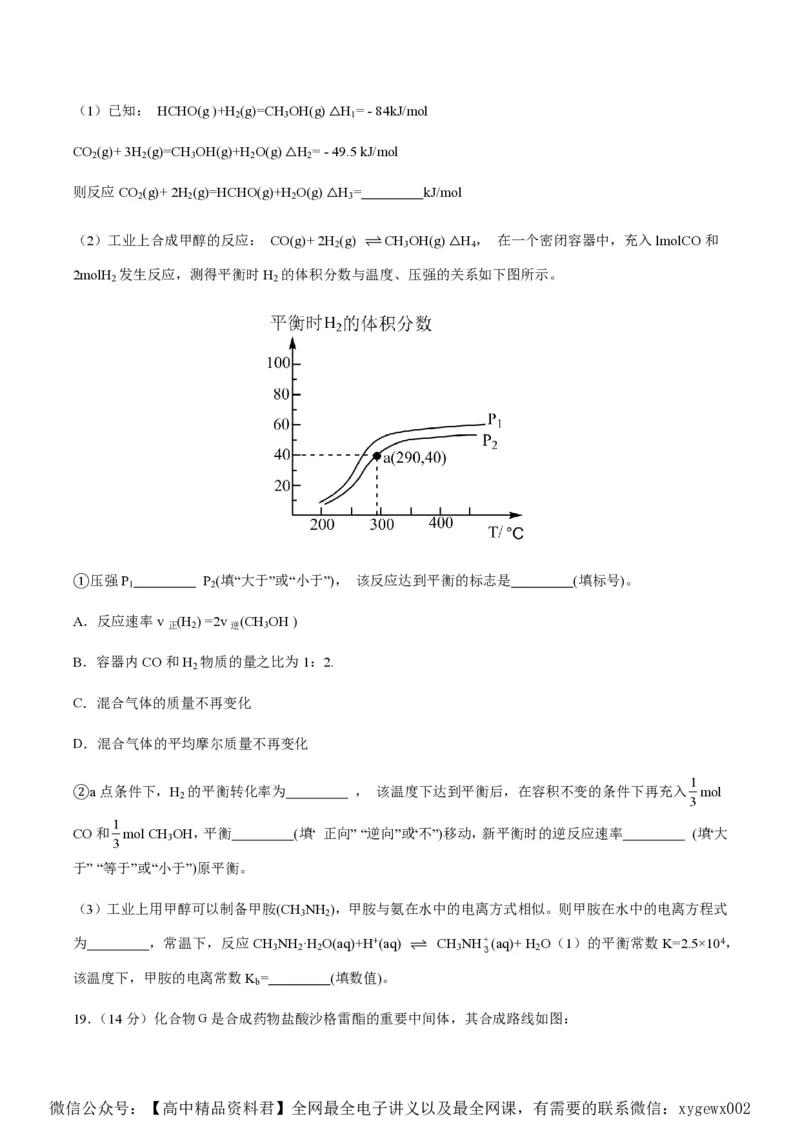
(2)工业上合成甲醇的反应: CO(g)+ 2H (g) CH OH(g) △H , 在一个密闭容器中,充入lmolCO和
2 3 4
2molH 发生反应,测得平衡时H 的体积分数与温度、压强的关系如下图所示。
2 2
①压强P P (填“大于”或“小于”), 该反应达到平衡的标志是 (填标号)。
1 2
A.反应速率v (H ) =2v (CH OH )
正 2 逆 3
B.容器内CO和H 物质的量之比为1:2.
2
C.混合气体的质量不再变化
D.混合气体的平均摩尔质量不再变化
1
②a点条件下,H 的平衡转化率为 , 该温度下达到平衡后,在容积不变的条件下再充入 mol
2
3
1
CO和 mol CH OH,平衡 (填“ 正向” “逆向”或“不”)移动,新平衡时的逆反应速率 (填“大
3
3
于” “等于”或“小于”)原平衡。
(3)工业上用甲醇可以制备甲胺(CH NH ),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式
3 2
为 ,常温下,反应CH NH ·H O(aq)+H+(aq) CH NH(aq)+ H O(1)的平衡常数K=2.5×104,
3 2 2 3 3 2
该温度下,甲胺的电离常数K = (填数值)。
b
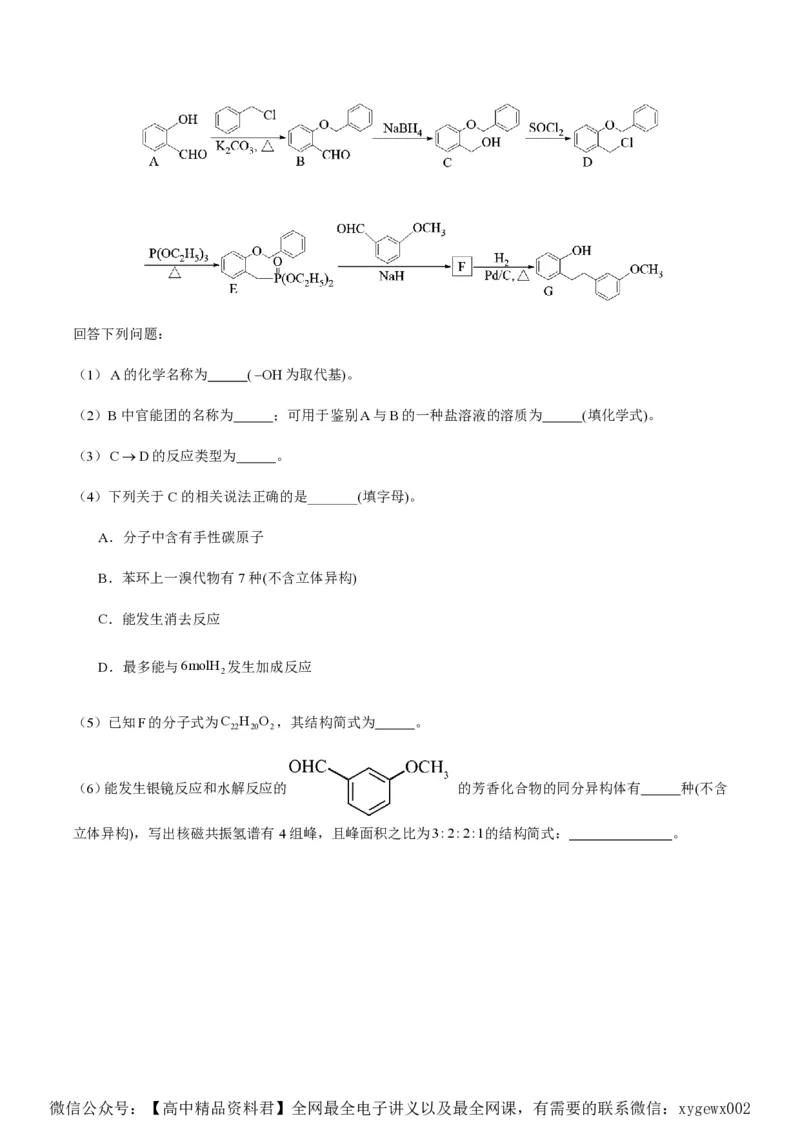
19.(14分)化合物G是合成药物盐酸沙格雷酯的重要中间体,其合成路线如图:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002回答下列问题:
(1)A的化学名称为 (OH为取代基)。
(2)B中官能团的名称为 ;可用于鉴别A与B的一种盐溶液的溶质为 (填化学式)。
(3)CD的反应类型为 。
(4)下列关于C的相关说法正确的是_______(填字母)。
A.分子中含有手性碳原子
B.苯环上一溴代物有7种(不含立体异构)
C.能发生消去反应
D.最多能与6molH 发生加成反应
2
(5)已知F的分子式为C H O ,其结构简式为 。
22 20 2
(6)能发生银镜反应和水解反应的 的芳香化合物的同分异构体有 种(不含
立体异构),写出核磁共振氢谱有4组峰,且峰面积之比为3:2:2:1的结构简式: 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002