文档内容
合肥一中 2026 届高三 10 月份教学质量测评
化学试题
(考试时间:75分钟 满分:100分)
注意事项:
1.答题前,务必在答题卡和答题卷规定的地方填写自己的姓名、准考证号和座位号后两位。
2.答题时,每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。
3.答题时,必须使用0.5毫米的黑色墨水签字笔在答题卷上书写,要求字体工整、笔迹清晰。作图
题可先用铅笔在答题卷规定的位置绘出,确认后再用0.5毫米的黑色墨水签字笔描清楚。必须在题
...
号所指示的答题区域作答,超.出.答.题.区.域.书.写.的.答.案.无.效.,在.试.题.卷.、草.稿.纸.上.答.题.无.效.。
4.考试结束,务必将答题卡和答题卷一并上交。
5.可能用到的相对原子质量:H1、C-12、O-16、Fe-56
一、选择题(本题包含14小题,每题只有一个正确答案,每题3分,共42分。)
1.合肥在科技创新领域的发展令人瞩目,被誉为“科教名城”和“创新之都”。下列说法正确的是
A.合肥的低空经济领域中,实现飞行器性能突破的碳纤维材料属于有机材料
B.合肥科学研究院的全超导托卡马克核聚变实验装置中的玻璃钢属于无机材料
C.科大讯飞智能办公本为实现快递充电添加的SiC属于新型无机非金属材料
D.蔚来汽车的电池的正极材料主要成分磷酸铁锂(LiFePO )属于金属材料
4
2.下列物质的性质及其用途对应关系不正确的是
A.CaSO 微溶于水,可用作制豆腐时的凝固剂
B.B电负性小于H,NaBH 可用作强还原剂
4
C.聚四氟乙烯具有抗酸碱等性能,可用于制作滴定管活塞
4
D.ClO 具有强氧化性,可用于自来水消毒
2
3.下列实验的对应操作中,合理的是
实
验
操
作
A.检验浓硫酸与 D.用玻璃棒摩擦试管
选 B.检验蔗糖的水解产 C.将化学能转化
铜反应的产物中 壁后,可析出晶体
项 物具有还原性 为电能
含有Cu2+ Cu NH SO H O
[ ( 3)4] 4⋅ 2
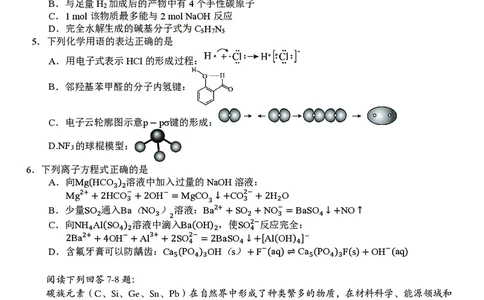
合肥一中2026届高三10月份教学质量测评·化学 第1页(共8页)4.腺嘌呤核苷酸是重要的遗传物质,其结构如图所示。下列有关该物质的说法正确的是
A.可发生取代反应、消去反应和氧化反应
B.与足量H 加成后的产物中有4个手性碳原子
2
C.1 mol该物质最多能与2 mol NaOH反应
D.完全水解生成的碱基分子式为C H N
5 7 5
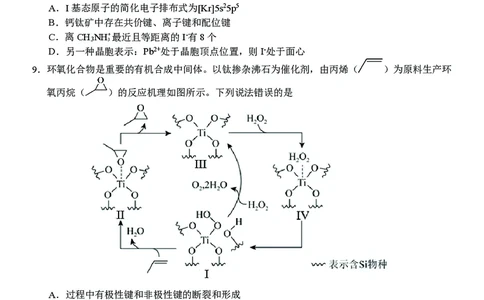
5.下列化学用语的表达正确的是
A.用电子式表示HCl的形成过程:
B.邻羟基苯甲醛的分子内氢键:
C.电子云轮廓图示意p pσ键的形成:
D.NF 的球棍模型: −
3
6.下列离子方程式正确的是
A.向Mg HCO 溶液中加入过量的NaOH溶液:
Mg HCO OH MgCO CO H O
( 3)2
B.少量2+SO 通入B−a(NO )− 溶液:Ba SO2− NO BaSO NO
+2 3 +2 = 3 ↓+ 3 +2 2
C.向NH Al SO 溶液中滴入Ba OH 2+,使SO 反应−完全:
2 3 2 + 2+ 3 = 4 ↓+ ↑
Ba OH Al SO BaSO 2− Al OH
4 ( 4)2 ( )2 4
D.含氟2牙+ 膏可以−防龋齿3:+ Ca PO2− OH(s) F aq C−a PO F s OH aq
2 +4 + +2 4 =2 4 ↓+[ ( )4]
− −
5( 4)3 + ( )⇌ 5( 4)3 ( )+ ( )
阅读下列回答7-8题:
碳族元素(C、Si、Ge、Sn、Pb)在自然界中形成了种类繁多的物质,在材料科学、能源领域和
生命活动中均有重要应用。含碳有机物如乳酸和乙醇胺(HOCHCHNH)作用得到呈液态且能导电的
2 2 2
离子液体─乙醇胺乳酸盐;工业上可用焦炭还原石英砂制备粗硅;镀锡马口铁因其独特的性能在高端
包装领域的应用广泛。
7.下列物质性质推断错误的是
A.常温下[MEA]L呈液态时,可推知离子键强度:[MEA]L < NaCl
高温
B.粗硅制备原理为:SiO +2C=====Si+2CO↑,推知非金属性:C >Si
2
C.CO 通入Na SiO 溶液产生硅胶,推知酸性:H CO >H SiO
2 2 3 2 3 2 3
D.镀锡马口铁镀层破坏后加速铁的腐蚀,推知金属活泼性:Sn < Fe
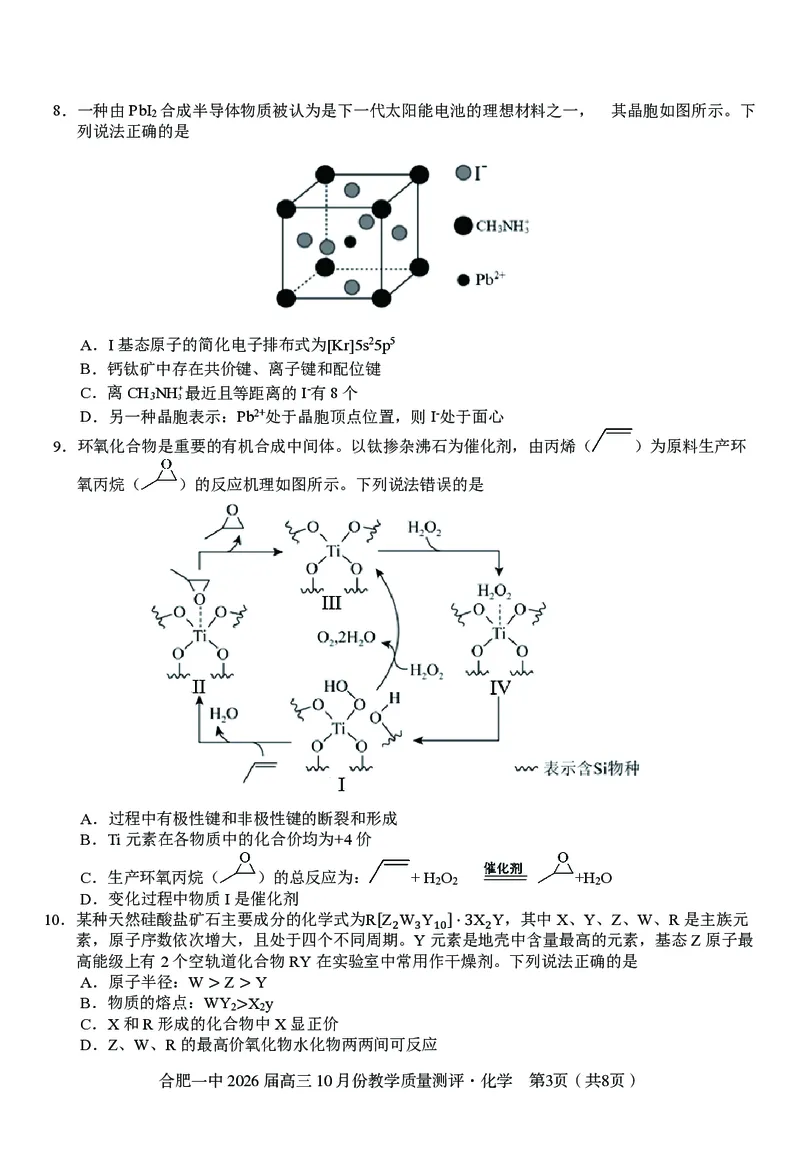
合肥一中2026届高三10月份教学质量测评·化学 第2页(共8页)8.一种由PbI 合成半导体物质被认为是下一代太阳能电池的理想材料之一, 其晶胞如图所示。下
2
列说法正确的是
A.I基态原子的简化电子排布式为[Kr]5s25p5
B.钙钛矿中存在共价键、离子键和配位键
C.离CH NH+ 最近且等距离的I-有8个
3 3
D.另一种晶胞表示:Pb2+处于晶胞顶点位置,则I-处于面心
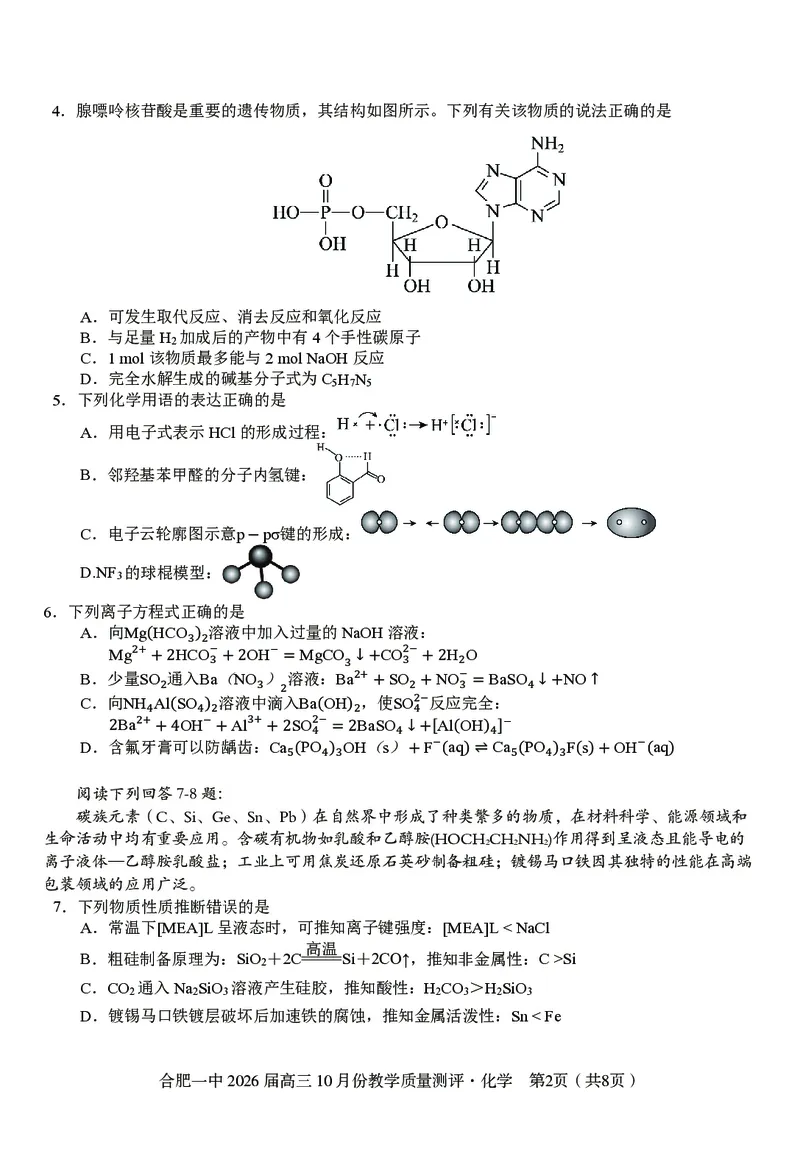
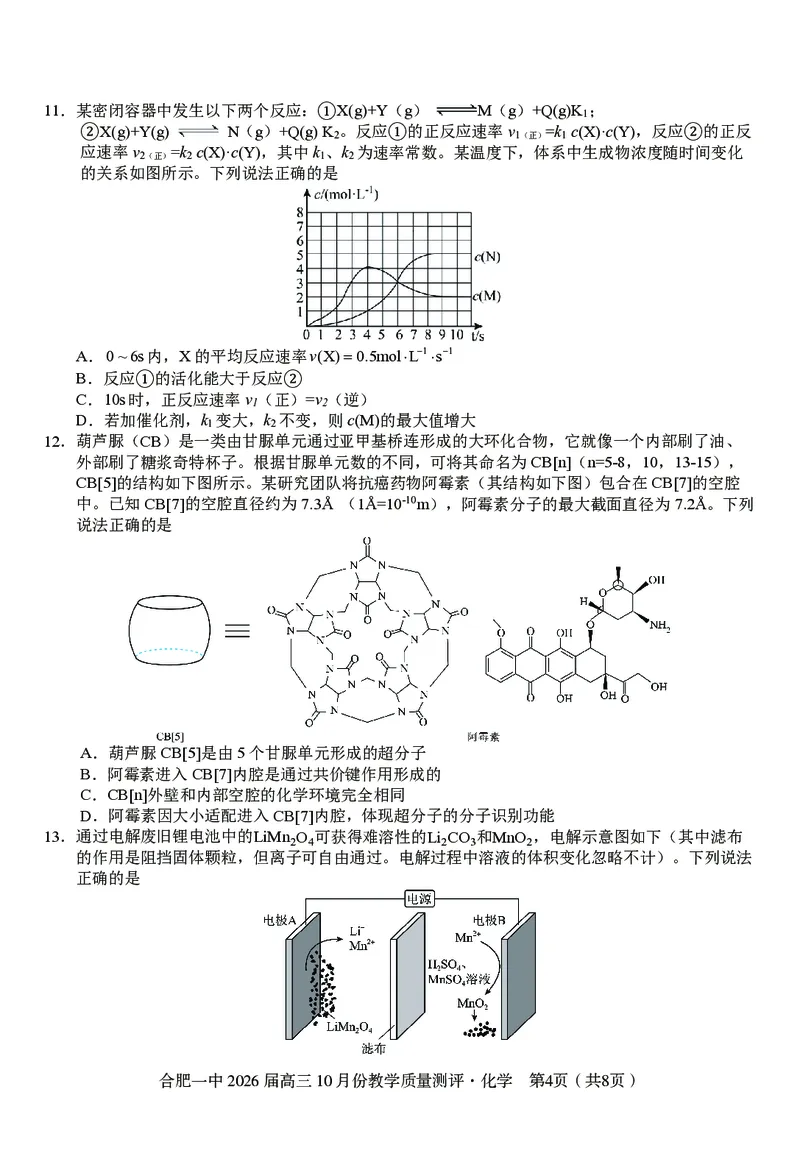
9.环氧化合物是重要的有机合成中间体。以钛掺杂沸石为催化剂,由丙烯( )为原料生产环
氧丙烷( )的反应机理如图所示。下列说法错误的是
A.过程中有极性键和非极性键的断裂和形成
B.Ti元素在各物质中的化合价均为+4价
C.生产环氧丙烷( )的总反应为: + H O +H O
2 2 2
D.变化过程中物质I是催化剂
10.某种天然硅酸盐矿石主要成分的化学式为R Z W Y X Y,其中X、Y、Z、W、R是主族元
素,原子序数依次增大,且处于四个不同周期。Y元素是地壳中含量最高的元素,基态Z原子最
高能级上有2个空轨道化合物RY在实验室
[
中
2
常用
3
作
10
干
]·燥3剂 2
。下列说法正确的是
A.原子半径:W Z Y
B.物质的熔点:WY X y
2 2
C.X和R形成的化>合物>中X显正价
D.Z、W、R的最高价>氧化物水化物两两间可反应
合肥一中2026届高三10月份教学质量测评·化学 第3页(共8页)11.某密闭容器中发生以下两个反应: X(g)+Y(g) M(g)+Q(g)K ;
1
X(g)+Y(g) N(g)+Q(g) K 。反应 的正反应速率v =k c(X)·c(Y),反应 的正反
2 1(正) 1
应速率v =k c(X)·c(Y),其中k ①、k 为速率常数。某温度下,体系中生成物浓度随时间变化
2(正) 2 1 2
的②关系如图所示。下列说法正确的是 ① ②
A.0~6s内,X的平均反应速率v(X)=0.5mol⋅L−1⋅s−1
B.反应 的活化能大于反应
C.10s时,正反应速率v (正)=v (逆)
1 2
D.若加①催化剂,k 变大,k 不②变,则c(M)的最大值增大
1 2
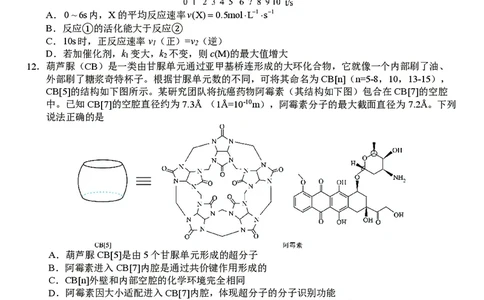
12.葫芦脲(CB)是一类由甘脲单元通过亚甲基桥连形成的大环化合物,它就像一个内部刷了油、
外部刷了糖浆奇特杯子。根据甘脲单元数的不同,可将其命名为CB[n](n=5-8,10,13-15),
CB[5]的结构如下图所示。某研究团队将抗癌药物阿霉素(其结构如下图)包合在CB[7]的空腔
中。已知CB[7]的空腔直径约为7.3Å (1Å=10-10m),阿霉素分子的最大截面直径为7.2Å。下列
说法正确的是
A.葫芦脲CB[5]是由5个甘脲单元形成的超分子
B.阿霉素进入CB[7]内腔是通过共价键作用形成的
C.CB[n]外壁和内部空腔的化学环境完全相同
D.阿霉素因大小适配进入CB[7]内腔,体现超分子的分子识别功能
13.通过电解废旧锂电池中的LiMn O 可获得难溶性的Li CO 和MnO ,电解示意图如下(其中滤布
2 4 2 3 2
的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法
正确的是
合肥一中2026届高三10月份教学质量测评·化学 第4页(共8页)A.电极A为阳极,发生氧化反应
B.电极B的电极反应:4OH-+Mn2+-2e-=MnO +2H O
2 2
C.电解一段时间撤去滤布后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节pH除去Mn2+,再加入Na CO 溶液以获得Li CO
2 3 2 3
14.工业废水除砷常利用NaClO将废水中的As(III)氧化为As(V),再加含钙试剂生成Ca (A O ) 沉淀。
3 S 4 2
As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)
与pH的关系如图所示。
已知: 一般把10-1>K >10-4的酸称为中强酸,把K <10-4的酸称为弱酸。
a a
室温时:Ksp[Ca (AsO ) ]=1×10-21.2、Ksp[CaCO ]=1×10-8.6;下列说法正确的是
3 4 2 3
①
②
A.H AsO 、H AsO 都是弱酸
3 4 3 3
B.保持溶液pH=10,用NaClO将As(III)氧化为As(V)的离子方程式:
H AsO- +ClO-+2OH-=AsO3- +Cl-+2H O
2 3 4 2
C.H AsO- +H AsO - HAsO2- +H AsO K=102.4
2 4 2 3 4 3 3
D.用0.1mol·L-1Na CO 溶液浸泡Ca (A O ) 沉淀,不会生成CaCO
2 3 3 S 4 2 3
二、填空题(本题包含4小题,共58分)
15.(14分) VIA族元素(氧、硫、硒等)及其化合物在生产、生活中有着广泛的应用
(1)我国是世界上硫储量丰富的国家,在岩层深处的无氧环境下,硫元素通常以硫化物矿石如
黄铁矿(FeS )存在,一种碱性条件下的电化学浸出法可有效回收矿石中的有色金属,其反
2
应原理如图所示:
(1)含硫物质FeS 转化的离子方程式 ,
2
(2)SOCl 是一种液态化合物,实验室可将SOCl 的与AlCl ·6H O混合加热得到无水AlCl ,
2 2 3 2 3
试用文字解释SOCl 在实验过程中所起的作用:
2
(3)甲硫醇(CH₃SH)具有一定的酸性,是合成农药、医药的重要中间体,工业上可通过硫化
氢(H₂S)与一氧化碳(CO)在催化剂作用下反应制备, CH₃SH的酸性 于H S的
2
酸性(填“强”或“弱”)
(4)硒的某种氧化物为链状聚合结构如下图所示,其中Se的杂化方式为 该氧化物的
化学式为 。
合肥一中2026届高三10月份教学质量测评·化学 第5页(共8页)(5)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用下图表示。已知光的波长
与其能量成反比,则图中实现光响应的波长:λ λ (填“>”或“<”或“=”)
1 2
(6)以工业硒为原料制备高纯硒的流程如图。
燃烧 水洗 还原 纯化
工业硒(Se) → SeO → H SeO → Se → 高纯硒
2 2 3
过程i 过程ii 过程iii 过程iv
下列说法正确的是 (填字母序号)。
a.过程i到过程ⅲ均为氧化还原反应
①
b.H SeO 既有氧化性,又有还原性
2 3
c.SeO 能与NaOH反应生成Na SeO 和H O
2 2 3 2
d.Se与H 化合比S与H 化合容易
2 2
过程ⅲ中使用的还原剂为N H ⋅nH O,对应产物是N 。理论上,过程i消耗的O 与过
2 4 2 2 2
程ⅲ中消耗的N H ⋅nH O的物质的量之比为 (工业硒中杂质与O 的
② 2 4 2 2
反应可忽略)。
16.(14分)采用两段焙烧-水浸法从铁锰氧化矿(主要含Fe O 、MnO 及Co、Ca、Si等元素的氧
2 3 2
化物)分离提取Fe、Mn、Co等元素,工艺流程如下:
已知: 该工艺条件下,(NH ) SO 低温分解生成NH HSO 和MH ;
4 2 4 4 4 3
Fe (SO ) 在650℃完全分解,本题中其他金属硫酸盐分解温度均高于700℃;
2 4 3
(1)“①低温焙烧”时金属氧化物均转化为硫酸盐。MnO 与NH HSO 反应转化为MnSO 时有
2 4 4 4
N ②生成,该反应的化学方程式为 。
2
(2)“低温焙烧”时产生的气体用稀硫酸吸收,从物质转化和资源综合利用的角度解释原
因: 。
(3)“沉钴”得到CoS。向“沉钴”后所得滤液中加入NH HCO 获得MnCO 沉淀,发生反应
4 3 3
的离子方程式为 。
(4)“溶解”时加入H O 可提高Co2+的浸出率,原因是 。
2 2
(5)“水浸”所得滤渣的主要成分为 、 和Fe O ,以该滤渣为原料制取绿矾
2 3
(FeSO ·7H O)。请补充实验方案:取一定量滤渣于反应器中, ,过
4 2
滤,冰水洗涤,低温干燥得绿矾(可选用的试剂:铁粉、铜粉、3.0mol·L-1 H SO )。
2 4
17.(14分)乙二胺四乙酸铁钠(NaFeY⋅3H O)是一种广泛用于食品、保健品和药品的添加剂,
2
是重要的铁强化剂。以铁屑为原料制备乙二胺四乙酸铁钠的过程和实验装置如下:
称取一定质量的铁屑,加入过量盐酸溶解,然后通入适量O ;
2
将上述溶液和乙二胺四乙酸(H Y)加入到如图所示的装置a中,控制反应温度为70~80℃,
① 4
滴加NaHCO 溶液调节pH为5,搅拌,直到溶液中出现少量浑浊;
3
②
合肥一中2026届高三10月份教学质量测评·化学 第6页(共8页)经分离提纯得到粗品。
③
已知:i.NaFeY⋅3H O是一种配合物,微溶于乙醇,20℃时在水中的溶解度为4.3g。
2
ii.乙二胺四乙酸(EDTA,用H Y表示)是一种弱酸。
4
回答下列问题:
(1)仪器a的名称为 。
(2)反应过程中有气泡产生,则过程 生成NaFeY⋅3H O的总反应的化学方程式为 。
2
(3)结合已知信息,从反应后的混合物中获得较高产率的NaFeY⋅3H O粗品的操作是 ,
② 2
过滤,水洗,干燥;可以用试剂 检验NaFeY⋅3H O是否洗涤干净。
2
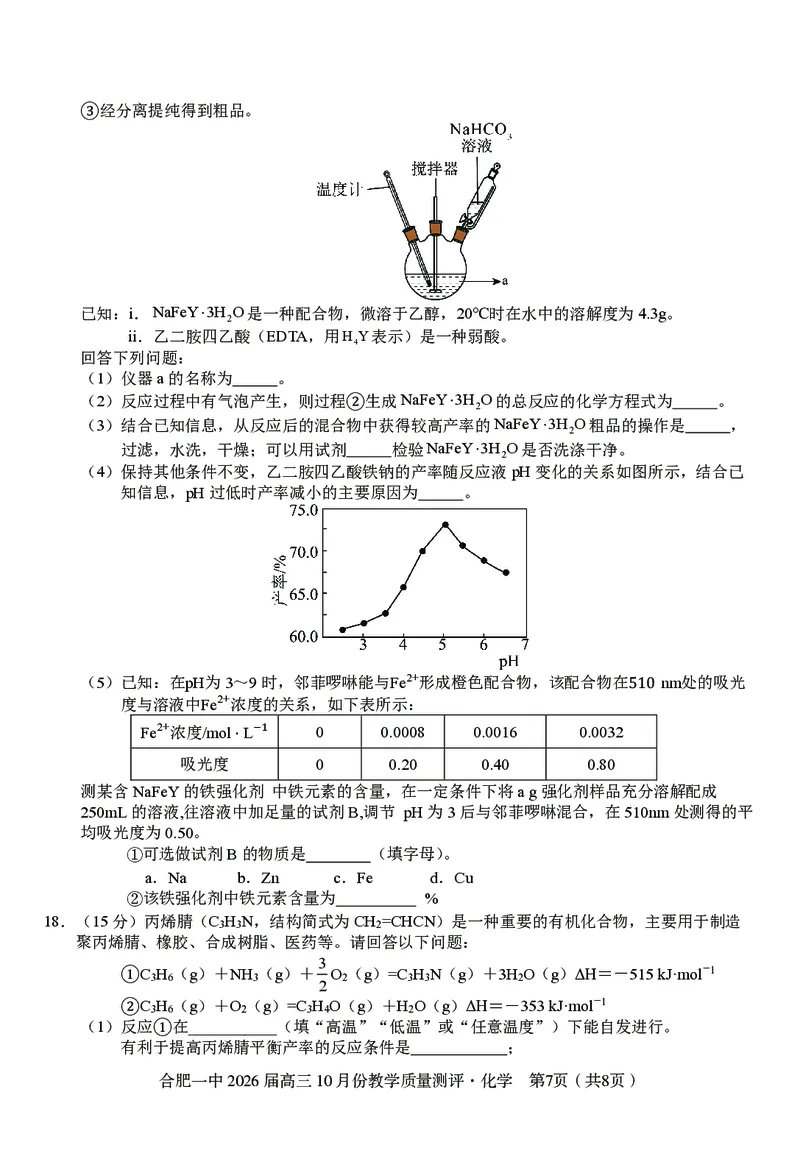
(4)保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液pH变化的关系如图所示,结合已
知信息,pH过低时产率减小的主要原因为 。
(5)已知:在pH为3~9时,邻菲啰啉能与Fe2+形成橙色配合物,该配合物在 nm处的吸光
度与溶液中Fe2+浓度的关系,如下表所示:
510
Fe2+浓度/mol L 0 0.0008 0.0016 0.0032
−1
吸光度 ⋅ 0 0.20 0.40 0.80
测某含NaFeY的铁强化剂 中铁元素的含量,在一定条件下将a g强化剂样品充分溶解配成
250mL的溶液,往溶液中加足量的试剂B,调节 pH为3后与邻菲啰啉混合,在510nm处测得的平
均吸光度为0.50。
①可选做试剂B的物质是 (填字母)。
a.Na b.Zn c.Fe d.Cu
②该铁强化剂中铁元素含量为 %
18.(15分)丙烯腈(C H N,结构简式为CH =CHCN)是一种重要的有机化合物,主要用于制造
3 3 2
聚丙烯腈、橡胶、合成树脂、医药等。请回答以下问题:
3
C H (g)+NH (g)+ O (g)=C H N(g)+3H O(g)ΔH=-515 kJ·mol-1
3 6 3 2 3 3 2
2
①C
3
H
6
(g)+O
2
(g)=C
3
H
4
O(g)+H
2
O(g)ΔH=-353 kJ·mol-1
(1)反应 在___________(填“高温”“低温”或“任意温度”)下能自发进行。
②有利于提高丙烯腈平衡产率的反应条件是 ;
①
合肥一中2026届高三10月份教学质量测评·化学 第7页(共8页)(2)向三个不同的恒压容器中分别充入2molC H 、2molNH 和3molO ,发生反应 和反应
3 6 3 2
n(C H N)
,平衡时丙烯腈的选择性[丙烯腈的选择= 3 3 ×100%]与温①度、压强
n(C H N)+n(C H O)
3 3 3 4
②的关系如图所示,则P 、 P 、P 的由大到小的大小顺序为 ;若M点C H 的转化
1 2 3 3 6
率为60%,则NH 的转化率为 ,550℃反应 的分压平衡常数Kp =
3
②
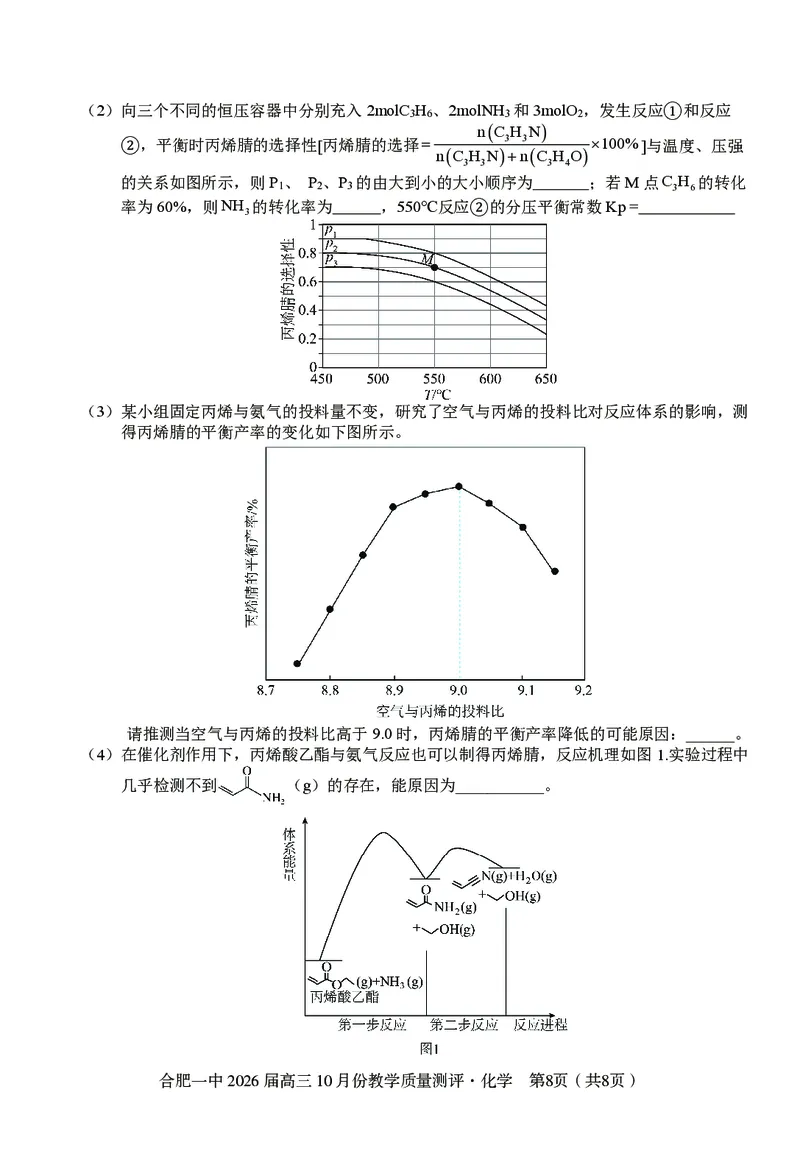
(3)某小组固定丙烯与氨气的投料量不变,研究了空气与丙烯的投料比对反应体系的影响,测
得丙烯腈的平衡产率的变化如下图所示。
请推测当空气与丙烯的投料比高于9.0时,丙烯腈的平衡产率降低的可能原因:______。
(4)在催化剂作用下,丙烯酸乙酯与氨气反应也可以制得丙烯腈,反应机理如图1.实验过程中
几乎检测不到 (g)的存在,能原因为___________。
合肥一中2026届高三10月份教学质量测评·化学 第8页(共8页)