文档内容
届高三 月质量检测化学
2026 11
参考答案、提示及评分细则
【答案】
1. A
【解析】 豆浆属于胶体 胶体粒子对光束具有散射作用 可以产生丁达尔效应 正确 钠 镁通过电解熔融
A. , , ,A ;B. 、
的 制得 因 是共价化合物 熔融不导电 制取单质铝需电解熔融的 错误 制作太
NaCl、MgCl2 ; AlCl3 , , Al2O3,B ;C.
阳能电池的主要原料是单晶硅 错误 葡萄糖口服液补充的是糖分而非电解质 腹泻需补充钠 钾等离子
,C ;D. , 、 ,
错误
D .
【答案】
2. D
【解析】 中子数为 的氯原子 质量数应为 错误 碳的基态原子轨道表示式为
A. 18 , 35,A ;B. : ,B
错误 用电子式表示 的形成过程 错误 的价层电子对数为 空间结
;C. HCl : ,C ;D.BF3 3,
构为平面三角形 正确
,D .
【答案】
3. B
【解析】 和 的最简式均为 混合气体可视为 总原子数为 N 正确 石墨中
A.NO2 N2O4 NO2, 4.6gNO2, 0.3 A,A ;B.
每个碳原子形成 个 键 但每个 键被 个碳原子共享 故 石墨中含有的 键数目为 N 错误
3 σ , σ 2 , 12g σ 1.5 A,B ;
溶液中含有 乙醇和 水 其中乙醇为 水为 故氧原子总数为 N 正确
C.100g 46g 54g , 1mol, 3mol, 4 A,C ;D.
为强碱弱酸盐 醋酸根水解促进水的电离 的溶液中c
- -5
该
-
全部
CH3COONa , ,pH=9 (OH )=10 mol/L, OH
来自水的电离 因此水电离出的 - 数目为 -5N 正确
, OH 10 A,D .
【答案】
4. C
【解析】 溶液具有强氧化性 应选用酸式滴定管盛装 错误 实验室保存液溴应用玻璃塞 错
A.KMnO4 , ,A ;B. ,B
误 将C管位置提高 若装置气密性好 则BC管会有稳定的液面差 正确 与瓷坩埚中二氧化
;C. , , 、 ,C ;D.Na2CO3
硅在高温下发生化学反应 错误
,D .
【答案】
5. B
【解析】 向硫酸铜溶液中通入过量氨气的离子方程式为 错误 泡沫灭
2+ 2+
A. Cu +4NH3[Cu(NH3)4] ,A ;B.
火器的反应原理为 正确 的还原性比 强 向 溶液
3+ - - 2+
Al +3HCO3 Al(OH)3↓+3CO2↑,B ;C.I Fe , FeI2
滴入少量 的离子方程式为 错误 同浓度同体积的 溶液与
- -
Br2 :2I +Br2I2+2Br ,C ;D. NH4HSO4 NaOH
溶液混合的离子方程式为 错误
+ -
H +OH H2O,D .
【答案】
6. C
【解析】 与 反应能放出 的溶液可能呈酸性 可能呈碱性 若为酸性溶液 且含有 则该溶液与 反
-
A. Al H2 , . , NO3 , Al
应无 放出 不符合题意 错误 在 氨水中 分别与氨水反应生成 和
-1 + 2+ +
H2 , ,A ;B. 0.1molL ,Ag 、Cu [Ag(NH3)2]
不能在 氨水中大量共存 错误 为酸性溶液
2+ + 2+ -1 + 2+ -
[Cu(NH3)4] ,Ag 、Cu 0.1molL ,B ;C.pH=1 ,Na 、Fe 、Cl 、
在酸性溶液中均能大量共存 正确 与 能反应生成 而不能大量共存 错误
2- 3+ -
SO4 ,C ;D.Fe SCN Fe(SCN)3 ,D .
高三化学试题参考答案 第 页 共 页
【 1 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}【答案】
7. A
【解析】 四种物质两两之间均能反应 与 中和 与
A.a(NH3)、e(HNO3)、u(H2S)、y(H2SO3) :NH3 HNO3( )、NH3
生成铵盐 与 中和 与 氧化还原 与 氧化还原 与
H2S( )、NH3 H2SO3( )、HNO3 H2S( )、HNO3 H2SO3( )、H2S
归中 均能反应 正确 中心原子的价层电子对数均为 杂化类型均为 但
2
H2SO3( ), ,A ;B.w(SO2)、x(SO3) 3, sp,
有孤电子对 故 的空间结构为 型 的空间结构为平面三角形 错误
SO2 , SO2 V ,SO3 ,B ;C.c(NO)、d(NO2)、
四种物质 为酸性氧化物 不是 错误 的浓溶液
w(SO2)、x(SO3) ,SO2、SO3 ,NO、NO2 ,C ;D.e(HNO3)、z(H2SO4)
中 浓 不稳定 保存在棕色试剂瓶中 浓硫酸保存在无色试剂瓶中 错误
, HNO3 , , ,D .
【答案】
8. C
【解析】 与 同主族 且 的质子数为 的两倍 可知 为氧元素 为硫元素 为原子序数依
“Q M , M Q ”, Q ,M ;X、Y、Z
次增大的短周期主族元素 结合题给结构简式中 形成的共价键个数 可知 为氢元素 为碳元素
, X、Y、Z , X 、Y 、Z
为氮元素 元素可形成正一价阳离子 且原子序数小于硫元素 可知 元素为钠元素 为
2-
;W , , W .A.M2O8
因含有过氧键而具有强氧化性 正确 元素为碳元素 含氧酸盐水溶液中 溶液显酸
2-
S2O8 , ,A ;B.Y , ,NaHC2O4
性 溶液显碱性 正确 元素为氧元素 所在周期中 第一电离能大于氧元素有 共 种
,Na2CO3 ,B ;C.Q , , N、F、Ne 3 ,
错误 四种元素分别为 既可以组成离子化合物 如 也可以组成共价化
C ;D.X、Y、Z、Q H、C、N、O, ( NH4NO3),
合物 如 正确
( CO(NH2)2),D .
【答案】
9. B
【解析】 由该有机物的结构简式可得分子式为 错误 该分子中含 个手性碳原子 如图
A. C14H18N2O5,A ;B. 2 , :
正确 该分子中 杂化的碳原子数目为 错误
3
,B ;C. sp 5,C ;
该有机物含酯基和酰胺基均能与强酸和强碱反应 还含有一个羧基 故 该物质最多能与
D. , , 1mol 3molNaOH
发生反应 错误
,D .
【答案】
10. B
【解析】生物浸出 在合适温度下进行可以提高浸出率 过滤分离出滤渣为 浸出液含
2+ 2+
“ ” , SiO2, Co 、Fe 、
加入萃取剂 萃取后有机相含 加入稀硫酸进行反萃取 分离出硫酸铜 再发生置换反
3+ 2+ 2+
Fe 、Cu , HA Cu . , ,
应生成 水相 氧化后调节 沉淀铁离子 生成的滤渣为氢氧化铁 电解含 的溶液
2+ 2+ 3+ 2+
Cu, Co 、Fe 、Fe , pH , , Co
生成粗 温度过高细菌失去活性 浸出率下降 只能在适当温度下进行 生物浸出 错误 根据平
Co.A. , , “ ”,A ;B.
衡移动原理可知 反萃取需加入酸 由流程图可知反萃取后得到硫酸铜溶液 则应加入稀硫酸 正确 分
, , , ,B ;C.
液时 应先打开分液漏斗玻璃塞 错误 除铁过程应先加入双氧水将亚铁离子氧化成铁离子 再加氢氧化
, ,C ;D. ,
钴调节 错误
pH,D .
【答案】
11. C
【解析】 冰晶体中 水分子采取分子非密堆积 因为水分子间的氢键具有方向性 错误 该晶胞中最近的
A. , , ,A ;B.
两个水分子之间的距离为 3a 错误 这种冰晶胞中四面体空隙共 个 水分子占据 个 则四面体
pm,B ;C. 8 , 4 ,
4
30
空隙填充率为 正确 该晶体的密度应为 144×10 -3 错误
50%,C ;D. ρ= Na3 gcm ,D .
A
高三化学试题参考答案 第 页 共 页
【 2 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}【答案】
12. A
【解析】 无水硫酸铜为白色固体 遇水后会生成蓝色晶体 该反应是检验水的特征反应 且
A. , CuSO45H2O, ,
乙醇与无水硫酸铜不反应 无干扰现象 正确 浓盐酸能与高锰酸钾溶液反应使溶液褪色 则将铁锈溶于
, ,A ;B. ,
浓盐酸 滴入高锰酸钾溶液 紫色逐渐褪去不能确定铁锈中含有二价铁 错误 金属钠放置在空气中一段
, , ,B ;C.
时间 最终会生成 错误 搅拌会使生成的微小 粒子被剧烈扰动 无法形成稳定的胶体
, Na2CO3,C ;D. Fe(OH)3 ,
分散系 反而相互碰撞团聚 直接生成 红褐色沉淀 错误
, , Fe(OH)3 ,D .
【答案】
13. C
【解析】待测液和氯化钡溶液反应得到沉淀 则溶液中可能含有 向沉淀中加入稀硝酸
2- 2- 2-
A, SO4 、CO3 、SO3 ,
生成气体 且有部分沉淀不溶解 则溶液中存在 不含有 可能存在 中的一种或两种
2- 2+ 2- 2-
, , CO3 , Cu , SO4 、SO3 ,
根据离子共存可知 溶液中不存在 滤液 中有 加入过量的 溶液得到气体 白色沉淀
2+ 2+
, Ba ; A Ba , NaOH B、
则溶液中一定含有 气体 为 白色沉淀 为 滤液 中加入硝酸银 硝酸溶液
+ -
B, NH4 、HCO3 , B NH3, B BaCO3, B 、
得到白色沉淀 为 说明滤液 中含有 不含有 由于加入了氯化钡溶液 不能确定原溶液中
- -
C,C AgCl, B Cl , I , ,
是否含有 据此分析 根据分析知滤液 中含有 加入 溶液生成白色沉淀 为
- 2+
Cl , .A. A Ba , NaOH B BaCO3,
反应的离子方程式为 错误 若无色气体是混合气体 则溶
2+ - -
:Ba +HCO3 +OH BaCO3↓+H2O,A ;B. ,
液中一定含有
2-
不能确定是否含有
2-
原溶液中c
2-
错误 由分析可知
SO3 、 SO4 , (SO3 )≤0.05mol/L,B ;C. ,
c + c + c - c 2- c 2-
(K )=0.2mol/L,(NH4 )=0.1mol/L,(HCO3 )=0.1mol/L,(CO3 )=0.1mol/L,(SO4 )+
c 2- 则由电荷守恒知 一定含有 + 当溶液中没有 - + 浓度最小 故c +
(SO3 )=0.05mol/L, , Na , Cl ,Na , (Na )≥
正确 向溶液 中加入 与 的操作不是多余的 是为了判断是否含有碘离子
0.1mol/L,C ;D. B AgNO3 HNO3 , ,D
错误
.
【答案】
14. C
【解析】先计算样品物质的量 的物质的量为 结合固体残留率可推算各温度
:36.5gCaC2O4H2O 0.25mol.
段残留固体 时为 失去结晶水 时为 时为
:300℃ CaC2O4( ),600℃ CaCO3,900℃ CaO.
是 分解失去结晶水生成 的过程 有新物质生成 属于化学反应 错
A.100℃~300℃ CaC2O4H2O CaC2O4 , , ,A
误 时 残留固体质量为 为 和 的混合物 设 为
;B.500℃ , 36.50g×76.16%≈27.8g, CaC2O4 CaCO3 . CaC2O4
x 为y 则x y 钙原子守恒 x y 解得x y
mol、CaCO3 mol, + =0.25( ),128 +100 =27.8, =0.1mol、 =0.15mol,
n n 错误 时残留固体为 时
(Ca)∶ (C)=(0.1+0.15)∶(0.2+0.15)=5∶7≠1∶2,B ;C.300℃ CaC2O4,600℃
残留固体为 加入足量的盐酸后 都是生成 根据钙原子守恒 消耗 的物质的量为相等
CaCO3, , CaCl2, , HCl ,C
正确 时的残留固体为 其水溶液呈碱性 滴加酚酞试液后溶液会变为红色 错误
;D.900℃ CaO, , ,D .
【答案】 分 除特殊标注外每空 分
15. (15 , 2 )
球形干燥管 分
(1) (1 )
防止反应体系 过低从而产生钨的水合氧化物沉淀
(2) pH
△
(3)12Na2WO4+Na2SiO3+13H2SO4H4(SiW12O40)+13Na2SO4+11H2O
(4)H2SiO3
(5)B
(6)Na2SO4
或溴水等其他合适氧化剂
(7)H2O2( )
(8)74.3
高三化学试题参考答案 第 页 共 页
【 3 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}【解析】 由装置图可知 为球形干燥管
(1) b .
通过已知信息 缓慢滴加稀硫酸 而不是一次性加入是为了防止局部 过低从而产生钨的水合氧化物
(2) , , pH
沉淀
.
过量的 与稀硫酸在加热时产生硅酸沉淀杂质 因此萃取前要先过滤除去杂质
(4) Na2SiO39H2O , .
乙醇与水互溶 四氯化碳沸点过高 后续蒸发除四氯化碳时可能会导致十二钨硅酸分解 因此萃取剂选择
(5) , , ,
乙醚
.
静置分层后液体分上 中 下三层 下层为油状醚合物 上层为乙醚 即中层为 溶液
(6) 、 、 , , , Na2SO4 .
水浴蒸发过程中液体变蓝色 说明十二钨硅酸被还原了 因此需及时滴加 或溴水等其他合适氧化剂
(7) , , H2O2( ).
实际产量
产率 20g 1
(8) =理论产量=10.8g÷( × ×2880g/mol)×100%≈74.3%.
330g/mol 12
【答案】 分 每空 分
16. (16 , 2 )
将褐铁矿型金 银矿粉碎 搅拌 加热等
(1) - , ,
2+ + 2+ 3+
(2)MnO2+2Fe +4H Mn +2Fe +2H2O
(3)Ag、Au、SiO2
3+ 2+
(4)MnO2>Fe >Cu
5- 2+ - 2-
(5)4[Cu(S2O3)3] +16NH3+O2+2H2O4[Cu(NH3)4] +4OH +12S2O3
与 结合形成 提高 的还原性
+ 3-
(6) Au [Au(S2O3)2] , Au
溶液碱性太强 可能生成
(7)Na2CO3 , Mn(OH)2
中含有过氧键不稳定 氧化性强于 难以被 氧化生成 原子半径较大 键难以形成 或其
(8)(b) , Ⅰ2, Ⅰ2 ;S ,S=S (
他合理答案
)
【解析】由流程可知 矿石经 还原酸浸 被还原为 和 被溶解为
2+ 2+ 2+
, “ ”,Fe2O3、MnO2 Fe Mn ,CuO Cu ,Au、Ag、
不溶进入 滤渣 沉铜 时 被铁粉还原为 氧化 时 被氧化为 沉铁 时 转
2+ 2+ 3+ 3+
SiO2 “ 1”;“ ” ,Cu Cu;“ ” Fe Fe ;“ ” ,Fe
化为沉淀 后续转化为氧化铁 沉锰 时 沉淀为碳酸锰 浸金银 时 被混合液浸出 后续提炼
2+
, ;“ ” ,Mn ;“ ” ,Au、Ag ,
出
Au、Ag.
还原酸浸 时发生氧化还原反应
3+ 2- 2+ 2- + 2- +
(4)“ ” :2Fe +SO3 +H2O2Fe +SO4 +2H ,MnO2+SO3 +2H
而 未发生氧化还原反应 说明 氧化 过程发生氧化还原反应
2+ 2- 3+ 2+
Mn +SO4 +H2O, CuO , Fe >Cu ;“ ” :
根据氧化剂的氧化性大于氧化产物可得氧化性
2+ + 2+ 3+
MnO2+2Fe +4H Mn +2Fe +2H2O, MnO2>
可得氧化剂由强到弱的顺序为
3+ 3+ 2+
Fe ; MnO2>Fe >Cu .
浸金银 时 在空气中的 作用下 催化 溶解 结合第一步反应可知第一步的生成物
2+
(5)“ ” , O2 ,[Cu(NH3)4] Au ,
在第二步与氧气反应生成 离子方程式配平后为
5- 2+ 5-
[Cu(S2O3)3] 4[Cu(NH3)4] , :4[Cu(S2O3)3] +
2+ - 2-
16NH3+O2+2H2O4[Cu(NH3)4] +4OH +12S2O3 .
与 结合形成 提高 的还原性
+ 3-
(6) Au [Au(S2O3)2] , Au .
沉锰 是生成 由于 溶液碱性太强 可能生成
(7)“ ” MnCO3, Na2CO3 , Mn(OH)2.
中含有过氧键 氧化性强于 难以被 氧化生成 原子半径较大 键难以形成 或其他合理
(8)(b) , Ⅰ2, Ⅰ2 ;S ,S=S (
答案
).
高三化学试题参考答案 第 页 共 页
【 4 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}【答案】除特殊标注外 每空 分 共 分
17. ( , 2 , 15 )
环己醇
(1)
酯基 酮羰基 写对一个给 分 写错不给分
(2) , ( 1 , )
取代反应 酯化反应
(3) ( )
(4)
(5)
(6)15
(7)
分
(3 )
【解析】 由分析可知 的名称为环己醇
(1) ,B .
由分析可知 中所含官能团的名称为酯基 酮羰基
(2) ,G , .
由分析可知 反应条件中有乙醇和浓硫酸 再结合 中的酯基 逆推反应可得 为 故该
(3) ,C→D , D , C ,
反应为酯化反应 或取代反应
( ).
的分子式为 不饱和度为 对比 和 结构简式可以发现 中多了一个 结构
(4)F C4H6O, 2, E G G ,
可以推测 含碳氧双键 又 为加成反应 故推测 中含碳碳双键 结合以上信息推出 从而得出
F , E+F→G , F , F,
方程式为
.
中 碳氧双键发生加成反应断键 上加 碳与碳相连成环 故第 步反应产物
(5)G ,O H, , 1
高三化学试题参考答案 第 页 共 页
【 5 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}的结构简式为
.
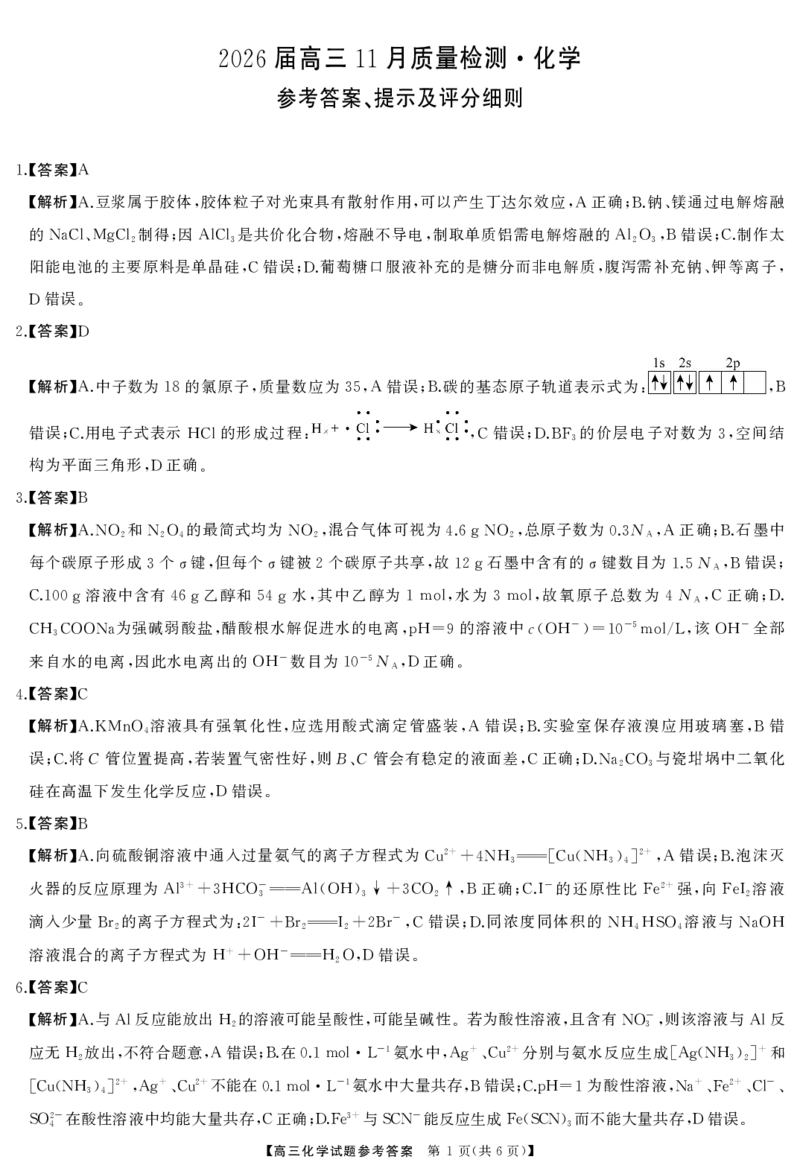
的分子式为 由 是 的同系物和比 少两个碳原子可得该 的分子式为 不饱
(6)H C12H16O3, I H H I C10H12O3,
和度为 由 遇 发生显色反应可推断含 由 能发生水解反应和银镜反应可推断含甲酸
3+
5, ① Fe , ②
某酯 由 苯环上只有两个取代基 可知苯环上有两条支链 结合以上信息可以推断出
(HCOO-), ③ , , HCOO-
可以在如图 个位置 再考虑邻 间 对 故有 种同分异构体
5 , 、 、 , 15 .
由流程图中 可推断
(7) E→G→H,
再与氢气发生加成反应
,
得
.
【答案】 分
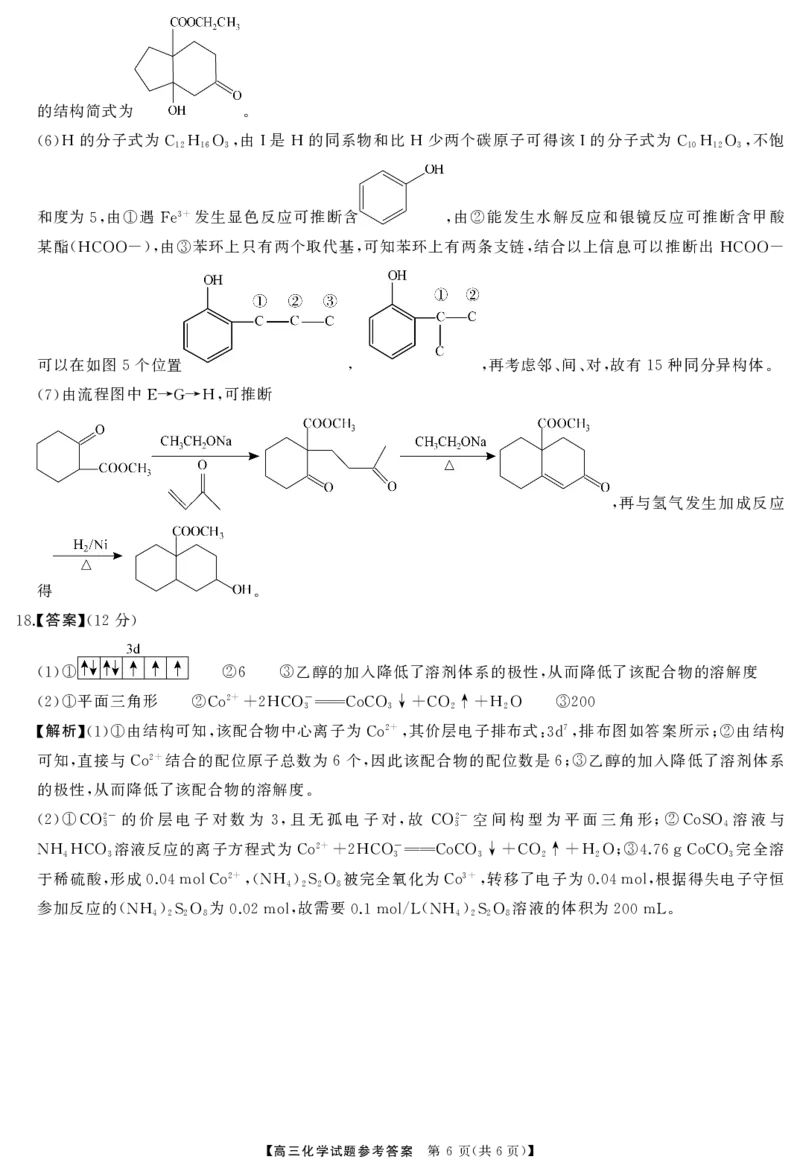
18. (12 )
乙醇的加入降低了溶剂体系的极性 从而降低了该配合物的溶解度
(1)① ②6 ③ ,
平面三角形
2+ -
(2)① ②Co +2HCO3CoCO3↓+CO2↑+H2O ③200
【解析】 由结构可知 该配合物中心离子为 其价层电子排布式 排布图如答案所示 由结构
2+ 7
(1)① , Co , :3d, ;②
可知 直接与 结合的配位原子总数为 个 因此该配合物的配位数是 乙醇的加入降低了溶剂体系
2+
, Co 6 , 6;③
的极性 从而降低了该配合物的溶解度
, .
的价层电子对数为 且无孤电子对 故 空间构型为平面三角形 溶液与
2- 2-
(2)①CO3 3, , CO3 ;②CoSO4
溶液反应的离子方程式为 完全溶
2+ -
NH4HCO3 Co +2HCO3CoCO3↓+CO2↑+H2O;③4.76gCoCO3
于稀硫酸 形成 被完全氧化为 转移了电子为 根据得失电子守恒
2+ 3+
, 0.04molCo ,(NH4)2S2O8 Co , 0.04mol,
参加反应的 为 故需要 溶液的体积为
(NH4)2S2O8 0.02mol, 0.1mol/L(NH4)2S2O8 200mL.
高三化学试题参考答案 第 页 共 页
【 6 ( 6 )】
{#{QQABKQQsxgowkoSACI5qBwUWCkuYkJAjLIgMARCduAQqAQFIBIA=}#}