文档内容
【试卷总评】2012年高考重庆理科综合化学试题保持相对稳定的特点,总体上比较平和,
题目简洁明了,无偏题、怪题,充分地体现了高考的相对稳定性,有利于教育改革的平稳过
渡,也有利于高中化学教学和学生备考。突出中学化学主干知识、基础知识和基本技能的
考查,突出化学学科素养的考查。试题背景注重与生活、技术、社会等方面密切联系,适当
加大了元素化学的考查。
【试题解析】
6.化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是
A.氮肥厂用氢气和氮气合成氨 B.钢铁厂用热还原法冶炼铁
C.硫酸厂用接触法生产硫酸 D.炼油厂用分馏法生产汽油
7.下列叙述正确的是
A.F 与S混合加热生成FeS
e 2
B. NaHCO 的热稳定性大于Na CO
3 2 3
C.过量的铜与浓硫酸反应用一氧化氮生成
D.白磷在空气中加热到一定温度能转化成红磷
8.对实验:①中和滴定、②中和热的测定、③实验室制备乙烯、④乙酸乙酯的制取,叙述正
第1页 | 共10页确的是
A.①④必须加热 B.②③必须隔热 C.①②必须用指示剂 D.③④必须用催化剂
【答案】D
【解析】中和滴定不需要加热,A项错误;制备乙烯不需要隔热,B项错误;中和热测定
不需要指示剂,C项错误;实验室制备乙烯,乙酸乙酯制取都需要浓硫酸作催化剂,D项正
确。
【考点定位】本题考查化学实验的基本操作,考查的知识点有中和滴定、中和热的测定、乙
烯的实验室制法、乙酸乙酯的制取。
[来源:Zxxk.Com]
9.萤火虫发光原理如下
关于荧光素及氧化荧光素的叙述,正确的是
A.互为同系物 B.均可发生硝化反应
C.均可与碳酸氢钠反应 D.均最多有7个碳原子共平面
[来源:Z|xx|k.Com]
10.下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变
D.沸水中滴加适量饱和FeCl 溶液,形成带电的胶体,导电能力增强
3
第2页 | 共10页11.向10mL 0.1mol·L1 NH Al(SO ) 溶液中,滴加等浓度Ba(OH) 溶液x mL,下列叙述
4 4 2 2
正确的是
A. x=10时,溶液中有NH、Al3、SO2,且c(NH)c(Al3)
4 4 4
B. x=10时,溶液中有NH、AlO、SO2,且c(NH)c(SO2)
4 2 4 4 4
C. x=30时,溶液中有Ba2、AlO、OH,且c(OH)c(AlO)
2 2
D. x=30时,溶液中有Ba2、Al3、OH,且c(OH)c(Ba2)
12.
肼(H NNH )是一种高能燃料,有关化学反应的能量变化如题12图所示,已知断裂1mol
2 2
化学键所需的能量(kJ):NºN为942、O=O为500、N-N为154,则断裂1molN-H键所需
的能量(KJ)是
A.194 B.391 C.516 D.658
13.在一个不导热的密闭反应器中,只发生两个反应:
第3页 | 共10页a(g)+b(g) ‡ ˆˆ ˆ † ˆ 2c(g); V H 1 <0
x(g)+3y(g) ‡ ˆˆ ˆ † ˆ 2z(g); V H 1 >0 [来源:学.科.网Z.X.X.K]
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入x气体,y的物质的量浓度增大
26.(15分)金刚石SiC具有优良的耐磨、耐腐蚀特性,应用广泛.
(1) 碳与周期元素Q 的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非
极性分子,碳元素在周期表中的位置是 ,Q 是 ,R的电子
式为 .
(2) 一定条件下,Na还原CCl 可制备金刚石,反应结束冷却至室温后,回收其中CCL 的
4 4
实验操作名称为 ,除去粗产品中少量钠的试剂为 .
(3)碳还原SiO 制SiC,其粗产品中杂质为Si和SiO .先将 20.0gSiC粗产品加入到过量的
2 2
NaOH 溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生
成氢气的离子方程式为 ,硅盐酸的物质量浓度为 。
(4)下列叙述正确的有 (填序号),
①Na还原CCl 的反应、Cl 与H O的反应均是置换反应
4 2 2
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na SiO 溶液与SO 的反应可用于推断Si与S的非金属性强弱
2 3 3
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2
第4页 | 共10页27.(15分)氯离子插层镁铝水滑石Mg
2
Al(OH)
6
Cl
g
xH
2
O是一种新型离子交换材料,其
在高温下完全分解为MgO、Al、HCl和水蒸气,现用题27图装置进行试验确定其化学式
2
(固定装置略去)。
(1) Mg
2
A(l OH)
6
Cl
g
xH
2
O热分解的化学方程式为 。
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为 (按气流
方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的
操作名称是 。
第5页 | 共10页(3)加热前先通N 排尽装置中的空气,称取C、D的初始质量后,再持续通入N 的作用
2 2
是 、 等.
(4)完全分解后测得C增重3.65g 、D增重9.90g ,则x= .若取消冷却玻管B
后进行试验,测定x值将 (填“偏高”或“偏低”)
(5)上述水滑石在空气中放置时易发生反应生成[Mg Al(OH) Cl (CO ) ·zH O],该生成物
2 6 1—2y 3 y 2
能发生类似的热分解反应,现以此物为样品,用(2)中连接的装置和试剂进行实验测定
z ,除测定D的增重外,至少还需测定 .
28.(16分) 衣康酸M是制备高效除臭剂、粘合剂等多种精细化学品的重要原料,可经下列反
应路线得到(部分反应条件略).
第6页 | 共10页(1)A 发生加聚反应的官能团名称是 ,所得聚合物分子的结构型式是
(填“线型”或“体型”)。
(2)B®D的化学方程式为 。
(3)M的同分异构体Q是饱和二元羧酸,则Q的结构简式为 (只写一种)
(4)已知 ,E经五步转成变成M的
合成反应流程为:
①E ®G的化学反应类型为 ,G®H 的化学反应方程式为
②J ®L的离子方程式为
[来源:学科网ZXXK]
③已知: ,E经三步转变成M的合成反应流
程为
①E ®G的化学反应类型为 ,G®H 的化学反应方程式为 。
②J ®L的离子方程式为 。
自动脱水
③已知:C(OH) —— COOH H O,E经三步转变成M的合成反应流
3 2
程为 (实例如题28图);第二步反应试剂及条件限用NaOH 水溶液、加热)
第7页 | 共10页③
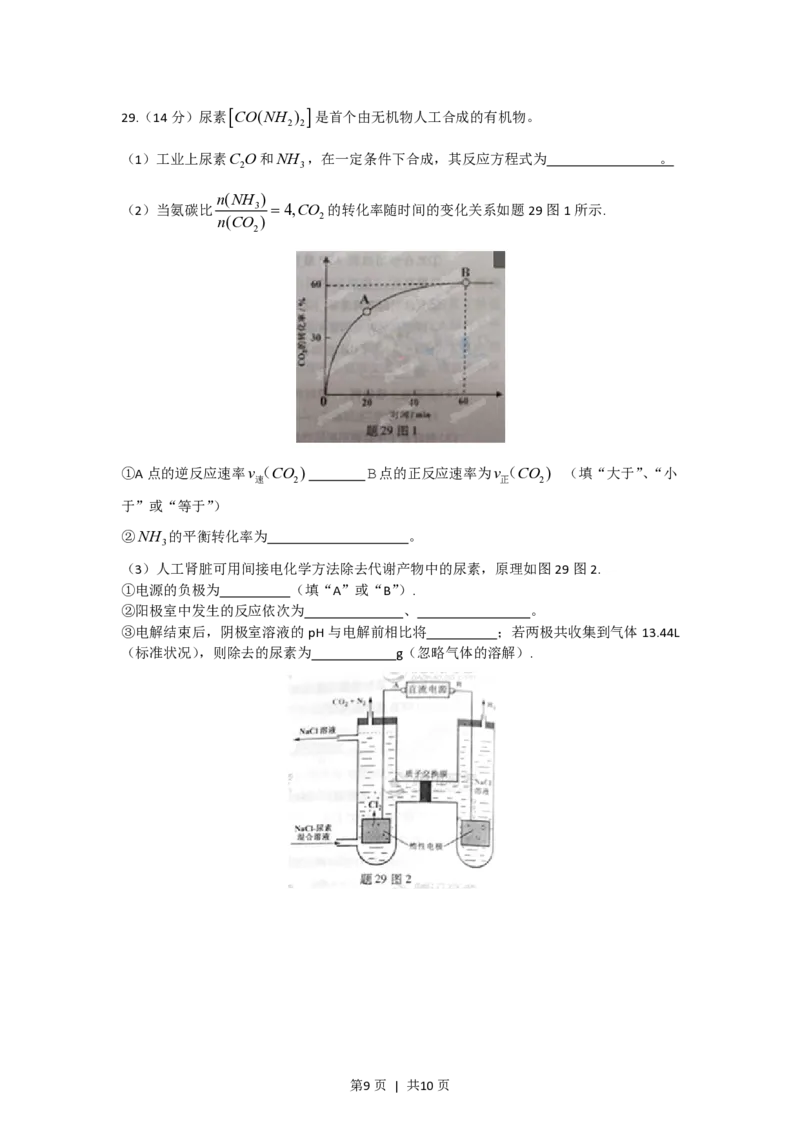
第8页 | 共10页29.(14分)尿素CO(NH ) 是首个由无机物人工合成的有机物。
2 2
(1)工业上尿素C O和NH ,在一定条件下合成,其反应方程式为 。
2 3
n(NH )
(2)当氨碳比 3 4,CO 的转化率随时间的变化关系如题29图1所示.
n(CO ) 2
2
①A点的逆反应速率v(CO ) B点的正反应速率为v(CO ) (填“大于”、“小
速 2 正 2
于”或“等于”)
②NH 的平衡转化率为 。
3
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图29图2.
[来源:学科网]
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 。
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L
(标准状况),则除去的尿素为 g(忽略气体的溶解).
第9页 | 共10页第10页 | 共10页