文档内容
永州市 2024 年高考第三次模拟考试
化 学
命题人:张慧坚(祁阳一中) 黄崇银(永州四中) 周祁山(江永二中)
审题人:陶爱玲(东安一中)
注意事项:
1.本试卷共18道小题,满分为100分,考试时量75分钟。
2.考生务必将各题的答案填写在答题卡的相应位置,在本试卷上作答无效。考试结
束后只交答题卡。
3.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ti-48 As
-75
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. 开发新材料、新能源,促进形成新质生产力,与化学知识密切相关。下列说法正确的
是
A.利用CO 合成脂肪酸,脂肪酸属于有机高分子
2
B.航天员手臂“延长器”中的碳纤维属于无机非金属材料
C.铜铟硫(CuInS)量子点是纳米级的半导体材料,属于胶体
2
D.长征系列运载火箭使用的燃料有液氢和煤油等化学品,属于新能源
2. 下列化学用语表述错误的是
A.碳化钙的电子式:
B.聚丙烯的结构简式:
C.HO 的分子结构示意图:
2 2
D.邻羟基苯甲醛分子内氢键示意图:
3. 下列实验不能达到目的的是
A.除去苯中混有的苯酚,可加入浓溴水过滤
B.除去NO中混有的NO,可将混合气通入水中
2
C.除去Cl 中混有的HCl,可将混合气通过饱和食盐水
2
D.除去CO 中混有的SO ,可将混合气通过酸性高锰酸钾溶液
2 2
4. 下列有关物质结构和性质的说法正确的是
永州市2024年高考第三次模拟考试·化学 第1页(共9页)
学科网(北京)股份有限公司A.晶体中有阳离子,不一定有阴离子
B.HO+中的H-O-H键角比水中的小
3
C.共价键的键能越大,分子晶体的熔点越高
D.非金属元素都位于元素周期表中的p区
5. 能正确表示下列变化的离子方程式是
A.甲醇碱性燃料电池负极方程式:CHOH-6e-+HO=CO↑+6H+
3 2 2
B.铁粉与过量稀硝酸反应:Fe+NO +4H+=Fe3++NO↑+2HO
2
C.亚硫酸氢钠的水解:HSO +HO SO +HO+
2 3
D.硫酸铜溶液中通入硫化氢:Cu2++S2-=CuS↓
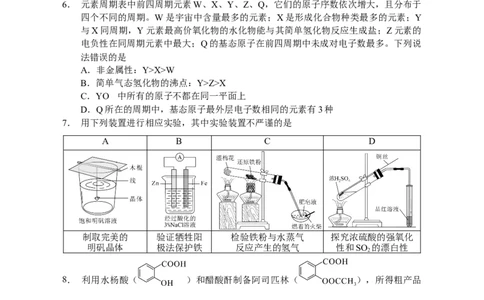
6. 元素周期表中前四周期元素W、X、Y、Z、Q,它们的原子序数依次增大,且分布于
四个不同的周期。W是宇宙中含量最多的元素;X是形成化合物种类最多的元素;Y
与X同周期,Y元素最高价氧化物的水化物能与其简单氢化物反应生成盐;Z元素的
电负性在同周期元素中最大;Q的基态原子在前四周期中未成对电子数最多。下列说
法错误的是
A.非金属性:Y>X>W
B.简单气态氢化物的沸点:Y>Z>X
C.YO 中所有的原子不都在同一平面上
D.Q所在的周期中,基态原子最外层电子数相同的元素有3种
7. 用下列装置进行相应实验,其中实验装置不严谨的是
A B C D
制取完美的 验证牺牲阳 检验铁粉与水蒸气 探究浓硫酸的强氧化
明矾晶体 极法保护铁 反应产生的氢气 性和SO 的漂白性
2
8. 利用水杨酸( )和醋酸酐制备阿司匹林( ),所得粗产品
含有水杨酸和水杨酸聚合物,利用如下方法提纯阿司匹林:
已知:①阿司匹林微溶于水,可与NaHCO 溶液反应生成水溶性钠盐。pH=3时,阿
3
司匹林沉淀完全;②水杨酸聚合物难溶于水和NaHCO 溶液。下列说法错误的
3
永州市2024年高考第三次模拟考试·化学 第2页(共9页)
学科网(北京)股份有限公司是
A.试剂a、b可以分别选用NaHCO 溶液、盐酸
3
B.操作Ⅱ为过滤
C.洗涤滤渣①的主要目的是得到较纯净的水杨酸聚合物
D.可用FeCl 溶液检验产品中是否含有水杨酸
3
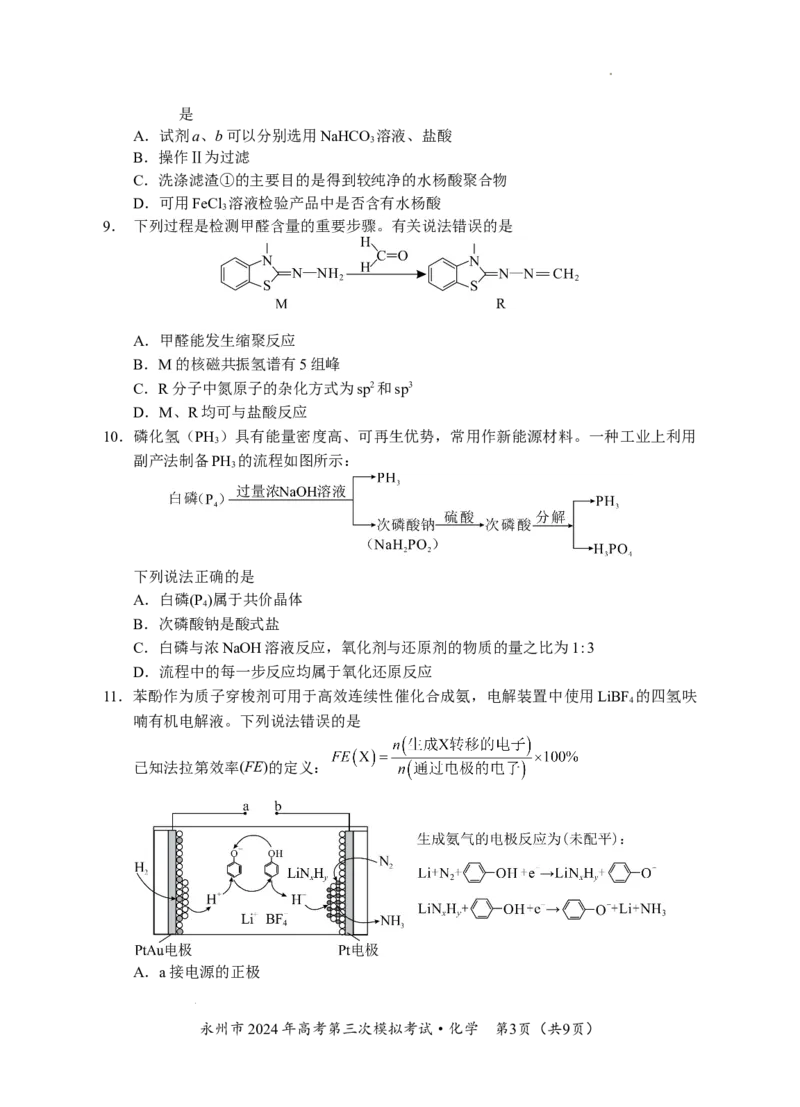
9. 下列过程是检测甲醛含量的重要步骤。有关说法错误的是
A.甲醛能发生缩聚反应
B.M的核磁共振氢谱有5组峰
C.R分子中氮原子的杂化方式为sp2和sp3
D.M、R均可与盐酸反应
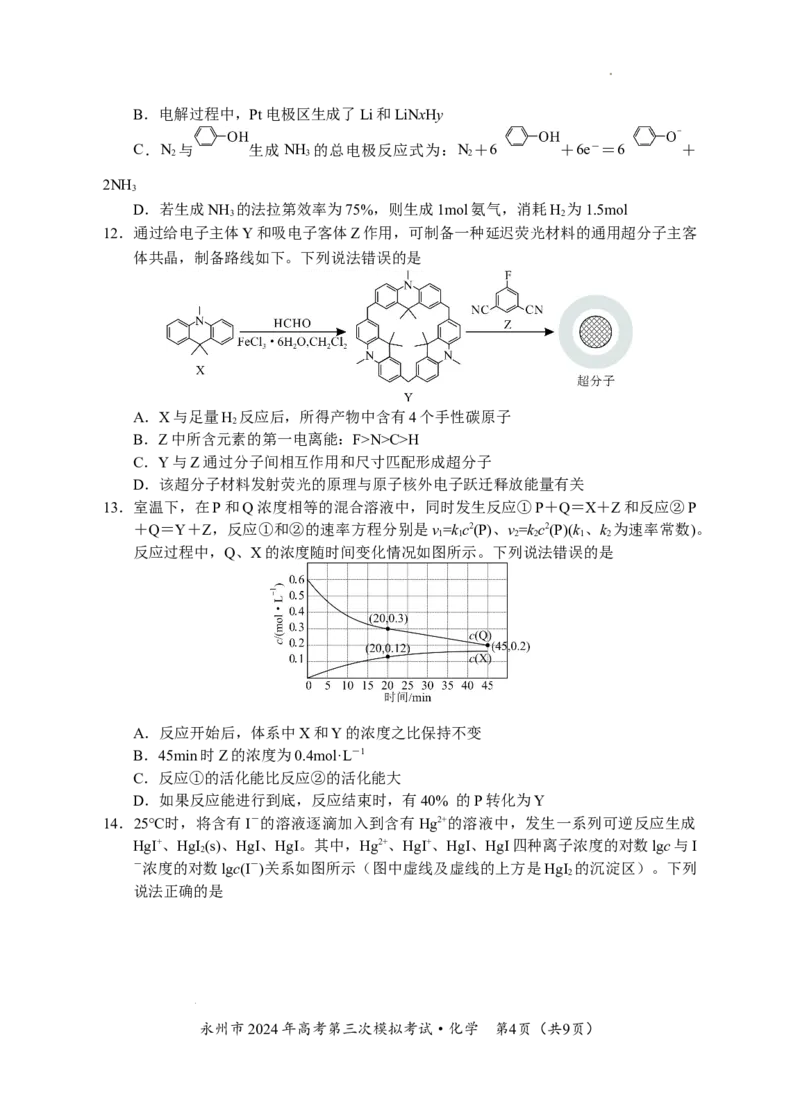
10.磷化氢(PH )具有能量密度高、可再生优势,常用作新能源材料。一种工业上利用
3
副产法制备PH 的流程如图所示:
3
下列说法正确的是
A.白磷(P )属于共价晶体
4
B.次磷酸钠是酸式盐
C.白磷与浓NaOH溶液反应,氧化剂与还原剂的物质的量之比为1:3
D.流程中的每一步反应均属于氧化还原反应
11.苯酚作为质子穿梭剂可用于高效连续性催化合成氨,电解装置中使用LiBF 的四氢呋
4
喃有机电解液。下列说法错误的是
已知法拉第效率(FE)的定义:
A.a接电源的正极
永州市2024年高考第三次模拟考试·化学 第3页(共9页)
学科网(北京)股份有限公司B.电解过程中,Pt电极区生成了Li和LiNxHy
C.N 与 生成NH 的总电极反应式为:N +6 +6e-=6 +
2 3 2
2NH
3
D.若生成NH 的法拉第效率为75%,则生成1mol氨气,消耗H 为1.5mol
3 2
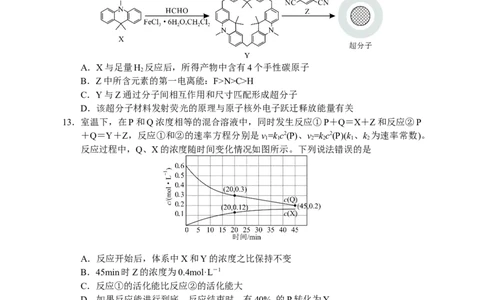
12.通过给电子主体Y和吸电子客体Z作用,可制备一种延迟荧光材料的通用超分子主客
体共晶,制备路线如下。下列说法错误的是
A.X与足量H 反应后,所得产物中含有4个手性碳原子
2
B.Z中所含元素的第一电离能:F>N>C>H
C.Y与Z通过分子间相互作用和尺寸匹配形成超分子
D.该超分子材料发射荧光的原理与原子核外电子跃迁释放能量有关
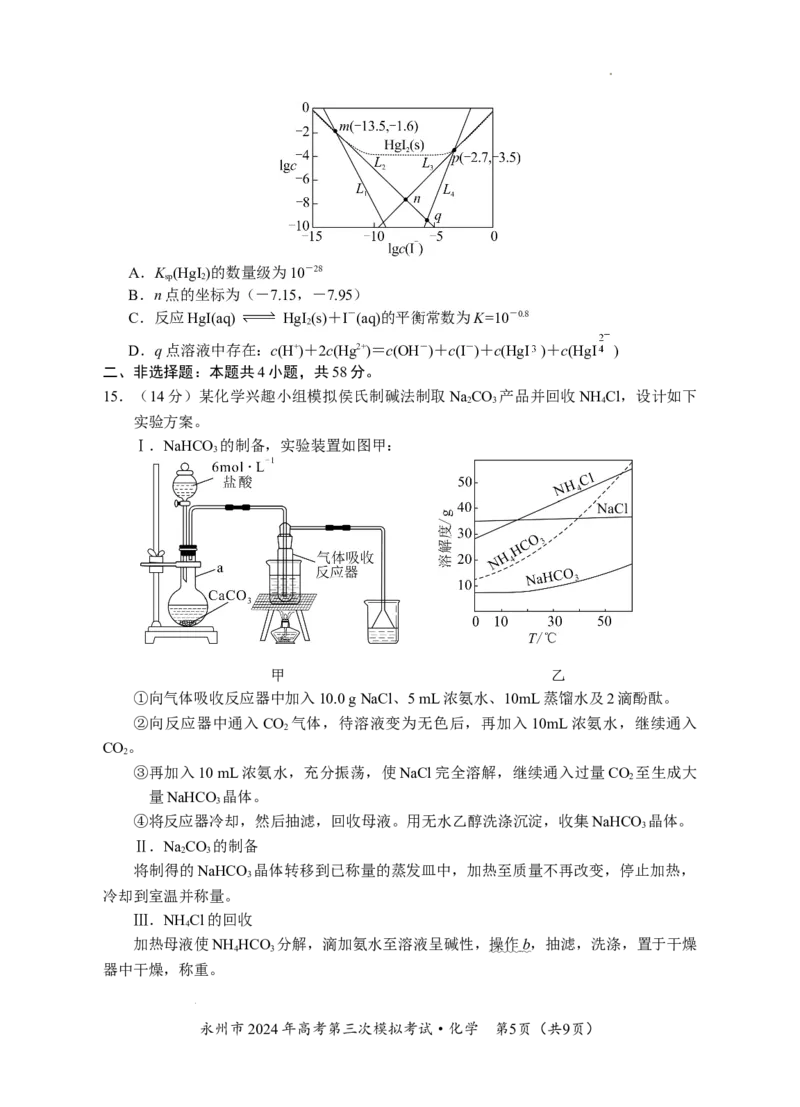
13.室温下,在P和Q浓度相等的混合溶液中,同时发生反应①P+Q=X+Z和反应②P
+Q=Y+Z,反应①和②的速率方程分别是v=kc2(P)、v=kc2(P)(k 、k 为速率常数)。
1 1 2 2 1 2
反应过程中,Q、X的浓度随时间变化情况如图所示。下列说法错误的是
A.反应开始后,体系中X和Y的浓度之比保持不变
B.45min时Z的浓度为0.4mol·L-1
C.反应①的活化能比反应②的活化能大
D.如果反应能进行到底,反应结束时,有40% 的P转化为Y
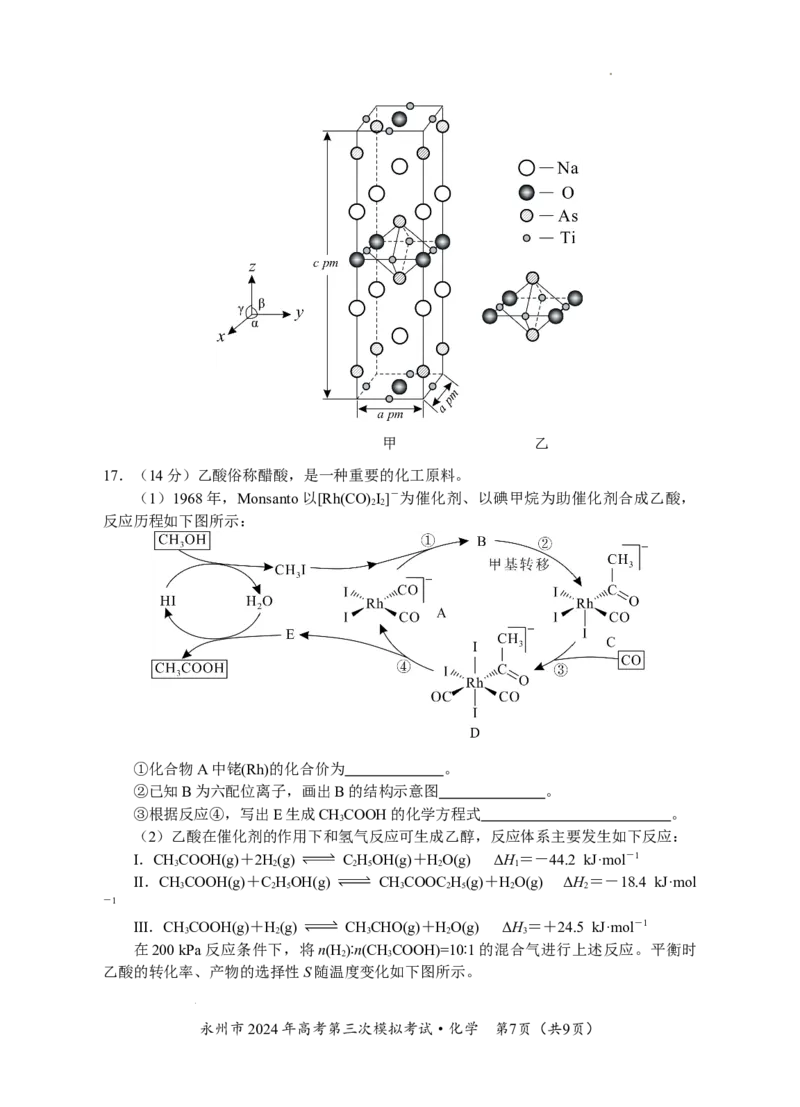
14.25℃时,将含有I-的溶液逐滴加入到含有Hg2+的溶液中,发生一系列可逆反应生成
HgI+、HgI (s)、HgI、HgI。其中,Hg2+、HgI+、HgI、HgI四种离子浓度的对数lgc与I
2
-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI 的沉淀区)。下列
2
说法正确的是
永州市2024年高考第三次模拟考试·化学 第4页(共9页)
学科网(北京)股份有限公司A.K (HgI )的数量级为10-28
sp 2
B.n点的坐标为(-7.15,-7.95)
C.反应HgI(aq) HgI (s)+I-(aq)的平衡常数为K=10-0.8
2
D.q点溶液中存在:c(H+)+2c(Hg2+)=c(OH-)+c(I-)+c(HgI )+c(HgI )
二、非选择题:本题共4小题,共58分。
15.(14分)某化学兴趣小组模拟侯氏制碱法制取NaCO 产品并回收NH Cl,设计如下
2 3 4
实验方案。
Ⅰ.NaHCO 的制备,实验装置如图甲:
3
甲 乙
①向气体吸收反应器中加入10.0 g NaCl、5 mL浓氨水、10mL蒸馏水及2滴酚酞。
②向反应器中通入CO 气体,待溶液变为无色后,再加入10mL浓氨水,继续通入
2
CO。
2
③再加入10 mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO 至生成大
2
量NaHCO 晶体。
3
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO 晶体。
3
Ⅱ.NaCO 的制备
2 3
将制得的NaHCO 晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,
3
冷却到室温并称量。
Ⅲ.NH Cl的回收
4
加热母液使NH HCO 分解,滴加氨水至溶液呈碱性, 操作 b,抽滤,洗涤,置于干燥
4 3
器中干燥,称重。
永州市2024年高考第三次模拟考试·化学 第5页(共9页)
学科网(北京)股份有限公司(1)仪器a的名称是 。
(2)步骤③中通入过量CO 生成NaHCO 晶体的离子方程式为 。
2 3
(3)已知0℃时NaHCO 的溶解度是0.8 mol·L-1,不考虑溶液混合时体积的变化及对
3
NaHCO 溶解度的影响,若10.0 g NaCl全部转化成NaHCO ,则在0℃时从溶液中能析出
3 3
NaHCO 固体 g(保留1位小数)。
3
(4)已知碳酸氢钠分解反应的ΔH=+135.6 kJ·mol-1·K-1、ΔS=+333.3 J·mol-1·K-
1。在下列哪些温度下该反应能自发进行 (填标号)。
A.308K B.373K C.421K D.573K
(5)①回收NH Cl时加入氨水的目的是 。
4
②结合图乙,简单说明操作b的过程 。
(6)若制得的NaHCO 中含有未反应的NaCl,则分解后所得固体的质量 (填
3
“大于”、“小于”或“等于”)理论上生成NaCO 的质量。
2 3
16.(15分)二硼化钛(TiB )是一种高熔点、高硬度、电阻小的导电陶瓷材料,在工业领
2
域具有广泛的应用。利用废弃SCR催化剂(主要含TiO 、VO 、Al O 、SiO 等),
2 2 5 2 3 2
制备TiB 并回收钒的工艺流程如图所示:
2
已知:①TiO 、VO 都能与 NaOH 溶液反应,生成不溶性的 NaTiO 和可溶性的
2 2 5 2 3
NaVO ;
3
②B O 高温下蒸气压大、易挥发;
2 3
③溶液酸性较强时,五价钒粒子主要以VO的形式存在。
回答下列问题:
(1)“酸浸”中生成TiO2+的离子方程式为 。
(2)“滤渣①”的主要成分为 (填化学式)。
(3)“热水解”工艺中,经处理可循环利用的物质是 (填化学式)。
(4)“热还原”时生成一种可燃性气体,每制备1 molTiB ,转移电子的物质的量为
2
mol。过程中B O 的实际用量超过了理论用量,主要原因是 。
2 3
(5)“沉钒”时,溶液 pH 过低或过高均不利于生成 NHVO 沉淀,原因是
4 3
。
(6)含钛X晶体是一种高温超导母体,其晶胞结构如图甲所示(α=β=γ=90°),Ti原子
与As原子构成的八面体如图乙所示,阿伏伽德罗常数的值为N 。回答下列问题:
A
①一个晶胞中,由Ti原子与As原子构成的八面体的平均数目为 。
②X晶体的密度为 g·cm-3。
永州市2024年高考第三次模拟考试·化学 第6页(共9页)
学科网(北京)股份有限公司甲 乙
17.(14分)乙酸俗称醋酸,是一种重要的化工原料。
(1)1968年,Monsanto以[Rh(CO) I]-为催化剂、以碘甲烷为助催化剂合成乙酸,
2 2
反应历程如下图所示:
①化合物A中铑(Rh)的化合价为 。
②已知B为六配位离子,画出B的结构示意图 。
③根据反应④,写出E生成CHCOOH的化学方程式 。
3
(2)乙酸在催化剂的作用下和氢气反应可生成乙醇,反应体系主要发生如下反应:
I.CHCOOH(g)+2H(g) C HOH(g)+HO(g) ΔH=-44.2 kJ·mol-1
3 2 2 5 2 1
II.CHCOOH(g)+C HOH(g) CHCOOC H(g)+HO(g) ΔH =-18.4 kJ·mol
3 2 5 3 2 5 2 2
-1
III.CHCOOH(g)+H(g) CHCHO(g)+HO(g) ΔH=+24.5 kJ·mol-1
3 2 3 2 3
在200 kPa反应条件下,将n(H )∶n(CHCOOH)=10∶1的混合气进行上述反应。平衡时
2 3
乙酸的转化率、产物的选择性S随温度变化如下图所示。
永州市2024年高考第三次模拟考试·化学 第7页(共9页)
学科网(北京)股份有限公司已知:
①CHCHO(g)+H(g) C HOH(g)的ΔH= kJ·mol-1。
3 2 2 5
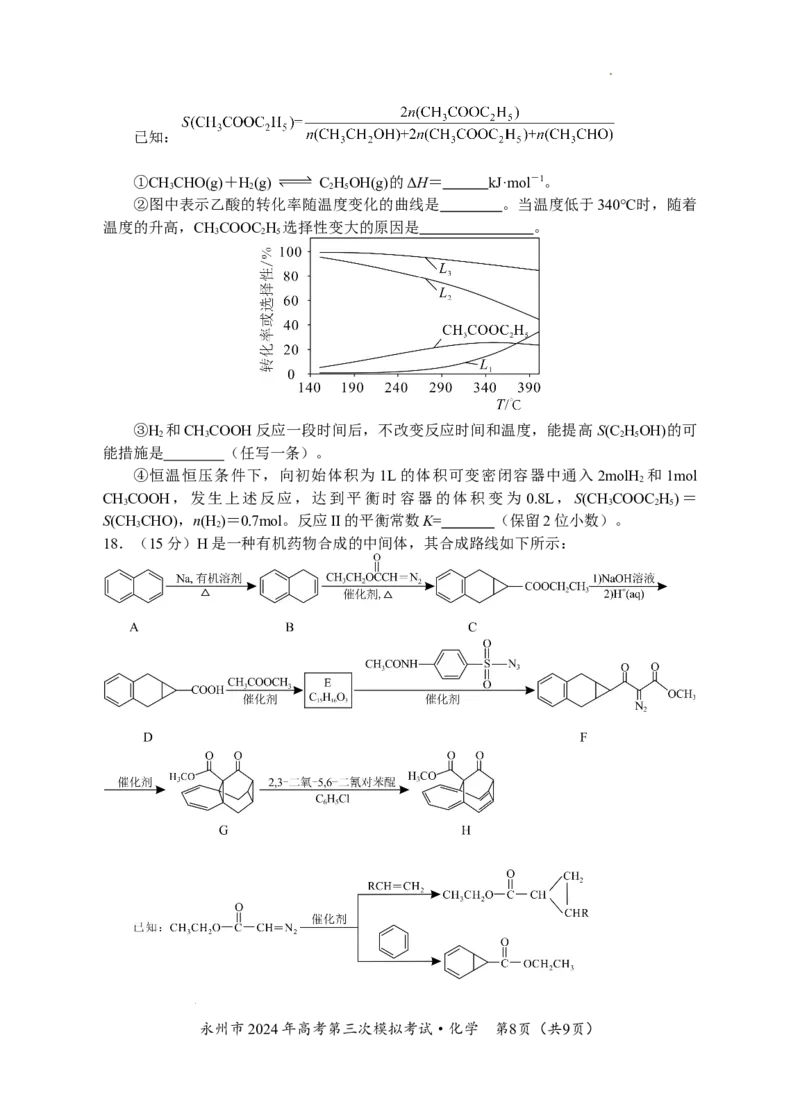
②图中表示乙酸的转化率随温度变化的曲线是 。当温度低于340℃时,随着
温度的升高,CHCOOC H 选择性变大的原因是 。
3 2 5
③H 和CHCOOH反应一段时间后,不改变反应时间和温度,能提高S(C HOH)的可
2 3 2 5
能措施是 (任写一条)。
④恒温恒压条件下,向初始体积为1L的体积可变密闭容器中通入2molH 和1mol
2
CHCOOH,发生上述反应,达到平衡时容器的体积变为 0.8L,S(CHCOOC H)=
3 3 2 5
S(CHCHO),n(H )=0.7mol。反应II的平衡常数K= (保留2位小数)。
3 2
18.(15分)H是一种有机药物合成的中间体,其合成路线如下所示:
永州市2024年高考第三次模拟考试·化学 第8页(共9页)
学科网(北京)股份有限公司回答下列问题:
(1)A的名称是 。
(2)H中含氧官能团的名称是 。
(3)B→C的反应中,还生成一种气体,该气体为 。
(4)D→E化学方程式是 。
(5)在D的同分异构体中,满足下列条件的有 种(不考虑立体异构)。
①含有苯环;②含有两个六元环;③1mol该物质与足量银氨溶液反应可得4molAg
其中,核磁共振氢谱图上有4组峰,且峰面积之比为1∶1∶2∶2的同分异构体的结构简式
为 (写出任意一种)。
(6)参照上述合成路线,设计以CH =CH—CH=CH 和 为
2 2
原料合成 的路线 (无机试剂和有机溶剂任用)。
永州市2024年高考第三次模拟考试·化学 第9页(共9页)
学科网(北京)股份有限公司