文档内容
试卷第1页,共6页
2023-2024 学年度高三化学月考试卷(东校)
一、单选题(每道3 分,共51 分)
1.中华古诗文华丽优美且富含哲理,下列叙述不涉及氧化还原反应的是
A.落红不是无情物,化作春泥更护花
B.白日登山望烽火,黄昏饮马傍交河
C.欲渡黄河冰塞川,将登太行雪满山
D.蜡烛有心还惜别,替人垂泪到天明
2.北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”核
电海外投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
A.冬奥会“飞扬”火炬所用的燃料
2
H 为氧化性气体
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D.核电站反应堆所用铀棒中含有的
235
92 U 与
238
92 U 互为同位素
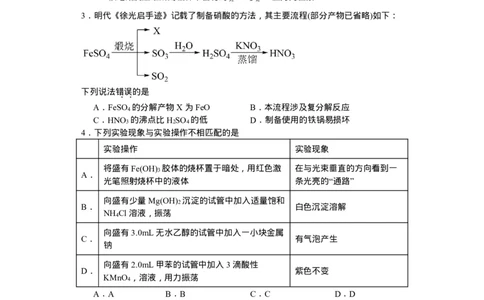
3.明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误
..的是
A.FeSO4 的分解产物X 为FeO
B.本流程涉及复分解反应
C.HNO3 的沸点比H2SO4 的低
D.制备使用的铁锅易损坏
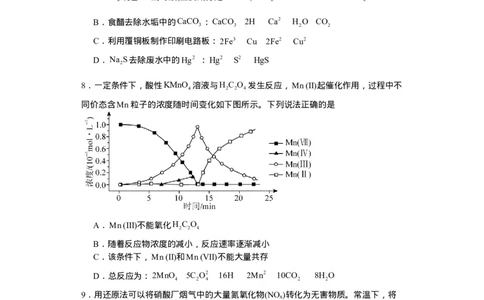
4.下列实验现象与实验操作不相匹配的是
实验操作
实验现象
A.
将盛有Fe(OH)3 胶体的烧杯置于暗处,用红色激
光笔照射烧杯中的液体
在与光束垂直的方向看到一
条光亮的“通路”
B.
向盛有少量Mg(OH)2 沉淀的试管中加入适量饱和
NH4Cl 溶液,振荡
白色沉淀溶解
C.
向盛有3.0mL 无水乙醇的试管中加入一小块金属
钠
有气泡产生
D.
向盛有2.0mL 甲苯的试管中加入3 滴酸性
KMnO4,溶液,用力振荡
紫色不变
A.A
B.B
C.C
D.D
5.部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.a 可与e 反应生成b
B.b 既可被氧化,也可被还原
C.可将e加入浓碱液中制得d 的胶体
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}
试卷第2页,共6页
D.可存在b
c
d
e
b
的循环转化关系
6.下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气:
2+
-
3+
-
2
2
2Fe +2I +2Cl
2Fe +I +4Cl
B.向次氯酸钙溶液通入足量二氧化碳:
-
-
2
2
3
ClO +CO +H O
HClO+HCO
C.铜与稀硝酸:
+
-
2+
3
2
2
Cu+4H +2NO
Cu
+2NO
+2H O
D.向硫化钠溶液通入足量二氧化硫:
2-
-
2
2
2
3
S +2SO +2H O
H S+2HSO
7.下列离子方程式与所给事实不相符的是
A.
2
Cl 制备84 消毒液(主要成分是NaClO):
2
2
Cl
2OH
Cl
ClO
H O
B.食醋去除水垢中的
3
CaCO :
2
3
2
2
CaCO
2H
Ca
H O
CO
C.利用覆铜板制作印刷电路板:
3
2
2
2Fe
Cu
2Fe
Cu
D.
2
Na S去除废水中的
2
Hg :
2
2
Hg
S
HgS
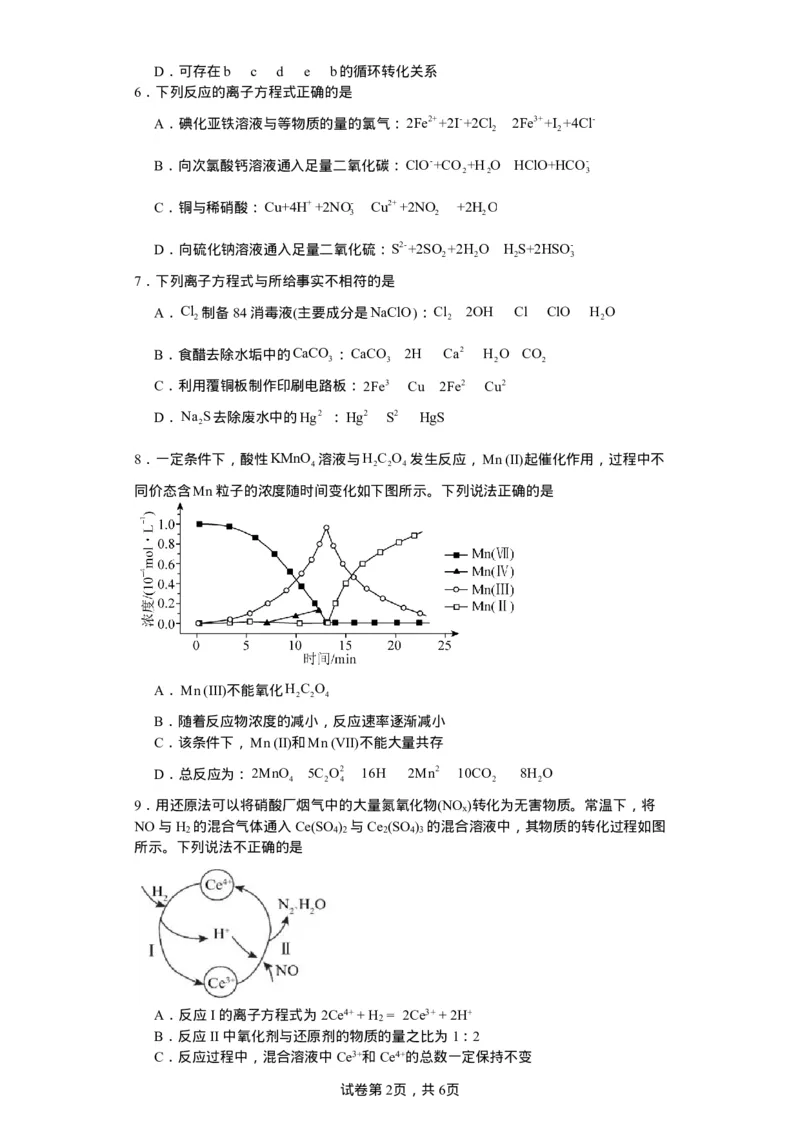
8.一定条件下,酸性
4
KMnO 溶液与
2
2
4
H C O 发生反应,Mn (Ⅱ)起催化作用,过程中不
同价态含Mn 粒子的浓度随时间变化如下图所示。下列说法正确的是
A.Mn (Ⅲ)不能氧化
2
2
4
H C O
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn (Ⅱ)和Mn (Ⅶ)不能大量共存
D.总反应为:
2
2
4
2
4
2
2
2MnO
5C O
16H
2Mn
10CO
8H O
9.用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将
NO 与H2 的混合气体通入Ce(SO4)2 与Ce2(SO4)3 的混合溶液中,其物质的转化过程如图
所示。下列说法不正确的是
A.反应I 的离子方程式为2Ce4+ + H2 = 2Ce3+ + 2H+
B.反应II 中氧化剂与还原剂的物质的量之比为1:2
C.反应过程中,混合溶液中Ce3+和Ce4+的总数一定保持不变
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}
试卷第3页,共6页
D.理论上,每消耗2.24 L 氢气,转移的电子的物质的量为0.2 mol
10.关于反应
5
2
4
2
2
2Fe(CO)
7N O
2FeO
14NO
10CO
,下列说法正确的是
A.
2
4
N O 发生氧化反应
B.生成
2
1molCO ,转移2mol电子
C.氧化产物与还原产物的物质的量之比为5:7
D.
2
FeO 可以和Fe 反应生成
2
3
Fe O
11.25℃时,下列各组离子中可以在水溶液中大量共存的是
A.H、
4
NH
、ClO、Cl
B.H、
2
Mg 、I、
3
NO
C.Na 、
3
Al 、
3
HCO
、
2
4
SO
D.K、Na 、
2
3
SO 、O H
12.常温下,下列粒子能在指定的溶液中大量共存的是
A.遇KSCN 变红色的溶液:Na 、
2
Mg 、
2
2
H O 、Cl
B.
13
1
w
1 10
mol L
H
K
c
的溶液中:
4
NH
、
2
Ca 、Cl、
3
NO
C.pH=0 的溶液中:
4
NH
、
2
Fe 、
2
2
3
S O 、ClO
D.在溶质为
3
KHCO 溶液中:K、Cl、
3
Al 、
2
4
SO
13.室温下,下列各组离子在指定溶液中一定能大量共存的是
A.在
4
NH SCN溶液中:K、
3
Fe 、Cl、
2
4
SO
B.含大量H的溶液中:
2
Zn 、
2
Cu 、
3
NO、
2
4
SO
C.加入Al 产生
2
H 的溶液中:Na 、
2
Mg 、
3
NO、
3
HCO
D.由水电离的
12
1
OH
1 10
mol L
c
的溶液中:K、
2
Ca 、Cl、ClO
14.某学习小组为探究氯化铜与亚硫酸钠的反应,设计了如下实验:
1
2mL0.2mol L
2
CuCl 溶液
1
2mL0.2mol L
2
3
Na SO 溶液
橙黄色沉淀
(含Cu、
2
Cu 、
2
4
SO )
白色沉淀
(CuCl)
已知:
2
Cu
Cu
Cu
稀硫酸
。
下列分析中,不正确
...的是
A.
1
0.2mol L
的
2
CuCl 溶液呈弱酸性
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}
试卷第4页,共6页
B.由实验可知,生成橙黄色沉淀的速率较快,而生成白色沉淀的反应趋势更大
C.取洗涤后的橙黄色沉淀于试管中,加入稀硫酸,若溶液变蓝,则说明橙黄色沉
淀含有Cu
D.本实验中,
2
CuCl 溶液和
2
3
Na SO 溶液的总反应离子方程式为:
2
2
2
3
2
4
2Cu
SO
2Cl
H O
2CuCl
SO
2H
15.下列有关反应
2
2
2
2
2Na O
2H O
4NaOH
O
的说法正确的是
A.该反应是吸热反应
B.生成物的总键能小于反应物的总键能
C.反应物总能量高于生成物总能量
D.涉及的四种物质均属于电解质
16.下列离子方程式书写正确的是
A.二氧化氮气体通入水中:
2
2
3
2NO
H O 2H
NO
NO
B.小块钠放入
4
CuSO 溶液中:
2
2Na
Cu
2Na
Cu
C.草酸加入酸性
4
KMnO 溶液中:
2
2
4
2
4
2
2
2MnO
5C O
16H
2Mn
10CO
8H O
D.少量氯气通入到冷的NaOH 溶液中:
2
2
Cl
2OH
Cl
ClO
H O
17.卤素的应用广泛,常运用于化学工业尤其是有机合成工业上。下列关于卤素单质或
其化合物的叙述正确的是
A.漂白液中次氯酸钠的电离方程式:NaClO =Na+ +Cl
-+O2-
B.向溴化亚铁溶液中滴入少量氯水的离子方程式:2Fe2+ +Cl2=2Fe3++2Cl
-
C.在含有KI 的溶液中可以大量存在H+、Mg2+、
3
NO、
2-
4
SO
D.加热含1molHCl 的浓盐酸与足量MnO2 的混合物,产生5.6L(标准状况)的氯气
二、填空题(共49 分)
18(12 分).电解质在人体内的作用是十分广泛和十分重要的,当电解质紊乱时,人体
就要出现一系列不适症状,甚至会危及生命。现有下列几种物质:①铜;②NH3;③H2SO4;
④Ba(OH)2 固体;⑤熔融的NaHSO4;⑥稀盐酸。
(1)将上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
分类标准
能导电的
电解质
非电解质
属于该类的物质
(2)上述六种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的
化学方程式为
。
(3)⑤在水中的电离方程式为
。
(4)将少量④的溶液加入⑤的溶液中,溶液呈中性,反应的离子方程式为
。
19(11 分).Ⅰ.Na2O2 具有很强的氧化性,其与FeCl2 溶液能发生反应:
Na2O2+FeCl2+H2O→Fe(OH)3↓+FeCl3+NaCl(未配平)。
(1)已知FeCl2 的化学计量数为6,配平上述化学方程式,并标出电子转移的方向和数
目:
。该反应中氧化产物是
。
Ⅱ.碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}
试卷第5页,共6页
(2)泡沫灭火器中主要成分是NaHCO3 溶液和Al2(SO4)3 溶液,二者混合后发生相互促进
的水解反应生成Al(OH)3 和CO2 进行灭火,写出该反应的化学方程式:
。
(3)向NaHCO3 溶液中加入少许Ba(OH)2 固体,忽略溶液体积变化,溶液中c(CO
2
3
)的变
化是
(填“增大”“减小”或“不变”)。
(4)NaHCO3 是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化
铵有两种方法:①通入氨,冷却、加食盐,过滤;②不通入氨,冷却、加食盐,过滤。
这两种方法中,
(填“①”或“②”)析出的氯化铵纯度更高。
20(12 分).写出下列反应的离子方程式。
(1)Ca(OH)2 溶液与NaHCO3 溶液反应
①NaHCO3 少量:
;
②NaHCO3 足量:
。
类似该反应的还有Ca(HCO3)2 溶液与NaOH 溶液的反应。
(2)NaHSO4 溶液与Ba(OH)2 溶液反应
①加Ba(OH)2 溶液至
2
4
SO 恰好沉淀完全:
;
②加Ba(OH)2 溶液至溶液呈中性:
。
(3)KAl(SO4)2 溶液与Ba(OH)2 溶液反应
①Ba(OH)2 少量:
;
②Ba(OH)2 足量:
。
21(14 分).从钒铬锰矿渣(主要成分为
2
5
V O 、
2
3
Cr O 、MnO)中提铬的一种工艺流程如
下:
已知:pH 较大时,二价锰[ Mn(II) ](在空气中易被氧化.回答下列问题:
(1)Cr 元素位于元素周期表第
周期
族。
(2)用
3
FeCl 溶液制备
3
Fe OH
胶体的化学方程式为
。
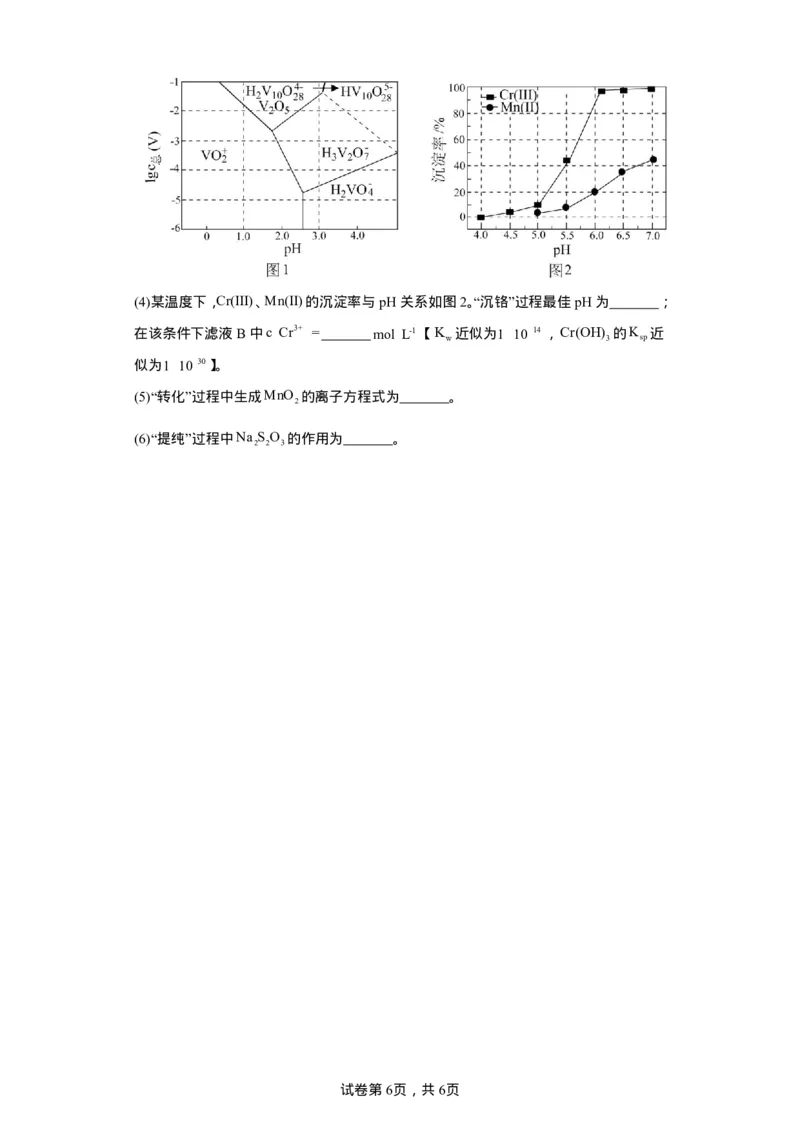
(3)常温下,各种形态五价钒粒子总浓度的对数[
总
lgc
V ]与pH 关系如图1。已知钒铬
锰矿渣硫酸浸液中
1
总
-
c (V)=0.01mol
L
,“沉钒”过程控制pH=3.0,则与胶体共沉降的五
价钒粒子的存在形态为
(填化学式)。
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}
试卷第6页,共6页
(4)某温度下,Cr(III) 、Mn(II) 的沉淀率与pH 关系如图2。“沉铬”过程最佳pH 为
;
在该条件下滤液B 中
3+
c Cr
=
-1
mol L
【
w
K 近似为
14
1 10
,
3
Cr(OH) 的
sp
K 近
似为
30
1 10
】。
(5)“转化”过程中生成
2
MnO 的离子方程式为
。
(6)“提纯”过程中
2
2
3
Na S O 的作用为
。
{#{QQABSQqAoggAAAAAARgCQQUCCkCQkBGCCIgOhFAIMAAASAFABAA=}#}