文档内容
江苏省扬州中学 2024 届高三第一学期开学考试
化学试题
可能用到的相对原子质量:H—1 C—12 O—16 Ti—48 Ba—137
一、 单项选择题:共13题,每题3分,共39分。每小题只有一个选项最符合题意。
1.科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是
A.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO ) ]”:其成分属于无机盐
8 4 7
C.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
2. 反应2NH +NaClO=N H +NaCl+H O用于合成N H 。下列说法不正确的是
3 2 4 2 2 4
· ·
·· ··
A. NH 的空间结构为正三角形 B. NaClO的电子式为Na+[· O Cl ]-
3 ·
······
C. N H 含有极性键和非极性键 D. H O和N H 之间可以形成氢键
2 4 2 2 4
3. 短周期主族元素X、Y、Z、W原子序数依次增大。基态X原子的2p轨道上有1个电
子的自旋方向与其他电子的自旋方向相反,基态Y原子M层上有两个未成对电子,基
态W原子的电子总数是其最高能级电子数的4倍。下列说法正确的是
A.第一电离能:W>Z>Y
B.原子半径:W>Y>X
C. 简单氢化物的沸点:W>Z>X
D.最高价氧化物对应水化物的酸性:W>Z>Y
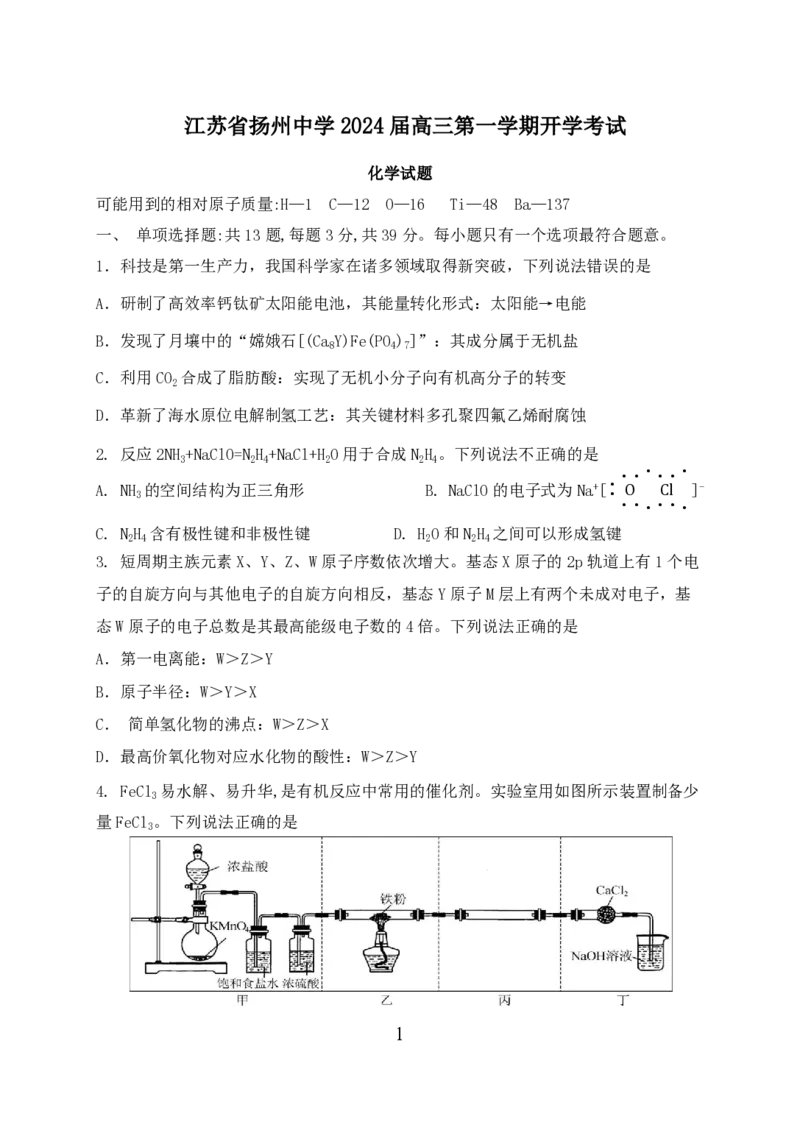
4. FeCl 易水解、易升华,是有机反应中常用的催化剂。实验室用如图所示装置制备少
3
量FeCl 。下列说法正确的是
3
1
学科网(北京)股份有限公司A. 实验开始,先点燃酒精灯,再滴加浓盐酸
B. 实验时若Cl 不足量,则可能生成FeCl
2 2
C. 装置丙的作用是收集FeCl
3
D. 装置丁中CaCl 的作用是吸收未反应的Cl
2 2
阅读下列材料,完成5~7题:
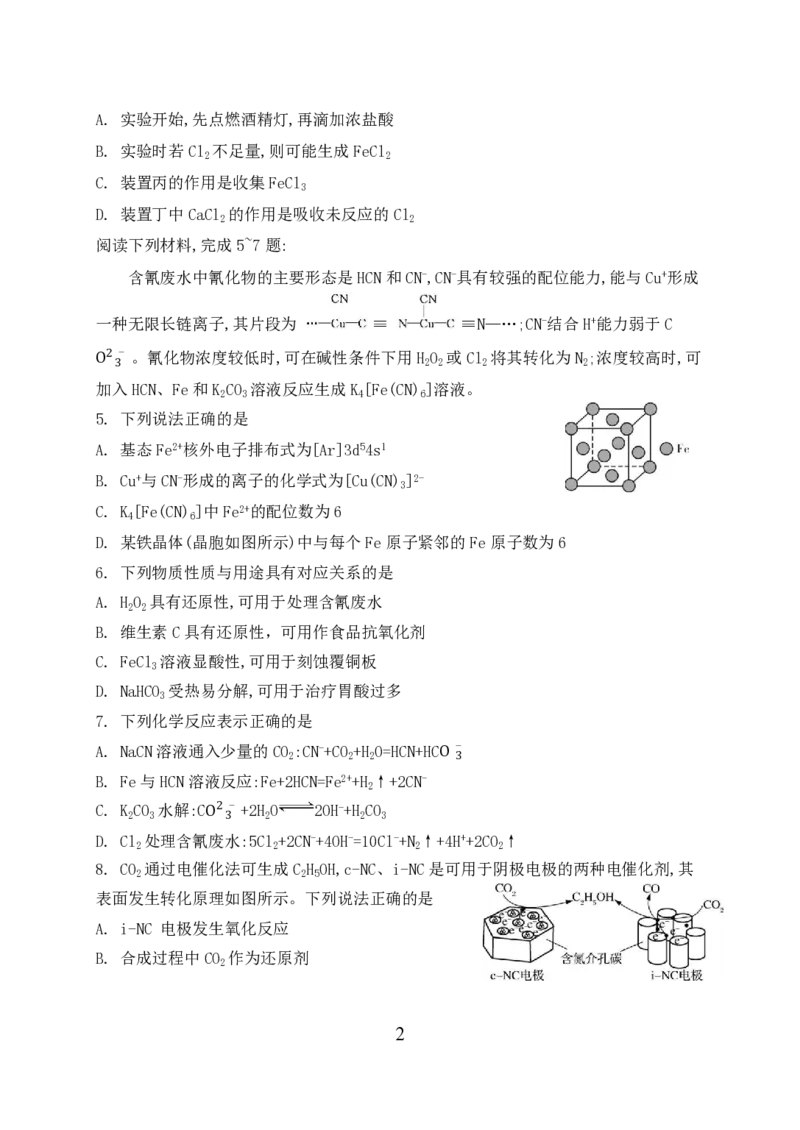
含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成
一种无限长链离子,其片段为 ≡ ≡N—…;CN-结合H+能力弱于C
O2 - 。氰化物浓度较低时,可在碱性条件下用H O 或Cl 将其转化为N ;浓度较高时,可
3 2 2 2 2
加入HCN、Fe和K CO 溶液反应生成K [Fe(CN) ]溶液。
2 3 4 6
5. 下列说法正确的是
A. 基态Fe2+核外电子排布式为[Ar]3d54s1
B. Cu+与CN-形成的离子的化学式为[Cu(CN) ]2-
3
C. K [Fe(CN) ]中Fe2+的配位数为6
4 6
D. 某铁晶体(晶胞如图所示)中与每个Fe原子紧邻的Fe原子数为6
6. 下列物质性质与用途具有对应关系的是
A. H O 具有还原性,可用于处理含氰废水
2 2
B. 维生素C具有还原性,可用作食品抗氧化剂
C. FeCl 溶液显酸性,可用于刻蚀覆铜板
3
D. NaHCO 受热易分解,可用于治疗胃酸过多
3
7. 下列化学反应表示正确的是
A. NaCN溶液通入少量的CO :CN-+CO +H O=HCN+HCO -
2 2 2 3
B. Fe与HCN溶液反应:Fe+2HCN=Fe2++H ↑+2CN-
2
C. K CO 水解:CO2 - +2H O 2OH-+H CO
2 3 3 2 2 3
D. Cl 处理含氰废水:5Cl +2CN-+4OH-=10Cl-+N ↑+4H++2CO ↑
2 2 2 2
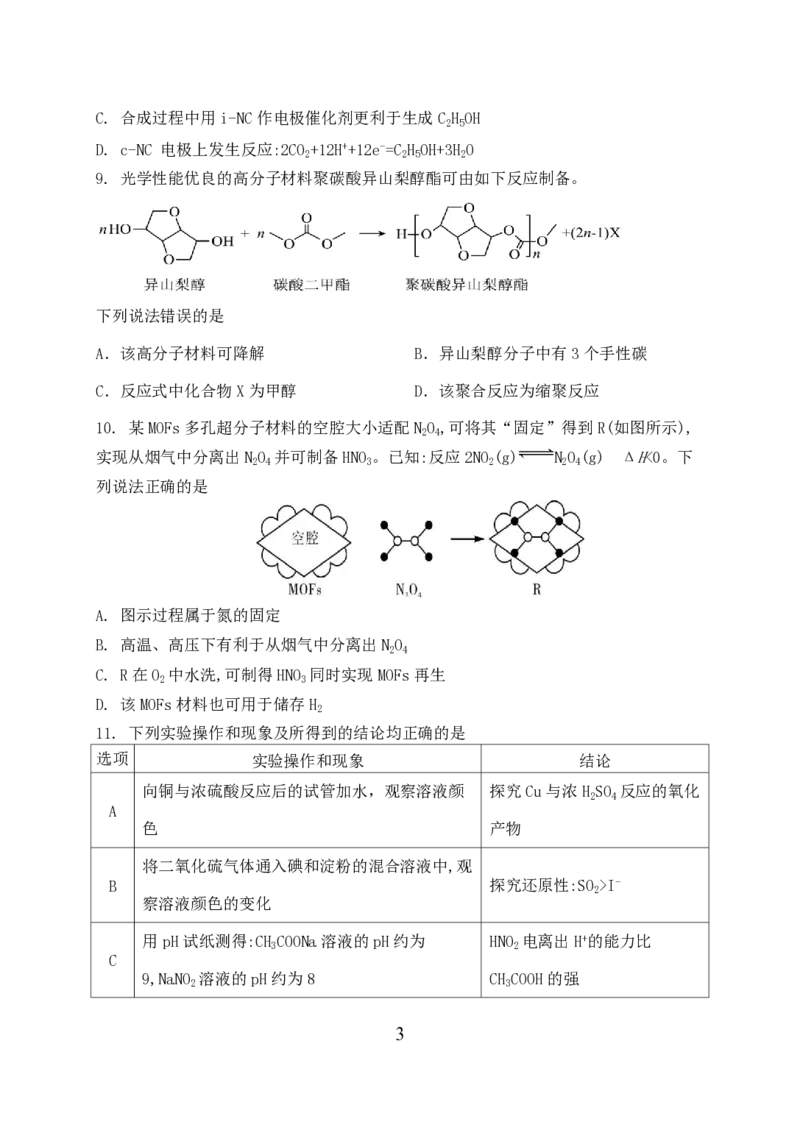
8. CO 通过电催化法可生成C H OH,c-NC、i-NC是可用于阴极电极的两种电催化剂,其
2 2 5
表面发生转化原理如图所示。下列说法正确的是
A. i-NC 电极发生氧化反应
B. 合成过程中CO 作为还原剂
2
2
学科网(北京)股份有限公司C. 合成过程中用i-NC作电极催化剂更利于生成C H OH
2 5
D. c-NC 电极上发生反应:2CO +12H++12e-=C H OH+3H O
2 2 5 2
9. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A.该高分子材料可降解 B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇 D.该聚合反应为缩聚反应
10. 某MOFs多孔超分子材料的空腔大小适配N O ,可将其“固定”得到R(如图所示),
2 4
实现从烟气中分离出N O 并可制备HNO 。已知:反应2NO (g) N O (g) ΔH<0。下
2 4 3 2 2 4
列说法正确的是
A. 图示过程属于氮的固定
B. 高温、高压下有利于从烟气中分离出N O
2 4
C. R在O 中水洗,可制得HNO 同时实现MOFs再生
2 3
D. 该MOFs材料也可用于储存H
2
11. 下列实验操作和现象及所得到的结论均正确的是
选项 实验操作和现象 结论
向铜与浓硫酸反应后的试管加水,观察溶液颜 探究Cu与浓H SO 反应的氧化
2 4
A
色 产物
将二氧化硫气体通入碘和淀粉的混合溶液中,观
B 探究还原性:SO >I-
2
察溶液颜色的变化
用pH试纸测得:CH COONa溶液的pH约为 HNO 电离出H+的能力比
3 2
C
9,NaNO 溶液的pH约为8 CH COOH的强
2 3
3
学科网(北京)股份有限公司向20%蔗糖溶液中加入少量稀硫酸,加热;再加
D 蔗糖未水解
入银氨溶液;未出现银镜
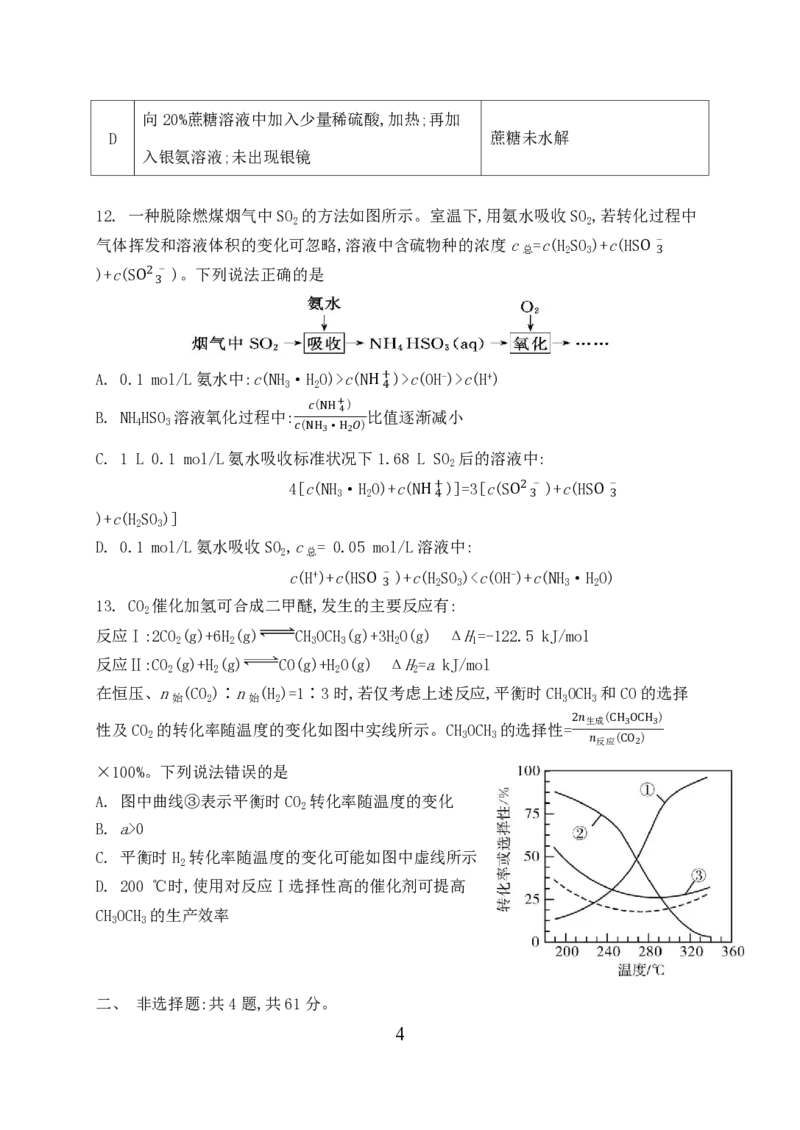
12. 一种脱除燃煤烟气中SO 的方法如图所示。室温下,用氨水吸收SO ,若转化过程中
2 2
气体挥发和溶液体积的变化可忽略,溶液中含硫物种的浓度c =c(H SO )+c(HSO -
总 2 3 3
)+c(SO2 - )。下列说法正确的是
3
A. 0.1 mol/L氨水中:c(NH ·H O)>c(NH+)>c(OH-)>c(H+)
3 2 4
𝑐(NH+)
4
B. NH HSO 溶液氧化过程中: 比值逐渐减小
4 3 𝑐(NH ·H 𝑂)
3 2
C. 1 L 0.1 mol/L氨水吸收标准状况下1.68 L SO 后的溶液中:
2
4[c(NH ·H O)+c(NH+)]=3[c(SO2 - )+c(HSO -
3 2 4 3 3
)+c(H SO )]
2 3
D. 0.1 mol/L氨水吸收SO ,c = 0.05 mol/L溶液中:
2 总
c(H+)+c(HSO - )+c(H SO )0
C. 平衡时H 转化率随温度的变化可能如图中虚线所示
2
D. 200 ℃时,使用对反应Ⅰ选择性高的催化剂可提高
CH OCH 的生产效率
3 3
二、 非选择题:共4题,共61分。
4
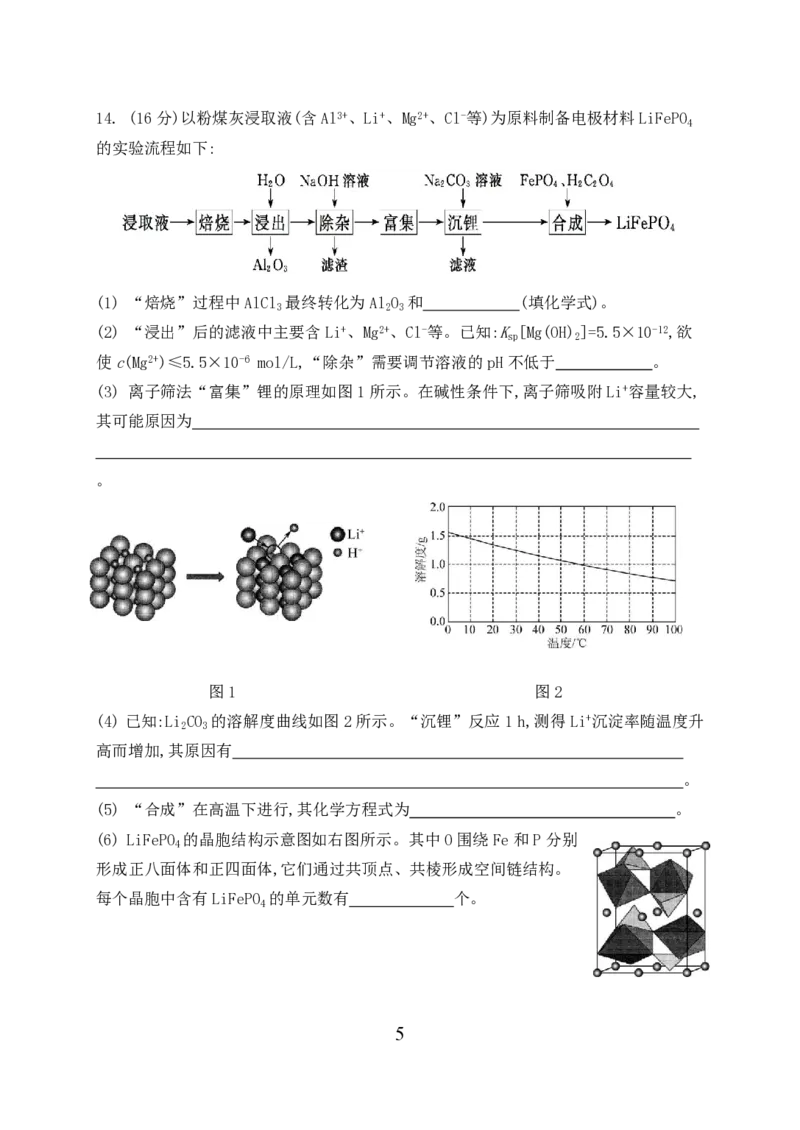
学科网(北京)股份有限公司14. (16分)以粉煤灰浸取液(含Al3+、Li+、Mg2+、Cl-等)为原料制备电极材料LiFePO
4
的实验流程如下:
(1) “焙烧”过程中AlCl 最终转化为Al O 和 (填化学式)。
3 2 3
(2) “浸出”后的滤液中主要含Li+、Mg2+、Cl-等。已知:K [Mg(OH) ]=5.5×10-12,欲
sp 2
使c(Mg2+)≤5.5×10-6 mol/L,“除杂”需要调节溶液的pH不低于 。
(3) 离子筛法“富集”锂的原理如图1所示。在碱性条件下,离子筛吸附Li+容量较大,
其可能原因为
。
图1 图2
(4) 已知:Li CO 的溶解度曲线如图2所示。“沉锂”反应1 h,测得Li+沉淀率随温度升
2 3
高而增加,其原因有
。
(5) “合成”在高温下进行,其化学方程式为 。
(6) LiFePO 的晶胞结构示意图如右图所示。其中O围绕Fe和P分别
4
形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。
每个晶胞中含有LiFePO 的单元数有 个。
4
5
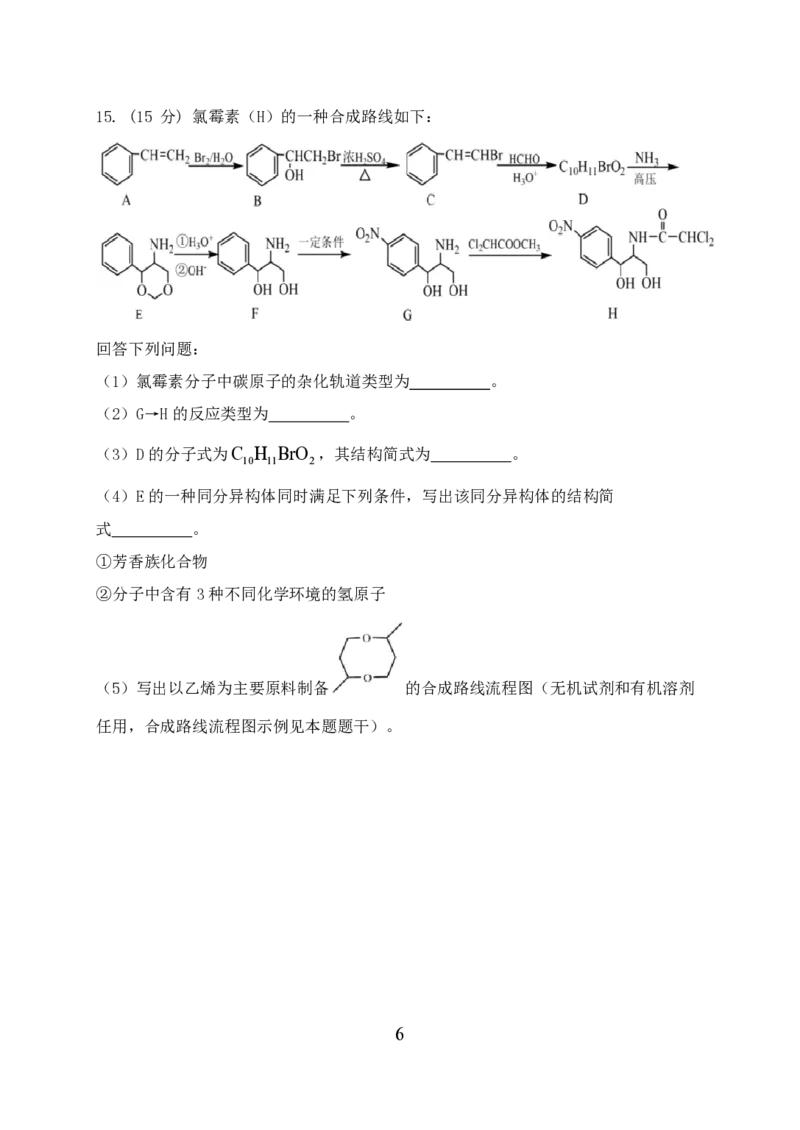
学科网(北京)股份有限公司15. (15 分) 氯霉素(H)的一种合成路线如下:
回答下列问题:
(1)氯霉素分子中碳原子的杂化轨道类型为 。
(2)G→H的反应类型为 。
(3)D的分子式为C H BrO ,其结构简式为 。
10 11 2
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简
式 。
①芳香族化合物
②分子中含有3种不同化学环境的氢原子
(5)写出以乙烯为主要原料制备 的合成路线流程图(无机试剂和有机溶剂
任用,合成路线流程图示例见本题题干)。
6
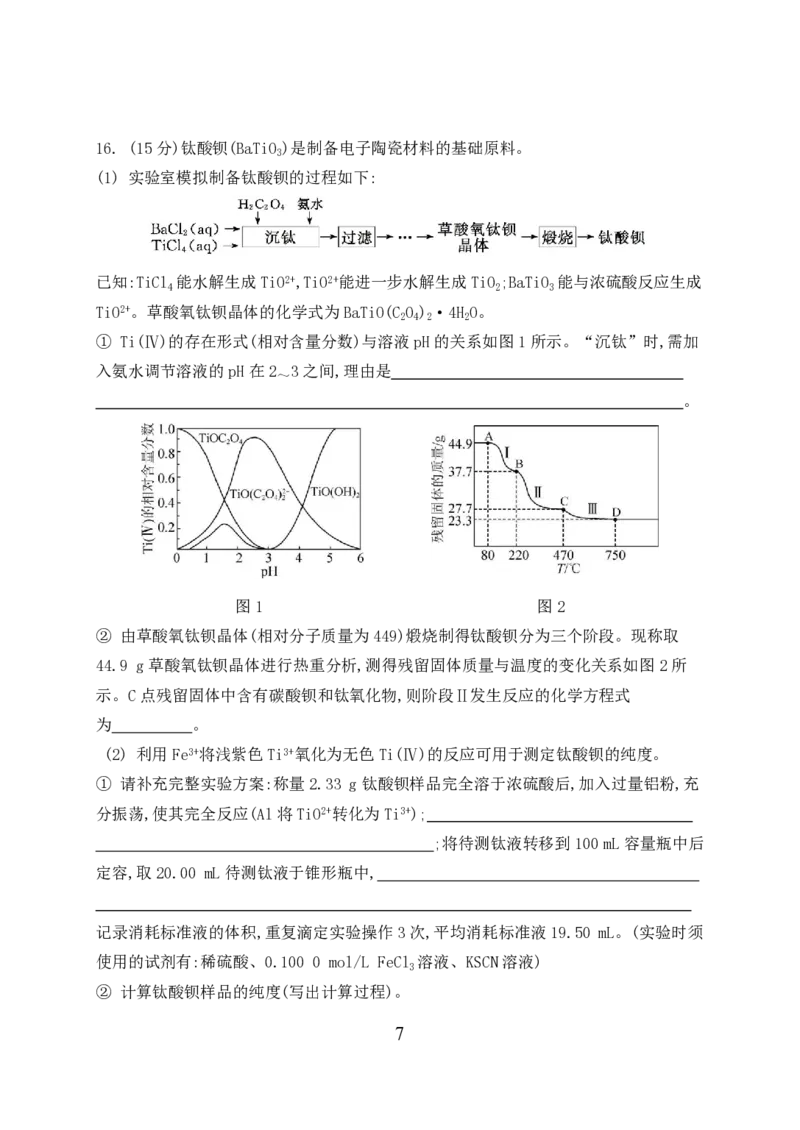
学科网(北京)股份有限公司16. (15分)钛酸钡(BaTiO )是制备电子陶瓷材料的基础原料。
3
(1) 实验室模拟制备钛酸钡的过程如下:
已知:TiCl 能水解生成TiO2+,TiO2+能进一步水解生成TiO ;BaTiO 能与浓硫酸反应生成
4 2 3
TiO2+。草酸氧钛钡晶体的化学式为BaTiO(C O ) ·4H O。
2 4 2 2
① Ti(Ⅳ)的存在形式(相对含量分数)与溶液pH的关系如图1所示。“沉钛”时,需加
入氨水调节溶液的pH在2 3之间,理由是
~
。
图1 图2
② 由草酸氧钛钡晶体(相对分子质量为449)煅烧制得钛酸钡分为三个阶段。现称取
44.9 g草酸氧钛钡晶体进行热重分析,测得残留固体质量与温度的变化关系如图2所
示。C点残留固体中含有碳酸钡和钛氧化物,则阶段Ⅱ发生反应的化学方程式
为 。
(2) 利用Fe3+将浅紫色Ti3+氧化为无色Ti(Ⅳ)的反应可用于测定钛酸钡的纯度。
① 请补充完整实验方案:称量2.33 g钛酸钡样品完全溶于浓硫酸后,加入过量铝粉,充
分振荡,使其完全反应(Al将TiO2+转化为Ti3+);
;将待测钛液转移到100 mL容量瓶中后
定容,取20.00 mL待测钛液于锥形瓶中,
记录消耗标准液的体积,重复滴定实验操作3次,平均消耗标准液19.50 mL。(实验时须
使用的试剂有:稀硫酸、0.100 0 mol/L FeCl 溶液、KSCN溶液)
3
② 计算钛酸钡样品的纯度(写出计算过程)。
7
学科网(北京)股份有限公司17. (15分)将CO 还原为HCOOH是实现“碳中和”的有效途径。
2
(1) 利用反应CO (g)+H (g) HCOOH(g) ΔH=+14.9 kJ/mol不能实现CO 直接加氢合
2 2 2
成HCOOH,原因是 。
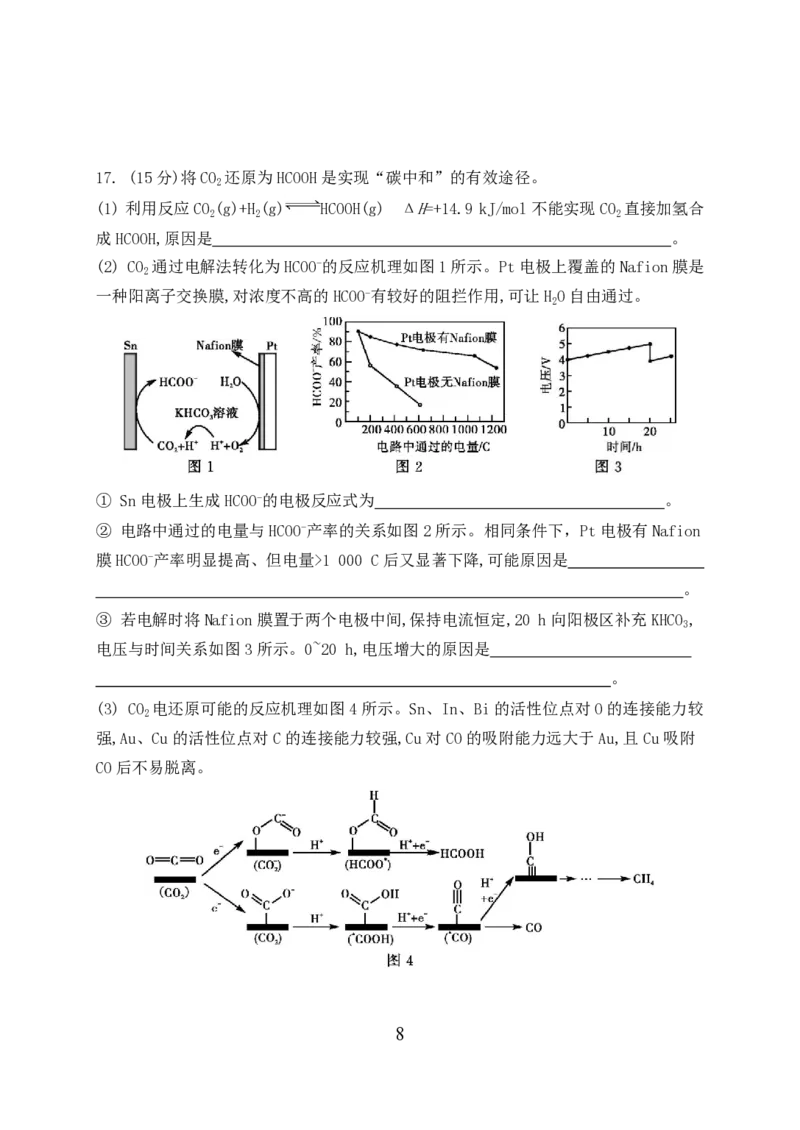
(2) CO 通过电解法转化为HCOO-的反应机理如图1所示。Pt电极上覆盖的Nafion膜是
2
一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可让H O自由通过。
2
① Sn电极上生成HCOO-的电极反应式为 。
② 电路中通过的电量与HCOO-产率的关系如图2所示。相同条件下,Pt电极有Nafion
膜HCOO-产率明显提高、但电量>1 000 C后又显著下降,可能原因是
。
③ 若电解时将Nafion膜置于两个电极中间,保持电流恒定,20 h向阳极区补充KHCO ,
3
电压与时间关系如图3所示。0~20 h,电压增大的原因是
。
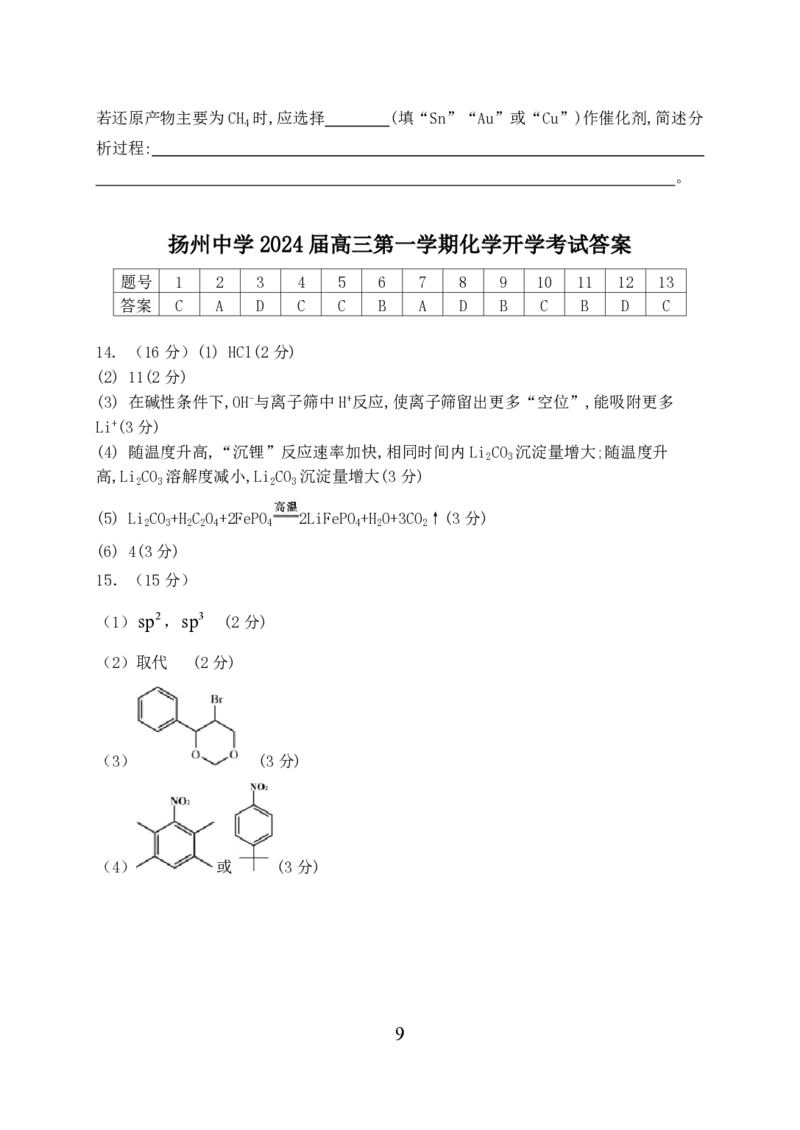
(3) CO 电还原可能的反应机理如图4所示。Sn、In、Bi的活性位点对O的连接能力较
2
强,Au、Cu的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附
CO后不易脱离。
8
学科网(北京)股份有限公司若还原产物主要为CH 时,应选择 (填“Sn”“Au”或“Cu”)作催化剂,简述分
4
析过程:
。
扬州中学 2024 届高三第一学期化学开学考试答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案 C A D C C B A D B C B D C
14. (16分)(1) HCl(2分)
(2) 11(2分)
(3) 在碱性条件下,OH-与离子筛中H+反应,使离子筛留出更多“空位”,能吸附更多
Li+(3分)
(4) 随温度升高,“沉锂”反应速率加快,相同时间内Li CO 沉淀量增大;随温度升
2 3
高,Li CO 溶解度减小,Li CO 沉淀量增大(3分)
2 3 2 3
(5) Li CO +H C O +2FePO 2LiFePO +H O+3CO ↑(3分)
2 3 2 2 4 4 4 2 2
(6) 4(3分)
15.(15分)
(1)sp2,sp3 (2分)
(2)取代 (2分)
(3) (3分)
(4) 或 (3分)
9
学科网(北京)股份有限公司(5) (5
分)
16. (15分)(1) ①pH在2 3之间时,Ti(Ⅳ)主要以TiO(C O )2 - 的形式存在,可直接
~ 2 4 2
与Ba2+反应,有利于草酸氧钛钡晶体的生成(3分)
②BaTiO(C O ) BaCO +TiO +2CO↑+CO ↑(3分)
2 4 2 3 2 2
(2) ①过滤,洗涤滤渣2 3次,将洗涤液与原滤液合并,向合并后的溶液中加入稀硫酸酸
~
化(3分)
向锥形瓶中滴加2 3滴KSCN溶液,用0.100 0 mol/L FeCl 溶液滴定,当滴入最后
~ 3
半滴标准液时,溶液由浅紫色变成红色,且半分钟内红色不褪去(3分)
②根据反应:Ti3++Fe3+ Ti(Ⅳ)+Fe2+可知,
20 mL待测钛液中,
n(Ti3+)=n(Fe3+)=0.019 5 L×0.100 0 mol/L=0.001 95 mol
0.001 95mol×5×233 g/mol
钛酸钡样品的纯度= ×100%=97.5%(3分)
2.33 g
17. (15分)(1) 该反应的ΔH>0、ΔS<0,不能自发进行(2分)
(2) ① H++CO +2e- HCOO-或HCO - +CO +2e- HCOO-+CO2 - (2分)
2 3 2 3
② Nafion膜可以阻止HCOO-在阳极放电;电量>1 000 C后,c(HCOO-)增大,Nafion膜阻拦
作用下降(3分)
③ 阳极区pH减小,HCO - 浓度下降,K+部分迁移至阴极区,阳极区离子浓度下降,导电能
3
力减弱(3分)
(3) Cu(2分) 回溯CH 生成机理,第1步是C与催化剂活性位点相连,排除Sn;Au
4
对CO的吸附能力较小,易脱离;Cu对CO的吸附能力强,不易从催化剂表面脱离(3分)
10
学科网(北京)股份有限公司