文档内容
2024 届高三第一次质量监测
化 学
(考试时间:75 分钟 满分:100 分)
可能用到的相对原子质量:H 1 C 12 O 16 F 19 Na 23 Cu 64 Zn 65
选 择 题(共 39 分)
单项选择题:本题包括 13 小题,每小题 3 分,共计 39 分。每小题只有一个选项符合题意。
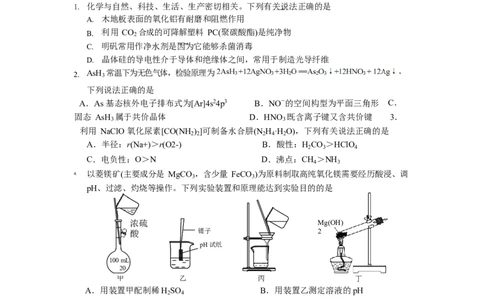
1. 化学与自然、科技、生活、生产密切相关。下列有关说法正确的是
A. 木地板表面的氧化铝有耐磨和阻燃作用
B. 利用 CO 2 合成的可降解塑料 PC(聚碳酸酯)是纯净物
C. 明矾常用作净水剂是因为它能够杀菌消毒
D. 晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
2. AsH 3 常温下为无色气体,检验原理为
下列说法正确的是
A.As 基态核外电子排布式为[Ar]4s24p3 B.NO-的空间构型为平面三角形 C.
3
固态 AsH 属于共价晶体 D.HNO 既含离子键又含共价键 3.
3 3
利用 NaClO 氧化尿素[CO(NH ) ]可制备水合肼(N H ·H O),下列有关说法正确的是
2 2 2 4 2
A.半径:r(Na+)>r(O2-) B.酸性:H CO >HClO
2 3 4
C.电负性:O>N D.沸点:CH >NH
4 3
4. 以菱镁矿(主要成分是 MgCO 3 ,含少量 FeCO 3 )为原料制取高纯氧化镁需要经历酸浸、调
pH、过滤、灼烧等操作。下列实验装置和原理能达到实验目的的是
浓硫 Mg(OH)
酸 镊子 2
pH试纸
100 mL
20
甲 乙 丙 丁
A.用装置甲配制稀H SO B.用装置乙测定溶液的pH
2 4
C.用装置丙过滤悬浊液 D.用装置丁灼烧Mg(OH) 固体
2
5. 下列物质性质与用途具有对应关系的是 A.
银氨溶液具有弱氧化性,可用于制银镜
B. MgO 在水中的溶解度小,可用作耐火材料
C.NH 具有还原性,可用作制冷剂 D.
3
NH HCO 受热易分解,可用作氮肥
4 3
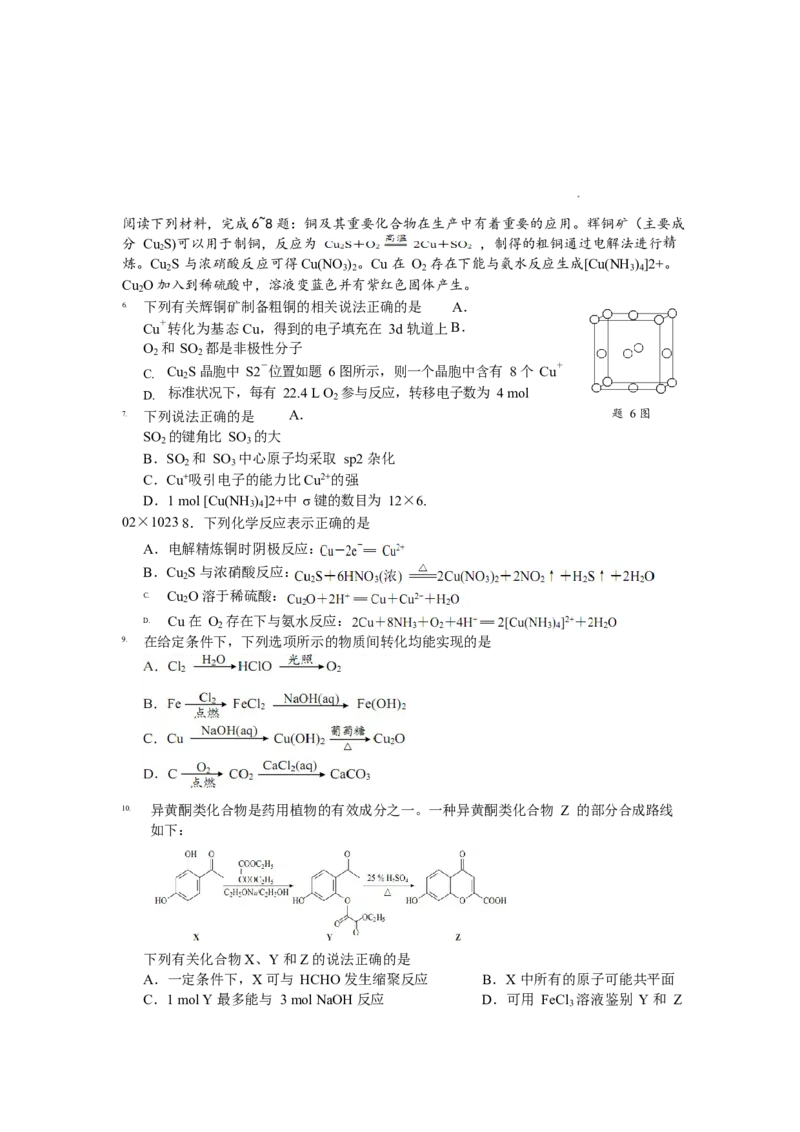
学科网(北京)股份有限公司阅读下列材料,完成6~8题:铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成
分 Cu S)可以用于制铜,反应为 ,制得的粗铜通过电解法进行精
2
炼。Cu S 与浓硝酸反应可得Cu(NO ) 。Cu 在 O 存在下能与氨水反应生成[Cu(NH ) ]2+。
2 3 2 2 3 4
Cu O 加入到稀硫酸中,溶液变蓝色并有紫红色固体产生。
2
6. 下列有关辉铜矿制备粗铜的相关说法正确的是 A.
Cu+转化为基态Cu,得到的电子填充在 3d 轨道上B.
O 和 SO 都是非极性分子
2 2
C. Cu 2 S 晶胞中 S2-位置如题 6 图所示,则一个晶胞中含有 8 个 Cu+
D. 标准状况下,每有 22.4 L O 2 参与反应,转移电子数为 4 mol
7. 下列说法正确的是 A. 题 6 图
SO 的键角比 SO 的大
2 3
B.SO 和 SO 中心原子均采取 sp2 杂化
2 3
C.Cu+吸引电子的能力比Cu2+的强
D.1 mol [Cu(NH ) ]2+中 σ 键的数目为 12×6.
3 4
02×1023 8.下列化学反应表示正确的是
A.电解精炼铜时阴极反应:
B.Cu S 与浓硝酸反应:
2
C. Cu 2 O 溶于稀硫酸:
D. Cu 在 O 2 存在下与氨水反应:
9. 在给定条件下,下列选项所示的物质间转化均能实现的是
10. 异黄酮类化合物是药用植物的有效成分之一。一种异黄酮类化合物 Z 的部分合成路线
如下:
下列有关化合物X、Y 和Z 的说法正确的是
A.一定条件下,X 可与 HCHO 发生缩聚反应 B.X 中所有的原子可能共平面
C.1 mol Y 最多能与 3 mol NaOH 反应 D.可用 FeCl 溶液鉴别 Y 和 Z
3
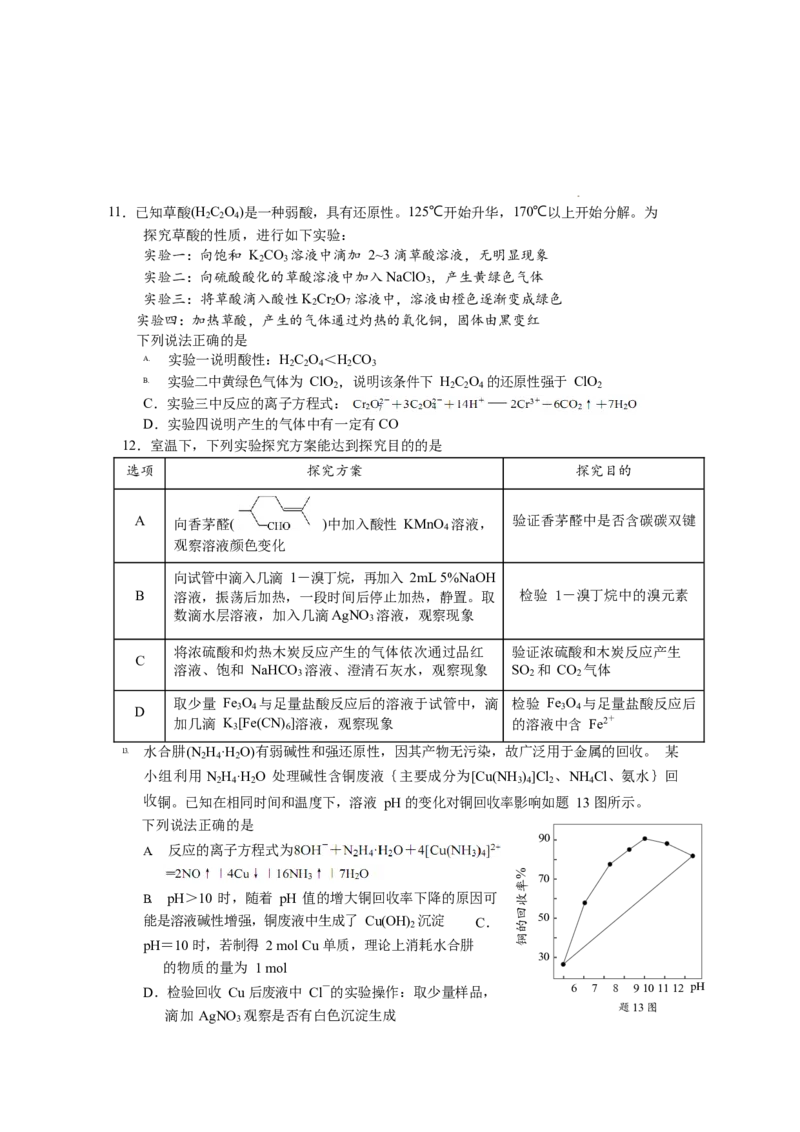
学科网(北京)股份有限公司11.已知草酸(H C O )是一种弱酸,具有还原性。125℃开始升华,170℃以上开始分解。为
2 2 4
探究草酸的性质,进行如下实验:
实验一:向饱和 K CO 溶液中滴加 2~3 滴草酸溶液,无明显现象
2 3
实验二:向硫酸酸化的草酸溶液中加入NaClO ,产生黄绿色气体
3
实验三:将草酸滴入酸性K Cr O 溶液中,溶液由橙色逐渐变成绿色
2 2 7
实验四:加热草酸,产生的气体通过灼热的氧化铜,固体由黑变红
下列说法正确的是
A. 实验一说明酸性:H 2 C 2 O 4 <H 2 CO 3
B. 实验二中黄绿色气体为 ClO 2 ,说明该条件下 H 2 C 2 O 4 的还原性强于 ClO 2
C.实验三中反应的离子方程式:
D.实验四说明产生的气体中有一定有CO
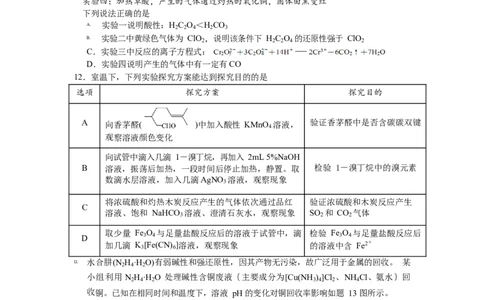
12.室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
A 向香茅醛( )中加入酸性 KMnO 溶液, 验证香茅醛中是否含碳碳双键
4
观察溶液颜色变化
向试管中滴入几滴 1-溴丁烷,再加入 2mL 5%NaOH
B 溶液,振荡后加热,一段时间后停止加热,静置。取 检验 1-溴丁烷中的溴元素
数滴水层溶液,加入几滴AgNO 溶液,观察现象
3
将浓硫酸和灼热木炭反应产生的气体依次通过品红 验证浓硫酸和木炭反应产生
C
溶液、饱和 NaHCO 溶液、澄清石灰水,观察现象 SO 和 CO 气体
3 2 2
取少量 Fe O 与足量盐酸反应后的溶液于试管中,滴 检验 Fe O 与足量盐酸反应后
D 3 4 3 4
加几滴 K [Fe(CN) ]溶液,观察现象 的溶液中含 Fe2+
3 6
13. 水合肼(N 2 H 4 ·H 2 O)有弱碱性和强还原性,因其产物无污染,故广泛用于金属的回收。 某
小组利用N H ·H O 处理碱性含铜废液{主要成分为[Cu(NH ) ]Cl 、NH Cl、氨水}回
2 4 2 3 4 2 4
收铜。已知在相同时间和温度下,溶液 pH 的变化对铜回收率影响如题 13 图所示。
下列说法正确的是
90
A. 反应的离子方程式为
70
B. pH>10 时,随着 pH 值的增大铜回收率下降的原因可
能是溶液碱性增强,铜废液中生成了 Cu(OH)
2
沉淀 C. 50
pH=10 时,若制得 2 mol Cu 单质,理论上消耗水合肼
30
的物质的量为 1 mol
D.检验回收 Cu 后废液中 Cl—的实验操作:取少量样品, 6 7 8 9 10 11 12 pH
题13图
滴加 AgNO 观察是否有白色沉淀生成
3
学科网(北京)股份有限公司
%率收回的铜非 选 择 题(共 61 分)
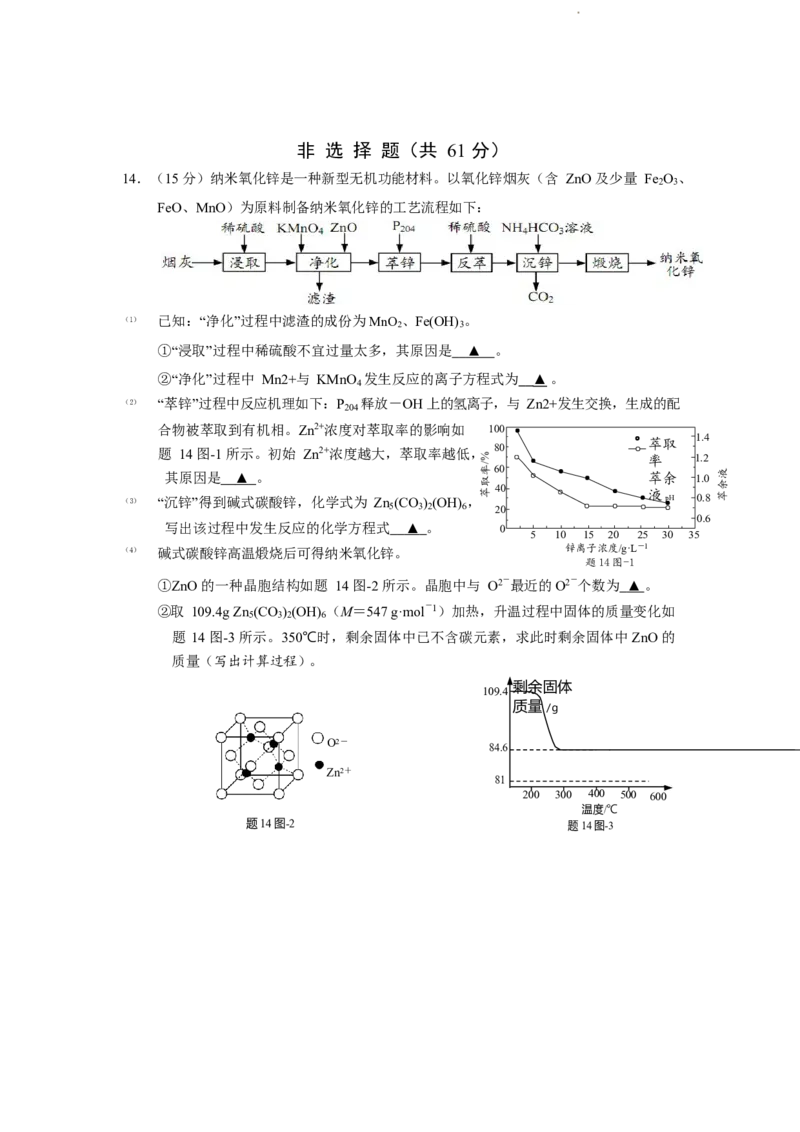
14.(15 分)纳米氧化锌是一种新型无机功能材料。以氧化锌烟灰(含 ZnO 及少量 Fe O 、
2 3
FeO、MnO)为原料制备纳米氧化锌的工艺流程如下:
(1) 已知:“净化”过程中滤渣的成份为MnO 、Fe(OH) 。
2 3
①“浸取”过程中稀硫酸不宜过量太多,其原因是 ▲ 。
②“净化”过程中 Mn2+与 KMnO 发生反应的离子方程式为 ▲。
4
(2) “萃锌”过程中反应机理如下:P 释放-OH 上的氢离子,与 Zn2+发生交换,生成的配
204
合物被萃取到有机相。Zn2+浓度对萃取率的影响如 100
1.4
题 14 图-1 所示。初始 Zn2+浓度越大,萃取率越低, 80 1.2
60 其原因是 ▲ 。 1.0
40
(3) “沉锌”得到碱式碳酸锌,化学式为 Zn (CO ) (OH) , 0.8
5 3 2 6 20
0.6
写出该过程中发生反应的化学方程式 ▲ 。 0
5 10 15 20 25 30 35
(4) 碱式碳酸锌高温煅烧后可得纳米氧化锌。
锌离子浓度/g·L-1
题14图-1
①ZnO 的一种晶胞结构如题 14 图-2 所示。晶胞中与 O2-最近的O2-个数为 ▲ 。
②取 109.4g Zn (CO ) (OH) (M=547 g·mol-1)加热,升温过程中固体的质量变化如
5 3 2 6
题 14 图-3 所示。350℃时,剩余固体中已不含碳元素,求此时剩余固体中ZnO 的
质量(写出计算过程)。
109.4
O2-
84.6
Zn2+
81
200 300 400 500 600
温度/℃
题14图-2 题14图-3
学科网(北京)股份有限公司
%/率取萃
液余萃
Hp
萃取
率
萃余
液
pH
剩余固体
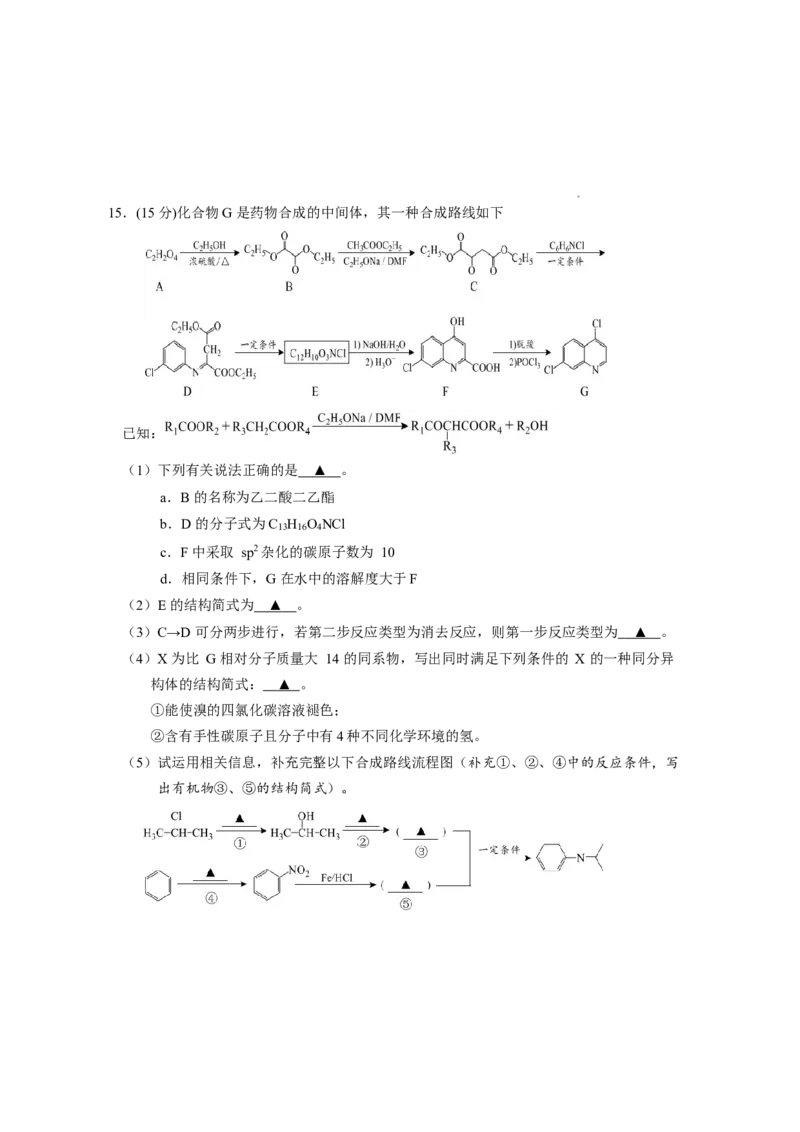
质量/g15.(15 分)化合物G 是药物合成的中间体,其一种合成路线如下
已知:
(1)下列有关说法正确的是 ▲ 。
a.B 的名称为乙二酸二乙酯
b.D 的分子式为C H O NCl
13 16 4
c.F 中采取 sp2 杂化的碳原子数为 10
d.相同条件下,G 在水中的溶解度大于F
(2)E 的结构简式为 ▲ 。
(3)C→D 可分两步进行,若第二步反应类型为消去反应,则第一步反应类型为 ▲ 。
(4)X 为比 G 相对分子质量大 14 的同系物,写出同时满足下列条件的 X 的一种同分异
构体的结构简式: ▲ 。
①能使溴的四氯化碳溶液褪色;
②含有手性碳原子且分子中有4种不同化学环境的氢。
(5)试运用相关信息,补充完整以下合成路线流程图(补充①、②、④中的反应条件,写
出有机物③、⑤的结构简式)。
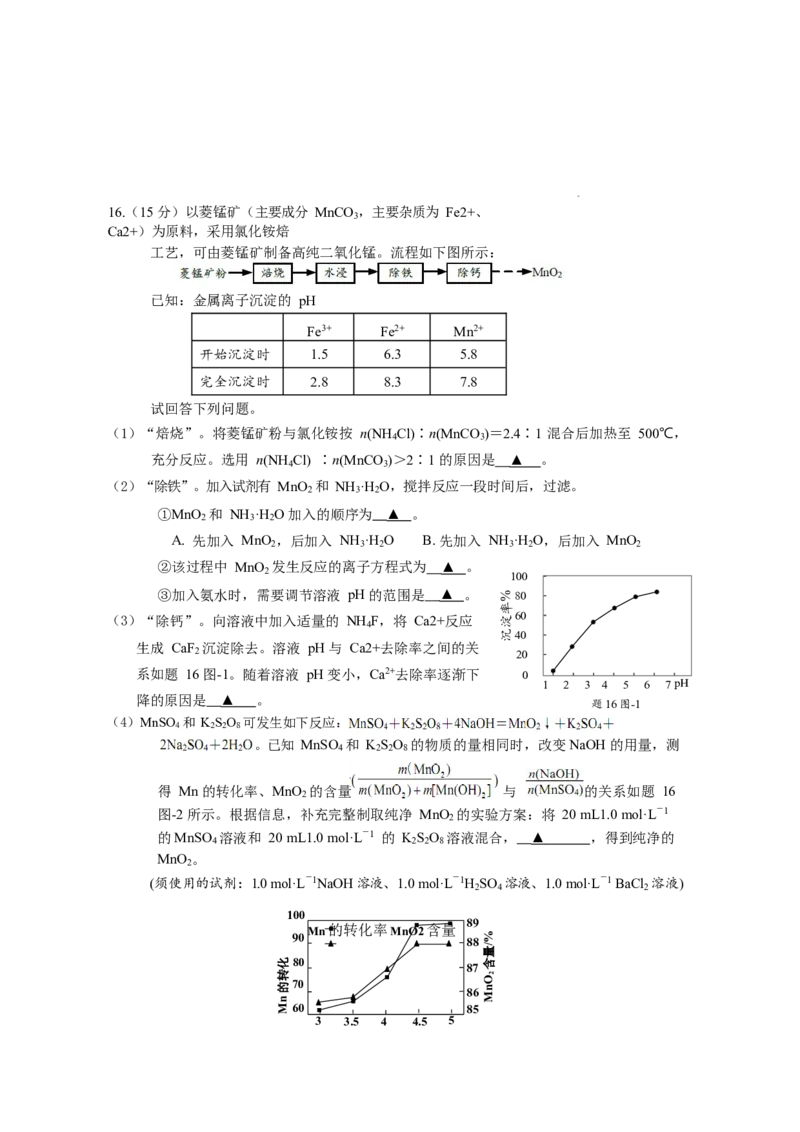
学科网(北京)股份有限公司16.(15 分)以菱锰矿(主要成分 MnCO ,主要杂质为 Fe2+、
3
Ca2+)为原料,采用氯化铵焙
工艺,可由菱锰矿制备高纯二氧化锰。流程如下图所示:
已知:金属离子沉淀的 pH
Fe3+ Fe2+ Mn2+
开始沉淀时 1.5 6.3 5.8
完全沉淀时 2.8 8.3 7.8
试回答下列问题。
(1)“焙烧”。将菱锰矿粉与氯化铵按 n(NH Cl)∶n(MnCO )=2.4∶1 混合后加热至 500℃,
4 3
充分反应。选用 n(NH Cl) ∶n(MnCO )>2∶1 的原因是 ▲ 。
4 3
(2)“除铁”。加入试剂有 MnO 和 NH ·H O,搅拌反应一段时间后,过滤。
2 3 2
①MnO 和 NH ·H O 加入的顺序为 ▲ 。
2 3 2
A. 先加入 MnO ,后加入 NH ·H O B. 先加入 NH ·H O,后加入 MnO
2 3 2 3 2 2
②该过程中 MnO 发生反应的离子方程式为 ▲ 。
2
100
③加入氨水时,需要调节溶液 pH 的范围是 ▲ 。 80
(3)“除钙”。向溶液中加入适量的 NH F,将 Ca2+反应 60
4
40
生成 CaF 沉淀除去。溶液 pH 与 Ca2+去除率之间的关
2 20
系如题 16 图-1。随着溶液 pH 变小,Ca2+去除率逐渐下 0
1 2 3 4 5 6 7 pH
降的原因是 ▲ 。
题16图-1
(4)MnSO 和 K S O 可发生如下反应:
4 2 2 8
。已知 MnSO 和 K S O 的物质的量相同时,改变NaOH 的用量,测
4 2 2 8
得 Mn 的转化率、MnO 的含量 与 的关系如题 16
2
图-2 所示。根据信息,补充完整制取纯净 MnO 的实验方案:将 20 mL1.0 mol·L-1
2
的MnSO 溶液和 20 mL1.0 mol·L-1 的 K S O 溶液混合, ▲ ,得到纯净的
4 2 2 8
MnO 。
2
(须使用的试剂:1.0 mol·L-1NaOH 溶液、1.0 mol·L-1H SO 溶液、1.0 mol·L-1 BaCl 溶液)
2 4 2
100
89
90
88
80
87
70
86
60 85
3 3.5 4 4.5 5
学科网(北京)股份有限公司
化转的nM
%/率
%/量含
OnM 2
%率淀沉
Mn的转化率MnO2含量n(NaOH)/n(MnSO)
4
题 16 图-2
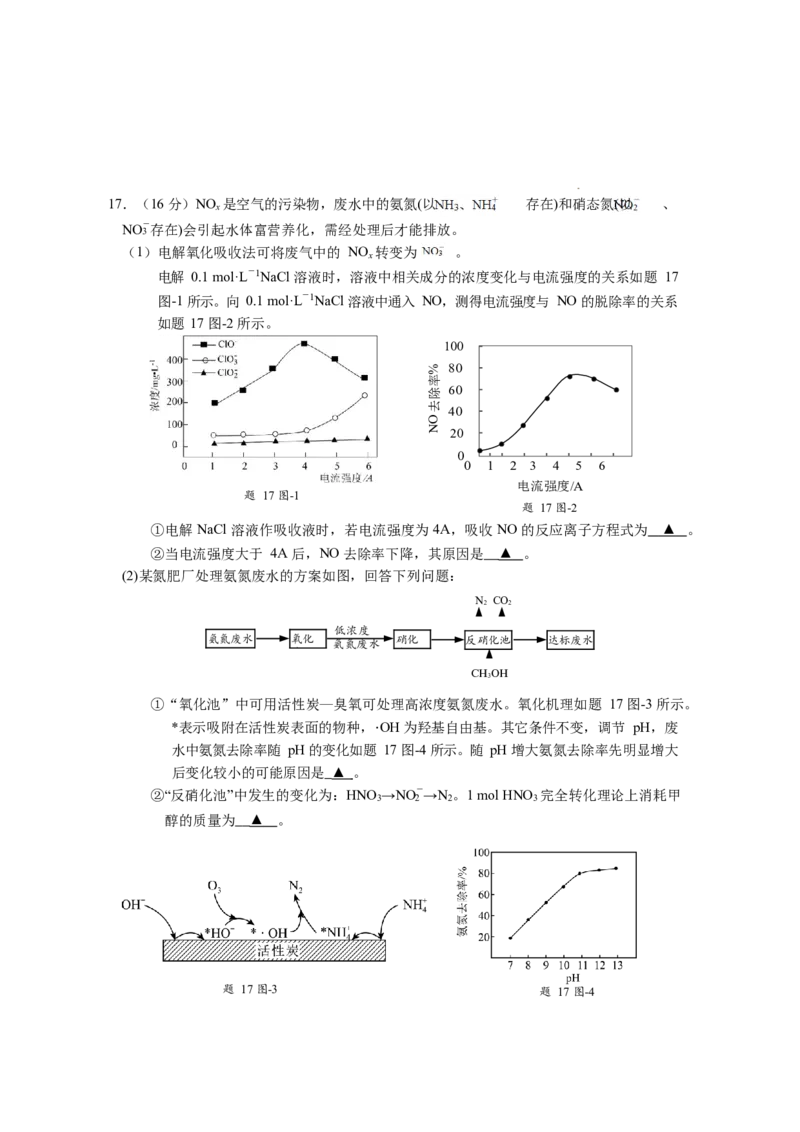
学科网(北京)股份有限公司17.(16 分)NO
x
是空气的污染物,废水中的氨氮(以 存在)和硝态氮(以 、
NO-存在)会引起水体富营养化,需经处理后才能排放。
3
(1)电解氧化吸收法可将废气中的 NO 转变为 。
x
电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如题 17
图-1 所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系
如题 17 图-2 所示。
100
80
60
40
20
0
0 1 2 3 4 5 6
电流强度/A
题 17 图-1
题 17 图-2
①电解 NaCl 溶液作吸收液时,若电流强度为 4A,吸收 NO 的反应离子方程式为 ▲ 。
②当电流强度大于 4A 后,NO 去除率下降,其原因是 ▲ 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
N CO
2 2
低浓度
氨氮废水 氧化 氨氮废水 硝化 反硝化池 达标废水
池 池
CHOH
3
①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如题 17 图-3 所示。
*表示吸附在活性炭表面的物种,·OH 为羟基自由基。其它条件不变,调节 pH,废
水中氨氮去除率随 pH 的变化如题 17 图-4 所示。随 pH 增大氨氮去除率先明显增大
后变化较小的可能原因是 ▲ 。
②“反硝化池”中发生的变化为:HNO →NO-→N 。1 mol HNO 完全转化理论上消耗甲
3 2 2 3
醇的质量为 ▲ 。
题 17 图-3 题 17 图-4
学科网(北京)股份有限公司
%率除去ON(3)纳米Fe 可还原去除水中的硝酸盐污染物。
已知:i.纳米 Fe 具有很高的活性,易被氧化使表面形成氧化层
ii.纳米 Fe 将 还原为 的转化关系如下:
①纳米 Fe 的制备原理:FeSO +2NaBH +6H O=2B(OH) +Fe+7H ↑+
4 4 2 3 2
Na SO 已知电负性 H>B,则该反应中氧化剂是 ▲(填化学式) 。
2 4
②检验还原后的溶液中存在 NH+的实验方法是 ▲ 。
4
③溶液初始 pH 较低有利于 NO-的去除,其可能的原因是 ▲ 。
3
学科网(北京)股份有限公司