文档内容
江苏省泰州中学 2023~2024 学年秋学期高三年级期初调研考试
化学学科试卷
可能用到的相对原子质量:H-1 Li-12 C-12 N-14 O-16 F-19 P-31
S-16 V-51 Fe-56 Co-59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.有利于实现“碳达峰、碳中和”的是( )
A.风能发电 B.粮食酿酒 C.燃煤脱硫 D.石油裂化
2.下列化学用语或图示表达正确的是( )
A. 分子的球棍模型:
B. 的VSEPR模型:
C.基态 原子价层电子轨道表示式:
D. 电子云轮廓图:
3.X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有X、Y元素相
邻。X基态原子核外有2个未成对电子, 原子在同周期中原子半径最大。下列说法不正确的是( )
A.第一电离能:
B.X单质中只有共价键
C.Z、W原子形成稀有气体电子构型的简单离子的半径:
D. 与水反应生成产物之一是非极性分子
4.完成下述实验,装置或试剂不正确的是( )
A.图①装置可除去 中混有的少量
学科网(北京)股份有限公司B.图②装置可用于制取并收集氨气
C.图③操作可排出盛有 溶液滴定管尖嘴内的气泡
D.图④装置可用于测量 体积
阅读下列资料,完成5~7题:含氯化合物在生产生活中应用广泛。舍勒发现将软锳矿和浓盐酸混合加热可产
生氯气,该方法仍是当今实验室制备氮气的主要方法之一。工业上以 为原料可制得 、 、
、 和 等。在催化剂 作用下,通过氧气直接篻化氯化氢制备氮气。该反应为可逆反应,
热化学方程式为 。
5.下列有关说法正确的是( )
A. 与 的晶体类型相同
B. 和 中的 夹角都为
C. 中 基态时末成对电子数为5
D. 与 都是由极性键构成的极性分子
6.下列化学反应表示正确的是( )
A.实验室制氯气:
B.电解饱和 溶液的阴极反应:
C.
D.氯气溶于水具有漂白性:
7.下列有关物质的性质与用途具有对应关系的是( )
A. 能溶于水,可用于工业制盐酸 B. 有强篻化性,可用于水体消毒
C. 溶液显酸性,可用作漂白剂 D. 受热易分解,可用作氮肥
8.硫及其化合物的转化具有重要应用。下列说法不正确的是( )
A.废水中的 可以被 还原后除去
B.大气中的 遇雨水最终形成 进入地面或海洋
学科网(北京)股份有限公司C.工业排放尾气中的 可与 和 反应生成
D.水垢中的 可与饱和 溶液反应生成
9.化合物 是合成用于降低体重、缩小腰围药物利莫那班的重要中间体。
下列有关 、 、 的说法不正确的是( )
A. 、 都是取代反应
B. 分子中所有碳原子可能在同一平面上
C. 在浓硫酸催化下加热可发生消去反应
D. 与足量 溶液反应最多消耗
10.一定温度下,在容积恒为 的容器中通入一定量 ,发生反应 ,
体系中各组分浓度随时间 的变化如下表。下列说法不正确的是( )
0 20 40 60 80
0.10 0.06 0.04 0.04 0.04
0 2 8 0 0
0.07 0.10 0.12 0.12
0
6 4 0 0
A. , 的平均反应速率为
B.升高温度,反应 化学平衡常数值增大
C. 时,再充入 、 各 ,平衡不移动
D.若压缩容器使压强增大,达新平衡后混合气颜色比原平衡时深
11.下列方案设计、现象和结论都正确的是( )
实验目的 方案设计 现象和结论
探究 生成
A 烧瓶内气体颜色变浅, 生成 的
将充有 的密闭烧瓶放入热水中
反应的吸 反应为吸热反应
放热
学科网(北京)股份有限公司比较
相同条件下,分别用pH试纸测定
NaF溶液的 溶液的pH,
B 和 溶液、
HF的酸性强弱
溶液的pH
证明 的酸性比HF的酸性强
比较氢氧化铜和
向浓度均为 的 、 先出现蓝色沉淀,
C
氢氧化镁 的 混合溶液中逐滴加入NaOH
大小
溶液
镀锌铁皮锌镀层 装有镀锌铁皮的烧杯中加入足量稀 产生气泡的速率突然减小,证明镀锌层完全
D
厚度的测定 硫酸 反应
12. 为二元弱碱。室温下,配制一组 的
与 的混合溶液,溶液中相关组分的物质的量分数随溶液 变化的曲线如下图所示,下列说法
正确的是( )
A.由图可知 的
B. 的溶液中:
C.等物质的量的 和 混合溶液中
D.在 的水溶液中,
13.用草酸二甲酯 和氢气为原料制备乙二醇的反应原理如下:
乙醇酸甲酯
在 条件下,将氢气和草酸二甲酯体积比(氢酯比)为 的混合气体以一定流速通过装有催化剂的
反应管,草酸二甲酯的转化率、产物的选择性与温度的关系如下图所示。产物的选择性
学科网(北京)股份有限公司。下列说法不正确的是( )
A.曲线I表示草酸二甲酯的转化率随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在 温度范围,随着温度升高,出口处乙醇酸甲酯的量不断增大
D.其他条件不变,在 温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比
逐渐减小且大于2
二、非选择题:共4题,共61分
14.(15分)锌冶炼过程中产生的锌渣主要成分为铁酸锌 和二氧化硅,以及少量的铜、铁、锌的
氧化物和硫化物。利用酸溶的方法可溶出金属离子,使锌渣得到充分利用。
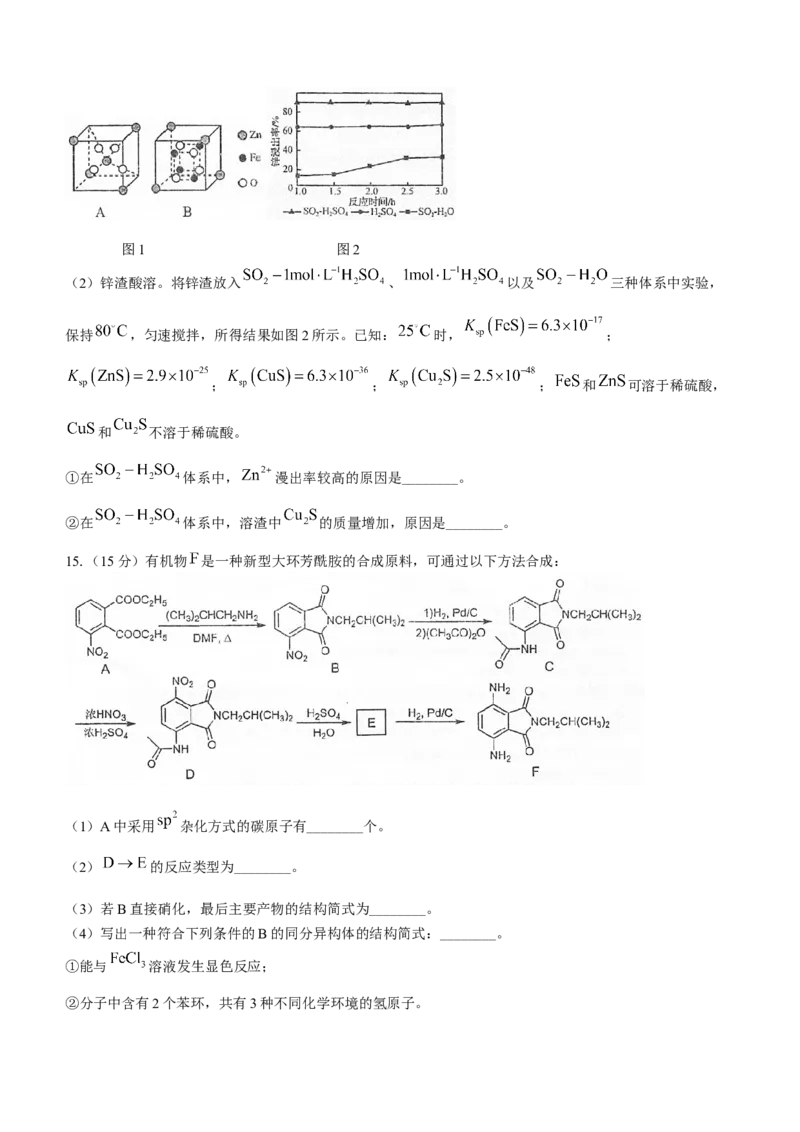
(1)铁酸锌酸溶。铁酸锌难溶于水,其晶胞由A、B结构按照 交替累积而成,如图1所示。将铁酸锌粉
末投入到 中,保温 ,匀速搅拌。浸出液中 和 的浓度随时间的变化如下表
所示。
0.5 1.0 1.5 2.0 2.5
0.1 0.1 0.1 0.2 0.2
0 1 5 1 1
0.1 0.1 0.1 0.2 0.3
2 3 6 1 0
①B结构的化学式为________。
②铁酸锌和硫酸反应的离子方程式为________。
③酸溶时,溶出效率较高的金属离子是________。
学科网(北京)股份有限公司图1 图2
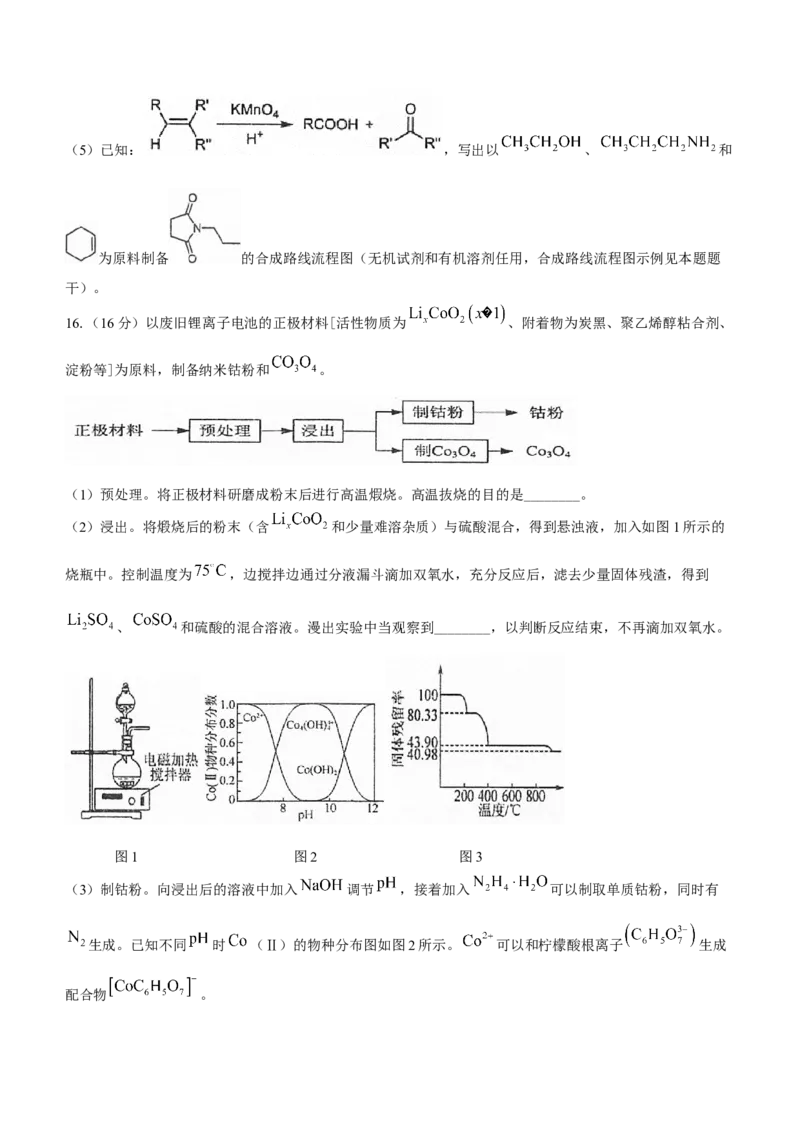
(2)锌渣酸溶。将锌渣放入 、 以及 三种体系中实验,
保持 ,匀速搅拌,所得结果如图2所示。已知: 时, ;
; ; ; 和 可溶于稀硫酸,
和 不溶于稀硫酸。
①在 体系中, 漫出率较高的原因是________。
②在 体系中,溶渣中 的质量增加,原因是________。
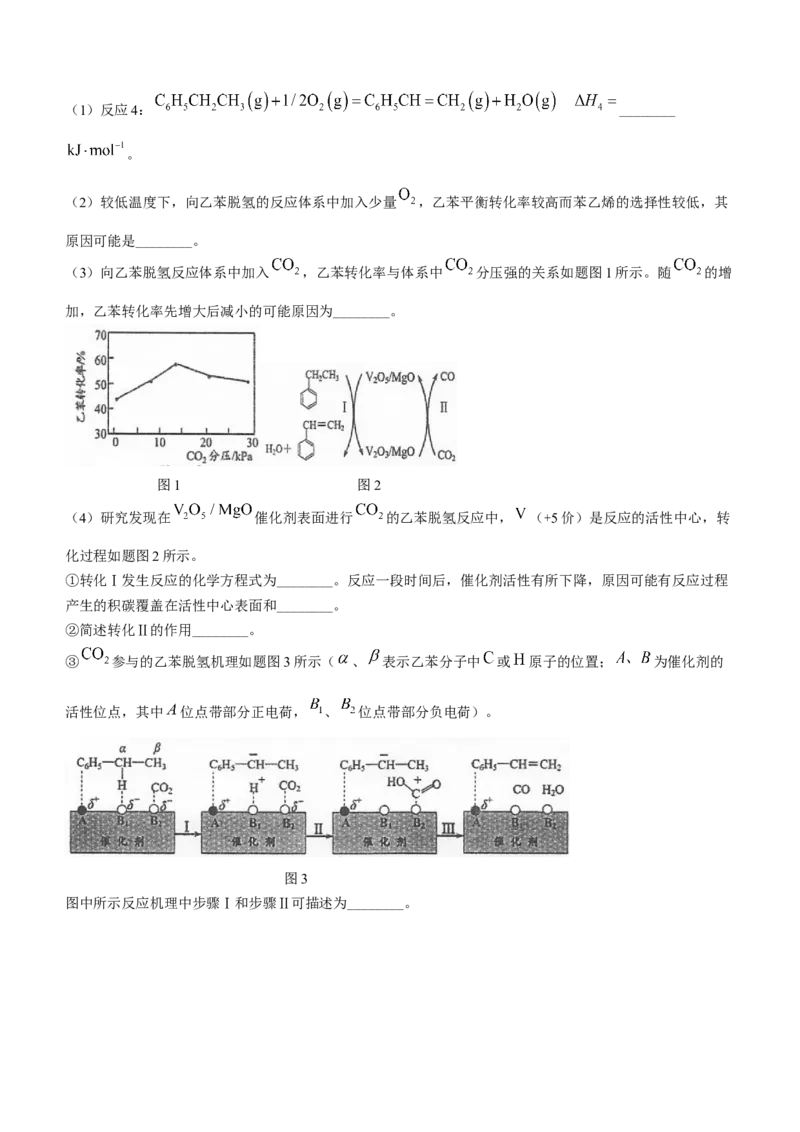
15.(15分)有机物 是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
(1)A中采用 杂化方式的碳原子有________个。
(2) 的反应类型为________。
(3)若B直接硝化,最后主要产物的结构简式为________。
(4)写出一种符合下列条件的B的同分异构体的结构简式:________。
①能与 溶液发生显色反应;
②分子中含有2个苯环,共有3种不同化学环境的氢原子。
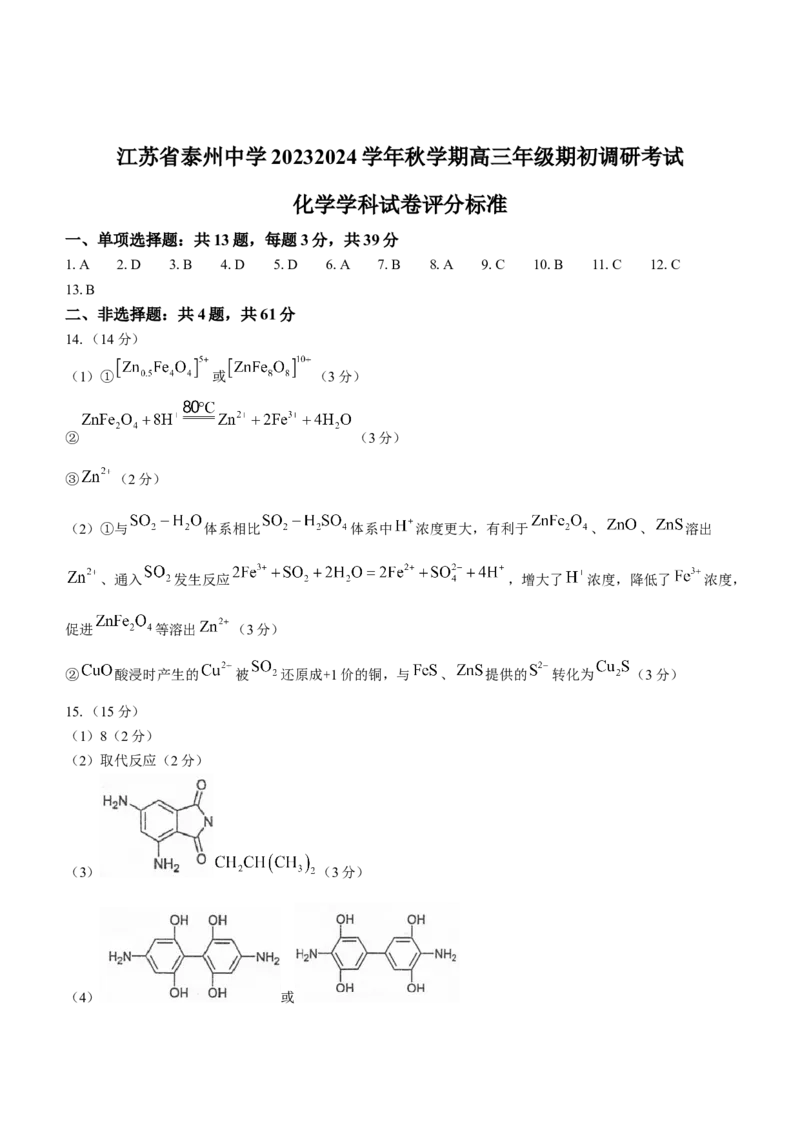
学科网(北京)股份有限公司(5)已知: ,写出以 、 和
为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题
干)。
16.(16分)以废旧锂离子电池的正极材料[活性物质为 、附着物为炭黑、聚乙烯醇粘合剂、
淀粉等]为原料,制备纳米钴粉和 。
(1)预处理。将正极材料研磨成粉末后进行高温煆烧。高温抜烧的目的是________。
(2)浸出。将煅烧后的粉末(含 和少量难溶杂质)与硫酸混合,得到悬浊液,加入如图1所示的
烧瓶中。控制温度为 ,边搅拌边通过分液漏斗滴加双氧水,充分反应后,滤去少量固体残渣,得到
、 和硫酸的混合溶液。漫出实验中当观察到________,以判断反应结束,不再滴加双氧水。
图1 图2 图3
(3)制钴粉。向浸出后的溶液中加入 调节 ,接着加入 可以制取单质钴粉,同时有
生成。已知不同 时 (Ⅱ)的物种分布图如图2所示。 可以和柠檬酸根离子 生成
配合物 。
学科网(北京)股份有限公司①写出 时制钴粉的离子方程式:________。
② 后所制钴粉中由于含有 而导致纯度降低。若向 的溶液中加入柠檬酸钠
,可以提高钴粉的纯度,原因是________。
(4)请补充完整由浸取后滤液先制备 ,并进一步制取 的实验方案:取浸取后滤液,
________,得到 。[已知: 易溶于水, 难溶于水, 在空气中加热时
的固体残留率 )与随温度的变化如图3所示。实验中须使用的试剂有
溶液、 溶液]
(5)用下列实验可以测定 的组成:
实验1:准确称取一定质量的 样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在
和 ),冷却后转移到容量瓶中并定容至 。
实验2:移取 实验1容量瓶中溶液,加入指示剂,用 溶液滴定
至终点(滴定反应为 ),平行滴定3次,平均消耗EDTA溶液 。
实验3:准确称取与实验1中等质量的 样品,加入一定量的硝酸和 溶液,加热至固体完全溶
解。冷却后转移到容量瓶中并定容至 。移取 溶液,通过火焰原子吸收光谱法测定其中
浓度为 。
计算化学式 中 的值,并写出计算过程。
17.(15分)乙苯被吸附在催化剂表面发生脱氢可生成苯乙烯、苯甲醛等,生成苯乙烯的相关反应如下。反
应1:
反应2:
反应3:
学科网(北京)股份有限公司(1)反应4: ________
。
(2)较低温度下,向乙苯脱氢的反应体系中加入少量 ,乙苯平衡转化率较高而苯乙烯的选择性较低,其
原因可能是________。
(3)向乙苯脱氢反应体系中加入 ,乙苯转化率与体系中 分压强的关系如题图1所示。随 的增
加,乙苯转化率先增大后减小的可能原因为________。
图1 图2
(4)研究发现在 催化剂表面进行 的乙苯脱氢反应中, (+5价)是反应的活性中心,转
化过程如题图2所示。
①转化Ⅰ发生反应的化学方程式为________。反应一段时间后,催化剂活性有所下降,原因可能有反应过程
产生的积碳覆盖在活性中心表面和________。
②简述转化Ⅱ的作用________。
③ 参与的乙苯脱氢机理如题图3所示( 、 表示乙苯分子中 或 原子的位置; 为催化剂的
活性位点,其中 位点带部分正电荷, 、 位点带部分负电荷)。
图3
图中所示反应机理中步骤Ⅰ和步骤Ⅱ可描述为________。
学科网(北京)股份有限公司江苏省泰州中学 20232024 学年秋学期高三年级期初调研考试
化学学科试卷评分标准
一、单项选择题:共13题,每题3分,共39分
1.A 2.D 3.B 4.D 5.D 6.A 7.B 8.A 9.C 10.B 11.C 12.C
13.B
二、非选择题:共4题,共61分
14.(14分)
(1)① 或 (3分)
② (3分)
③ (2分)
(2)①与 体系相比 体系中 浓度更大,有利于 、 、 溶出
、通入 发生反应 ,增大了 浓度,降低了 浓度,
促进 等溶出 (3分)
② 酸浸时产生的 被 还原成+1价的铜,与 、 提供的 转化为 (3分)
15.(15分)
(1)8(2分)
(2)取代反应(2分)
(3) (3分)
(4) 或
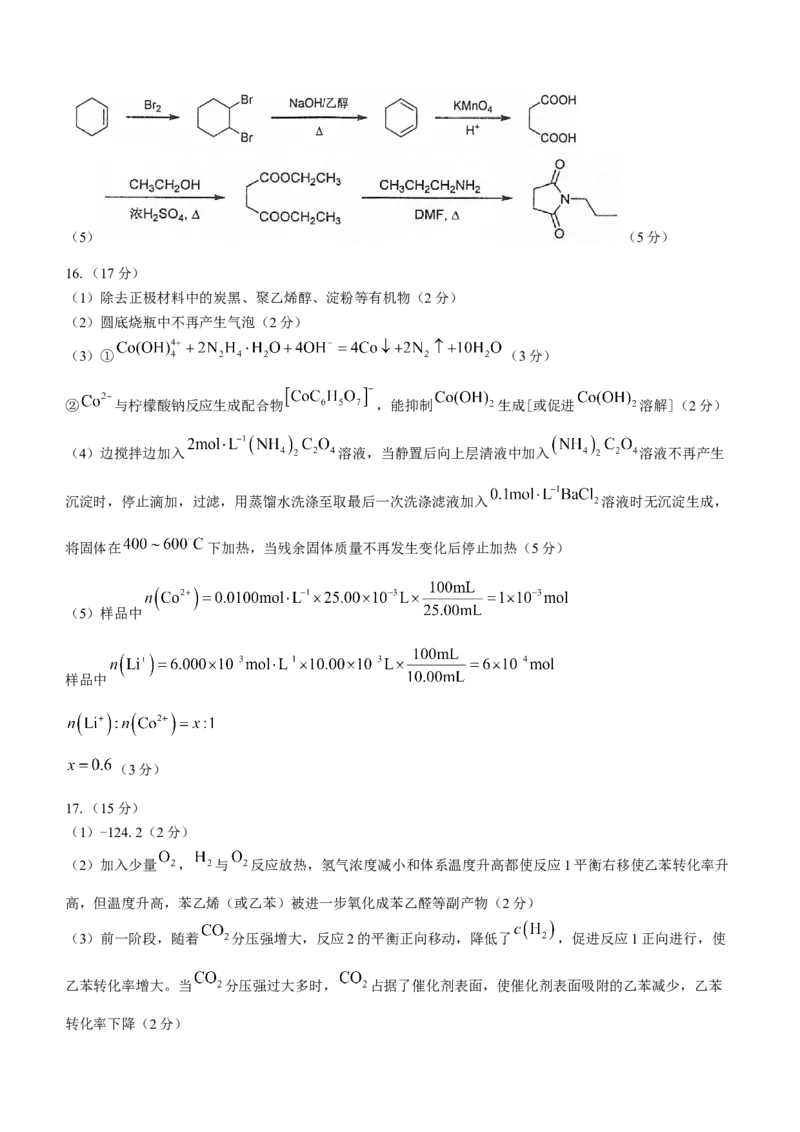
学科网(北京)股份有限公司(5) (5分)
16.(17分)
(1)除去正极材料中的炭黑、聚乙烯醇、淀粉等有机物(2分)
(2)圆底烧瓶中不再产生气泡(2分)
(3)① (3分)
② 与柠檬酸钠反应生成配合物 ,能抑制 生成[或促进 溶解](2分)
(4)边搅拌边加入 溶液,当静置后向上层清液中加入 溶液不再产生
沉淀时,停止滴加,过滤,用蒸馏水洗涤至取最后一次洗涤滤液加入 溶液时无沉淀生成,
将固体在 下加热,当残余固体质量不再发生变化后停止加热(5分)
(5)样品中
样品中
(3分)
17.(15分)
(1)-124.2(2分)
(2)加入少量 , 与 反应放热,氢气浓度减小和体系温度升高都使反应1平衡右移使乙苯转化率升
高,但温度升高,苯乙烯(或乙苯)被进一步氧化成苯乙醛等副产物(2分)
(3)前一阶段,随着 分压强增大,反应2的平衡正向移动,降低了 ,促进反应1正向进行,使
乙苯转化率增大。当 分压强过大多时, 占据了催化剂表面,使催化剂表面吸附的乙苯减少,乙苯
转化率下降(2分)
学科网(北京)股份有限公司(4)① (2分)
催化剂中V(+5价)的含量减少(2分)
②将 转化为 ,使催化剂获得再生,同时可以消除积碳(2分)
③乙苯 带部分正电荷,被带部分负电荷的 位点吸引,随后解离出 并吸附在 位点上; 位点
上的 与 位点上 中带部分负电荷的 作用生成生成 ,带部分正电荷的 吸附在带部分负电
荷的 位点上(3分)
学科网(北京)股份有限公司