文档内容
丰城中学校本资料
丰城中学 2023-2024 学年上学期高四化学入学考试试卷
命题人:吴志强 审题人: 涂传兵 2023.9.2
本试卷总分值为100分 考试时间100分钟
可能用到的相对原子质量:Al-27 Fe-56 O-16 N-14 Cl-35.5 S-32 Mn-55
一、 单选题(每小题3分,共45分)
1. 设N 表示阿伏加德罗常数的值。下列叙述正确的是
A
A.71gCl 溶于适量水中,所得溶液中Cl 和ClO-微粒总数为N
2 2 A
B.1L1mol/LH O 溶液完全反应,转移的电子数目一定为2N
2 2 A
C. 标准状况下,22.4LCCl 中含有C-Cl键的个数为4N
4 A
D.7.8gNa S和Na O 的混合物中,含有的离子总数为0.3N
2 2 2 A
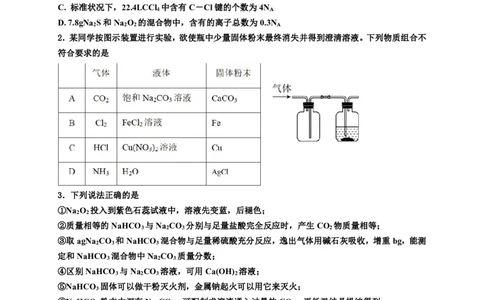
2.某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不
符合要求的是
3.下列说法正确的是
①Na O 投入到紫色石蕊试液中,溶液先变蓝,后褪色;
2 2
②质量相等的NaHCO 与Na CO 分别与足量盐酸完全反应时,产生CO 物质量相等;
3 2 3 2
③取agNa CO 和NaHCO 混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,能测
2 3 3
定和NaHCO 混合物中Na CO 质量分数;
3 2 3
④区别NaHCO 与Na CO 溶液,可用Ca(OH) 溶液;
3 2 3 2
⑤NaHCO 固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
3
⑥NaHCO 粉末中混有Na CO ,可配制成溶液通入过量的CO ,再低温结晶提纯得到。
3 2 3 2
A.①⑥ B.②⑤ C.②④ D.③④
4.下列离子方程式书写正确的是
A. Cl 通入水中制氯水:Cl H O2HClClO
2 2 2
B. 可用Na SO 溶液吸收少量Cl :3SO2 Cl H O 2HSO 2Cl SO2
2 3 2 3 2 2 3 4
C. 过量铁粉与稀硝酸反应:FeNO 4H Fe3 NO+2H O
3 2
1
学科网(北京)股份有限公司丰城中学校本资料
NaHCO BaOH HCO Ba2 OH BaCO H O
D 3溶液与少量 2溶液混合: 3 3 2
.
5.下列指定反应的离子方程式正确的是
A. 向Ba(HCO ) 溶液中加入少量KOH溶液:Ba2++2HCO- +2OH-=BaCO ↓+ CO2- +2H O
3 2 3 3 3 2
B. 向Fe(SCN) 溶液中滴入几滴0.01mol•L-1NaOH溶液:Fe3++3OH-=Fe(OH) ↓
3 3
C. 已知次磷酸(NaH PO )属于正盐,向次磷酸(H PO 为弱酸)溶液中加入足量NaOH溶液:
2 2 3 2
H PO
+3OH-=PO3-
+3H O
3 2 2 2
D.K S溶液久置于空气中会变浑浊:2S2-+2H O+O =2S↓+4OH-
2 2 2
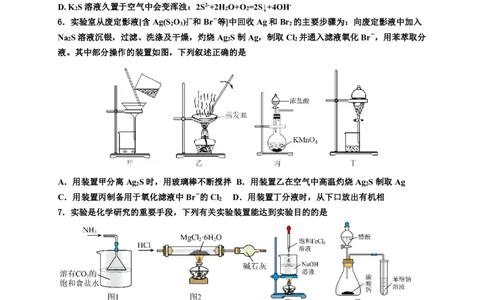
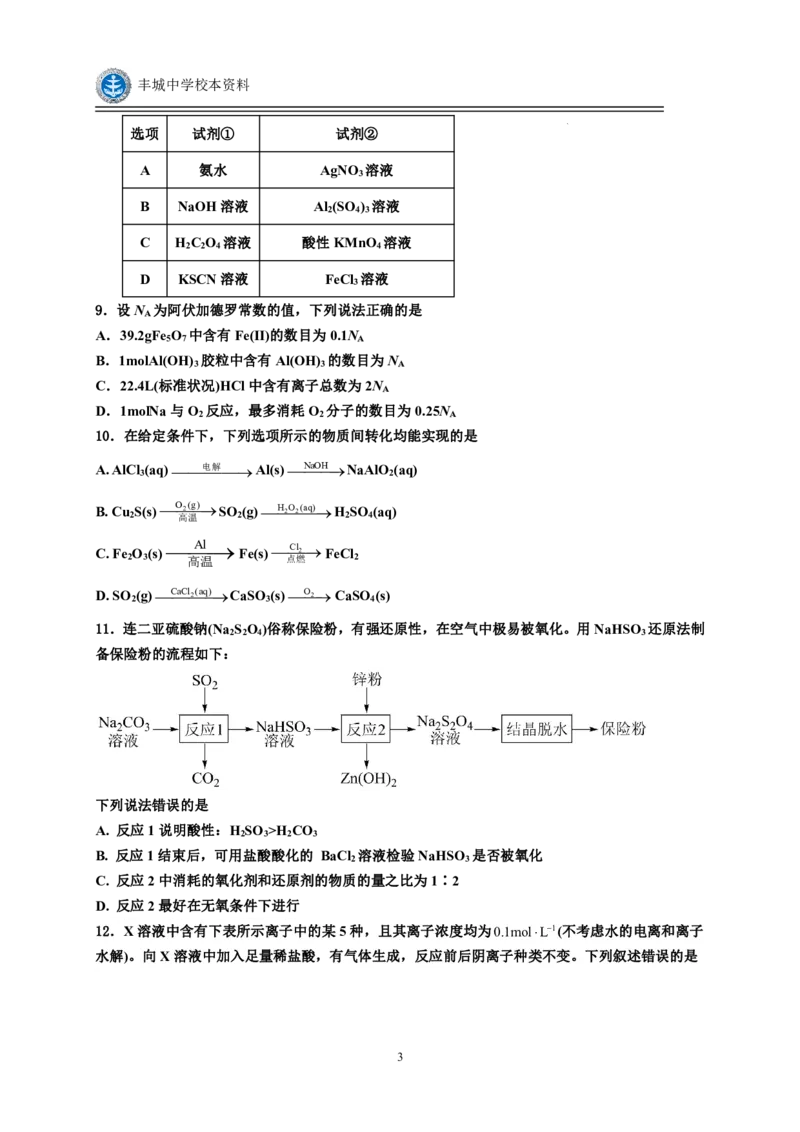
6.实验室从废定影液[含Ag(S O )3-和Br-等]中回收Ag和Br 的主要步骤为:向废定影液中加入
2 3 2 2
Na S溶液沉银,过滤、洗涤及干燥,灼烧Ag S制Ag,制取Cl 并通入滤液氧化Br-,用苯萃取分
2 2 2
液。其中部分操作的装置如图,下列叙述正确的是
A.用装置甲分离Ag S时,用玻璃棒不断搅拌 B.用装置乙在空气中高温灼烧Ag S制取Ag
2 2
C.用装置丙制备用于氧化滤液中Br-的Cl D.用装置丁分液时,从下口放出有机相
2
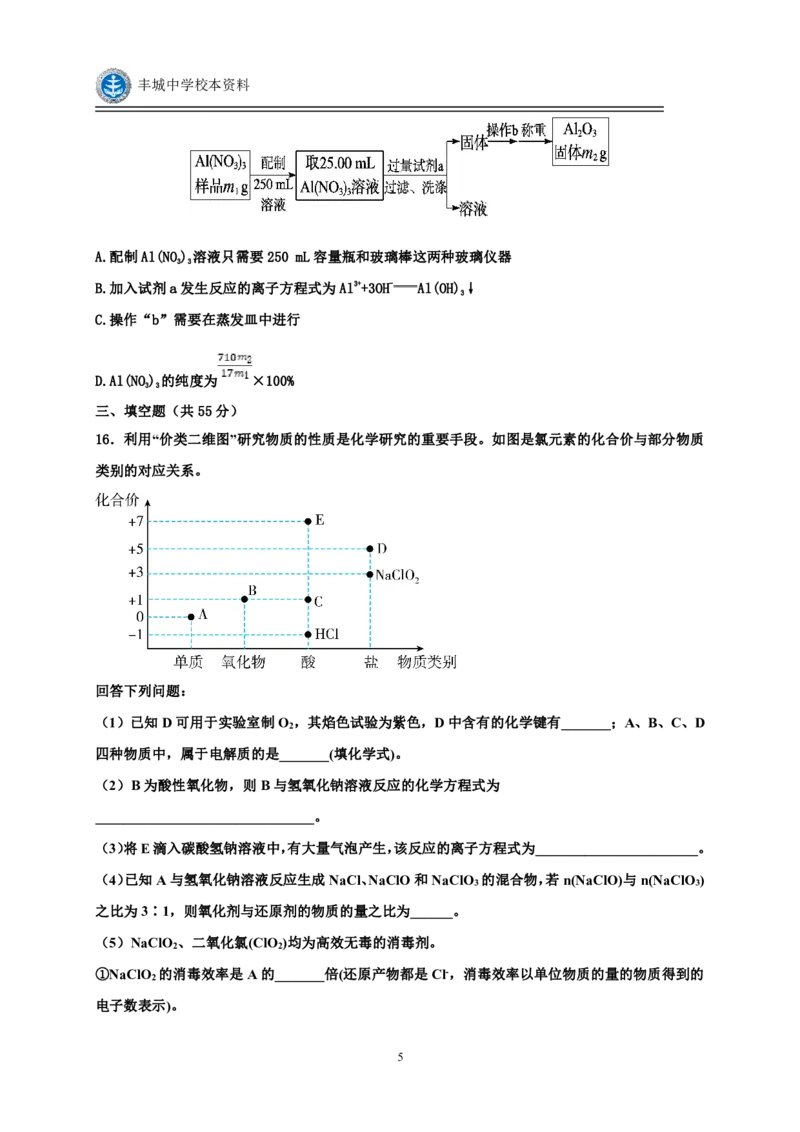
7.实验是化学研究的重要手段,下列有关实验装置能达到实验目的的是
A. 图1装置制备大量NaHCO B. 图2装置制备无水MgCl
3 2
C. 图3装置制备Fe(OH) 胶体 D. 图4装置可比较醋酸、碳酸、苯酚酸性强弱
3
8.取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为0.1mol·L-1),反应现象
没有明显差别的是
2
学科网(北京)股份有限公司丰城中学校本资料
选项 试剂① 试剂②
A 氨水 AgNO 溶液
3
B NaOH溶液 Al (SO ) 溶液
2 4 3
C H C O 溶液 酸性KMnO 溶液
2 2 4 4
D KSCN溶液 FeCl 溶液
3
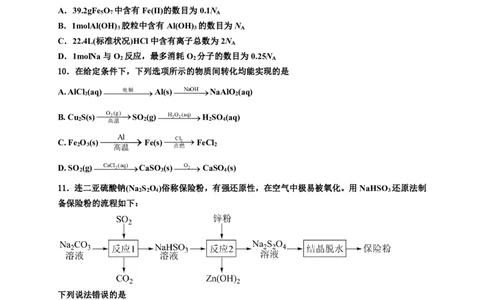
9.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.39.2gFe O 中含有Fe(Ⅱ)的数目为0.1N
5 7 A
B.1molAl(OH) 胶粒中含有Al(OH) 的数目为N
3 3 A
C.22.4L(标准状况)HCl中含有离子总数为2N
A
D.1molNa与O 反应,最多消耗O 分子的数目为0.25N
2 2 A
10.在给定条件下,下列选项所示的物质间转化均能实现的是
A.AlCl (aq)电解Al(s)NaOHNaAlO (aq)
3 2
B.Cu
2
S(s) O
高
2 (
温
g) SO
2
(g)H2 O2 (aq)H
2
SO
4
(aq)
C.Fe O (s)
Al
Fe(s)
Cl 2
FeCl
2 3 高温 点燃 2
D.SO
2
(g)CaCl2 (aq)CaSO
3
(s)O2CaSO
4
(s)
11.连二亚硫酸钠(Na S O )俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO 还原法制
2 2 4 3
备保险粉的流程如下:
下列说法错误的是
A. 反应1说明酸性:H SO >H CO
2 3 2 3
B. 反应1结束后,可用盐酸酸化的 BaCl 溶液检验NaHSO 是否被氧化
2 3
C. 反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2
D. 反应2最好在无氧条件下进行
12.X溶液中含有下表所示离子中的某5种,且其离子浓度均为0.1molL1(不考虑水的电离和离子
水解)。向X溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是
3
学科网(北京)股份有限公司丰城中学校本资料
阳离子 Na、Fe3、Ba2+、Fe2+、Mg2、Al3
阴离子 OH、NO、CO2、SO2、Cl
3 3 4
A.原溶液中一定含有Mg2 B.X溶液中一定没有CO2
3
C.X溶液中含有3种阳离子、2种阴离子
D.生成气体的离子方程式为3Fe2NO4H 3Fe3+NO2H O
3 2
13.氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。某研究性学习小组模
拟热分解CuCl •2H O制备CuCl的过程,并进行相关物质转化的探究。
2 2
已知:酸性条件下Cu+不稳定
下列说法不正确的是
A.X气体是HCl,可抑制CuCl •2H O加热时水解
2 2
B. 途径1中产生的Cl 可以回收利用,也可以通入饱和NaOH溶液中除去
2
200℃
C. 途径2中200℃时反应的化学方程式为Cu (OH) Cl 2CuO+2HCl↑
2 2 2
D.CuCl与稀硫酸反应的离子方程式为2Cu++4H++SO 2 =2Cu2++SO ↑+2H O
4 2 2
14.双碱法脱硫过程如图所示,下列说法不正确的是
A.双碱法脱硫过程中,NaOH可以循环利用
B.过程I中,SO 表现出酸性氧化物的性质
2
C.总反应为2CaOH 2SO O 2CaSO 2H O
2 2 2 4 2
D.过程Ⅱ中,1molO 参加反应时可氧化1molNa SO
2 2 3
15.实验室测量Al(NO) 纯度的步骤如图所示。下列说法正确的是( )
3 3
4
学科网(北京)股份有限公司丰城中学校本资料
A.配制Al(NO) 溶液只需要250 mL容量瓶和玻璃棒这两种玻璃仪器
3 3
B.加入试剂a发生反应的离子方程式为Al3++3OH- Al(OH)↓
3
C.操作“b”需要在蒸发皿中进行
D.Al(NO) 的纯度为 ×100%
3 3
三、填空题(共55分)
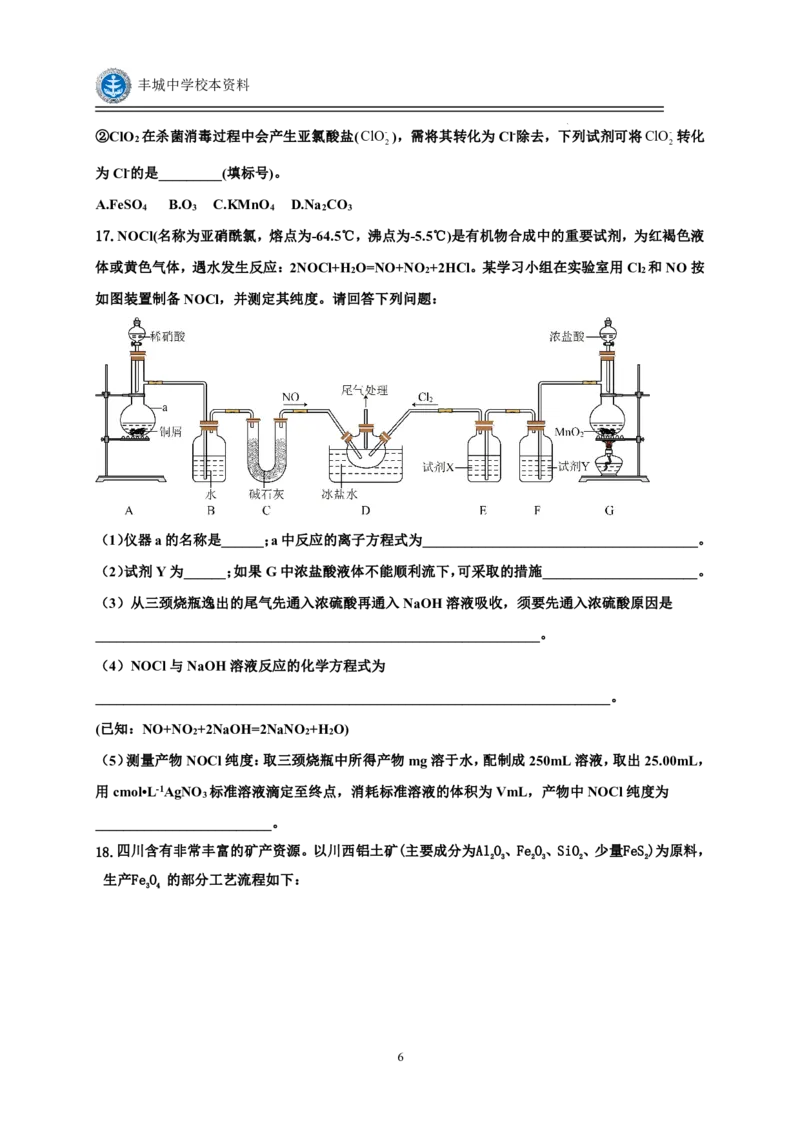
16.利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质
类别的对应关系。
回答下列问题:
(1)已知D可用于实验室制O ,其焰色试验为紫色,D中含有的化学键有_______;A、B、C、D
2
四种物质中,属于电解质的是_______(填化学式)。
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
_______________________________。
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______________________。
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO 的混合物,若n(NaClO)与n(NaClO )
3 3
之比为3∶1,则氧化剂与还原剂的物质的量之比为______。
(5)NaClO 、二氧化氯(ClO )均为高效无毒的消毒剂。
2 2
①NaClO 的消毒效率是A的_______倍(还原产物都是Cl-,消毒效率以单位物质的量的物质得到的
2
电子数表示)。
5
学科网(北京)股份有限公司丰城中学校本资料
②ClO 在杀菌消毒过程中会产生亚氯酸盐(ClO- ),需将其转化为Cl-除去,下列试剂可将ClO- 转化
2 2 2
为Cl-的是_________(填标号)。
A.FeSO B.O C.KMnO D.Na CO
4 3 4 2 3
17.NOCl(名称为亚硝酰氯,熔点为-64.5℃,沸点为-5.5℃)是有机物合成中的重要试剂,为红褐色液
体或黄色气体,遇水发生反应:2NOCl+H O=NO+NO +2HCl。某学习小组在实验室用Cl 和NO按
2 2 2
如图装置制备NOCl,并测定其纯度。请回答下列问题:
(1)仪器a的名称是______;a中反应的离子方程式为_______________________________________。
(2)试剂Y为______;如果G中浓盐酸液体不能顺利流下,可采取的措施______________________。
(3)从三颈烧瓶逸出的尾气先通入浓硫酸再通入NaOH溶液吸收,须要先通入浓硫酸原因是
_______________________________________________________________。
(4)NOCl与NaOH溶液反应的化学方程式为
_________________________________________________________________________。
(已知:NO+NO +2NaOH=2NaNO +H O)
2 2 2
(5)测量产物NOCl纯度:取三颈烧瓶中所得产物mg溶于水,配制成250mL溶液,取出25.00mL,
用cmol•L-1AgNO 标准溶液滴定至终点,消耗标准溶液的体积为VmL,产物中NOCl纯度为
3
_________________________。
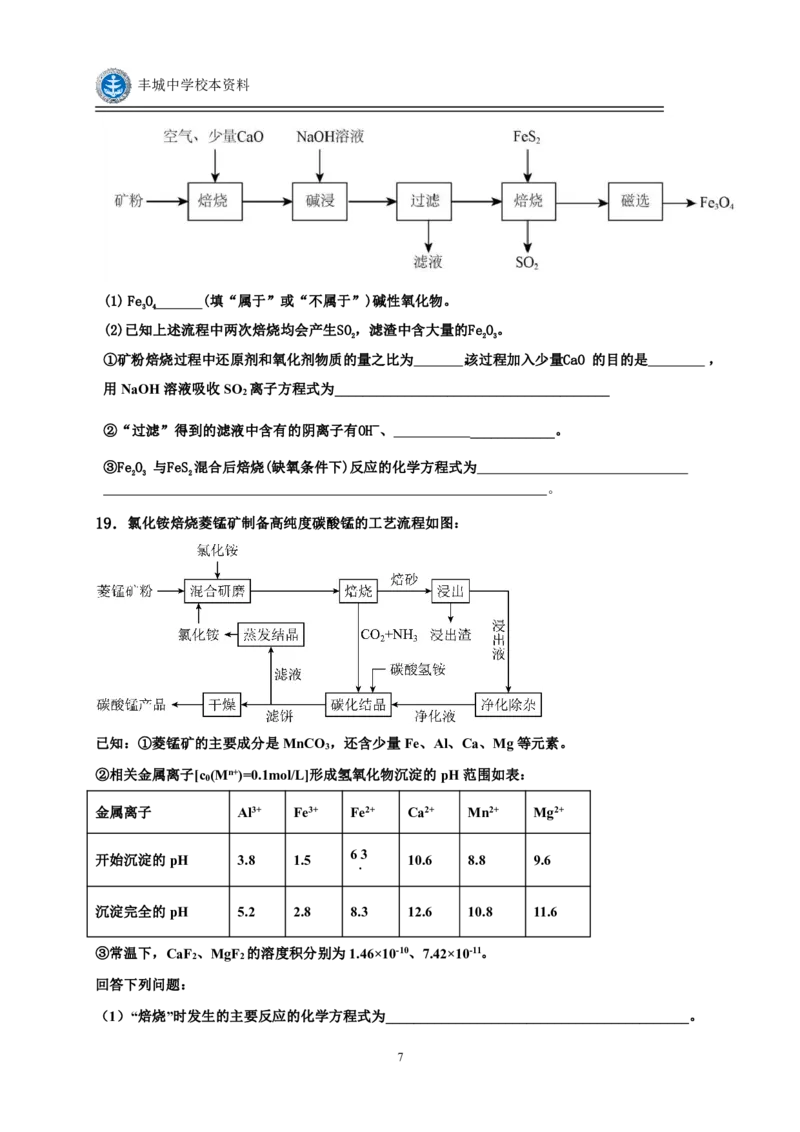
18.四川含有非常丰富的矿产资源。以川西铝土矿(主要成分为AlO、FeO、SiO、少量FeS)为原料,
2 3 2 3 2 2
生产FeO 的部分工艺流程如下:
3 4
6
学科网(北京)股份有限公司丰城中学校本资料
(1)FeO (填“属于”或“不属于”)碱性氧化物。
3 4
(2)已知上述流程中两次焙烧均会产生SO,滤渣中含大量的FeO。
2 2 3
①矿粉焙烧过程中还原剂和氧化剂物质的量之比为 ,该过程加入少量CaO 的目的是 ,
用NaOH溶液吸收SO 离子方程式为_______________________________________
2
-
②“过滤”得到的滤液中含有的阴离子有OH 、 ____________。
③FeO 与FeS 混合后焙烧(缺氧条件下)反应的化学方程式为
2 3 2
。
19.氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如图:
已知:①菱锰矿的主要成分是MnCO ,还含少量Fe、Al、Ca、Mg等元素。
3
②相关金属离子[c (Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如表:
0
金属离子 Al3+ Fe3+ Fe2+ Ca2+ Mn2+ Mg2+
开始沉淀的pH 3.8 1.5 6 . 3 10.6 8.8 9.6
沉淀完全的pH 5.2 2.8 8.3 12.6 10.8 11.6
③常温下,CaF 、MgF 的溶度积分别为1.46×10-10、7.42×10-11。
2 2
回答下列问题:
(1)“焙烧”时发生的主要反应的化学方程式为___________________________________________。
7
学科网(北京)股份有限公司丰城中学校本资料
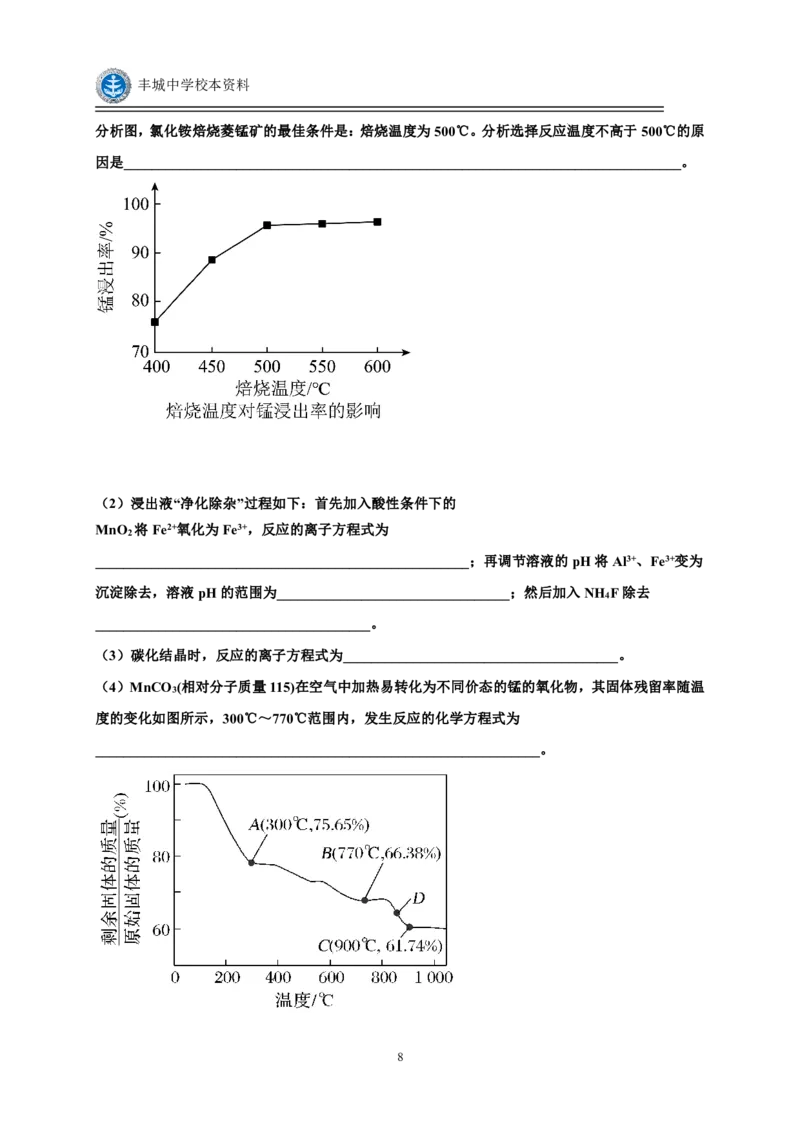
分析图,氯化铵焙烧菱锰矿的最佳条件是:焙烧温度为500℃。分析选择反应温度不高于500℃的原
因是_______________________________________________________________________________。
(2)浸出液“净化除杂”过程如下:首先加入酸性条件下的
MnO 将Fe2+氧化为Fe3+,反应的离子方程式为
2
_____________________________________________________;再调节溶液的pH将Al3+、Fe3+变为
沉淀除去,溶液pH的范围为_________________________________;然后加入NH F除去
4
_______________________________________。
(3)碳化结晶时,反应的离子方程式为_______________________________________。
(4)MnCO (相对分子质量115)在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温
3
度的变化如图所示,300℃~770℃范围内,发生反应的化学方程式为
_______________________________________________________________。
8
学科网(北京)股份有限公司