文档内容
试卷类型:A
潍坊市高考模拟考试
化学
2024.3
注意事项:
1.答题前,考生先将自己的学校、班级、姓名、考生号、座号填写在相应位置。
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用 0.5毫米黑
色签字笔书写,字体工整、笔迹清楚。
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试题卷
上答题无效。保持卡面清洁,不折叠、不破损。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 F 19 Na 23 Al 27 S 32
Cu 64 Bi 209
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与科技、生产、生活息息相关。下列说法正确的是( )
A.第19届亚运会使用零碳甲醇(由回收 合成)作燃料,符合“碳中和”理念
B.铜铟硫 量子点是纳米级的半导体材料,属于胶体
C.食品中的膳食纤维含纤维素,纤维素可以为运动员提供能量
D.“嫦娥五号”探测器使用GaAs太阳能电池,该电池将化学能转化为电能
2.下列物质性质与用途对应关系错误的是( )
A.金属钠导热性好,可用作传热介质 B. 熔点高,可用于制造耐高温材料
C.维生素C具有还原性,可用作食品抗氧化剂 D. 具有碱性,可用作消毒剂
3.完成下列实验,选用仪器(非玻璃仪器任选)正确的是( )
A.由浓硫酸配制 的稀硫酸:①②③④
B.测定 晶体中结晶水的含量:③⑤
学科网(北京)股份有限公司C. 胶体的制备:①④⑤
D.食盐精制:①③④⑤⑥
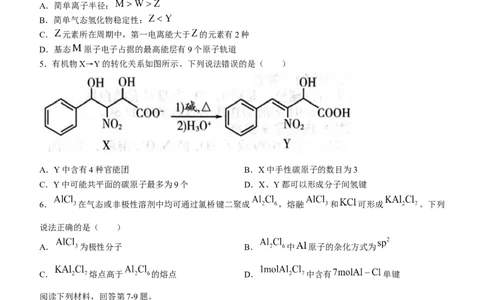
4.一种有机物催化剂由原子序数依次递增的前20号元素 组成,结构式如下图。下列说
法正确的是( )
A.简单离子半径:
B.简单气态氢化物稳定性:
C. 元素所在周期中,第一电离能大于 的元素有2种
D.基态 原子电子占据的最高能层有9个原子轨道
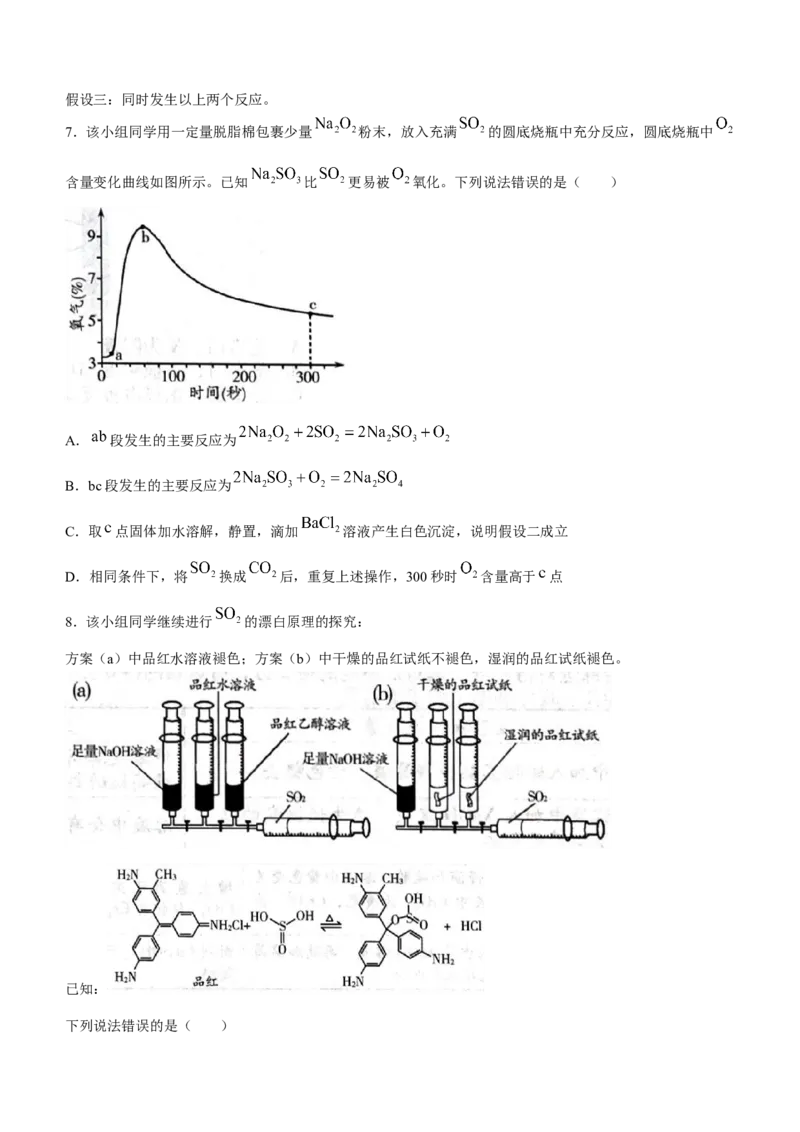
5.有机物X→Y的转化关系如图所示。下列说法错误的是( )
A.Y中含有4种官能团 B.X中手性碳原子的数目为3
C.Y中可能共平面的碳原子最多为9个 D.X、Y都可以形成分子间氢键
6. 在气态或非极性溶剂中均可通过氯桥键二聚成 ,熔融 和 可形成 。下列
说法正确的是( )
A. 为极性分子 B. 中 原子的杂化方式为
C. 熔点高于 的熔点 D. 中含有 单键
阅读下列材料,回答第7-9题。
某化学小组探究二氧化硫与过氧化钠的反应。取适量 粉末放入燃烧匙中,伸入充满 气体的集气瓶
中, 气体与 粉末接触时剧烈反应,淡黄色粉末变成白色粉末,并放出大量的热。根据反应现象,
作如下假设:
假设一:发生反应 ;
假设二:发生反应 ;
学科网(北京)股份有限公司假设三:同时发生以上两个反应。
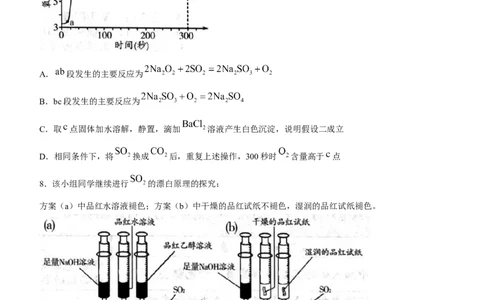
7.该小组同学用一定量脱脂棉包裹少量 粉末,放入充满 的圆底烧瓶中充分反应,圆底烧瓶中
含量变化曲线如图所示。已知 比 更易被 氧化。下列说法错误的是( )
A. 段发生的主要反应为
B.bc段发生的主要反应为
C.取 点固体加水溶解,静置,滴加 溶液产生白色沉淀,说明假设二成立
D.相同条件下,将 换成 后,重复上述操作,300秒时 含量高于 点
8.该小组同学继续进行 的漂白原理的探究:
方案(a)中品红水溶液褪色;方案(b)中干燥的品红试纸不褪色,湿润的品红试纸褪色。
已知:
下列说法错误的是( )
学科网(北京)股份有限公司A.(a)中品红乙醇溶液不褪色
B. 能使品红水溶液褪色,是因为 本身具有漂白性
C.(a)和(b)中 溶液的作用为吸收剩余的
D. 漂白的织物易恢复原来颜色
9.该小组收集上述实验(a)中吸收了 的 溶液,并测定其中 的含量。向圆底烧瓶中加入
上述溶液和足量稀硫酸,加热使 全部逸出并与 完全反应,除去过量的 ,然后用
标准溶液进行滴定,消耗 溶液 。下列说法正确的是( )
A.实验时圆底烧瓶中加入液体体积不超过圆底烧瓶的
B.滴定终点时溶液的 ,可选择石蕊为指示剂
C.测得 含量为
D.用盐酸代替硫酸,则 . 含量测定值偏高
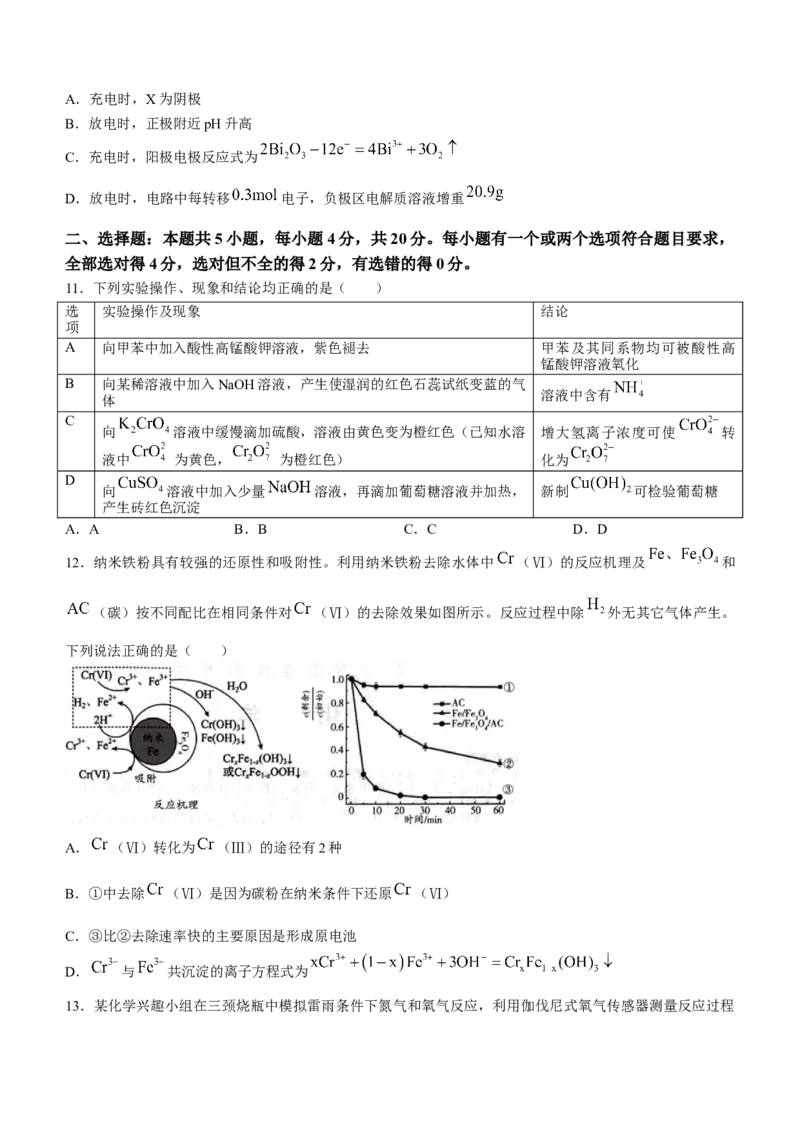
10.复旦大学设计了一种可充电的铋-空气电池,有较强稳定性。该电池使用了三氟甲磺酸铋
非碱性水系电解质溶液,简写为 ,工作原理如图所示。已
知: 水解方程式为 。下列说法错误的是( )
学科网(北京)股份有限公司A.充电时,X为阴极
B.放电时,正极附近pH升高
C.充电时,阳极电极反应式为
D.放电时,电路中每转移 电子,负极区电解质溶液增重
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
11.下列实验操作、现象和结论均正确的是( )
选 实验操作及现象 结论
项
A 向甲苯中加入酸性高锰酸钾溶液,紫色褪去 甲苯及其同系物均可被酸性高
锰酸钾溶液氧化
B 向某稀溶液中加入NaOH溶液,产生使湿润的红色石蕊试纸变蓝的气
溶液中含有
体
C
向 溶液中缓慢滴加硫酸,溶液由黄色变为橙红色(已知水溶 增大氢离子浓度可使 转
液中 为黄色, 为橙红色) 化为
D
向 溶液中加入少量 溶液,再滴加葡萄糖溶液并加热, 新制 可检验葡萄糖
产生砖红色沉淀
A.A B.B C.C D.D
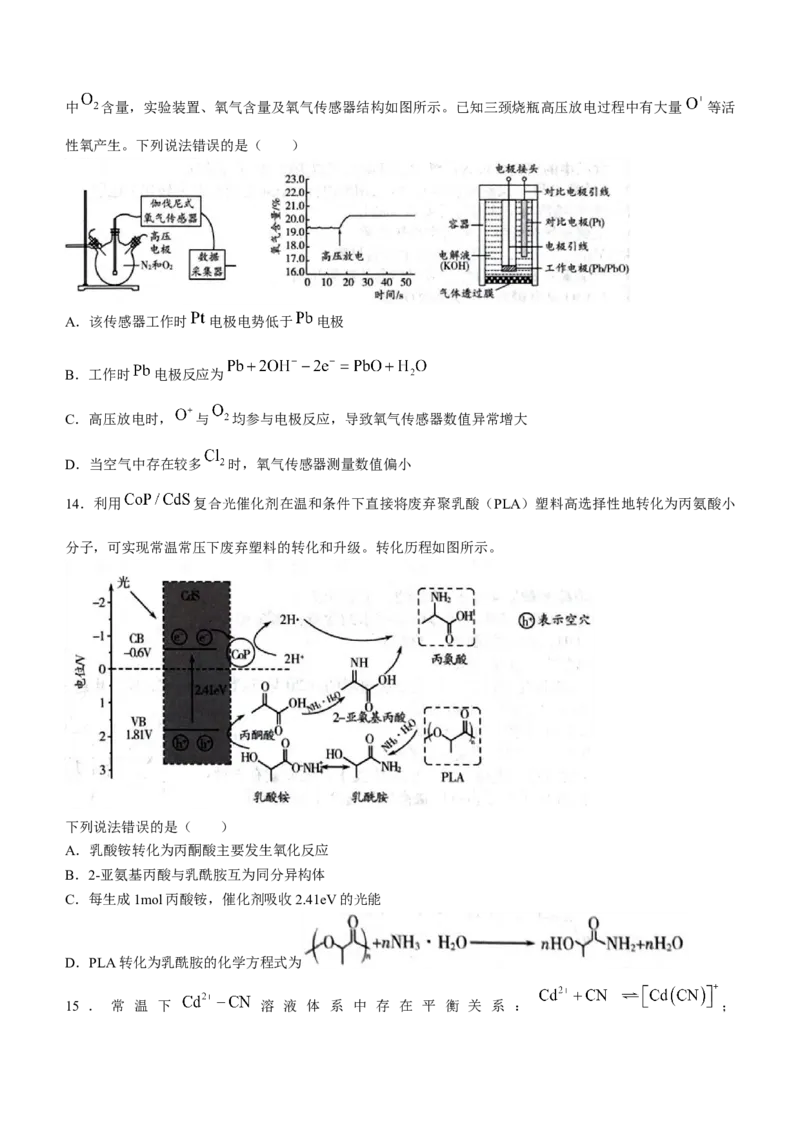
12.纳米铁粉具有较强的还原性和吸附性。利用纳米铁粉去除水体中 (Ⅵ)的反应机理及 和
(碳)按不同配比在相同条件对 (Ⅵ)的去除效果如图所示。反应过程中除 外无其它气体产生。
下列说法正确的是( )
A. (Ⅵ)转化为 (Ⅲ)的途径有2种
B.①中去除 (Ⅵ)是因为碳粉在纳米条件下还原 (Ⅵ)
C.③比②去除速率快的主要原因是形成原电池
D. 与 共沉淀的离子方程式为
13.某化学兴趣小组在三颈烧瓶中模拟雷雨条件下氮气和氧气反应,利用伽伐尼式氧气传感器测量反应过程
学科网(北京)股份有限公司中 含量,实验装置、氧气含量及氧气传感器结构如图所示。已知三颈烧瓶高压放电过程中有大量 等活
性氧产生。下列说法错误的是( )
A.该传感器工作时 电极电势低于 电极
B.工作时 电极反应为
C.高压放电时, 与 均参与电极反应,导致氧气传感器数值异常增大
D.当空气中存在较多 时,氧气传感器测量数值偏小
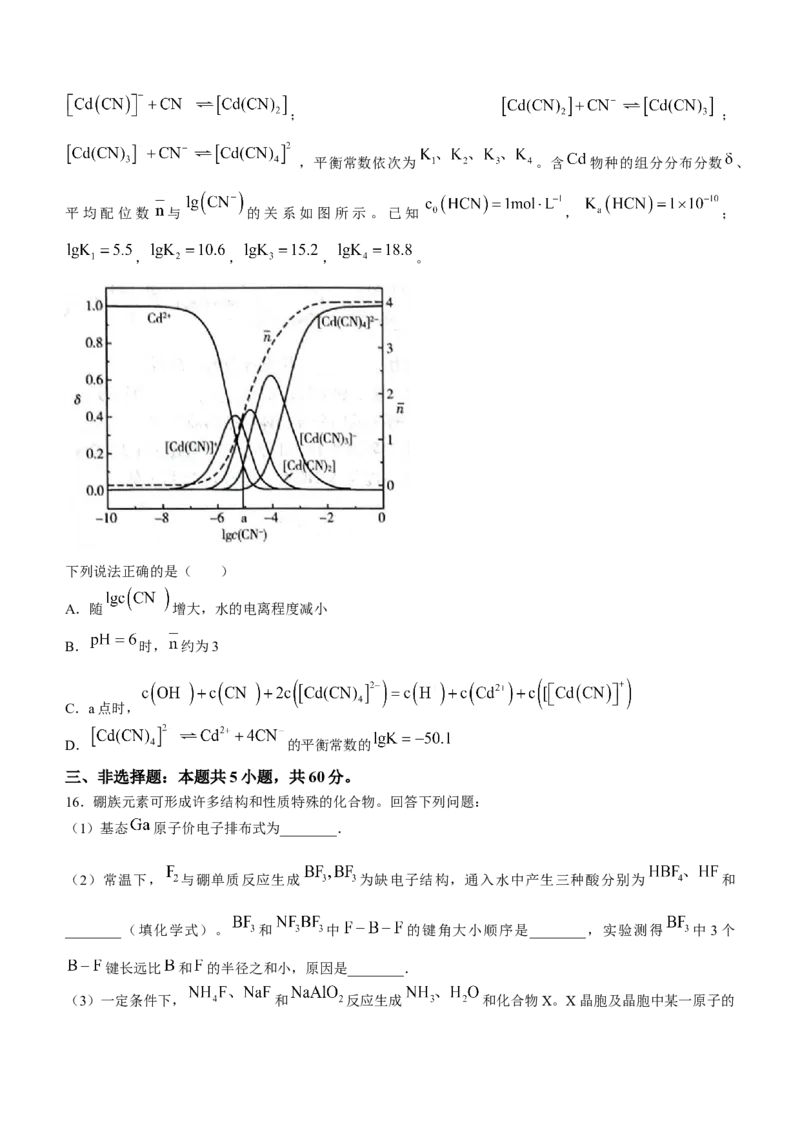
14.利用 复合光催化剂在温和条件下直接将废弃聚乳酸(PLA)塑料高选择性地转化为丙氨酸小
分子,可实现常温常压下废弃塑料的转化和升级。转化历程如图所示。
下列说法错误的是( )
A.乳酸铵转化为丙酮酸主要发生氧化反应
B.2-亚氨基丙酸与乳酰胺互为同分异构体
C.每生成1mol丙酸铵,催化剂吸收2.41eV的光能
D.PLA转化为乳酰胺的化学方程式为
15 . 常 温 下 溶 液 体 系 中 存 在 平 衡 关 系 : ;
学科网(北京)股份有限公司; ;
,平衡常数依次为 。含 物种的组分分布分数 、
平均配位数 与 的关系如图所示。已知 , ;
, , , 。
下列说法正确的是( )
A.随 增大,水的电离程度减小
B. 时, 约为3
C.a点时,
D. 的平衡常数的
三、非选择题:本题共5小题,共60分。
16.硼族元素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)基态 原子价电子排布式为________.
(2)常温下, 与硼单质反应生成 为缺电子结构,通入水中产生三种酸分别为 和
________(填化学式)。 和 中 的键角大小顺序是________,实验测得 中 3 个
键长远比 和 的半径之和小,原因是________.
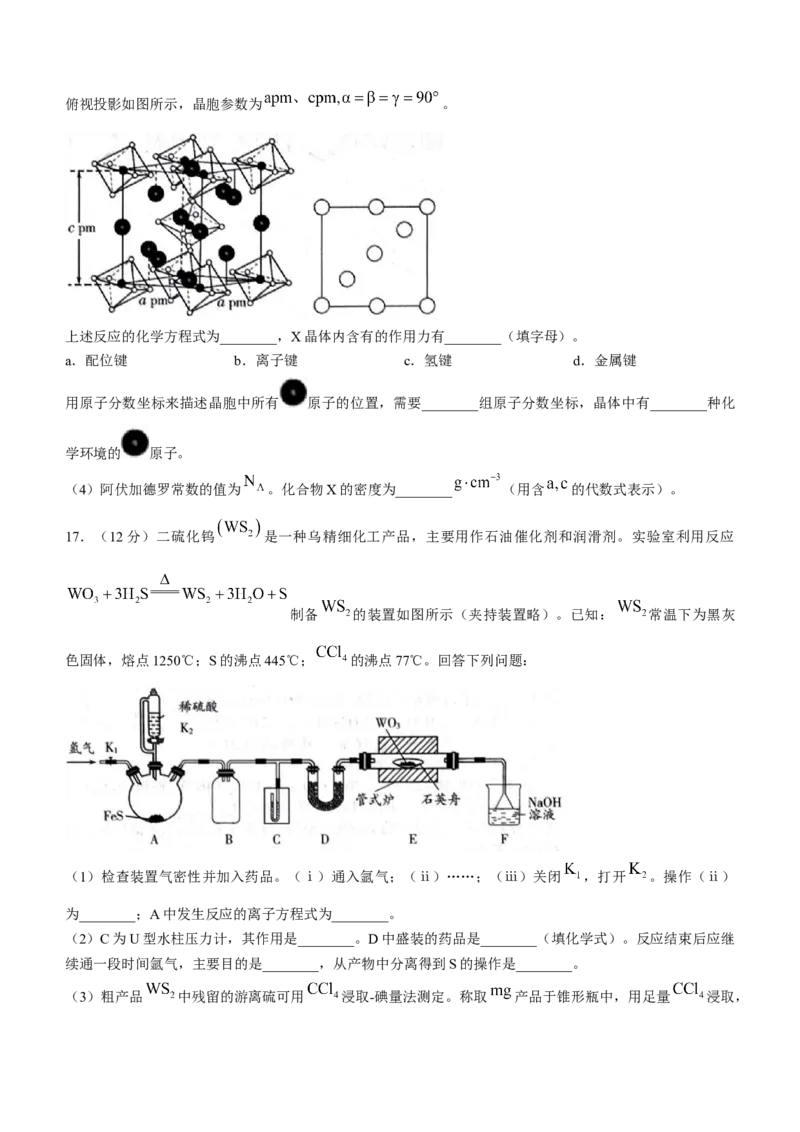
(3)一定条件下, 和 反应生成 和化合物X。X晶胞及晶胞中某一原子的
学科网(北京)股份有限公司俯视投影如图所示,晶胞参数为 。
上述反应的化学方程式为________,X晶体内含有的作用力有________(填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
用原子分数坐标来描述晶胞中所有 原子的位置,需要________组原子分数坐标,晶体中有________种化
学环境的 原子。
(4)阿伏加德罗常数的值为 。化合物X的密度为________ (用含 的代数式表示)。
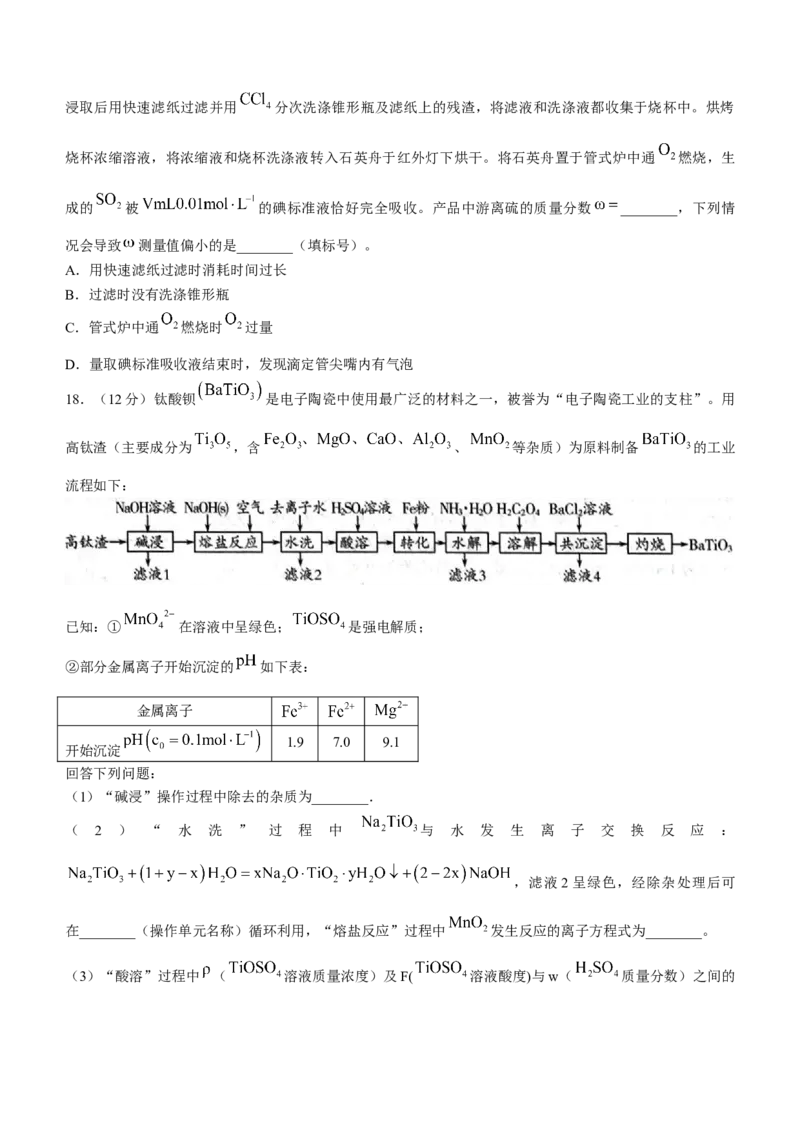
17.(12分)二硫化钨 是一种乌精细化工产品,主要用作石油催化剂和润滑剂。实验室利用反应
制备 的装置如图所示(夹持装置略)。已知: 常温下为黑灰
色固体,熔点1250℃;S的沸点445℃; 的沸点77℃。回答下列问题:
(1)检查装置气密性并加入药品。(ⅰ)通入氩气;(ⅱ)……;(ⅲ)关闭 ,打开 。操作(ⅱ)
为________;A中发生反应的离子方程式为________。
(2)C为U型水柱压力计,其作用是________。D中盛装的药品是________(填化学式)。反应结束后应继
续通一段时间氩气,主要目的是________,从产物中分离得到S的操作是________。
(3)粗产品 中残留的游离硫可用 浸取-碘量法测定。称取 产品于锥形瓶中,用足量 浸取,
学科网(北京)股份有限公司浸取后用快速滤纸过滤并用 分次洗涤锥形瓶及滤纸上的残渣,将滤液和洗涤液都收集于烧杯中。烘烤
烧杯浓缩溶液,将浓缩液和烧杯洗涤液转入石英舟于红外灯下烘干。将石英舟置于管式炉中通 燃烧,生
成的 被 的碘标准液恰好完全吸收。产品中游离硫的质量分数 ________,下列情
况会导致 测量值偏小的是________(填标号)。
A.用快速滤纸过滤时消耗时间过长
B.过滤时没有洗涤锥形瓶
C.管式炉中通 燃烧时 过量
D.量取碘标准吸收液结束时,发现滴定管尖嘴内有气泡
18.(12分)钛酸钡 是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用
高钛渣(主要成分为 ,含 、 等杂质)为原料制备 的工业
流程如下:
已知:① 在溶液中呈绿色; 是强电解质;
②部分金属离子开始沉淀的 如下表:
金属离子
1.9 7.0 9.1
开始沉淀
回答下列问题:
(1)“碱浸”操作过程中除去的杂质为________.
( 2 ) “ 水 洗 ” 过 程 中 与 水 发 生 离 子 交 换 反 应 :
,滤液2呈绿色,经除杂处理后可
在________(操作单元名称)循环利用,“熔盐反应”过程中 发生反应的离子方程式为________。
(3)“酸溶”过程中 ( 溶液质量浓度)及F( 溶液酸度)与w( 质量分数)之间的
学科网(北京)股份有限公司关系如图所示。当 值恒定时,随 溶液质量浓度增大,所需硫酸的质量分数________(填“增大”
“减小”或“不变”)。
(4)“水解”操作加入 目的是调节溶液 ,可适当提高水解速率。已知:
,水解反应 的平衡常数 ________;
“转化”过程加入铁粉的目的是________,滤液3中含有的金属阳离子有________。
(5)“共沉淀”过程发生反应: ,
“灼烧”时隔绝空气,发生反应的化学方程式为________。
19.(12分)苯乙烯是重要的基础化工原料,工业上常利用乙苯催化脱氢制备苯乙烯。涉及的反应如下:
ⅰ.
ⅱ.
ⅲ.
回答下列问题:
(1)已知部分化学键的键能:
化学键
键 能
332 611 414 436
________ .
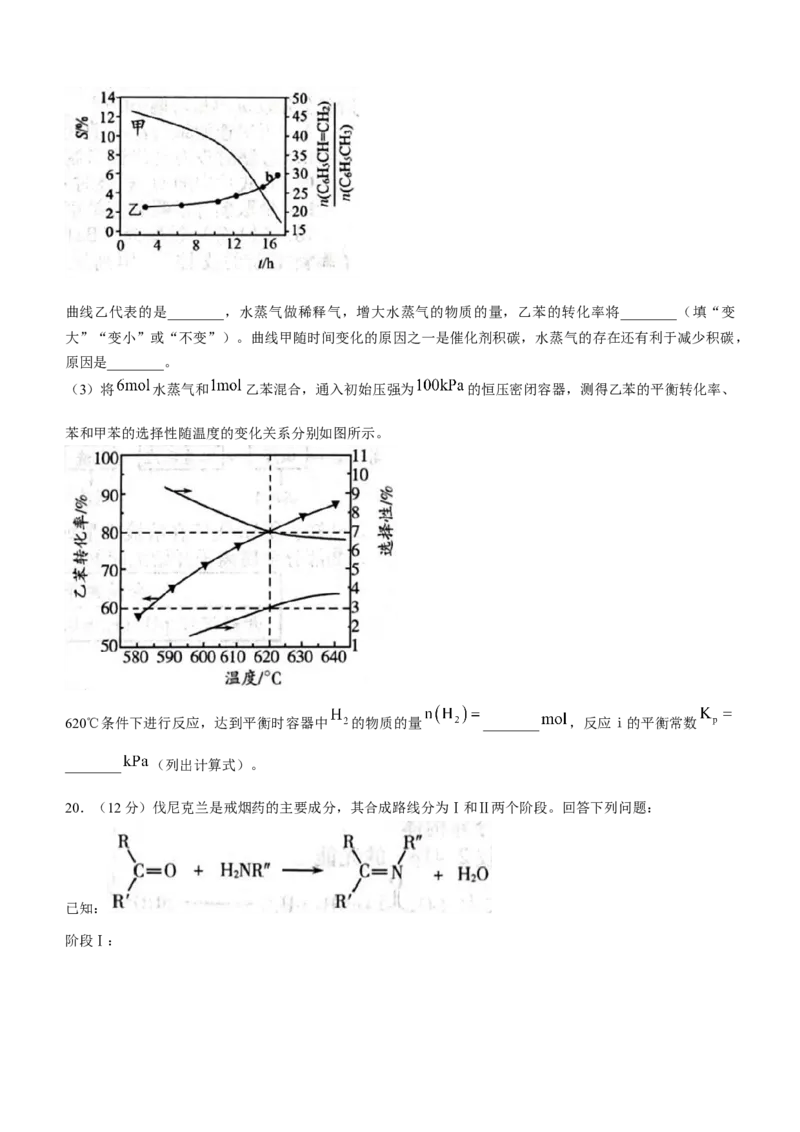
(2)一定温度下,在恒压密闭容器中充入乙苯和水蒸气,在催化剂作用下发生上述反应,测得反应体系中甲
苯的选择性S( )及 随时间变化曲线
如图所示。
学科网(北京)股份有限公司曲线乙代表的是________,水蒸气做稀释气,增大水蒸气的物质的量,乙苯的转化率将________(填“变
大”“变小”或“不变”)。曲线甲随时间变化的原因之一是催化剂积碳,水蒸气的存在还有利于减少积碳,
原因是________。
(3)将 水蒸气和 乙苯混合,通入初始压强为 的恒压密闭容器,测得乙苯的平衡转化率、
苯和甲苯的选择性随温度的变化关系分别如图所示。
620℃条件下进行反应,达到平衡时容器中 的物质的量 ________ ,反应ⅰ的平衡常数
________ (列出计算式)。
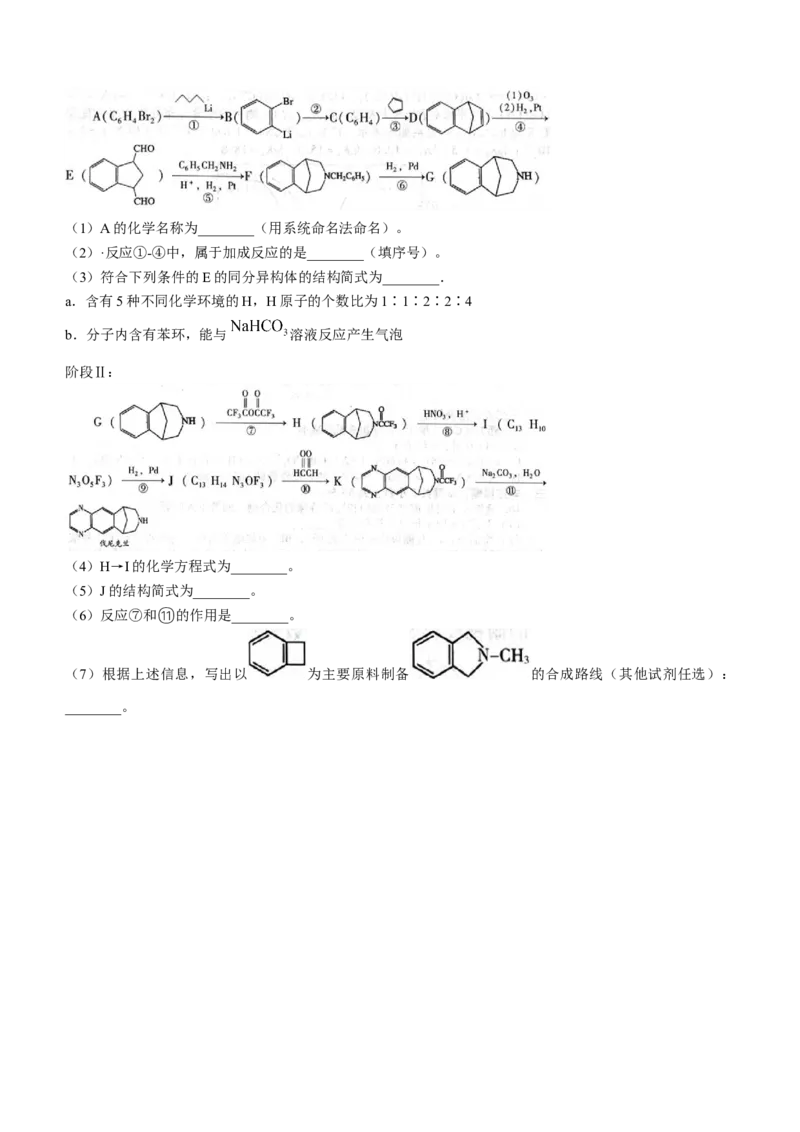
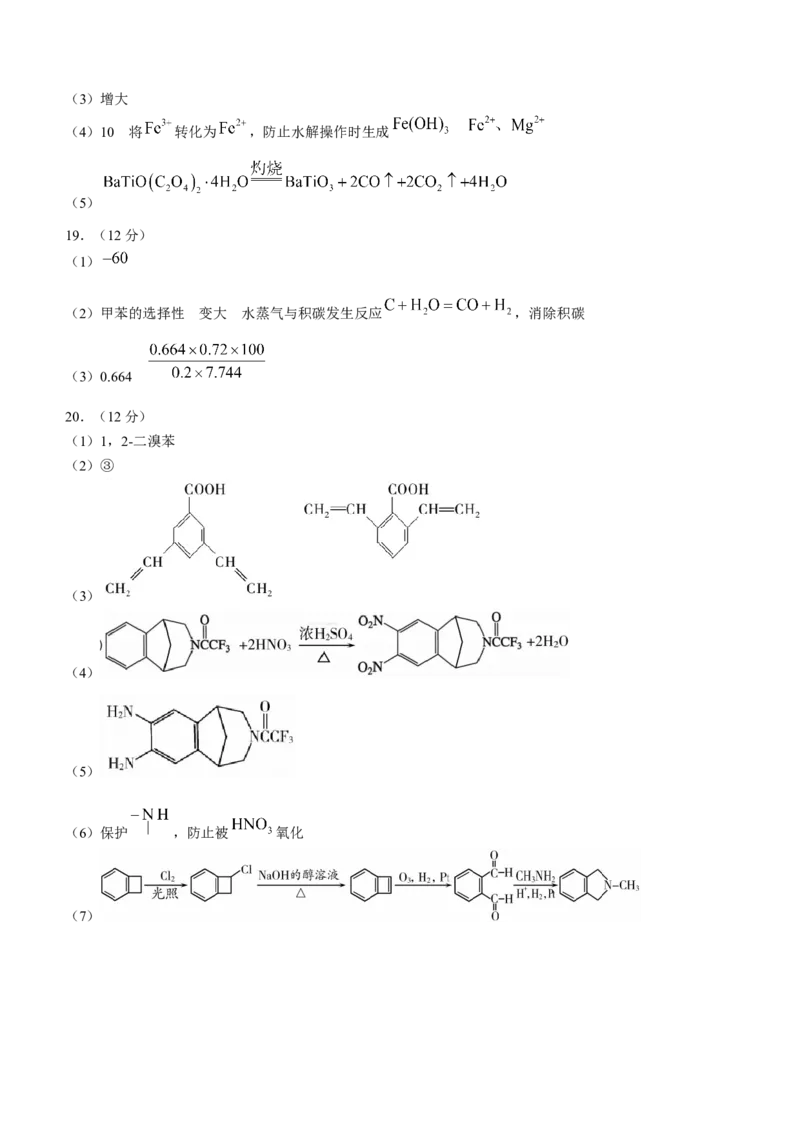
20.(12分)伐尼克兰是戒烟药的主要成分,其合成路线分为Ⅰ和Ⅱ两个阶段。回答下列问题:
已知:
阶段Ⅰ:
学科网(北京)股份有限公司(1)A的化学名称为________(用系统命名法命名)。
(2)·反应①-④中,属于加成反应的是________(填序号)。
(3)符合下列条件的E的同分异构体的结构简式为________.
a.含有5种不同化学环境的H,H原子的个数比为1∶1∶2∶2∶4
b.分子内含有苯环,能与 溶液反应产生气泡
阶段Ⅱ:
(4)H→I的化学方程式为________。
(5)J的结构简式为________。
(6)反应⑦和⑪的作用是________。
(7)根据上述信息,写出以 为主要原料制备 的合成路线(其他试剂任选):
________。
学科网(北京)股份有限公司高三化学参考答案及评分标准
2024.3
说明:1.本答案供阅卷评分使用,考生若写出其它正确答案,可参照评分标准给分。
2.化学专用名词中出现错别字、元素符号有错误,书写不规范,都不得分。
3.化学方程式、离子方程式不按要求书写、未配平都不得分。漏掉或写错反应条件扣1分。漏
掉↑、↓不扣分。
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.A 2.D 3.A 4.D 5.C 6.C 7.C 8.B 9.D 10.D
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全都
选对得4分,选对但不全的得2分,有选错的得0分。
11.C 12.AC 13.AD 14.BC 15.BD
三、非选择题:本题共5小题,共60分。
16.(12分)
(1)
(2) 中心硼原子为 杂化, 有一条未杂化的 轨道与三个 原子的 轨道重
叠,生成大 键 ,从而使 键长远比 和 的半径之和小
(3) ab
6 2
(4)
17.(12分)
(1)加热管式炉至一定温度
(2)测量装置内压强,防止压力过大,超压时可作为安全阀
或 排尽装置内残留的 蒸馏
(3) BD
18.(12分)
(1)
(2)碱浸
学科网(北京)股份有限公司(3)增大
(4)10 将 转化为 ,防止水解操作时生成
(5)
19.(12分)
(1)
(2)甲苯的选择性 变大 水蒸气与积碳发生反应 ,消除积碳
(3)0.664
20.(12分)
(1)1,2-二溴苯
(2)③
(3)
(4)
(5)
(6)保护 ,防止被 氧化
(7)
学科网(北京)股份有限公司