文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第1课时 分子结构的测定和多样性 价层电子对互斥模型
培优第一阶——基础过关练
1.(2022·云南省石屏县第一中学高二阶段练习)下列分子或离子中,中心原子含有孤电子对的是
A.PCl B.NO C.SiCl D.PbCl
5 4 2
【答案】D
【分析】分子中孤电子对个数= (中心原子价电子数-配原子个数×配原子形成稳定结构需要的电子数),
阳离子中孤电子对个数= (中心原子价电子数-电荷数-配原子个数×配原子形成稳定结构需要的电子数),
阴离子中孤电子对个数= (中心原子价电子数+电荷数-配原子个数×配原子形成稳定结构需要的电子数),
以此解答。
【详解】A.PCl 中心原子碳原子孤电子对个数= (5-5×1)=0,没有孤对电子,故A不选;
5
B.NO 中心原子碳原子孤电子对个数= (5+1-3×2)=0,没有孤对电子,故B不选;
C.SiCl 中心原子碳原子孤电子对个数= (4-4×1)=0,没有孤对电子,故C不选;
4
D.PbCl 中心原子碳原子孤电子对个数= (4-2×1)=1,有孤对电子,故D选;
2
故选D。
2.(2022·海南·儋州川绵中学高二阶段练习)下列分子的中心原子的价层电子对数是3的是
A. B. C. D.
【答案】B
【详解】水分子中氧原子、甲烷分子中碳原子和氨分子中氮原子的价层电子对数都为4,三氟化硼分子中
硼原子的价层电子对数为3,故选B。
3.(2022·北京石景山·高二期末)下列化学用语或图示表达正确的是
A.NaCl的电子式 B.SO 的VSEPR模型
2
C.p-p σ键电子云轮廓图 D.NO 的空间结构模型
【答案】D
【详解】A.氯化钠是离子化合物,由钠离子与氯离子构成,氯化钠的电子式为 ,故A错
误;B.SO 的价层电子数为 =3,含有1对孤电子对,其VSEPR模型为 ,故B错误;
2
C.p-pσ键电子云以“头碰头”方式形成,其电子云轮廓图为 , 是p-pπ键电
子云模型,故C错误;
D.CO 的价层电子数为 =3,无孤电子对,其VSEPR模型和空间构型均为平面三角形,即
,故D正确;
故选D。
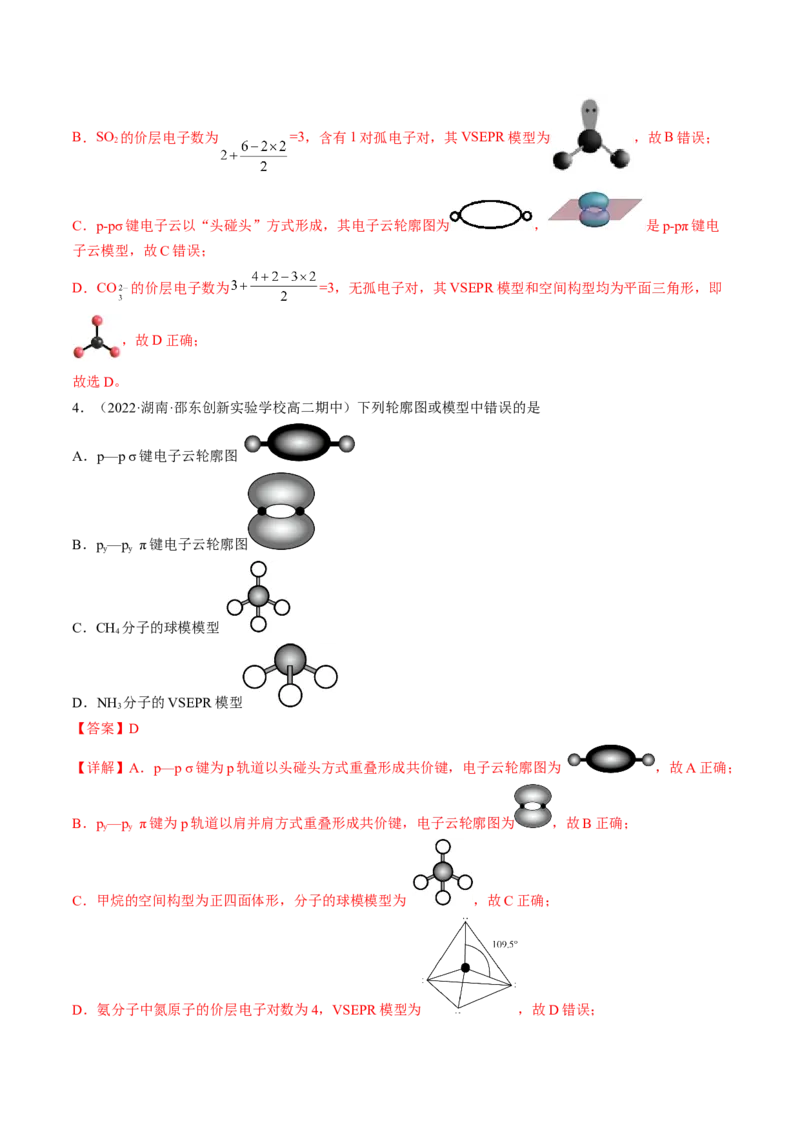
4.(2022·湖南·邵东创新实验学校高二期中)下列轮廓图或模型中错误的是
A.p—p σ键电子云轮廓图
B.p—p π键电子云轮廓图
y y
C.CH 分子的球模模型
4
D.NH 分子的VSEPR模型
3
【答案】D
【详解】A.p—p σ键为p轨道以头碰头方式重叠形成共价键,电子云轮廓图为 ,故A正确;
B.p—p π键为p轨道以肩并肩方式重叠形成共价键,电子云轮廓图为 ,故B正确;
y y
C.甲烷的空间构型为正四面体形,分子的球模模型为 ,故C正确;
D.氨分子中氮原子的价层电子对数为4,VSEPR模型为 ,故D错误;故选D。
5.(2022·浙江·高二期末)下列有关分子空间结构的说法正确的是
A.HClO、BF、NCl 分子中所有原子的最外层电子都满足了8电子稳定结构
3 3
B.P 和CCl 都是正四面体形分子且键角都为109°28′
4 4
C.分子中键角的大小:BeCl >SO>NH>CCl
2 3 3 4
D.BeF 分子中,中心原子Be的价层电子对数等于2,其空间结构为直线形,成键电子对数等于2,没有
2
孤电子对
【答案】D
【详解】A.HClO中H原子的最外层电子数为1+1=2,不满足8电子稳定结构,BF 中B元素化合价为
3
+3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构;F元素化合价为−1,F原子最外
层电子数为7,所以1+7=8,F原子满足8电子结构,NCl 中P元素化合价为+3,N原子最外层电子数
3
为5,所以3+5=8,N原子满足8电子结构;Cl元素化合价为−1,Cl原子最外层电子数为7,所以1+7
=8,Cl原子满足8电子结构,故A错误;
B.P 是四原子的正四面体,键角是60°,而CH 是五原子的正四面体键角都为109°28′,故B错误;
4 4
C.BeCl 中Be形成2个σ键,无孤电子对,为sp杂化,键角为180°;SO 中S原子是sp2杂化,分子为平
2 3
面正三角形构型,键角为120°;NH 中N形成3个σ键,孤电子对数= ,为sp3杂化,为三角锥
3
形,键角大约为107°;CCl 中C形成4个σ键,无孤电子对,为sp3杂化,为正四面体,键角为109°28′,
4
分子中键角的大小:BeCl >SO >CCl >NH ,故C错误;
2 3 4 3
D.BeF 分子中,铍原子含有两个共价单键,不含孤电子对,所以价层电子对数是2,中心原子以sp杂化
2
轨道成键,价层电子对个数是2且不含孤电子对,为直线形结构,故D正确;
故答案选D。
6.(2022·北京市第十二中学高二阶段练习)下列各组微粒的空间结构相似的是
A. 与 B. 与 C. 与 D. 与
【答案】A
【详解】A.SO 分子中S原子价层电子对数=2+ =3且含有1个孤电子对,则SO 的空间结构为V
2 2
形,O 与SO 互为等电子体,空间结构相似,均为V形,故A正确;
3 2
B.CO 中C原子价层电子对数=2+ =2且不含孤电子对,为直线形结构,NO 分子中N原子价层电
2 2
子对数=2+ =3且含有1个孤电子对,则NO 的空间结构为V形,故B错误;
2
C. 中心原子N的价层电子对数为3+ =3,无孤电子对,其空间结构为平面三角形, 中
S原子价层电子对数=3+ =3且含有1个孤电子对,空间结构为三角锥形,故C错误;D.PCl 中心原子价层电子对数为: =4,有1对孤电子对,为三角锥形结构,PCl 的价电子对数为:
3 5
5+ =5,不含有孤电子对,其分子的空间构型为三角双锥形,故D错误;
故选:A。
7.(2022·陕西西安·高二期末)下列微粒的空间结构与其 模型不一致的是
A.SO B.BF C.CH D.NH
2 3 4
【答案】A
【分析】当中心原子上有孤电子对时,微粒的空间结构与其VSEPR模型不一致,据此分析解答。
【详解】A.SO 的价层电子对数= ,含1对孤电子对,VSEPR模型为平面三角形,其空间
2
构型为V形,故A正确;
B.BF 的价层电子对数= ,无孤电子对,VSEPR模型和其空间构型均为平面三角形,故B
3
错误;
C.CH 的价层电子对数= ,无孤电子对,VSEPR模型和其空间构型均为正四面体,故C错
4
误;
D. 的价层电子对数= ,无孤电子对,V SEPR模型和其空间构型均为正四面体,故D
错误;
故答案选A。
8.(2022·山西运城·高二期末)经过X射线衍射实验等发现, 中存在 离子,下列粒子的VSEPR
模型与空间结构都与 相同的是
A. B. C. D.
【答案】C
【分析】 可以看作I·I ,价层电子对数为2+ =4,VSEPR模型为四面体形,空间构型为V形,
据此分析;
【详解】 的VSEPR模型为四面体形,空间构型为V形;
A.SO 的价层电子对数为2+ =3,VSEPR模型为平面三角形,空间构型为V形,与 不符,故A
2
不符合题意;
B.O 可以看作O·O ,价层电子对数为2+ =3,VSEPR模型为平面三角形,空间构型为V形,与
3 2
不符,故B不符合题意;C.OF 的价层电子对数为2+ =4,VSEPR模型为四面体形,空间构型为V形,与 相符,故C符
2
合题意;
D.NH 的价层电子对数为3+ =4,VSEPR模型为四面体形,空间构型为三角锥形,与 不符,故
3
D不符合题意;
答案为C。
9.(2022·新疆·乌苏市第一中学高二阶段练习)下列分子构型为正四面体且键角为109°28′的是
①P ②NH ③CCl ④CH ⑤HS ⑥CO
4 3 4 4 2 2
A.③④ B.⑤⑥ C.①③④ D.②③④
【答案】A
【详解】①P 分子构型为正四面体、键角为60°;
4
②NH 分子中的氮原子sp3杂化,有一个杂化轨道容纳弧对电子对,所以构型为三角锥;
3
③CCl 分子中碳原子sp3杂化,没有弧对电子对,所以构型为正四面体且键角为109°28′;
4
④CH 分子中碳原子sp3杂化,没有弧对电子对,所以构型为正四面体且键角为109°28′;
4
⑤HS分子中硫原子sp3杂化,有两对弧对电子对,所以构型为V形;
2
⑥CO 分子中碳原子sp杂化,所以构型为直线形,
2
所以③④正确,答案选A。
10.(2022·河南开封·高二阶段练习)关于价层电子对互斥理论说法错误的是
A.价层电子对包括σ键电子对和中心原子上的孤电子对
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测HS和BF 的空间结构为V形和平面三角形
2 3
D.该理论一定能预测出多中心原子的分子、离子或原子团的空间构型
【答案】D
【详解】A.价层电子对包括σ键电子对和中心原子上的孤电子对,不包含π键中的电子对,A正确;
B.分子中键角越大,价层电子对之间的距离越小,相互排斥力越小,则分子越稳定,B正确;
C.HS中S原子价层电子对数为:2+ =4,且含有2个孤电子对,分子呈V形结构;BF 中B原子价
2 3
层电子对数为:3+ =3,且不含孤电子对,分子呈平面三角形结构,C正确;
D.该理论不能预测所有分子或离子的空间构型,如:许多过渡金属化合物的几何构型不能用VSEPR模型
理论解释,D错误;
故合理选项是D。
11.(2021·湖北·华中师范大学潜江附属中学高二阶段练习)下列各组粒子的空间结构相同的是
①NH 和HO;②NH 和HO+;③NH 和HO+;④O 和SO ;⑤CO 和BeCl 。
3 2 3 3 3 3 2 2 2
A.全部 B.①②③⑤ C.③④⑤ D.②⑤【答案】C
【分析】根据价层电子对互斥理论确定微粒空间构型,价层电子对个数=σ键+孤电子对个数,孤电子对个
数= ×(a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子
最多能接受的电子数。
【详解】①NH 中价层电子对个数=3+ ×(5-3)=4且含有一个孤电子对,所以为三角锥形,HO中价层
3 2
电子对个数=2+ ×(6-2)=4且含有两个孤电子对,所以为V形结构,二者空间构型不同,故①错误;
②NH +中价层电子对个数是4且不含孤电子对,为正四面体形结构;HO+中O原子价层电子对个数=3+
4 3
(6-1-3×1)=4且含有一个孤电子对,所以为三角锥形结构,二者空间构型不同,故②错误;
③NH 为三角锥形结构、HO+中O原子价层电子对个数=3+ (6-1-3×1)=4且含有一个孤电子对,所以为
3 3
三角锥形结构,所以二者空间构型相同,故③正确;
④O、SO 中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故④正确;
3 2
⑤CO 分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+ (4-2×2)=2,二氧化碳是直线型结构,
2
BeCl 分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+ (2-2×1)=2,BeCl 是直线型结构,
2 2
CO 和BeCl 分子都是直线型分子,故⑤正确;
2 2
答案选C。
培优第二阶——拓展培优练
12.(2022·重庆市江津第五中学校高二期中)下列说法中正确的是
A.NO 、SO 、BF、NCl 分子中每原子的最外层电子都满足了8电子稳定结构
2 2 3 3
B.P 和CH 都是正四面体形分子且键角都为109°28′
4 4
C.NH 的电子式为 ,离子呈平面正方形结构
D.NH 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
3
【答案】D
【详解】A.BF 分子的电子式为 其中B原子未满足8电子稳定结构,A错误;
3
B.P 为正四面体分子,但其键角为60°,B错误;
4
C. 有4对价层电子对数,无孤对电子对数,则其为正四面体结构而非平面正方形结构,C错误;D.NH 分子电子式为 ,有一对未成键电子,由于未成键电子对成键电子的排斥作用较强,使
3
其键角为107°,呈三角锥形,D正确;
故选D。
13.(2022·新疆石河子一中高二阶段练习)下列粒子的VSEPR模型为四面体、且其空间结构为V形的是
A. B. C. D.SF
2
【答案】D
【详解】A.二氧化硫分子中硫原子的价层电子对数为3,VSEPR模型为平面三角形,孤对电子对数为1,
分子的空间结构为V形,故A错误;
B.甲烷分子中碳原子的价层电子对数4,VSEPR模型为正四面体形,孤对电子对数为0,分子的空间结构
为正四面体形,故B错误;
C.水合氢离子中氧原子的价层电子对数为4,VSEPR模型为四面体形,孤对电子对数为1,分子的空间结
构为三角锥形,故C错误;
D.二氟化硫分子中硫原子的价层电子对数为4,VSEPR模型为四面体形,孤对电子对数为2,分子的空间
结构为V形,故D正确;
故选D。
14.(2022·宁夏·贺兰县景博中学高二阶段练习)下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
【答案】B
【详解】A.亚硫酸根离子中硫原子的价层电子对数为4,孤对电子对数为1,离子的VSEPR模型为正四
面体形,空间结构为三角锥形,所以离子的空间结构模型与空间结构不一致,故A错误;
B.高氯酸根离子中氯原子的价层电子对数为4,孤对电子对数为0,离子的VSEPR模型和空间结构都为
正四面体形,所以离子的空间结构模型与空间结构一致,故B正确;
C.亚硝酸根离子中氮原子的价层电子对数为3,孤对电子对数为1,离子的VSEPR模型为三角锥形,空
间结构为V形,所以离子的空间结构模型与空间结构不一致,故C错误;
D.氯酸根离子中氯原子的价层电子对数为4,孤对电子对数为1,离子的VSEPR模型为正四面体形,空
间结构为三角锥形,所以离子的空间结构模型与空间结构不一致,故D错误;
故选B。
15.(2022·云南省石屏县第一中学高二阶段练习)用VSEPR模型预测下列分子或离子的立体结构,其中
正确的是
A.CH 与CHCl 均为正四面体 B.BeCl 与SO 为直线形
4 2 2 2 2
C.BF 与PCl 为三角锥形 D.NO 与CO 为平面三角形
3 3
【答案】D
【详解】A.CH 分子中价层电子对个数= ,采用sp3杂化,不含孤电子对,所以其空间
4构型为正四面体,CHCl 分子中价层电子对个数= ,采用sp3杂化,不含孤电子对,有H
2 2
和Cl,所以其空间构型为四面体,A错误;
B.BeCl 分子中价层电子对个数= ,采用sp杂化,且不含孤电子对,所以其空间构型为
2
直线型结构,SO 分子中价层电子对个数= ,采用sp2杂化,含1个孤电子对,所以其空
2
间构型为V形结构,B错误;
C.BF 分子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,所以其空间构型为平
3
面三角形结构,PCl 分子中价层电子对个数= ,采用sp3杂化,且含1个孤电子对,所以
3
其空间构型为三角锥形结构,C错误;
D. 离子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,所以其空间构型
为平面三角形结构, 离子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,
所以其空间构型为平面三角形结构,D正确;
故选D。
16.(2022·山东枣庄·高二期末)下列分子或离子中,键角由大到小排列正确的是
① ②NH ③HO④BF ⑤CO
3 2 3 2
A.⑤④①②③ B.⑤①④②③
C.④①②⑤③ D.③②④①⑤
【答案】A
【详解】① 为正四面体,键角为109°28′;
②NH 分子中N原子价层电子对个数是4且含有一个孤电子对,其空间构型是三角锥形,键角约为107°;
3
③HO为V形,键角约为105°;
2
④BF 中心原子的价电子都用来形成共价键,所以价层电子对数为3,为平面三角形,键角为120°;
3
⑤CO 中心原子的价电子都用来形成共价键,所以价层电子对数为2,为直线形,键角为180°;
2
所以键角由大到小排列顺序是⑤④①②③;故选:A。
17.(2022·浙江·湖州市教育科学研究中心高二期末)我国科学家成功合成了世界上首个五氮阴离子盐
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结
构角度分析,R中两种阳离子不同之处为A.电子总数 B.中心原子的价层电子对数
C.空间结构 D.共价键类型
【答案】C
【分析】R中两种阳离子分别是HO+和 。
3
【详解】A.HO+和 均含有10个电子,A不符合题意;
3
B.HO+的中心原子O的价电子对数为3+ =3+1=4, 的中心原子N的价电子对数为4+
3
=4+0=4,即两种离子的中心原子的价层电子对数相同,B不符合题意;
C.由B选项可知,HO+的中心原子O的价电子对数为4,采取sp3杂化,含有1个孤电子对,其空间构型
3
为三角锥形, 的中心原子N的价电子对数为4+ =4+0=4,采取sp3杂化,无孤电子对,其空间
构型为正四面体形,即两种离子的空间结构不同,C符合题意;
D.HO+和 都含有极性共价键,D不符合题意;
3
故选C。
18.(2022·北京市第三十九中学高二期中)下列粒子的VSEPR模型为四面体且其空间结构为V形的是
A.SO B.SO C.HO+ D.OF
2 3 2
【答案】D
【详解】A.SO 中S原子价电子对数为 ,有1个孤电子对,VSEPR模型为平面结构,其空间结构为
2
V形,故不选A;
B.SO 中S原子价电子对数为 ,无孤电子对,VSEPR模型为四面体,其空间结构为正四面体,
故不选B;
C.HO+中O原子价电子对数为 ,有1个孤电子对,VSEPR模型为四面体,其空间结构为三角
3
锥,故不选C;
D.OF 中O原子价电子对数为 ,有2个孤电子对,VSEPR模型为平四面体,其空间结构为V形,
2
故选D;
选D。19.(2022·河南·平顶山市龙河实验高级中学高二期中)计算HO、NH 、SO 、NH 、CO 分子的孤电子
2 3 3
对数。
分子或离子 中心原子 a x b 中心原子数的孤电子对数
___ ___
HO ____ ____ ____
2
_ _
___ ___
NH ____ ____ ____
3
_ _
___ ___
SO ____ ____ ____
3
_ _
___ ___
____ ____ ____
NH
_ _
___ ___
____ ____ ____
CO
_ _
【答案】
O 6 2 2 2 N 5 3 1 1 S 6 3 2 0 N 4 4 1 0 C 6
3 2 0
20.(2021·河北石家庄·高二阶段练习)有以下物质:①HF;②Br ;③HO;④N;⑤C H;⑥C H;
2 2 2 2 4 2 6
⑦H;⑧HO;⑨HCHO
2 2 2
(1)只含有σ键的是___________(填序号,下同);既含有σ键又含有π键的是___________。
(2)含有由两个原子的s轨道重叠形成σ键的物质是___________。
(3)写出以下分子或离子的空间构型:
NH :___________,HO:___________,SiH:___________,BeCl :___________,CO:
3 2 4 2 2
___________。
【答案】 ①②③⑥⑦⑧ ④⑤⑨ ⑦ 三角锥形 V形
正四面体形 直线形 直线形
【详解】(1)以上物质的结构式依次为:①H—F,②Br—Br,③H—O—H,④N≡N,⑤ ,⑥
,⑦H—H,⑧H—O—O—H,⑨ ,单键为σ键,双键含1个σ键,1个π键,三
键含1个σ键,2个π键,故只含有σ键的是:①②③⑥⑦⑧,既含有σ键又含有π键的是:④⑤⑨;
(2)氢原子价电子位于1s能级上,故H 中共价键由两个氢原子的s轨道重叠而成,故此处填⑦;
2
(3)NH 的中心原子N的价层电子对数= ,根据价层电子对互斥理论知NH VSEPR模型为四面
3 3体形,由于中心N原子含有1对孤电子对,故NH 的实际构型为三角锥形;
3
HO的中心原子O的价层电子对数= ,根据价层电子对互斥理论知HO VSEPR模型为四面体形,
2 2
由于中心O原子含有2对孤电子对,故HO的实际构型为V形;
2
SiH 的中心原子Si的价层电子对数= ,根据价层电子对互斥理论知SiH 空间构型为正四面体形;
4 4
BeCl 的中心原子Be的价层电子对数= ,根据价层电子对互斥理论知BeCl 空间构型为直线形;
2 2
CO 的中心原子C的价层电子对数= ,根据价层电子对互斥理论知CO 空间构型为直线形。
2 2
21.(2021·宁夏·贺兰县景博中学高二期中)用价层电子对互斥模型推测下列分子或离子的空间构型。
(1)BeCl ___________;
2
(2)SO ___________;
(3)SCl ___________;
2
(4)BF ___________;
3
(5)PF ___________;
3
(6)NH ___________;
【答案】 直线形 正四面体形 V形 平面三角形 三角锥
形 正四面体形
【详解】(1)BeCl 中心原子的价层电子对数为 =2,孤电子对数为0,为直线形;
2
(2)SO 中心原子的价层电子对数为 =4,孤电子对数为0,为正四面体形;
(3)SCl 中心原子的价层电子对数为 =4,孤电子对数为2,为V形;
2
(4)BF 中心原子的价层电子对数为 =3,孤电子对数为0,为平面三角形;
3
(5)PF 中心原子的价层电子对数为 =4,孤电子对数为1,为三角锥形;
3
(6)NH 中心原子的价层电子对数为 =4,孤电子对数为0,为正四面体形;
22.(2022·吉林·抚松县第一中学高二开学考试)在 分子中
(1) 的价层电子对的空间构型为___________
(2)以极性键相结合,具有正四面体结构的分子是___________
(3)以极性键相结合,具有三角锥型结构的分子是___________
(4)以极性键相结合,具有V型结构的分子是___________
(5)以极性键相结合,而且共价键的极性最大的是___________【答案】(1)平面正三角形
(2)
(3)
(4)
(5)
【分析】根据价层电子对理论及杂化轨道理论进行计算价层电子对数和孤对电子对数从而判断分子的空间
构型。
(1)
根据价层电子对理论价层电子对数为3+ =3,采用sp2杂化,无孤对电子,故空间构型为平面正
三角形。
(2)
极性键判断非金属元素不同,根据杂化轨道理论判断,正四面结构的分子是CH。
4
(3)
极性键判断非金属元素不同,根据杂化轨道理论判断,三角锥结构的分子是NH 。
3
(4)
极性键判断非金属元素不同,根据杂化轨道理论判断,V型结构的分子是HO。
2
(5)
极性键判断非金属元素不同,共价键极性最大,即非金属元素的电负性相差大,故应是HF。
【点睛】利用键的极性判断元素种类,根据分子的空间构型判断方法计算价层电子对数和孤对电子数来判
断分子的空间构型。
23.(2021·河北·邢台一中高二阶段练习)短周期元素A、B、C、D原子序数依次增大,且C元素最高价
氧化物对应的水化物在水溶液中能电离出电子数相等的阴、阳离子。A、C位于同一主族,A为非金属元
素,B的最外层电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。E单
质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。请回答下列问题:
(1)基态D原子的价电子轨道表示式___________________________。
(2)由上述A、B、D三种元素形成的ADB分子中存在的 键分别称为_________。
(3)B、D两种元素可形成多种阴离子,如 、 、 等,这三种阴离子的空间结构分别为
______________________。比较 和 的键角大小并说明理由:_______________________。
(4)E元素原子基态时电子所占据的轨道个数为:_________;试分析 具有较强还原性的原因
___________________________。
【答案】(1)
(2)s-p 键p-p 键
(3) V形、三角锥形、正四面体形 , 和 的VSEPR模型均为四面体形,而中存在孤电子对,孤电子对有较大的斥力(孤电子对与成键电子对间的斥力大于成键电子对间的斥
力)
(4) 15 的价电子为 ,易失去一个电子形成较稳定的半充满结构
【分析】短周期元素A、B、C、D原子序数依次增大;C元素最高价氧化物对应的水化物在水溶液中能电
离出电子数相等的阴、阳离子,C是Na元素;A、C位于同一主族,A为非金属元素,A是H元素;B的
最外层电子数是次外层电子数的3倍,B是 O元素;B、C的最外层电子数之和与D的最外层电子数相等,
D是Cl元素;E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏,E是Fe元素。
(1)
D是Cl元素,核外有17个电子,基态Cl原子的价电子排布式3s 2 3p 5,价电子轨道表示式
。
(2)
由H、O、Cl三种元素形成HClO分子的结构式为H-O-Cl,存在的 键分别称为s-p 键p-p 键。
(3)
中Cl原子杂化轨道数为 ,孤电子对数是2,所以空间构型为V形; 中Cl原子杂化轨道数
为 ,孤电子对数是1,所以空间构型为三角锥形; 中Cl原子杂化轨道数为 ,孤电子对
数是0,所以空间构型为正四面体形; 和 的VSEPR模型均为四面体形,而 中存在孤电子对,
孤电子对有较大的斥力,所以键角 < 。
(4)
E是Fe元素,Fe原子基态时电子排布式为1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2,电子所占据的轨道个数为
15; 的价电子为 ,易失去一个电子形成较稳定的半充满结构 ,所以 具有较强还原性。