文档内容
2023学年宝山区高三年级化学学科
等级考第二次模拟考试
考生注意:
1.本试卷满分100分,考试时间60分钟。
2.答题前,考生务必将自己的学校、班级、姓名、准考证号填写清楚,并将条形码粘贴在
规定位置。
3.本试卷设试卷和答题纸两部分,试卷包括试题与答题要求;所有答案必须涂或写在答题
纸上;做在试卷上一律不得分。答题纸与试卷在试题编号上是一一对应的,答题时应特
别注意,不能错位。
4.选择类试题中,标注“不定项”的试题,每小题有1~2个正确选项,只有1个正确选项
的,多选不给分,有2个正确选项的,漏选一个给一半分,错选不给分;未特别标注
的试题,每小题只有一个正确选项。
相对原子质量:H-1 O-16 S-32 Cu-64 Ni-59 K-39 Cl-35.5
一、大气污染及治理
大气污染物的主要成分是SO 、NO 、NO、CO及可吸入颗粒等,其主要来自于燃煤、
2 2
机动车尾气和工业废气,会导致雾霾、酸雨等。
1. 下列物质,能吸收SO 同时得到化肥的是________。
2
A. 碱石灰 B. 酸性KMnO 溶液 C. 氨水 D. 浓HSO
4 2 4
2. 硫及其部分化合物的“价-类”二维图如下图所示,下列说法正确的是____。(不定项)
A. X可与SO 反应生成S B. Y可由S和O 化合生成
2 2
C. Z的水溶液一定呈碱性 D. 不能用浓硫酸干燥SO
2
3. 某工厂采用(NH )SO 和 NH HSO 的混合溶液 A 吸收废气中的 SO 并制备
4 2 3 4 3 2
(NH )SO ·H O,过程如下图所示:
4 2 3 2
“吸收”过程中,溶液中(NH )SO 和NH HSO 物质的量之比________。
4 2 3 4 3
A. 变大 B. 变小 C. 不变“ 制 备 ” 过 程 中 , 溶 液 B 中 发 生 反 应 的 化 学 方 程 式 为
________________________________。
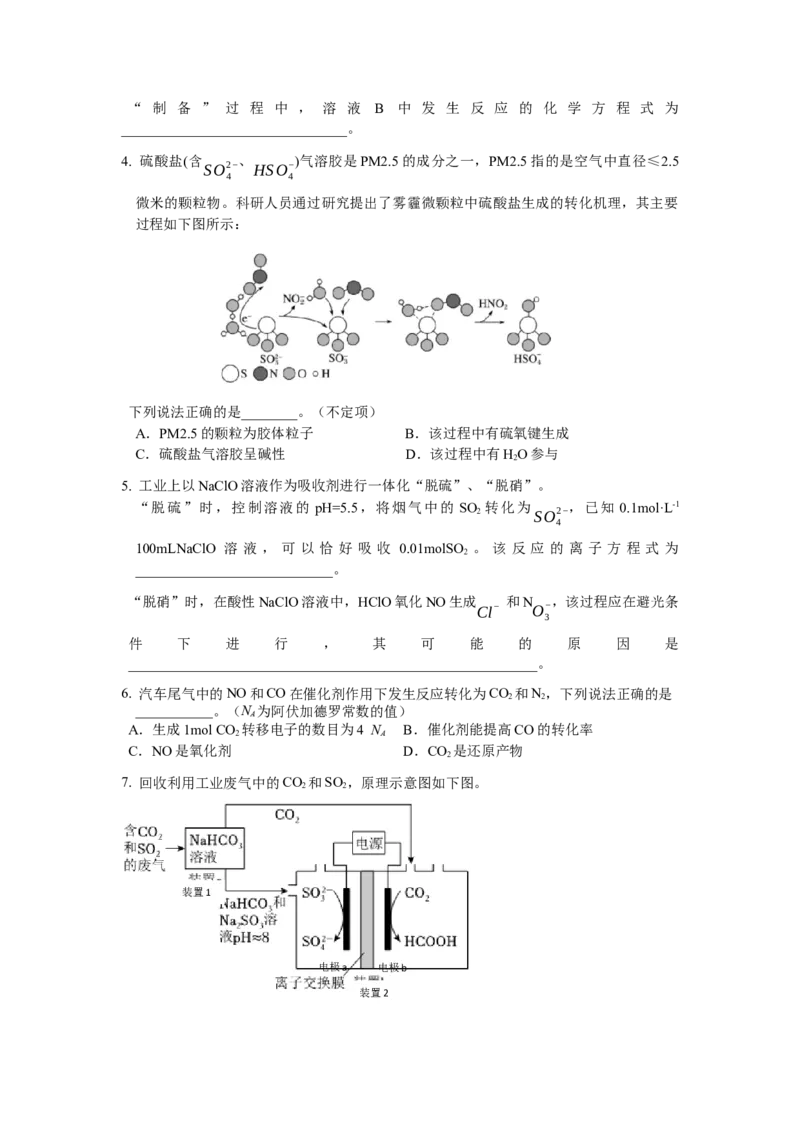
4. 硫酸盐(含 、 )气溶胶是PM2.5的成分之一,PM2.5指的是空气中直径≤2.5
SO2− HSO−
4 4
微米的颗粒物。科研人员通过研究提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要
过程如下图所示:
下列说法正确的是________。(不定项)
A.PM2.5的颗粒为胶体粒子 B.该过程中有硫氧键生成
C.硫酸盐气溶胶呈碱性 D.该过程中有HO参与
2
5. 工业上以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。
“脱硫”时,控制溶液的 pH=5.5,将烟气中的 SO 转化为 ,已知 0.1mol·L-1
2 SO2−
4
100mLNaClO 溶 液 , 可 以 恰 好 吸 收 0.01molSO 。 该 反 应 的 离 子 方 程 式 为
2
____________________________。
“脱硝”时,在酸性NaClO溶液中,HClO氧化NO生成 和N ,该过程应在避光条
Cl− O−
3
件 下 进 行 , 其 可 能 的 原 因 是
__________________________________________________________。
6. 汽车尾气中的NO和CO在催化剂作用下发生反应转化为CO 和N,下列说法正确的是
2 2
___________。(N 为阿伏加德罗常数的值)
A
A.生成1mol CO 转移电子的数目为4 N B.催化剂能提高CO的转化率
2 A
C.NO是氧化剂 D.CO 是还原产物
2
7. 回收利用工业废气中的CO 和SO,原理示意图如下图。
2 2
装置1
电极a 电极b
装置2下列说法正确的是_______。
A. 废气中CO 排放到大气中会形成酸雨
2
B. 装置 中溶液显碱性的原因是 的水解程度大于 的电离程度
1 HCO− HCO−
3 3
C. 装置1中溶液的作用是吸收废气中的CO 和SO
2 2
D. 装置2中电极b和电源的正极相连
写出装置2中电极a的反应式___________________________________________。
二、硅材料
硅材料在生活中占有重要地位。
8.太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为_________。
单晶硅的晶体类型为____________。
A. 离子晶体 B. 分子晶体 C. 共价晶体 D. 金属晶体
9.由硅原子核形成的三种微粒,电子排布式分别为:① 、② 、
③ ,有关这些微粒的叙述,正确的是___________。(不定项)
A.得电子能力:①>②
B.微粒半径:③>①>②
C.电离一个电子所需最低能量:①>②>③
D.电子排布属于基态原子(或离子)的是:①②
10.硅和卤素单质反应可以得到 , 的熔沸点如下表:
熔点/℃ -90.0 -69.8 5.6 120.7
沸点/℃ -85.8 57.8 154.2 287.7
(1)气态 分子的空间构型是___________。
A. 正四面体形 B. 三角锥形 C. 角形 D. 直线形
(2)0℃ 时, 、 、 、 呈液态的是___________。
A. B. C. D.
(3)比较上述 的熔沸点,分析其变化规律及原因____________________________。
( 4) 与N-甲基咪唑 反
应 可以得到 ,其结构如下图所示:N-甲基咪唑分子中碳原子的杂化轨道类型为_________________。
11.硅合金具有良好的性能。
(1)下列关于合金的说法错误的是______。
A. 熔点高于组成金属 B. 可能含有非金属
C. 硬度通常比组成金属大 D. 一般比单一金属用途更广
(2)白铜是我国使用最早的合金之一,白铜晶胞结构如右图所示(Cu位于面心),
该晶胞含有的Cu原子和Ni原子个数分别为______、_____。
已知晶体密度为d g·cm-3,设N 为阿伏加德罗常数的值。
A
Ni和Ni之间的最短距离为_____________ nm。
三、储氢载体——NH
3
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。通过氨热分解法
制取氢气,其反应的化学方程式如下:
12. 根据下表数据,写出氨热分解法的热化学方程式_______________________________。
相关化学键的键能数据
化学键 N N HH NH
键能E / (kJ·mol-1) 946 436.0 390.8
13. 已知该反应的∆S=198.9×10-3 kJ·mol-1·K-1,判断在300℃时反应是否能自发进行
_____(填“是”或“否”),理由是___________________________________________。
14. 在一定温度和催化剂的条件下,将0.1mol NH 通入3L的密闭容器中进行反应(此时容
3
器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。
(1)若保持容器体积不变,t 时反应达到平衡,
1
2.0 用H 的浓度变化表示0~t 时间内的反应速率
2 1
v(H )=_______mol·L-1·min-1(用含 t 的代数式
1.6 2 1
表示)
1.2
t
(2) 时将容器体积迅速缩小至原来的一半并保
a 2
0.8 b 持不变,图中能正确表示压缩后N 2 分压
c
变化
0.4
d 趋势的曲线是_______(用图中a、b、c、d
0 表
t t
1 2 示),理由是
t/min
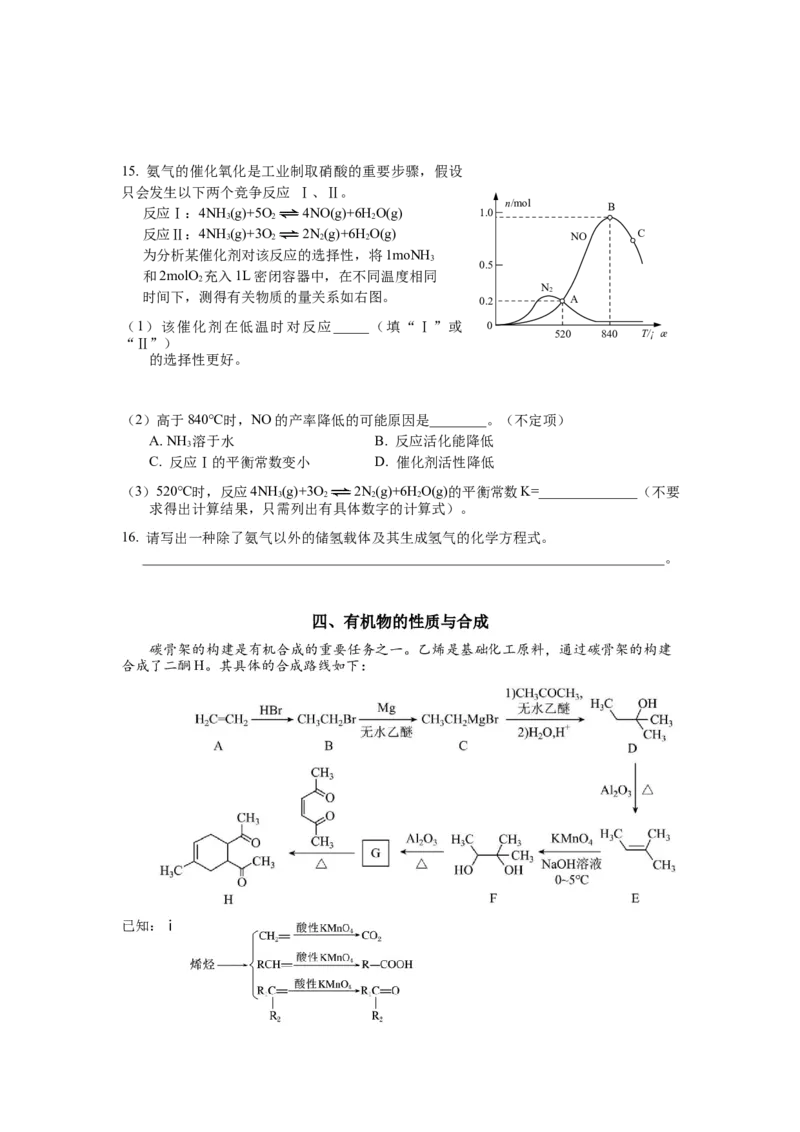
__________________________。15. 氨气的催化氧化是工业制取硝酸的重要步骤,假设
只会发生以下两个竞争反应 Ⅰ、Ⅱ。
n/mol
反应Ⅰ:4NH (g)+5O 4NO(g)+6H O(g) 1.0 B
3 2 2
反应Ⅱ:4NH 3 (g)+3O 2 2N 2 (g)+6H 2 O(g) NO C
为分析某催化剂对该反应的选择性,将1moNH
3
0.5
和2molO 充入1L密闭容器中,在不同温度相同
2
时间下,测得有关物质的量关系如右图。
N2
0.2 A
(1)该催化剂在低温时对反应_____(填“Ⅰ”或 0
520 840 T/¡ æ
“Ⅱ”)
的选择性更好。
(2)高于840℃时,NO的产率降低的可能原因是________。(不定项)
A. NH 溶于水 B. 反应活化能降低
3
C. 反应Ⅰ的平衡常数变小 D. 催化剂活性降低
(3)520℃时,反应4NH (g)+3O 2N(g)+6HO(g)的平衡常数K=______________(不要
3 2 2 2
求得出计算结果,只需列出有具体数字的计算式)。
16. 请写出一种除了氨气以外的储氢载体及其生成氢气的化学方程式。
__________________________________________________________________________。
四、有机物的性质与合成
碳骨架的构建是有机合成的重要任务之一。乙烯是基础化工原料,通过碳骨架的构建
合成了二酮H。其具体的合成路线如下:
已知:ⅰii
17. H中含有的含氧官能团是__________________。
D→E的反应类型是_______。
A. 取代反应 B. 加成反应 C. 消去反应 D. 加聚反应
18. A→B的反应中,乙烯的碳碳双键中的_________键断裂。
A. π B.σ
19. 写出符合下列条件的D的同分异构体的结构简式_________________。
(1)具有D相同的官能团 (2)核磁共振氢谱有三组峰,峰面积之比为
20. E与足量酸性 溶液反应生成的有机物的名称为____________、_____________。
21. G的结构简式为___________________________。
22. 在右图中用“*”标出F中的不对称碳原子。
23. 已知: ,H在碱性溶液中易发生分子
内缩合从而构建双环结构,主要产物为I ( )和另一种α,β-不饱和酮J。
(1)J的结构简式为______________________。
(2)若经此路线由H合成I,存在的问题有__________。(不定项)
A.原子利用率低 B.产物难以分离
C.反应条件苛刻 D.严重污染环境
五、汽车安全气囊的产气药剂
某汽车安全气囊的产气药剂主要含有NaN 、Fe O、KClO、NaHCO 等物质。当汽车发
3 2 3 4 3
生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
NaN 是气体发生剂,一种生产叠氮化钠的工艺流程如下:
3
24. 已知NaN 溶液呈碱性,
3
下列叙述正确的是_________。
A. NaN 中只含离子键
3
B.N−含有22个电子
3
C. 常温下,0.01 mol·L-1HN 溶液的pH>2
3
D. 0.01 mol·L-1 NaN 溶液中:c(H+)+ c(Na+ )= c(N− )+ c(HN )
3 3 325. 上述流程中可以循环利用的物质是__________。
A. N O B. NaOH C. Na D. NH
2 3
26. 发 生 器 I 中 的 反 应 与 “ 钠 和 水 ” 反 应 相 似 , 该 反 应 的 化 学 方 程 式 为
____________________。
27. 发生器Ⅱ中的反应如下:2NaNH +N O=NaN +NaOH+NH。写出实验室检验NH 气体的
2 2 3 3 3
方法_______________________________________________________________________。
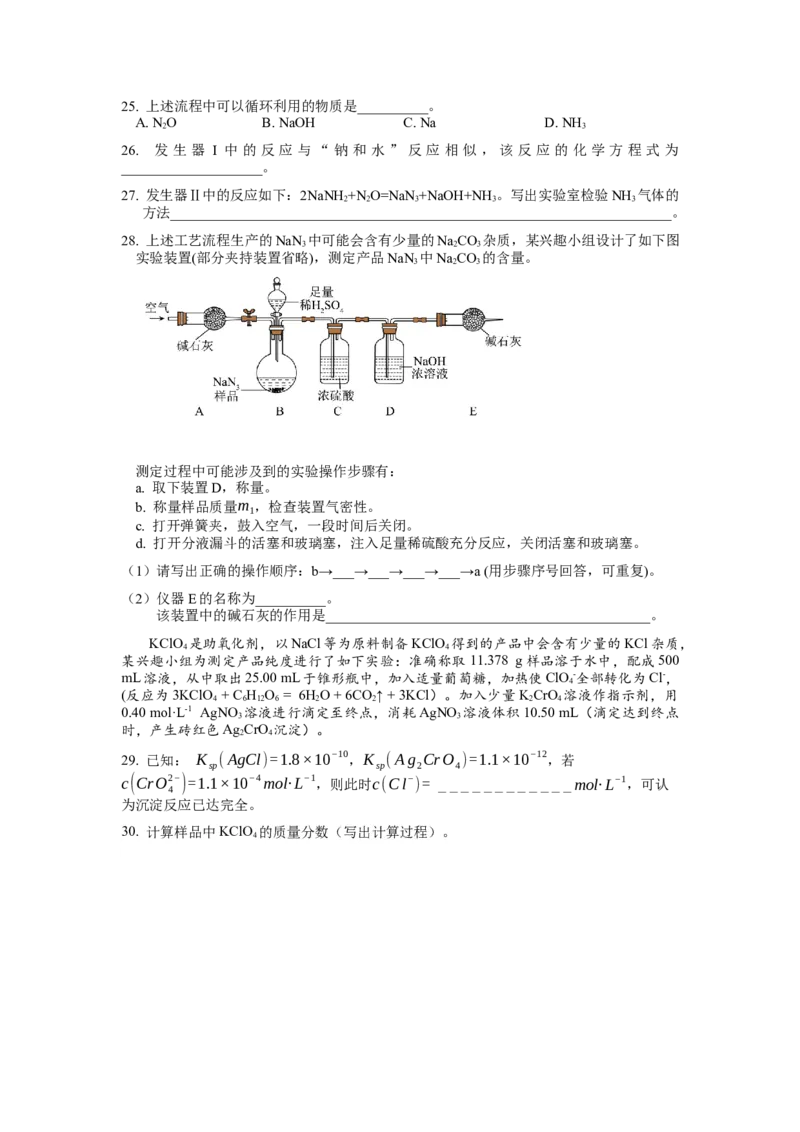
28. 上述工艺流程生产的NaN 中可能会含有少量的NaCO 杂质,某兴趣小组设计了如下图
3 2 3
实验装置(部分夹持装置省略),测定产品NaN 中NaCO 的含量。
3 2 3
测定过程中可能涉及到的实验操作步骤有:
a. 取下装置D,称量。
b. 称量样品质量m ,检查装置气密性。
1
c. 打开弹簧夹,鼓入空气,一段时间后关闭。
d. 打开分液漏斗的活塞和玻璃塞,注入足量稀硫酸充分反应,关闭活塞和玻璃塞。
(1)请写出正确的操作顺序:b→___→___→___→___→a (用步骤序号回答,可重复)。
(2)仪器E的名称为__________。
该装置中的碱石灰的作用是______________________________________________。
KClO 是助氧化剂,以NaCl等为原料制备KClO 得到的产品中会含有少量的KCl杂质,
4 4
某兴趣小组为测定产品纯度进行了如下实验:准确称取11.378 g样品溶于水中,配成500
mL溶液,从中取出25.00 mL于锥形瓶中,加入适量葡萄糖,加热使ClO -全部转化为Cl-,
4
(反应为3KClO + C H O = 6HO + 6CO ↑ + 3KCl)。加入少量KCrO 溶液作指示剂,用
4 6 12 6 2 2 2 4
0.40 mol·L-1 AgNO 溶液进行滴定至终点,消耗AgNO 溶液体积10.50 mL(滴定达到终点
3 3
时,产生砖红色Ag CrO 沉淀)。
2 4
29. 已知: K (AgCl)=1.8×10−10 ,K (Ag CrO )=1.1×10−12 ,若
sp sp 2 4
c(CrO2−)=1.1×10−4mol·L−1 ,则此时c(Cl− )= ____________mol·L−1,可认
4
为沉淀反应已达完全。
30. 计算样品中KClO 的质量分数(写出计算过程)。
4答案要点及评分标准
一、大气污染及治理(本题共20分)
1.(2分)C
2.(2分)A
3.(共4分)B(2分) NH HSO +NHHCO = (NH )SO ·H O + CO↑(2分)
4 3 4 3 4 2 3 2 2
4.(2分)BD
5.(共4分) HO+ClO-+SO= SO2− +Cl-+2H+ (2分) 避免HClO见光分解 (2分)
2 2 4
6.(2分)C
7.(共4分)B (2分) (2分)
SO2−−2e−+2OH−=SO2−+H O
3 4 2
二、硅材料(本题共20分)
8.(共4分)2(2分) C(2分)
9.(2分)BD
10.(共8分)(1)A(2分) (2)B(2分) (3)变化规律:SiF、SiCl 、SiBr 、
4 4 4
SiI 熔沸点逐渐升高,原因:SiX 都是结构相似的分子晶体,相对分子质量依次增大,分
4 4
子间作用力依次增大(2分) (4)sp2、sp3(2分)
√251×1021
3
11.(共6分)(1)A(2分) (2)3、1(2分) (2分)
N ×d
A
三、储氢载体——NH (本题共20分)
3
12.(2分)2NH (g)═N(g)+3H(g) ∆H=90.8kJ·mol-1
3 2 2
13.(共3分)是(1分) ∆H-T∆S=90.8-573╳198.9╳10-3=-23.17<0,所以该反应能自发进行
(2分)
0.02
t
14.(共6分)(1) 1 (2分)(2) b (2分) 开始体积减半,N 分压变为原来的
2
2倍,随后由于加压平衡逆向移动,N 分压比原来2倍要小 (2分)
2
15.(共6分)(1)Ⅱ(2分) (2)CD(2分) (3) (2分)
16.(共3分)HO(1分) 2HO 2H +O (合理即给分)(2分)
2 2 2 2
四、有机物的性质与合成(本题共20分)
17.(共4分)酮羰基或 (2分) C(2分) 18.(2分)A
19.(2分) 20.(共4分)乙酸(2分)丙酮(2分)(可互换)
*
21.(2分) 22.(2分)23. (共4分)(1) (2分) (2)AB(2分)
五、汽车安全气囊的产气药剂(本题共20分)
24.(2分)C
25.(2分)D
催化剂
26.(2分)2Na+2NH ══2NaNH +H ↑
3 2 2
27.(2分)用湿润的红色石蕊试纸接触该气体,如果试纸变蓝,则为NH (合理即给
3
分)
28.(共5分)(1)c→a→d→c (2分)(2)(球形)干燥管(1分) 吸收空气中的CO
2
和HO,防止影响测定结果(2分)
2
29.(2分)1.8×10-6
30.(共5分)
解:达到滴定终点时,消耗的AgNO 为0.40mol·L-1×10.50×10-3L=4.2×10-3mol(1分)
3
设25.00mL样品溶液中KClO 为xmol,KCl为ymol。
4
x+y=4.2×10-3
25
138.5x+74.5y=11.378×
500
解得:x=4.0×10-3 y=2.0×10-4
500
11.378g 样品中,KClO 的质量=4.0×10-3mol×138.5mol·L−1 × =11.080g(3分)
4 25
11.080g
KClO 的质量分数= ×100%≈97% (1分)
4 11.378g