文档内容
第三章 第三节 金属晶体与离子晶体
1.金属键的实质是( )
A.自由电子与金属阳离子之间的相互作用
B.金属原子与金属原子之间的相互作用
C.金属阳离子与阴离子之间的吸引力
D.自由电子与金属原子之间的相互作用
2.在金属晶体中,如果金属原子的价电子数越多,金属阳离子的半径越小,自由电子
与金属阳离子间的作用力越大,金属的熔点越高。由此判断下列各组金属熔点的高低
顺序,其中正确的是( )
A.Mg>Al>Ca B.Al>Na>Li
C.Al>Mg>Ca D.Mg>Ba>Al
3.已知金属钾的晶胞如图所示,下列有关叙述正确的是( )
A.该晶胞属于密置层的一种堆积方式
B.该晶胞是六棱柱
C.每个晶胞平均拥有9个K原子
D.每个K原子周围距离最近且相等的K原子有8个
4.下列关于金属晶体的叙述正确的是( )
A.用铂金做首饰不能用金属键理论解释
B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体C.Li、Na、K的熔点逐渐升高
D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。
5.下面有关晶体的叙述中,错误的是( )
A.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子
B.在NaCl晶体中每个 (或 )周围都紧邻6个 (或6个 )
C.白磷晶体中,分子之间通过共价键结合
D.离子晶体在熔化时,离子键被破坏;而分子晶体熔化时,化学键不被破坏
6.能证明NaCl是离子化合物的事实是( )
A.常温下是固体 B.熔融态能导电 C.水溶液能导电 D.易溶于水
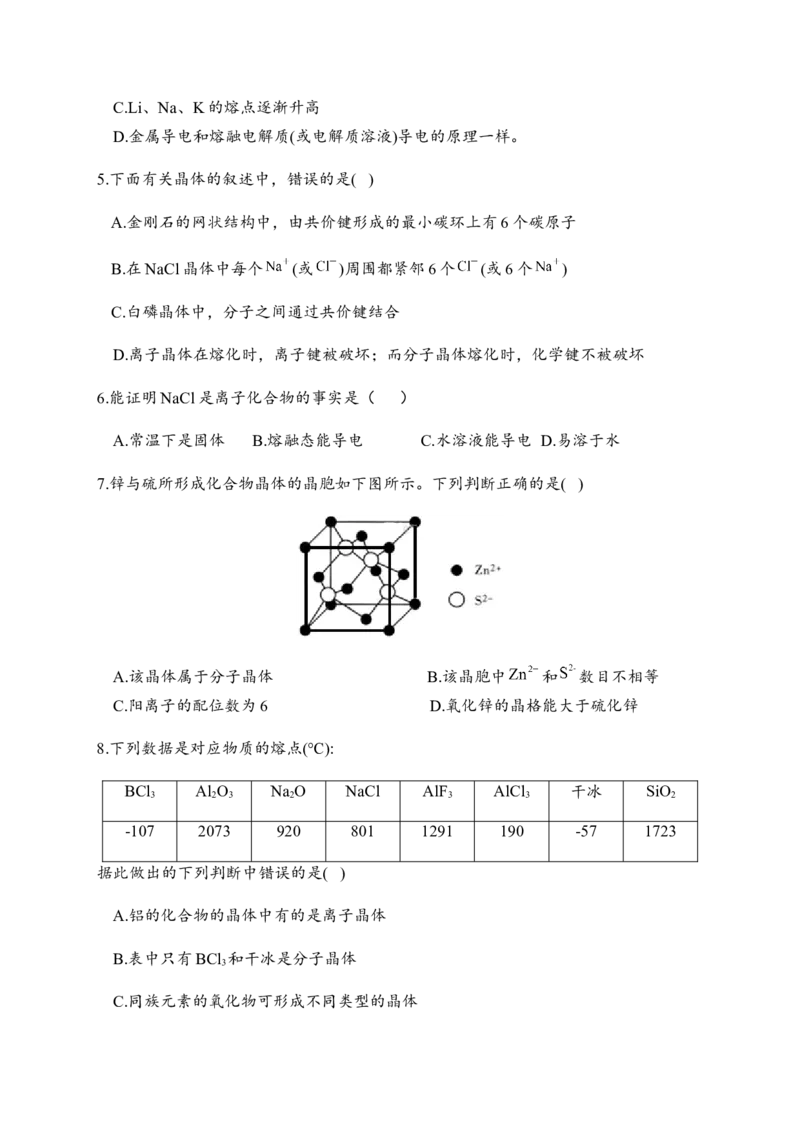
7.锌与硫所形成化合物晶体的晶胞如下图所示。下列判断正确的是( )
A.该晶体属于分子晶体 B.该晶胞中 和 数目不相等
C.阳离子的配位数为6 D.氧化锌的晶格能大于硫化锌
8.下列数据是对应物质的熔点(℃):
BCl Al O Na O NaCl AlF AlCl 干冰 SiO
3 2 3 2 3 3 2
-107 2073 920 801 1291 190 -57 1723
据此做出的下列判断中错误的是( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl 和干冰是分子晶体
3
C.同族元素的氧化物可形成不同类型的晶体D.不同族元素的氧化物可形成相同类型的晶体
9.下列说法不正确的是( )
A.离子晶体不一定都含有金属元素
B.离子晶体中除含离子键外,还可能含有其他化学键
C.金属元素与非金属元素构成的晶体不一定是离子晶体
D.熔化后能导电的晶体一定是离子晶体
10.下列说法不正确的是( )
A. 中离子键的百分数为62%,则 不是纯粹的离子晶体,是离子晶体与
共价晶体之间的过渡晶体
B. 通常当作离子晶体来处理,因为 是偏向离子晶体的过渡晶体,在许多性
质上与纯粹的离子晶体接近
C. 是偏向离子晶体的过渡晶体,当作离子晶体来处理; 是偏向共价晶体的
过渡晶体,当作共价晶体来处理
D.分子晶体、共价晶体、金属晶体和离子晶体都有过渡型
11.自然界中的 又称萤石,是一种难溶于水的固体,属于典型的离子晶体。下列能
说明 一定是离子晶体的是( )
A. 难溶于水,其水溶液的导电性极弱
B. 的熔、沸点较高,硬度较大
C. 固体不导电,但在熔融状态下可以导电
D. 在有机溶剂(如苯)中的溶解度极小
答案以及解析1.答案:A
解析:金属晶体由金属阳离子与自由电子构成,金属阳离子与自由电子之间的强烈的
相互作用称为金属键。
2.答案:C
解析:金属原子的价电子数:Al>Mg=Ca=Ba>Li=Na,金属阳离子的半径:
,则C正确。
3.答案:D
解析:钾晶胞是非密置层的两种堆积方式中的一种,A错误;晶胞呈立方体,不是六
棱柱,B错误;根据均摊法计算,每个晶胞有2个K原子,C错误。
4.答案:B
5.答案:C
解析:A. 金刚石晶体中,由共价键形成的最小碳环上有6个碳原子,每个碳原子形成
四个共价键,从而形成空间网状结构,故A正确;
B. 氯化钠晶体中钠离子或氯离子的配位数都是6,所以在NaCl晶体中每个 (或 )
周围都紧邻6个 (或 ),故B正确;
C. 白磷分子为正四面体结构,原子间通过共价键结合,键角为60°,分子间存在范德
华力,故C错误;
D. 离子晶体的构成微粒是阴阳离子,分子晶体的构成微粒是分子,所以离子晶体在熔
融状态下能电离出阴阳离子,而分子晶体在熔融状态下还是以分子存在,只破坏分子
间作用力不破坏化学键,故D正确;
6.答案:B
解析:离子化合物在熔融状态下能电离出自由移动的离 子,熔融态能导电。
7.答案:D
解析:选项A,该晶体属于离子晶体。选项B,从晶胞图分析,属于该晶胞的 数目为 , 数目也为4,
与 的数目相等。
选项C,在 晶胞中, 的配位数为4。
选项D, 和 中, 半径小于 ,所带的电荷数相等,所以 的晶格能
大于 。
8.答案:B
解析:A项,氧化铝的熔点高,属 于离子晶体,则铝的化合物的晶体中有的是离子晶
体,正确;B项,表中BCl 、AlCl 和干冰均是分子晶体,错误;C项,同族元素的氧
3 3
化物可形成不同类型的晶体,如干冰是分子晶体,SiO 是原子晶体,正确;D项,不
2
同族元素的氧化物可形成相同类型的晶体,如CO 、H O都是分子晶体,正确。
2 2
9.答案:D
解析:A、离子晶体中不一定含有金属离子,如氯化铵晶体,选项A正确;B、离子晶
体中除含离子键外,还可能含有其他化学键,如铵盐、 NaOH、 Na O 等离子晶体中
2 2
存在离子键和共价键,选项B正确;C、金属与非金属元素构成的晶体不一定是离子
晶体。如AlCl 为分子晶体,选项C正确;D、熔融状态下能导电的晶体可能是金属晶
3
体或离子晶体,选项D不正确。答案选D。
10.答案:C
解析: 、 均是偏向共价晶体的过渡晶体,当作共价晶体来处理,C项不正
确。
11.答案:C
解析:离子晶体在熔融状态下可以电离出自由移动的阴、阳离子,所以晶体在熔融状
态下能否导电,是判断该晶体是否为离子晶体的依据。