文档内容
[键入文字]
第七章 有机化合物
第一节 认识有机化合物
(第1课时 有机物中碳原子的成键特点 烷烃结构 )
一、选择题
1.下列关于有机物的说法正确的是
A.凡是含碳元素的化合物都属于有机物
B.有机物只含有碳、氢两种元素
C.有机物不但存在于动植物体内,而且可以通过人工的方法合成
D.燃烧生成 和 的有机物中一定含有碳、氢、氧三种元素
【答案】C
【解析】
A. 、 、碳酸、碳酸盐等含碳化合物因组成和性质都具有无机物的特点,属于无机
物,A项错误;
B.有机物一定含有碳元素,绝大多数有机物含有氢元素,部分有机物还含有氧、氮、硫等
元素,B项错误;
C.最初的有机物来自于动植物体内,现在,更多的有机物是人工合成的,C项正确;
D.甲烷完全燃烧的产物是 和 ,但甲烷仅由碳、氢两种元素组成,D项错误
答案选C。
2.下列说法不正确的是
A.甲烷的分子式能表示其元素组成和分子构成
B.甲烷的电子式能反映原子最外层电子的成键情况
C.甲烷的结构式能表示其分子的空间构型
D.甲烷分子中的化学键是极性键
【答案】C
【解析】
A.从分子式CH 可得出甲烷由碳、氢两种元素组成,1个甲烷分子是由1个碳原子和4个
4
学科网(北京)股份有限公司[键入文字]
氢原子构成的,A说法正确;
B.甲烷的电子式反映了碳原子和氢原子通过形成共用电子对而使其最外层达到稳定结构,
B说法正确;
C.结构式仅能反映原子间的结合情况及成键情况,不能反映其真实的空间结构,C说法错
误;
D.甲烷分子中的C-H键是极性键,D说法正确。
答案C。
3.大多数有机物分子中的碳原子与其他原子的结合方式是( )
A.形成4对共用电子 B.通过非极性键结合
C.通过2个共价键结合 D.通过离子键和共价键结合
【答案】A
【解析】
A.碳原子最外层有4个电子,可形成4对共用电子, 故A正确;
B.碳原子之间形成的共价键是非极性共价键,碳原子与其他原子形成的共价键是极性键,
故B错误;
C.碳原子最外层有4个电子,可形成4对共用电子,即形成4个共价键,故C错误;
D.碳原子最外层有4个电子,既不容易得到电子也不容易失去电子,即难形成离子键,故
D错误;
答案选A。
4.有机物种类繁多的主要原因是
A.有机物的分子结构十分复杂
B.碳原子能与其他原子形成四个共价键,且碳原子之间也能互相成键
C.有机物除含碳元素外,还含有其他多种元素
D.自然界中存在多种形式的、大量的有机物
【答案】B
【解析】
碳原子能与多种原子形成四个共价键(碳和碳之间可以形成双键,可以是单键,可以是叁
键),且碳原子之间相互成键可以成碳链,可以成碳环,此外含碳的有机物存在同分异构
现象,从而导致有机物种类繁多,答案选B。
5.如图是CH、CCl 、CHCl分子的球棍模型图。下列说法正确的是( )
4 4 3
学科网(北京)股份有限公司[键入文字]
A.CH、CCl 和CHCl都是正四面体结构
4 4 3
B.CH、CCl 都是正四面体结构
4 4
C.CH 和CCl 中的化学键完全相同
4 4
D.CH、CCl 的结构相同,性质也相同
4 4
【答案】B
【解析】CHCl中的C—Cl和C—H不同,故CHCl不是正四面体结构;CH 和CCl 中的
3 3 4 4
化学键不同,二者的性质也不相同。
6.下列叙述正确的是( )
A.分子式相同,各元素质量分数也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
【答案】C
【解析】
A、也可能是同分异构体,不正确;
B、结构相似,分子组成相差若干个CH 原子团的物质,互称为同系物,因此同系物的通式
2
相同,但通式相同的不一定是同系物,B不正确。
C、分子式相同,而结构不同的化合物是同分异构体,C正确。
D、相对分子质量相同,但分子式不一定相同,不正确。
答案选C。
7.下列物质中属于同系物的是
①CH CH C1 ②CH =CHCl ③CH CH CH C1
3 2 2 3 2 2
④CH ClCH Cl ⑤CH CH CH CH ⑥CH CH(CH )
2 2 3 2 2 3 3 3 2
A.①② B.①④ C.①③ D.⑤⑥
【答案】C
学科网(北京)股份有限公司[键入文字]
【解析】
同系物是结构相似,在分子组成上相差一个或多个CH 原子团的有机化合物。
2
A.①和②的结构不相似,不属于同系物,错误;
B.①和④的结构相似但不是相差一个或多个CH 原子团,不属于同系物,错误;
2
C.①和③结构相似,在分子组成上相差一个CH 原子团,属于同系物,正确;
2
D.⑤和⑥的分子式相同结构不同,属于同分异构体,错误;
答案选C。
8.大多数有机物分子中的碳原子与其他原子的结合方式是( )
A.形成4对共用电子 B.通过非极性键结合
C.通过2个共价键结合 D.通过离子键和共价键结合
【答案】A
【解析】
A.碳原子最外层有4个电子,可形成4对共用电子, 故A正确;
B.碳原子之间形成的共价键是非极性共价键,碳原子与其他原子形成的共价键是极性键,
故B错误;
C.碳原子最外层有4个电子,可形成4对共用电子,即形成4个共价键,故C错误;
D.碳原子最外层有4个电子,既不容易得到电子也不容易失去电子,即难形成离子键,故
D错误;
答案选A。
9.有机物种类繁多的主要原因是
A.有机物的分子结构十分复杂
B.碳原子能与其他原子形成四个共价键,且碳原子之间也能互相成键
C.有机物除含碳元素外,还含有其他多种元素
D.自然界中存在多种形式的、大量的有机物
【答案】B
【解析】
碳原子能与多种原子形成四个共价键(碳和碳之间可以形成双键,可以是单键,可以是叁
键),且碳原子之间相互成键可以成碳链,可以成碳环,此外含碳的有机物存在同分异构
现象,从而导致有机物种类繁多,答案选B。
10.下列说法正确的是
A.碳原子之间以单键结合,碳原子剩余的价键全部与氢原子结合的有机物一定是饱和链
学科网(北京)股份有限公司[键入文字]
烃
B.分子组成符合C H (n为正整数)的有机物一定是烷烃
n 2n+2
C.丙烷分子中所有碳原子均在同一条直线上
D.碳、氢原子个数比为1:3的烃有2种
【答案】B
【解析】
A.符合条件的有机物还可以是环烷烃,如 ,A说法错误;
B.只有饱和链状烷烃的通式为C H (n为正整数),则分子组成符合C H (n为正整数)的
n 2n+2 n 2n+2
有机物一定是烷烃,B说法正确;
C.在烷烃分子中,与饱和碳原子相连的4个原子一定位于四面体的4个顶点上,所以丙烷
中的所有碳原子不可能在同一条直线上,C项错误;
D.碳、氢原子个数比为1:3的烃只有乙烷,乙烷没有同分异构体,D项错误。
答案 B。
11.不属于有机物的特点是( )
A.大多数有机物难溶于水,易溶于有机溶剂
B.有机反应比较复杂,一般反应速率较慢
C.绝大多数有机物受热不易分解,且不易燃烧
D.绝大多数有机物是非电解质,不易导电,熔点较低
【答案】C
【解析】
A. 大多数有机物难溶于水,易溶于有机溶剂,正确;
B. 有机反应比较复杂,一般反应速率较慢,正确;
C. 绝大多数有机物受热易分解,且易燃烧,C错误;
D. 绝大多数有机物是非电解质,不易导电,熔点较低,正确。
故选C。
12.下列说法错误的是
①化学性质相似的有机物是同系物 ②分子组成上相差一个或若干个CH 原子团的有机物是
2
同系物 ③若有机物中碳、氢元素的质量分数相同,则它们必定是同系物 ④若两种有机物
的相对分子质量相差14n(n为正整数),则必为同系物
学科网(北京)股份有限公司[键入文字]
A.①②③④ B.只有②③ C.只有③④ D.只有①②③
【答案】A
【解析】
①同系物的结构相似,化学性质相似,但化学性质相似的有机物不一定是同系物,如正丁
烷(CH CH CH CH )和异丁烷( )的化学性质相似,但它们互为同分异构体,①说法
3 2 2 3
错误;
②结构相似,且分子组成上相差一个或若干个CH 原子团的有机物才互为同系物,②说法
2
错误;
③有机物中碳、氢元素的质量分数相同,它们可能是同分异构体,也可能是最简式相同的
有机物,③说法错误;
④两种有机物的相对分子质量相差14n(n为正整数),不一定满足结构相似、通式相同的条
件,如乙烯(CH =CH )和环丁烷( ),④说法错误。
2 2
综上所述,①②③④说法错误,答案A。
13.下列事实中能证明甲烷分子是以碳原子为中心的正四面体结构的是
A.CH Cl只代表一种物质 B.CH Cl 只代表一种物质
3 2 2
C.CHCl 只代表一种物质 D.CCl 只代表一种物质
3 4
【答案】B
【解析】
CH 分子中有四个等同的C—H键,可能有两种对称的结构:正四面体结构和平面正方形结
4
构.甲烷无论是正四面体结构还是正方形结构,一氯代物、三氯代物和四氯代物均不存在
同分异构体.而平面正方形中,四个氢原子的位置虽然也相同,但是相互间存在相邻和相
间的关系,其二氯代物有两种异构体:两个氯原子在邻位和两个氯原子在对位.若是正四
面体,则只有一种,因为正四面体的两个顶点总是相邻关系。由此,由CH Cl 只代表一种
2 2
物质,可以判断甲烷分子是空间正四面体结构,而不是平面正方形结构。故选B。
14.下列有关烷烃的说法正确的是
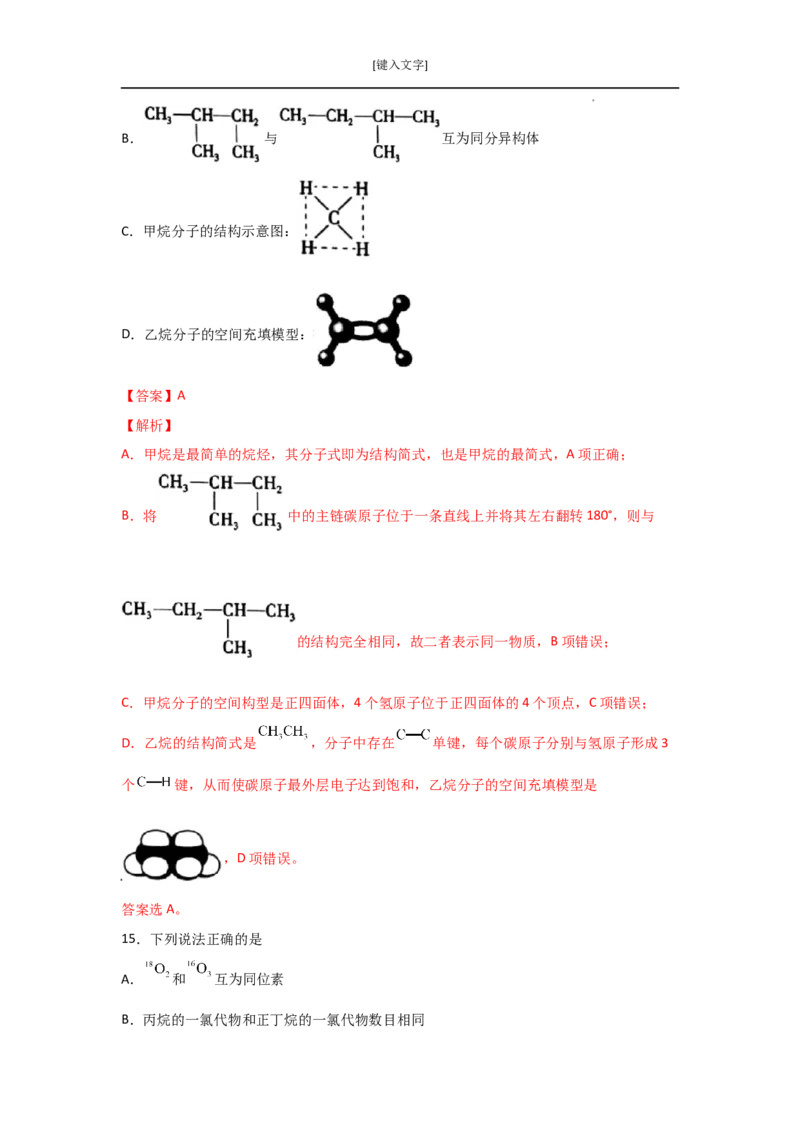
A.甲烷的结构简式:
学科网(北京)股份有限公司[键入文字]
B. 与 互为同分异构体
C.甲烷分子的结构示意图:
D.乙烷分子的空间充填模型:
【答案】A
【解析】
A.甲烷是最简单的烷烃,其分子式即为结构简式,也是甲烷的最简式,A项正确;
B.将 中的主链碳原子位于一条直线上并将其左右翻转180°,则与
的结构完全相同,故二者表示同一物质,B项错误;
C.甲烷分子的空间构型是正四面体,4个氢原子位于正四面体的4个顶点,C项错误;
D.乙烷的结构简式是 ,分子中存在 单键,每个碳原子分别与氢原子形成3
个 键,从而使碳原子最外层电子达到饱和,乙烷分子的空间充填模型是
,D项错误。
答案选A。
15.下列说法正确的是
A. 和 互为同位素
B.丙烷的一氯代物和正丁烷的一氯代物数目相同
学科网(北京)股份有限公司[键入文字]
C. 和 是具有相同质子数的不同核素
D. 和 是同分异构体
【答案】B
【解析】
A.同位素的研究对象为原子,而 和 为单质,A项错误;
B. 与 的一氯代物均有两种,B项正确;
C. 和 均为单质,不是核素,C项错误;
D. 的分子式为 ,而 的分子式为 ,两者不
是同分异构体,D项错误;
答案选B。
二、非选择题
16.(1)根据碳原子的4价键原则,可将下图中碳原子的价键用氢原子补齐,试在各模型下
面的横线上写出各物质的分子式。
①_______ ②______ ③______ ④______
⑤________ ⑥_______ ⑦_______
⑧_______ ⑨_______
(2)通过以上模型可知,碳原子间可形成碳碳单键、________________及________________。
(3)根据(1)中各物质的分子式,用序号填空。
分子式相同的物质有:①和________;③和________;⑥和________。
(4)分子中含4个碳原子的碳氢化合物除(1)中所列的9种外,你还能列举出其他可能的类型
吗__________(用球棍模型表示)?
学科网(北京)股份有限公司[键入文字]
【答案】 (1)①C H ②C H ③C H ④C H ⑤C H ⑥C H ⑦C H ⑧C H
4 10 4 10 4 8 4 8 4 8 4 6 4 6 4 8
⑨C H
4 8
(2)碳碳双键 碳碳三键
(3)② ④、⑤、⑧、⑨ ⑦
(4)
17.两种有机物的碳骨架如图所示。
已知它们结构中的碳原子余下的价键均与氢原子结合,请写出分子式:棱晶烷__;立方烷
__。
【答案】 C H C H
6 6 8 8
【解析】
从棱晶烷和立方烷的碳骨架结构可看出,每个碳原子均与另外3个碳原子形成3个碳碳单
键,故每个碳原子还剩余1个价键,即需要结合1个氢原子,则棱晶烷和立方烷的分子式
分别是C H 和C H 。
6 6 8 8
18.晋朝人常璩在《华阳国志》里有这样一段话:“有火井,夜时光映上昭。民欲其火,
先以家火投之。顷许,如雷声,火焰出,通耀数十里,以竹筒盛其光藏之,可拽行终日不
灭也”,请回答下列问题。
(1)话中描述的物质是一种最简单的有机物——甲烷,其分子的结构式为___________。
(2)写出“顷许,如雷声,火焰出”涉及的化学反应方程式:___________。
(3)下列有关甲烷的说法正确的是___________(填字母)。
A.它属于化石能源
B.它的分子中含有非极性键
C.它的分子中所有原子的最外层都达到了8电子稳定结构
D.(2)中反应发生时伴随有旧极性键的断裂和新极性键的形成
学科网(北京)股份有限公司[键入文字]
【答案】 AD
【解析】
(1)甲烷分子的结构式为 ;
(2) “顷许,如雷声,火焰出”叙述的是甲烷燃烧,涉及的化学反应方程式为
;
(3) A.甲烷属于化石能源,A项正确;
B.甲烷分子中只含有 键,故只含有极性键,B项错误;
C.甲烷分子中只有碳原子的最外层达到了8电子稳定结构,氢原子达到2电子稳定结构,
C项错误;
D.甲烷燃烧时伴随有旧极性键的断裂和新极性键的形成,D项正确;
答案选AD。
19.按要求写出下列烷烃:
(1)相对分子质量为44的烷烃的结构简式_________________________。
(2)碳、氢原子个数比为2∶5的烷烃的分子式_____________________。
(3)分子中含14个氢原子的烷烃的分子式_________________________。
【答案】
【解析】
运用烷烃的通式( )求解各题。
(1) , ,该烷烃的结构简式为 ,故答案为:
;
(2) , ,该烷烃的分子式为 ,故答案为: ;
学科网(北京)股份有限公司[键入文字]
(3) , ,该烷烃的分子式为 ,故答案为: 。
学科网(北京)股份有限公司[键入文字]
学科网(北京)股份有限公司