文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”真题完全解读(吉林、黑龙江卷)
试卷总评
试题评析
2024年吉林、黑龙江高考适应性演练试题“遵循高中化学课程标准,引导依标教学;依据中国高考评
价体系,突出关键能力考查,充分发挥高考育人功能和积极导向作用”。该试题精心遴选情境素材,注重
联系生产生活实际,体现学科社会功能,彰显化学学科的价值。以化学学科核心素养为主线,对标高中化
学新课程标准,加强对基本规律和基本方法的考查,突出了基础性;优化丰富问题情境,体现了时代性;
加强对分析综合能力、逻辑推能力的考查,体现了选拔性。这种命题思路,能较好扭转简单靠刷题获取高
分的不良倾向。试卷考查的知识内容基础、全面而不失新颖与创新,化学试卷保持了以往的命题风格,在
化学基础知识中融合对考生学习方法和思维能力的考查、关注对考生学科素养的培养与提高。整体呈现据
标立本、紧密联系生产生活实际、紧跟学科前沿的风格,融合考查学生的化学学科必备知识、基本技能和
学科核心素养,化学试题突出能力立意、突出学科特点、突出核心素养、突出创新能力的鲜明特色,有利
于发挥高考的导向功能,有利于推进化学新课程教学改革。试题主要特点如下:
一、精心遴选真实情境,彰显化学学科价值
通过设计不同陌生度和复杂度的真实情境,很好地检测了学生的素养水平,与素养导向的教学形成呼
应,有利于教考衔接、教考共振。试题注意真实情境的遴选,激发学生学习的兴趣,意在让学生完整解决
真实复杂问题。试题突出了对中学化学核心基础知识、基本技能、基本观点和基本方法的考查。考查学生
对基础知识的掌握,对基本概念的理解。掌握元素基础知识是能力提升的前提和保障,试卷中考查内容涵
盖高中化学重要的元素化合物知识、基本概念与理论、化学基础实验技能和化学计算,如第1题以“春节
是中华民族重要的传统节日”为情境考查蛋白质变性、彩妆用品、糯米年糕、 陈年老酒等;第2题考查中
华传统文化;第3题考查化学用语;第4题考查阿伏加德罗常数。
对核心主干知识不仅仅是体现在记忆层面,还将考查对其的在具体问题解决过程中的理解和应用水
平。第5题考查化学实验等核心主干知识;第6题和8题考查有机化学;第9题和10题考查物质结构与性
质。这必将引导中学化学教学要回归教材、注重基础,紧紧围绕核心主干知识,强化学生应用知识解决实
际问题所必备的关键能力。
二、突出关键能力考查,体现核心素养导向
化学试题突出关键能力的考查,体现素养导向,落实新课程理念。试题注重对学生学科素养和解决问
题能力的考查,要求学生从化学视角分析和解决问题,突出对信息摄取、吸收和整合的能力。强调科学思更多全科试卷,请关注公众号:高中试卷君
维和方法,试题贴近了新高考改革的趋势,突出对能力和化学学科核心素养的综合考查。如:第11题和
14题考查电化学综合,体现了“宏观辨识与微观探析”;第15题和18题将沉淀溶解平衡、平衡移动、平
衡常数、盖斯定律、产率的计算综合考查,体现了“变化观念与平衡思想”。“科学探究与创新意识”及
“科学态度与社会责任”在第5提、10题和第17题中得到充分体现,精心设置的问题灵活多样而又目标
指向明确,考查了学生综合分析和逻辑思维的能力。高度重视实验与探究能力的考查,体现创新性。实验
与探究能力与PISA科学测试能力目标中的“评价和设计科学探究”相对应,主要是指根据实验操作和过
程,分析实验目的或预测实验结果;根据实验目的和要求,设计或评价简单实验方案;描述实验现象,处
理、分析实验数据和结果,得出相应结论;在运用规律、原理和方法解决生产生活、实践探索、科学研究
等实际问题的过程中,构建解决问题的模型,清晰、准确而有逻辑地运用化学专业术语、数据图表和模型
等方式表达自己的观点和方案,科学而有创造性地解决问题。第6、8、9、10、14、15、18题数表信息往
往体现在化学原理知识的考查上,辨识模型、图表等各种类型的信息,从中提取关键内容并与已学知识进
行整合;辨析在解决生产、生活与社会问题过程中运用的基本化学原理和方法,并能解答简单化学问题。
例如:结合图表数据可以确定化学平衡状态、平衡移动方向及计算化学平衡常数或某一平衡状态的转化
率;图示包含二维坐标图、物质转化流程图等,解决这些图示信息的关键是需要把图示信息转化为物质或
反应信息,再结合核心知识方法进行解答。
三、深化必备知识融合,体现迁移应用价值
该套化学试题精心遴选最有素养发展价值的知识,注重知识的综合性和应用性,体现知识迁移应用的
价值。试卷关注学科内模块及学科间的有效融合,培养学生融会贯通、化知成智的信心与能力。化学是以
实验为基础,又是一门紧密联系生产生活实际的科学。化学试题一贯重视以真实问题情境为测试载体,主
要考查教材中的基础实验或者模拟生产生活实际中的真实实验情境。如第6题以烟气脱硫可有效减少大气
污染,第11题以生物质电池为情境,对基础知识、反应规律和反应原理进行综合考查,让学生运用化学知
识、运用化学原理,提高解决问题的能量,发挥化学高考试题的导向作用,引导化学教学改革。
总之,2024年的吉林、黑龙江高考适应性演练试题突出立德树人导向,在贴近教学和学生实际的同时
突出化学的育人价值,凸显化学实验学科特色,注重思维逻辑能力考查,试题素材选取范围广,内容富有
时代气息,试题内容综合性强,突出科学探究及科学研究思维方法。为实现高考改革的平稳过渡、引导高
中化学课堂教学提供了参考。
试卷结构更多全科试卷,请关注公众号:高中试卷君
考情分析
题 难度 考查内容 详细知识点
号
一、选择题(45分)
1 易 化学与STSE 蛋白质变性、无机物、酯的香味
2 易 传统文化 天然高分子、可逆反应、颜料
3 较易 化学用语 化学用语、结构式、电子式、电子排布式
4 较易 阿伏加德罗常数 中子数、转移的电子数、
5 中 化学实验 物质的分离提纯方法和理论依据
6 中 有机化学 反应类型、手性碳原子、官能团
7 中 离子方程式 离子方程式书写正误判断
8 中 有机化学 反应类型、杂化方式、同分异构体
9 中 物质结构与性质 电离能、电负性、化学键、元素推断
10 较难 物质结构与性质 晶胞结构的分析与计算、化学式的确定
11 较难 电化学综合 原电池原理、电极反应式、原电池相关计算
12 较难 工业流程 化合价、氧化还原反应、配平
13 中 化学实验 化学实验现象、结论或推论
14 较难 电化学综合 原电池原理、电解池原理、电极反应式
15 较难 沉淀溶解平衡 图像曲线分析、溶度积、平衡常数
二、非选择题(55分)
16 中 工艺流程 离子方程式、盐类的水解、除杂
17 较难 化学实验 HCl的制备、萃取、产率
18 较难 化学反应原理综合 盖斯定律、产率、价层电子对互斥理论、平衡移动
官能团名称、反应类型、同分异构体的书写、合成路
16 较难 有机合成与推断
线
备考指南
1.立足基础 回归课本
高考命题以课程标准为基本依据,以教材为重要参考,在最后的备考冲刺阶段,要对课本的知识体系
做一个回顾和归纳,建议可以课本目录为标准,将知识点重新串联起来,复习时做到不遗漏任何知识点。更多全科试卷,请关注公众号:高中试卷君
回归课本要关注基本概念(如:热化学方程式、燃烧热、中和热等),关注课本图像(如吸放热反应能量变化
图像、反应机理图等),关注模型的建立(如原电池、电解池模型等)。此外,回归课本还要重视课本实验的
回顾。许多基本概念、原理、规律及物质性质都是由实验推导和验证的,因此除了关注有关元素化合物的
性质实验外,还要重点复习实验证明过程。
2.科学诊断 对症下药
备考时,要分析自己在各次重要模拟考试中的答题情况,建立自己的学情诊断报告。一是找必拿分。
如:化学与STES的考点、N 的考查、化学用语、元素周期律、实验基础、有机基础等;二是找弱项。
A
如:如电化学、溶液中的离子反应与平衡、信息题、反应原理大题等,注意哪类型的题目常错或得分率
低;三是分析原因,比如:知识漏洞、能力不足或是解题模型的缺失导致失分;四是明确需求。要有针对
性地进行复习。对于不常错的题目,要隔三差五做两道,保持解决这类型题目的敏感度;对于常错题,要
回顾基础知识点,反复练典型试题,明确试题的题型特点和解题方法,构建试题的答题思维模型。
3.提高速度 保基础分
无论对于什么学科,提升做题速度都是至关重要的。在简单题目上用时越短,就能节约出时间来攻克
难题。同学们在备考冲刺阶段可采用多种方式进行限时训练(目的是练速度、练考点、练技巧、练准确
率)。化学考试中保基础分体现在做好选择题。高考选择题占比达到45分,属于容易得分也容易丢分的题
型,它的考点比较基础,因此复习阶段,同学们可以有意识训提高做选择题的速度。此外,还要提高选择
题的准确率,要活用选择题的解题技巧(如直接选择、间接选择、比较法等),切忌死算硬算,小题大作。
化学考试中保基础分还体现在规范答题、避免非智力因素失误上。如:化学用语使用不规范;不写反应热
单位;不注意有效数字处理,热化学方程式漏写状态;等号与可逆号乱用;多元弱酸根离子的水解反应不
分步写;有机物的结构简式氢原子写多或写少;酯化反应漏写水等;重视一些基本实验操作的规范答题:
沉淀是否完全、沉淀的洗涤、洗涤是否干净、结晶的基本方法等。
4.稳定情绪 树立信心
高考试题完美涵盖并依次进阶了化学学科关键能力的考查,很好地考查了学生在面对情境时认识问
题、分析问题和解决问题的能力。因此,在日常复习过程中,要合理拆解真实复杂情境,融入结构化的必
备知识,设计不同能力水平的驱动性问题,实现从“用中学”到“创中学”,真正发展学生的化学学科核心素
养。乐观复习,不要问自己还有多少问题,要想自己今天解决了什么问题;多看进步,时刻给自己积极的
心里暗示,树立自己一定能行的信心。平和积极的心态是成功的关键!
逐题精讲
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一更多全科试卷,请关注公众号:高中试卷君
项符合题目要求。
1. 春节是中华民族重要的传统节日,近日被确定为联合国假日。以下有关春节习俗中的化学知识说法错误
的是
A. 红烧肉烹饪过程中蛋白质变性涉及化学变化 B. 春晚演员的彩妆用品均属于无机物
C. 饺子与糯米年糕的口感差异与支链淀粉的含量有关 D. 陈年老酒的芳香气味与酯的形成有关
【答案】B
【解析】肉中含有蛋白质,烹饪过程中蛋白质变性涉及化学变化,故A正确;彩妆用品中含有甘油,属于
有机物,故B错误;饺子与糯米年糕中含有淀粉,口感差异与支链淀粉的含量有关,故C正确;酒精在与
氧气接触的过程中会氧化生成羧酸类物质,而羧酸类物质则会进一步与酒精反应形成酯类物质,具有芳香
气味,故D正确;故选B。
2. “银朱”主要成分为 。《天工开物》记载:“凡将水银再升朱用,故名曰银朱…即漆工以鲜物
采,唯(银朱)入桐油则显…若水银已升朱,则不可复还为汞。”下列说法错误的是
A. “银朱”可由 和S制备 B. “银朱”可用于制作颜料
C. “桐油”为天然高分子 D. “水银升朱”不是可逆反应
【答案】C
【解析】Hg和S反应可生成HgS,S+Hg=HgS,A正确;HgS是红色固体,可用于制作颜料,B正确;“桐
油”中含有油脂类物质,属于甘油三酯,不是高分子化合物,C错误;由“若水银已升朱,则不可复还为汞”
可知,生成Hg与S反应生成HgS不是可逆反应,D正确;故选C。
3. 下列化学用语表述正确的是
A. 的空间结构为V形 B. 顺 二溴乙烯结构式为
C. 的电子式为 D. 基态 原子价电子排布式为
【答案】B
【解析】根据价层电子对互斥理论, 的孤电子对为 , 个数为2,则 的空间结
构为直线形,A错误;烯烃的顺式指烯烃中碳碳双键同侧的两个基团相同,则顺 二溴乙烯结构式为
,B正确; 中每个N原子都满足8电子稳定结构,其电子式为: ,C错误;根据洪特更多全科试卷,请关注公众号:高中试卷君
规则的特例,基态 原子价电子排布式为 ,D错误;故选B。
4. 电解重水( )是制取氘气( )的一种方法。设 为阿伏加德罗常数的值。下列说法错误的是
A. 分子间存在氢键 B. 的熔、沸点比 高
C. 含中子数目为 D. 制取 转移的电子数目为
【答案】D
【解析】O原子电负性较大, 分子间存在氢键,故A正确; 和 分子间都能形成氢键,但
相对分子之间大于HO,范德华力较大,熔沸点较高,故B正确; 中含有2+16-8=10个中子,
2
的物质的量为 =0.1mol,含中子数目为 ,故C正确;未说明气体所处的温度和压
强,无法计算 的物质的量,故D错误;故选D。
5. 下列各组物质分离提纯方法及依据均正确的是
分离提纯方法 依据
A 重结晶法除去苯甲酸中的氯化钠 温度对溶解度的影响不同
B 氢氧化钠溶液洗气法除去 中的 化学性质不同
C 分液法分离乙酸正丁酯和正丁醇 沸点不同
D 加热法除去碳酸氢钠固体中的碳酸钠 热稳定性不同
【答案】A
【解析】温度对苯甲酸、氯化钠的溶解度的影响不同,可以重结晶法除去苯甲酸中的氯化钠,A正确;二
氧化碳和氯化氢都会被氢氧化钠溶液吸收,B错误;乙酸正丁酯和正丁醇互溶,不能分液分离,应该使用
蒸馏法分离,C错误;碳酸氢钠不稳定,受热分解为碳酸钠和水、二氧化碳,加热使得碳酸氢钠转化为碳
酸钠,故不可以加热法除去碳酸氢钠固体中的碳酸钠,D错误;故选A。
6. 某化合物具有抗癌活性,结构如图所示。下列有关该物质说法错误的是更多全科试卷,请关注公众号:高中试卷君
A. 可发生水解反应 B. 含有手性碳原子 C. 可发生消去反应 D. 含有2个酯基
【答案】D
【解析】该有机物中含有酯基和酰胺基,一定条件下能够发生水解反应,故A正确;手性碳原子是指与四
个各不相同原子或基团相连的碳原子,该有机物含有手性碳原子,如最右侧与羟基相连的碳原子等,故B
正确;该有机物中与羟基相连的碳原子相邻碳原子上含有H原子,可发生消去反应,故C正确;该有机物
中只含有1个酯基,故D错误;故选D。
7. 下列化学方程式或离子方程式正确的是
A. 氢氟酸溶蚀石英玻璃:
B. 盐酸除锅炉水垢:
C. 溶液吸收电石气中的 :
D. 候氏制碱法:
【答案】A
【解析】氢氟酸溶蚀石英玻璃的化学方程式为: ,故A正确;水垢中含有碳
酸钙,盐酸除锅炉水垢: ,故B错误; 溶液吸收电石气中的
: ,故C错误;候氏制碱法:
,故D错误;故选A。
8. 高分子的循环利用过程如下图所示。下列说法错误的是(不考虑立体异构)
A. b生成a的反应属于加聚反应更多全科试卷,请关注公众号:高中试卷君
B. a中碳原子杂化方式为 和
C. a的链节与b分子中氢元素的质量分数不同
D. b与 发生加成反应最多可生成4种二溴代物
【答案】D
【解析】由a和b的结构简式可知,b生成a的反应属于加聚反应,A正确;a中含有苯环和甲基,碳原子
杂化方式为 和 ,B正确;a的链节为 ,a与b的分子式不同,但碳原子个数相同,氢
元素的质量分数不同,C正确;b中含有碳碳双键,可以和 发生1,2加成生成2种二溴代物,发生1,
4加成生成1种二溴代物,最多可生成3种二溴代物,D错误;故选D。
9. 某离子液体结构如下图所示。W、X、Y、Z原子序数依次增大,W、X和Y的原子序数之和为14,X
和Y基态原子的核外未成对电子数之和为5,Z是第四周期元素。下列说法错误的是
的
A. X、Z 简单氢化物均可溶于水 B. 电负性:
C. 第一电离能: D. W、Y、Z可形成既含离子键又含共价键的化合物
【答案】A
【解析】W、X、Y、Z原子序数依次增大,W、X和Y的原子序数之和为14,X和Y基态原子的核外未成
对电子数之和为5,W只连接了1个共价键,W为H元素;X连接4个共价键,X为C元素;Y连接3个
共价键,Y为N元素;Z带1个负电荷,是第四周期元素,则Z为Br元素。CH 难溶于水,HBr易溶于
4
水,故A错误;同周期主族元素,从左往右,电负性增大,电负性:N>C>H,故B正确;同周期元素,
从左往右,元素第一电离能有增大的趋势,则第一电离能: ,故C正确;H、N、Br可形成既含离子
键又含共价键的化合物NH Br,故D正确;故选A。
4
10. 镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,具有催化活性的是 ,图①和图②是晶胞的不同
切面。下列说法错误的是更多全科试卷,请关注公众号:高中试卷君
A. 催化活性:①>② B. 镍酸镧晶体的化学式为
C. 周围紧邻的O有4个 D. 和 的最短距离为
【答案】C
【解析】具有催化活性的是 ,图②中没有Ni原子,则催化活性:①>②,故A正确;镍酸镧电催化剂
立方晶胞中含有1个Ni, =3个O,8 =1个La,镍酸镧晶体的化学式为 ,故B正确;由
晶胞结构可知, 在晶胞体心,O在晶胞的棱心,则La周围紧邻的O有12个,故C错误;由晶胞结构
可知, 和 的最短距离为体对角线得一半,为 ,故D正确;故选C。
11. 如图,b为 标准氢电极,可发生还原反应( )或氧化反应(
),a、c分别为 、 电极。实验发现:1与2相连a电极质量减小,2与3相连c电极质量
增大。下列说法正确的是更多全科试卷,请关注公众号:高中试卷君
A. 1与2相连,盐桥1中阳离子向b电极移动
B. 2与3相连,电池反应为
C. 1与3相连,a电极减小的质量等于c电极增大的质量
为
D. 1与2、2与3相连,b电极均 流出极
【答案】B
【解析】1与2相连,左侧两池构成原电池,a电极质量减小, 转化为 ,说明a为正极,b为负
极,b极反应为 ;2与3相连,右侧两池构成原电池,c电极质量增大, 转化为 ,说
明c为负极,b为正极,b极反应为: ,据此分析。1与2相连,a为正极,b为负极,盐
桥1中阳离子向a电极移动,A错误;2与3相连,右侧两池构成原电池,c电极质量增大, 转化为
,说明c为负极,b为正极,生成氢气,电池反应为 ,B正确;1与3相
连,由于 更难溶, 转化为 ,a极为正极, 转化为 ,a极质量减小,b极为负极,
转化为 ,b极质量增加,a电极减小的质量小于c电极增大的质量,C错误;1与2相连,b为负
极,b电极为 流出极;2与3相连,c为负极,c电极为 流出极,D错误;故选B。
12. 实验室合成高铁酸钾( )的过程如下图所示。下列说法错误的是
A. 气体a的主要成分为
B. 沉淀b的主要成分为更多全科试卷,请关注公众号:高中试卷君
C. 中 的化合价为
D. 反应2为
【答案】B
【解析】高锰酸钾和浓盐酸反应生成氯气,氯气中混有HCl气体,通过饱和食盐水洗气除去HCl气体,得
到气体a的主要成分为 ,氯气和饱和KOH溶液在10-15℃条件下反应生成 ,由于 得溶解
度小于KOH,会析出 白色沉淀,将 和KOH加入饱和次氯酸钾中发生反应生成
,以此解答。由分析可知,气体a的主要成分为 ,故A正确;由分析可知,沉淀b的主要成分为
,故B错误;由化合物化合价的代数和为零可知, 中 的化合价为 ,故C正确;反应
2中 和 在碱性条件下发生氧化还原反应生成 和KCl,根据得失电子守恒和原子
守恒配平化学方程式为: ,故D正
确;故选B。
13. 下列各组实验所得结论或推论正确的是
实验现象 结论或推论
A 向某有机物( )中滴加 溶液,显色 该有机物分子中含酚羟基
B 向酸性高锰酸钾溶液中加入甲苯,紫色褪去 甲苯同系物均有此性质
C 向银氨溶液中滴加某单糖溶液,形成银镜 该糖属于还原糖
D 测得两溶液导电能力相同 两溶液物质的量浓度相等
【答案】C
【解析】有机物( )中只有5个碳原子,没有苯环,不可能含酚羟基,故A错误;只有与苯环直
接相连的碳原子上有氢原子时,才能被酸性高锰酸钾氧化,当该碳原子上没有氢原子时,就不能与酸性高
锰酸钾反应,故B错误;向银氨溶液中滴加某单糖溶液,形成银镜,说明其中含有醛基,该糖属于还原更多全科试卷,请关注公众号:高中试卷君
糖,故C正确;若两溶液中溶质带的电荷数不同,则两溶液导电能力相同,不能说明两溶液物质的量浓度
相等,故D错误;故选C。
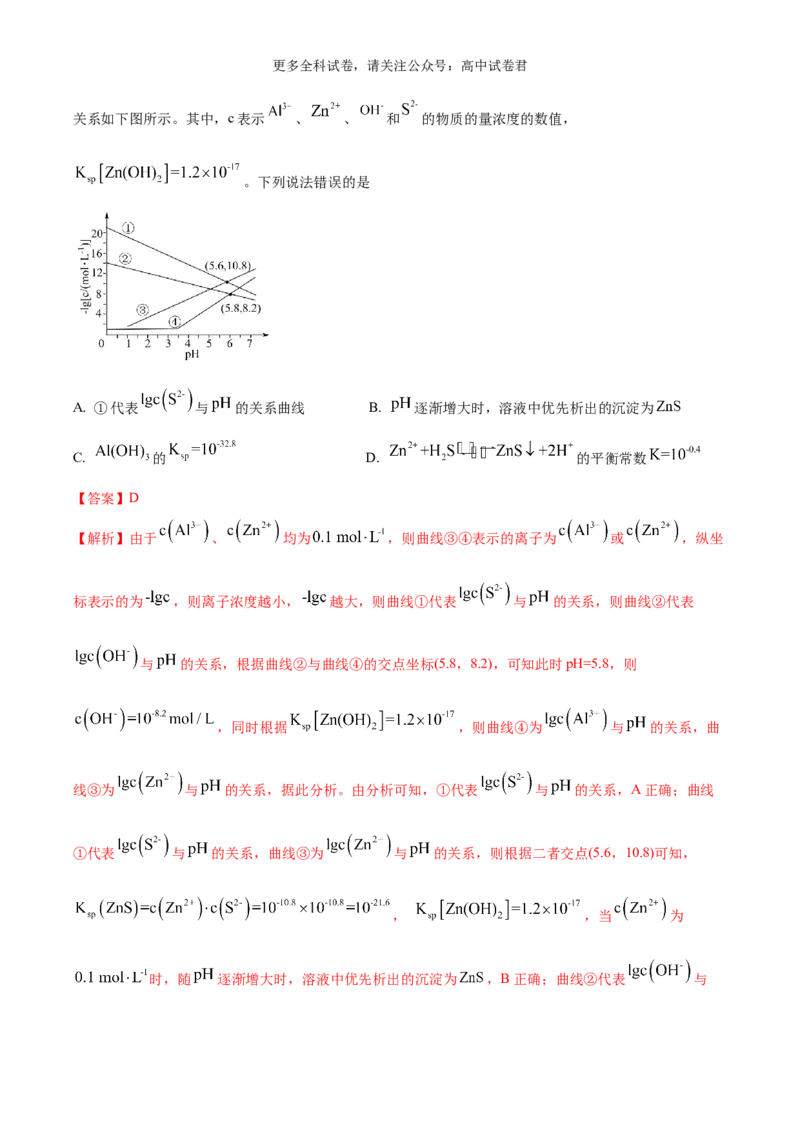
14. 某生物质电池原理如下图所示,充、放电时分别得到高附加值的醇和羧酸。下列说法正确的是
A. 放电时,正极电极反应为: +H O-2e-= +2H+
2
B. 放电时, 转化为
C. 充电时, 通过交换膜从左室向右室迁移
D. 充电时,阴极电极反应为: +2H O+2e-= +2OH-
2
【答案】D
【解析】放电时,负极发生氧化反应, 转化为 ,所以放电时,Rh/Cu是负极。充电
时,Rh/Cu是阴极。放电时,负极发生氧化反应,负极糠醛发生氧化反应生成 ,故A错误;放
电时,正极得电子, 转化为 ,故B错误;充电时,阳离子向阴极移动,
充电时,Rh/Cu是阴极, 通过交换膜从右室向左室迁移,故C错误;充电时,充电时,Rh/Cu 是阴极,
糠醛发生还原反应生成 ,阴极电极反应为 +2H O+2e-= +2OH-,故D正
2
确; 故选D。
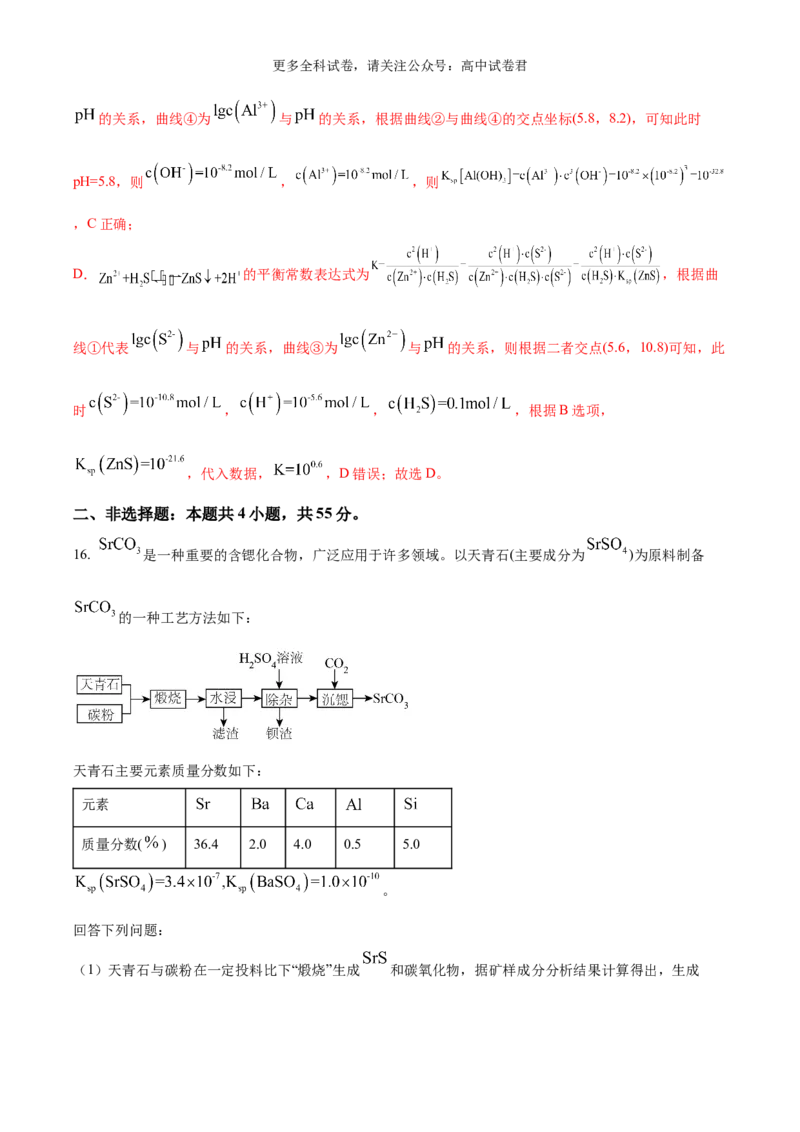
15. 室温下,向 、 均为 的混合溶液中持续通入 气体,始终保持 饱
和( 的物质的量浓度为 ),通过调节 使 、 分别沉淀,溶液中 与 的更多全科试卷,请关注公众号:高中试卷君
关系如下图所示。其中,c表示 、 、 和 的物质的量浓度的数值,
。下列说法错误的是
A. ①代表 与 的关系曲线 B. 逐渐增大时,溶液中优先析出的沉淀为
C. 的 D. 的平衡常数
【答案】D
【解析】由于 、 均为 ,则曲线③④表示的离子为 或 ,纵坐
标表示的为 ,则离子浓度越小, 越大,则曲线①代表 与 的关系,则曲线②代表
与 的关系,根据曲线②与曲线④的交点坐标(5.8,8.2),可知此时pH=5.8,则
,同时根据 ,则曲线④为 与 的关系,曲
线③为 与 的关系,据此分析。由分析可知,①代表 与 的关系,A正确;曲线
①代表 与 的关系,曲线③为 与 的关系,则根据二者交点(5.6,10.8)可知,
, ,当 为
时,随 逐渐增大时,溶液中优先析出的沉淀为 ,B正确;曲线②代表 与更多全科试卷,请关注公众号:高中试卷君
的关系,曲线④为 与 的关系,根据曲线②与曲线④的交点坐标(5.8,8.2),可知此时
pH=5.8,则 , ,则
,C正确;
D. 的平衡常数表达式为 ,根据曲
线①代表 与 的关系,曲线③为 与 的关系,则根据二者交点(5.6,10.8)可知,此
时 , , ,根据B选项,
,代入数据, ,D错误;故选D。
二、非选择题:本题共4小题,共55分。
16. 是一种重要的含锶化合物,广泛应用于许多领域。以天青石(主要成分为 )为原料制备
的一种工艺方法如下:
天青石主要元素质量分数如下:
元素
质量分数( ) 36.4 2.0 4.0 0.5 5.0
。
回答下列问题:
(1)天青石与碳粉在一定投料比下“煅烧”生成 和碳氧化物,据矿样成分分析结果计算得出,生成更多全科试卷,请关注公众号:高中试卷君
、 时失重率分别为 、 ,实际热重分析显示失重率为32.6%,则“煅烧”中主要生成的
碳氧化物为___________(填“ ”或“ ”)。
(2)“煅烧”过程中还可能产生少量对环境有危害的气体,化学式为___________和___________。
(3)“水浸”后滤渣的主要成分除 和C外,还有两种氧化物,化学式为___________和
___________。
(4)“水浸”时需加热, 与热水作用后的溶液呈碱性的主要原因为___________(用化学方程式表示)
(5)“水浸”后的滤液中 ,“除杂”过程中(忽略 溶
液引起的体积变化),为使 不沉淀,应控制溶液中 ___________ ,每升滤液中篇加
入 溶液的体积 ___________ 。
(6)“沉锶”过程中,可溶性 发生反应的离子方程式为___________。
【答案】(1)CO (2)CO SO (3)Al O SrO (4)SrS+2H O HS+Sr(OH)
2 2 2 3 2 2 2
(5)2×10-4 5×10-4 (6)Sr2++2OH-+CO =SrCO↓+H O
2 3 2
【解析】天青石与碳粉混合煅烧生成SrS和碳氧化物,水浸后滤液中加入硫酸,除去钡离子,过滤后滤液
中通入二氧化碳,生成碳酸锶。
(1)设生成的碳氧化物中CO 含量为x,则CO含量为1-x,则有0.304x+0.386(1-x)=0.326,解得x=73%,
2
因此煅烧中主要生成的碳氧化物为CO。
2
(2)煅烧过程中还可能生成少量对环境有危害的气体,天青石的主要成分为SrSO ,能生成的有害气体只
4
有SO ,碳粉能生成的有害气体只有CO,其他物质无法生成有害气体,则两种气体的化学式为SO 和
2 2
CO。
(3)天青石中含有Ba、Ca、Al和Si,已知Ba元素通过后续加入硫酸除去,Ca转化为硅酸钙,则Al转化
为Al O,同时Sr也会生成SrO,两种氧化物为Al O 和SrO。
2 3 2 3
(4)SrS溶于水电离出的硫离子水解生成氢氧根离子,使溶液呈碱性,化学方程式为SrS+2H O
2
HS+Sr(OH) 。
2 2更多全科试卷,请关注公众号:高中试卷君
(5)根据K (SrSO )=3.4×10-7可知,SrSO 开始沉淀时,硫酸根离子浓度为3.4×10-7÷0.68=5×10-
sp 4 4
7mol/L。为使Sr2+不沉淀,硫酸根离子浓度需小于5×10-7mol/L,则钡离子浓度需大于1×10-10÷(5×10-7)
=2×10-4mol/L,为使Sr2+不沉淀,硫酸根离子浓度需小于5×10-7mol/L,则每升滤液中含有硫酸根离子
5×10-7mol,需要加入1mol/L的硫酸的体积小于等于5×10-4mL。
(6)沉锶过程中,可溶性Sr(OH) 溶液与二氧化碳反应生成碳酸锶沉淀和水,离子方程式为Sr2++2OH-
2
+CO =SrCO↓+H O。
2 3 2
17. 芳基亚胺酯是重要的有机反应中间体,受热易分解,可由腈在酸催化下与醇发生Pinner反应制各,原
理如下图所示。
某实验小组以苯甲腈( , )和三氟乙醇( , ) 为原料合成苯甲亚
胺三氟乙脂。步骤如下:
I.将 苯甲腈与 三氟乙醇置于容器中,冰浴降温至 。
Ⅱ.向容器中持续通入 气体4小时,密封容器。
Ⅲ.室温下在 氛围中继续搅拌反应液24小时,冷却至 ,抽滤得白色固体,用乙腈洗涤。
IV.将洗涤后的白色固体加入饱和 溶液中,低温下反应,有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水 ,过滤,蒸去溶剂得产品 。
回答下列问题:
(1)实验室中可用浓盐酸和无水 制备干燥 气体,下列仪器中一定需要的为__________(填仪
器名称)。
(2)第Ⅱ步通气完毕后,容器密封的原因为__________。
(3)第Ⅲ步中得到的白色固体主要成分为__________。更多全科试卷,请关注公众号:高中试卷君
(4)第IV步中选择低温的原因为__________。
(5)第IV步萃取时可选用的有机溶剂为__________。
A. 丙酮 B. 乙酸 C. 乙酸乙酯 D. 甲醇
(6)第V步中无水 的作用为____________________。
(7)本实验的产率为__________。
【答案】(1)恒压滴液漏斗 (2)保证不漏液、不漏气 (3)C (4)防止芳基亚胺酯受热分解
(5)C (6)除去有机相中的水 (7)50%
【解析】由反应原理可知, 先在HCl的气体中反应转化为 , 再和
反应生成 , 和碳酸钠溶液反应生成芳基亚胺酯。
(1)实验室中可用浓盐酸和无水CaCl 制备干燥HCl气体,需要用到恒压滴液漏斗,不需要球形冷凝管、
2
容量瓶和培养皿。
(2)该反应过程中涉及到HCl气体,需要考虑不能有气体漏出,第Ⅱ步通气完毕后,容器密封的原因为保
证不漏液、不漏气。
(3)由反应原理可知, 先在HCl的气体中反应转化为 , 再和
反应生成 ,故选C。
(4)芳基亚胺酯受热易分解,第IV步中选择低温的原因为:防止芳基亚胺酯受热分解。
(5)苯甲亚胺三氟乙脂属于酯类,在乙酸乙酯中的溶解度较大,乙酸和甲酸能溶于水,不能用来萃取,
第IV步萃取时可选用的有机溶剂为乙酸乙酯中,故选C。
(6)第V步中无水MgSO 的作用为除去有机相中的水。
4
(7)实验中 苯甲腈的物质的量为 =0.2mol,21.6g三氟乙醇的物质的量为更多全科试卷,请关注公众号:高中试卷君
=0.216mol,由流程图可知,理论上可以制备0.2mol苯甲亚胺三氟乙脂,本实验的产率为
=50%。
18. 天然气、石油钻探过程会释放出CO、HS等气体。某种将CO 和HS共活化的工艺涉及反应如下:
2 2 2 2
①
②
③
④
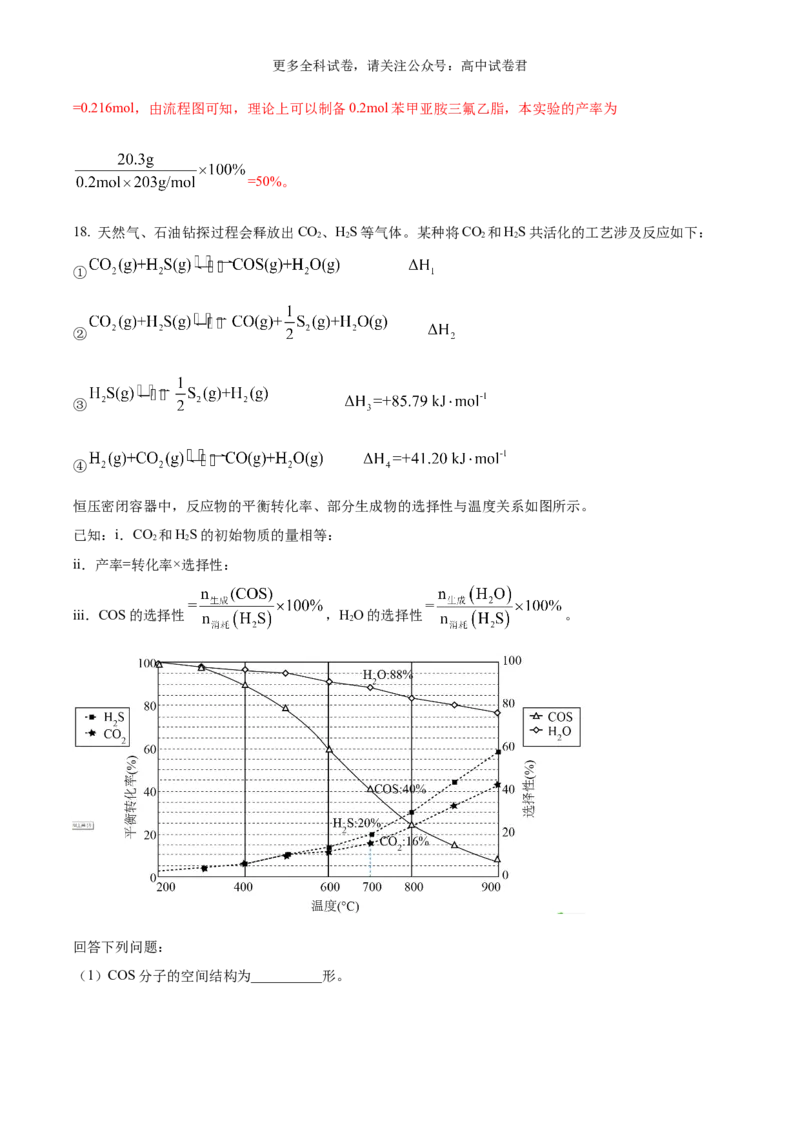
恒压密闭容器中,反应物的平衡转化率、部分生成物的选择性与温度关系如图所示。
已知:i.CO 和HS的初始物质的量相等:
2 2
ii.产率=转化率×选择性:
iii.COS的选择性 ,HO的选择性 。
2
回答下列问题:
(1)COS分子的空间结构为__________形。更多全科试卷,请关注公众号:高中试卷君
(2) _________ 。
(3)以下温度,COS的产率最高的是__________。
A. B. C. D.
(4)温度高于500℃时,HS的转化率大于CO,原因是____________________。
2 2
(5)可提高S 平衡产率的方法为__________。
2
A. 升高温度 B. 增大压强 C. 降低温度 D. 充入氩气
(6)700℃时反应①的平衡常数K=__________(精确到0.01)。
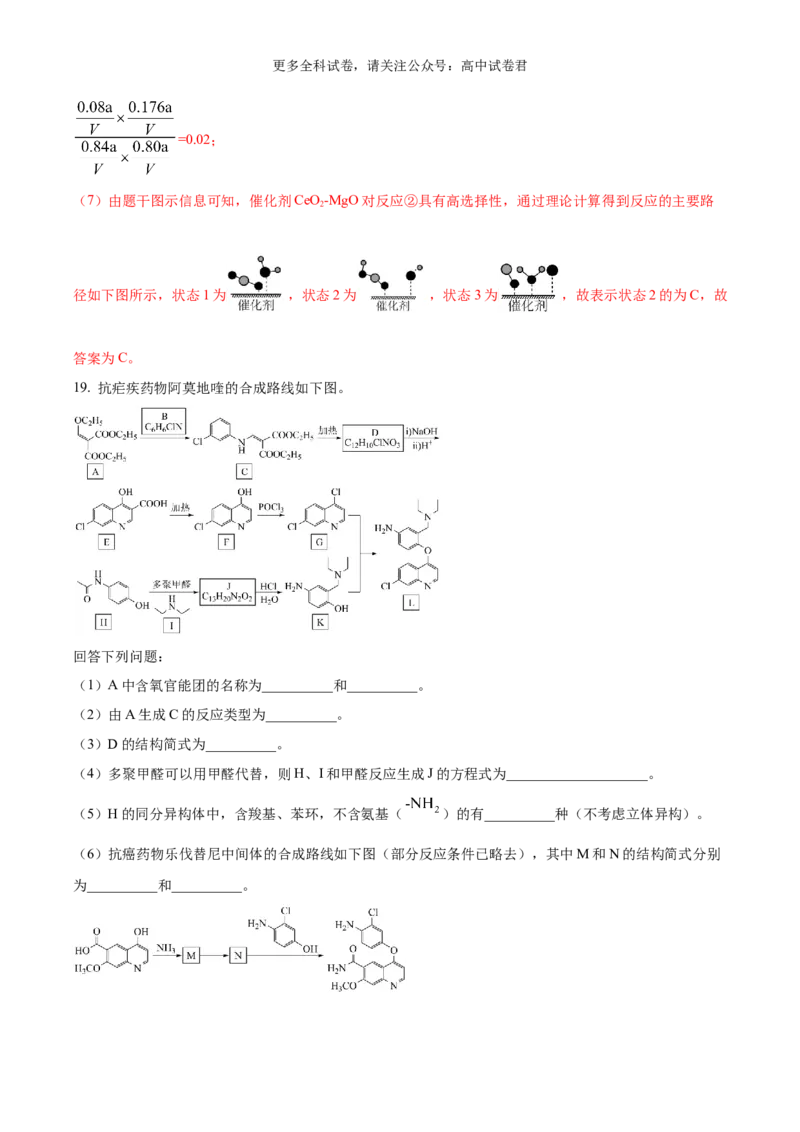
(7)催化剂CeO-MgO对反应②具有高选择性,通过理论计算得到反应的主要路径如下图所示。表示状
2
态2的为__________。
A. B. C.
【答案】(1)直线 (2)+126.99kJ/mol (3)B
(4)当温度高于500℃时,发生副反应③正向移动的幅度大于反应④ (5)AD
(6)0.02 (7)C
【解析】
(1)COS分子的中心原子C周围的价层电子对数为:2+ =2,根据价层电子对互斥理论可知,
该分子的空间结构为直线形,故答案为:直线;
(2)由题干信息可知,反应③ ;反应④更多全科试卷,请关注公众号:高中试卷君
,则由反应③+④可得反应②
,根据盖斯定律可知, =(+85.79kJ/mol)
+(+41.20kJ/mol)=+126.99kJ/mol,故答案为:+126.99kJ/mol;
(3)由题干信息可知,产率=转化率×选择性,结合题干图示信息可知:400℃时HS转化率为5%左右,
2
COS的选择性为:90%,则产率为5%×90%=4.5%,600℃时HS转化率为15%左右,COS的选择性为:
2
60%,则产率为15%×60%=9.0%,800℃时HS转化率为30%左右,COS的选择性为:25%,则产率为
2
30%×25%=7.5%,1000℃时HS转化率为58%左右,COS的选择性为:7%,则产率为58%×7%=4.06%,
2
故COS的产率最高的是600℃,故答案为:B;
(4)由题干图示信息可知,温度低于500℃时HS和CO 的转化率基本相同,说明此时反应只发生反应
2 2
①、②,而温度升高,反应①、②、③、④均正向移动,当温度高于500℃时,发生副反应③正向移动的
幅度大于反应④,导致HS的转化率大于CO,故答案为:当温度高于500℃时,发生副反应③正向移动
2 2
的幅度大于反应④;
(5)由题干信息可知,② >0 ③
两个反应均为正反应是一个气体体积增大的吸热反应:
A.升高温度 ,上述平衡正向移动,S 的平衡产率提高,A符合题意;
2
B.增大压强,上述平衡逆向移动,S 的平衡产率降低,B不合题意;
2
C.降低温度,上述平衡逆向移动,S 的平衡产率降低,C不合题意;
2
D.恒压下充入氩气,相当于减小压强,上述平衡正向移动,S 的平衡产率提高,D符合题意;
2
故答案为:AD;
(6)由题干图示信息可知,700℃时HS的平衡转化率为20%,CO 的平衡转化率为16%,COS的选择性
2 2
为40%,HO的选择性为88%,假设起始投入的CO 和HS的物质的量均为amol,则平衡时CO 的物质的
2 2 2 2
量为:a(1-16%)mol=0.84amol,HS的物质的量为:a(1-20%)mol=0.8amol,COS的物质的量为:
2
a×20%×40%mol=0.08amol,HO的物质的量为:a×20%×88%mol=0.176amol,反应①的平衡常数K==
2更多全科试卷,请关注公众号:高中试卷君
=0.02;
(7)由题干图示信息可知,催化剂CeO-MgO对反应②具有高选择性,通过理论计算得到反应的主要路
2
径如下图所示,状态1为 ,状态2为 ,状态3为 ,故表示状态2的为C,故
答案为C。
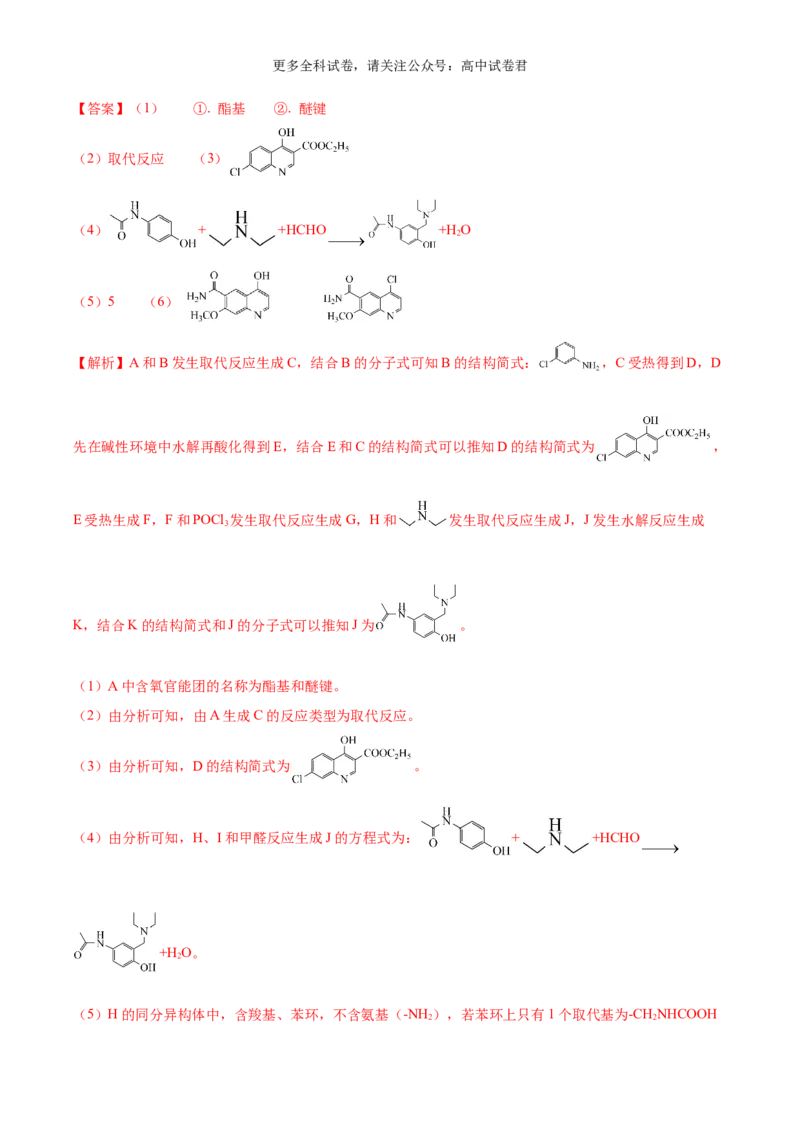
19. 抗疟疾药物阿莫地喹的合成路线如下图。
回答下列问题:
(1)A中含氧官能团的名称为__________和__________。
(2)由A生成C的反应类型为__________。
(3)D的结构简式为__________。
(4)多聚甲醛可以用甲醛代替,则H、I和甲醛反应生成J的方程式为____________________。
(5)H的同分异构体中,含羧基、苯环,不含氨基( )的有__________种(不考虑立体异构)。
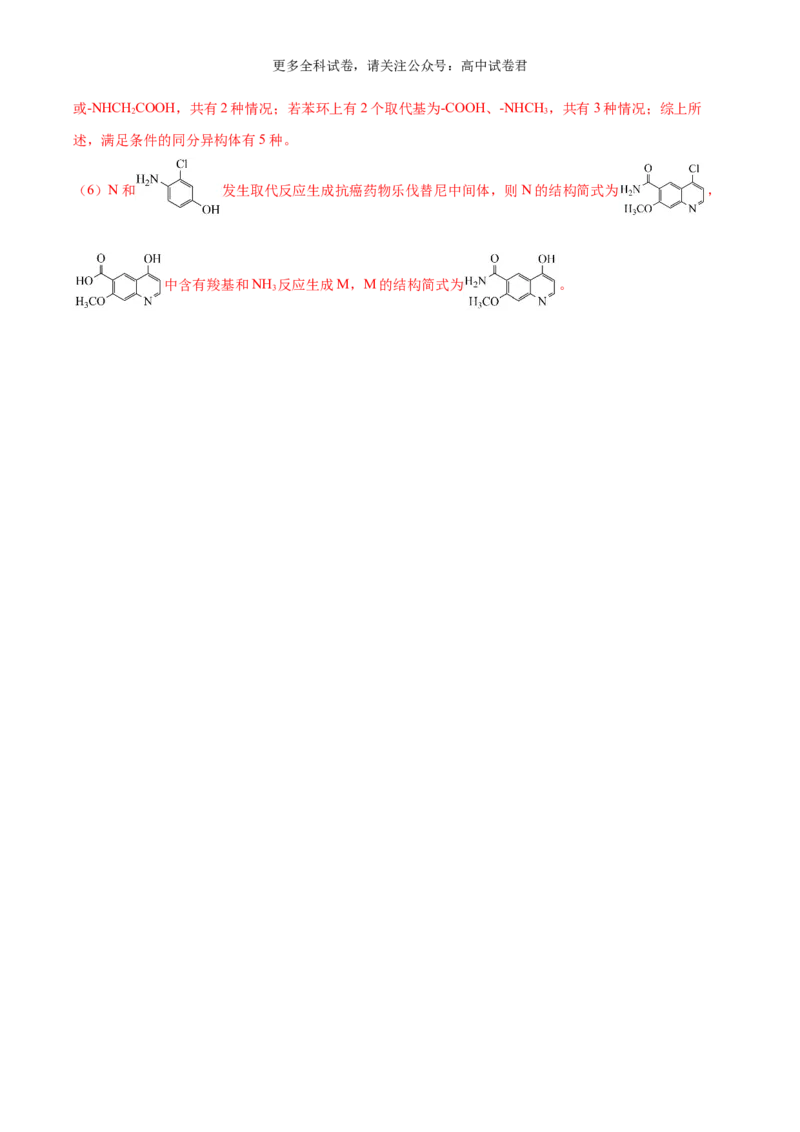
(6)抗癌药物乐伐替尼中间体的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别
为__________和__________。更多全科试卷,请关注公众号:高中试卷君
【答案】(1) ①. 酯基 ②. 醚键
(2)取代反应 (3)
(4) + +HCHO +H O
2
(5)5 (6)
【解析】A和B发生取代反应生成C,结合B的分子式可知B的结构简式: ,C受热得到D,D
先在碱性环境中水解再酸化得到E,结合E和C的结构简式可以推知D的结构简式为 ,
E受热生成F,F和POCl 发生取代反应生成G,H和 发生取代反应生成J,J发生水解反应生成
3
K,结合K的结构简式和J的分子式可以推知J为 。
(1)A中含氧官能团的名称为酯基和醚键。
(2)由分析可知,由A生成C的反应类型为取代反应。
(3)由分析可知,D的结构简式为 。
(4)由分析可知,H、I和甲醛反应生成J的方程式为: + +HCHO
+H O。
2
(5)H的同分异构体中,含羧基、苯环,不含氨基(-NH ),若苯环上只有1个取代基为-CHNHCOOH
2 2更多全科试卷,请关注公众号:高中试卷君
或-NHCHCOOH,共有2种情况;若苯环上有2个取代基为-COOH、-NHCH,共有3种情况;综上所
2 3
述,满足条件的同分异构体有5种。
(6)N和 发生取代反应生成抗癌药物乐伐替尼中间体,则N的结构简式为 ,
中含有羧基和NH 反应生成M,M的结构简式为 。
3