文档内容
第一章 物质及其变化
第二节 离子反应
第2课时 离子反应
一、选择题
1.下列各组离子在溶液中可以大量共存的是( )
A.Al3+、NH 、OH-、CO B.H+、Ca2+、CO 、Cl-
C.Ba2+、Na+、SO 、NO D.K+、Na+、SO 、Cl-
【答案】D
【解析】A.Al3+、NH 均能和OH-发生离子反应,不能大量共存,另外Al3+和CO 也能发生双水解反应,
不能大量共存,故A错误;
B.H+、Ca2+均能和CO 发生离子反应,不能大量共存,故B错误;
C.Ba2+和SO 发生离子反应,不能大量共存,故C错误;
D.K+、Na+、SO 、Cl-彼此间不发生离子反应,能大量共存,故D正确。
2.下列反应的离子方程式书写正确的是( )
A.Fe与盐酸反应:Fe + 2H+= Fe2++ H ↑
2
B.大理石与稀硝酸反应:CO2-+ 2H+= CO↑+ H O
3 2 2
C.Ba(OH) 溶液与稀硫酸反应:H++ OH-= H O
2 2
D.铜与硝酸银溶液反应:Cu + Ag+= Cu2++ Ag
【答案】A
【解析】A.Fe与盐酸反应生成氯化亚铁和氢气,Fe、氢气写化学式:Fe+2H+=Fe2++ H ↑,离子方程式正确,
2
A正确;
B.大理石与稀硝酸反应,大理石为碳酸钙,为沉淀,写化学式:CaCO +2H+=Ca2++CO ↑+ H O,离子方程式
3 2 2
错误,B错误;
C.Ba(OH) 溶液与稀硫酸反应生成硫酸钡沉淀和水,Ba2++2H++ SO 2-+2OH-=2H O+ BaSO ,离子方程式错误,
2 4 2 4
C错误;D.铜与硝酸银溶液反应:Cu +2Ag+=Cu2++2Ag,离子方程式错误,D错误;答案为A。
3.下列说法正确的是
A.离子反应中反应物和生成物都是离子
B.有单质参加或生成的反应一定属于氧化还原反应
C.金属氧化物不一定是碱性氧化物,酸酐不一定是酸性氧化物
D.金属单质只能做还原剂,非金属单质只能做氧化剂
【答案】C
【解析】A.有离子参加的反应是离子反应,离子反应中反应物和生成物不一定都是离子,如Fe+Cu2+=Fe2+
+Cu,故A错误;
B.有化合价变化的反应是氧化还原反应,有单质参加或生成的反应不一定属于氧化还原反应,如
3O=2O ,故B错误;
2 3
C.金属氧化物不一定是碱性氧化物,如NaO;酸酐不一定是酸性氧化物,醋酸酐不是酸性氧化物,故C
2 2
正确;
D.非金属单质既能做氧化剂又能做还原剂,如氢氧化钠和氯气反应生成次氯酸钠、氯化钠、水,氯气既
是氧化剂又是还原剂,故D错误;答案选C。
4.下列离子方程式的书写正确的是( )
A.实验室用大理石和稀盐酸制取CO:2H++CO 2-===CO ↑+H O
2 3 2 2
B.钠与水反应:Na+2HO=Na++2OH-+H ↑
2 2
C.将稀硫酸滴在铜片上: Cu+2H+=Cu2++H ↑
2
D.NaHCO 溶液与NaOH溶液反应:OH﹣+ HCO -=== CO 2-+H O
3 3 3 2
【答案】D
【解析】A. 大理石是碳酸钙,不溶于水,不能拆成离子形式,故离子方程式2H++CO 2-===CO ↑+H O是错
3 2 2
误的,故错误;
B. 电荷不守恒,应为:2Na+2HO=2Na++2OH-+H ↑,A项错误;
2 2
C. 铜与稀硫酸不反应,故错误;
D. NaHCO 溶液与NaOH溶液反应生成碳酸钠和水,离子方程式为:OH﹣+ HCO -= CO2-+H O,故正确。
3 3 3 2
故选D。
5.在含有大量H+、Ba2+、Cl-的溶液中,还可能大量共存的离子是( )
A.Ag+ B.K+ C. D.
【答案】B
【解析】A.Ag+与Cl-会发生反应生成AgCl沉淀,不能大量共存,A不合题意;B.K+与H+、Ba2+、Cl-都不反应,能大量共存,B符合题意;
C. 与Ba2+会发生反应生成BaCO 沉淀,不能大量共存,C不合题意;
3
D. 与Ba2+会发生反应生成BaSO 沉淀,不能大量共存,D不合题意;故选B。
4
6.下列各组离子在无色溶液中能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】C
【解析】A. 、 反应生成水和 ,故A不符合题意;
B. 在溶液中呈黄色,故B不符合题意;
C. 、 、 、 互不反应,在溶液中可以大量共存,故C符合题意;
D. 、 反应生成二氧化碳和水, 、 生成沉淀, 、 生成微溶物,故D不符合题
意。答案为C。
7.在某无色透明的酸性溶液中,能共存的离子组是
A.Na+、K+、 、 B.Cu2+、K+、Cl-、
C.Na+、K+、Cl-、 D.Ba2+、K+、 、Cl-
【答案】C
【解析】A.酸性溶液中存在大量H+,H+与 会发生复分解反应,不能大量共存,故A不符合题意;
B.含Cu2+的溶液呈蓝色,故B不符合题意;
C.离子之间均不发生反应,能够大量共存,故C符合题意;
D.Ba2+与 能够发生复分解反应,不能大量共存,故D不符合题意;故答案为:C。
8.下列离子方程式书写正确的是( )
A.铁和硝酸银溶液反应 Fe+3Ag+=3Ag+Fe3+B.氢氧化铜与硫酸溶液反应 OH-+H+=H O
2
C.碳酸钙与盐酸溶液反应:CaCO +2H+=Ca2++HO+CO↑
3 2 2
D.铁与稀硫酸反应 2Fe+6H+=2Fe3++3H↑
2
【答案】C
【解析】A. 铁和硝酸银溶液反应生成硝酸亚铁,离子方程式为:Fe+2Ag+=2Ag+Fe2+,A错误;
B. 氢氧化铜不溶于水,应该用化学式表示,离子方程式为:Cu(OH) +2H+= Cu2++2H O, B错误;
2 2
C. 碳酸钙难溶于水的,用化学式表示,离子方程式为:CaCO +2H+=Ca2++HO+CO↑,C正确;
3 2 2
D. 铁与稀硫酸反应生成硫酸亚铁,离子方程式为:Fe+2H+=Fe2++H↑,D错误。答案选C。
2
9.能用H+ + OH- = H O 表示的是( )
2
A.Ba(OH) 溶液和稀硫酸的反应 B.NaOH溶液和稀硫酸的反应
2
C.Cu(OH) 和稀HNO 的反应 D.Ba(OH) 溶液NaHSO 溶液的反应
2 3 2 4
【答案】B
【解析】H++OH-=H O表示强酸与可溶性强碱生成可溶性盐的中和反应,并且溶液中仅存在H+和OH-的反
2
应。
A.Ba(OH) 溶液和稀硫酸的反应中钡离子和硫酸根离子会产生硫酸钡沉淀,此反应一定要写入方程中,故
2
A不符合题意;
B.NaOH溶液和稀硫酸的反应生成水和硫酸钠,溶液中仅存在H+和OH-的反应,钠离子和硫酸根离子不
反应,离子反应方程式为:H+ + OH- = H O,故B符合题意;
2
C.Cu(OH) 和稀HNO 的反应中Cu(OH) 难溶于水,与稀HNO 的反应的离子方程式为Cu(OH) +2H+=Cu2+
2 3 2 3 2
+2H O,故C不符合题意;
2
D.Ba(OH) 溶液NaHSO 溶液的反应中钡离子和硫酸根离子会产生硫酸钡沉淀,此反应过程要写入方程中,
2 4
故D不符合题意;答案选B。
10.下列实验过程中产生的现象与图形相符合的是( )
A.稀硫酸滴加到 B a (O H) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
B.铁粉加到一定量 CuSO 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
4
C.CO 通入一定量 NaOH 溶液中(横坐标是 CO 的体积,纵坐标为溶液的导电能力)
2 2D.稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
【答案】A
【解析】A. 滴入的硫酸与氢氧化钡反应,生成硫酸钡沉淀和水,溶液中离子浓度减少,导电能力下降,恰
好完全反应导电性变为零,再随着稀硫酸的滴入,溶液导电能力增加,直到变为定值,所以A选项是正确
的;
B.铁粉加到一定量CuSO 溶液中发生反应Fe+CuSO=FeSO+Cu,根据方程式知每当消耗56g铁,生成64g
4 4 4
固体,所以固体的质量一直在增加,而图象中的固体的质量先变小后变大,故B错误;
C. CO 通入一定量NaOH溶液中,发生的化学反应是CO+2NaOH=Na CO+H O、NaCO+H O +CO =
2 2 2 3 2 2 3 2 2
2NaHCO ,根据方程式知钠离子浓度基本不变,所以导电能力基本不变,故C错误;
3
D. HCl+NaOH=NaCl+H O,氢氧化钠和氯化钠都是强电解质,在水中完全电离,所以钠离子的物质的量不
2
变,而图象中的钠离子先变小后变大,故D错误。所以A选项是正确的。
二、非选择题
11.(1)书写下列反应的离子方程式
①NaOH溶液和HSO 溶液:___________________________;
2 4
②NaCl溶液和AgNO 溶液:___________________________;
3
③Ba(OH) 溶液和HSO 溶液:_________________________;
2 2 4
④Fe与CuSO 溶液反应:______________________________;
4
⑤NaCO 溶液与Ca(OH) 溶液反应: ___________________。
2 3 2
(2)写出下列离子方程式表示的化学方程式。
①CO2-+2H+=CO ↑+HO_________________________;
3 2 2
②Ag++Cl-=AgCl↓________________________________;
③Cu2++2OH-=Cu(OH) ↓__________________________;
2
④SO +2OH-=SO2-+HO___________________________;
2 3 2
⑤Fe O+6H+=2Fe3++3HO_______________________;
2 3 2
⑥Ba2++2OH-+CO=BaCO ↓+HO_______________;
2 3 2
⑦Ba2++SO 2-=BaSO ↓____________________________;
4 4
⑧Fe(OH) +3H+=Fe3++3HO_______________________。
3 2
【答案】(1)H++OH-=HO Ag++Cl-=AgCl↓ Ba2++2OH-+2H++SO 2-=BaSO↓+2HO Fe+Cu2+
2 4 4 2
=Cu+Fe2+ CO2-+Ca2+=CaCO ↓
3 3
(2)Na CO+2HNO=CO ↑+HO+2NaNO AgNO+NaCl=AgCl↓+NaNO Cu(NO )+2NaOH=Cu(OH) ↓
2 3 3 2 2 3 3 3 3 2 2
+2NaNO SO +2NaOH=Na SO +HO Fe O+6HNO=2Fe(NO)+3HO Ba(OH) +CO=BaCO ↓+HO
3 2 2 3 2 2 3 3 3 3 2 2 2 3 2Ba(NO )+NaSO =BaSO ↓+2NaNO Fe(OH) +3HNO=Fe(NO)+3HO
3 2 2 4 4 3 3 3 3 3 2
【解析】 (1) ① NaOH溶液和HSO 溶液反应生成硫酸钠和水,离子方程式为H++OH-=HO;
2 4 2
②NaCl溶液和AgNO 溶液反应生成AgCl沉淀和硝酸钠,离子方程式为Ag++Cl-=AgCl↓;
3
③Ba(OH) 溶液和HSO 溶液反应生成硫酸钡沉淀和水,离子方程式为Ba2++2OH-+2H++SO 2-=
2 2 4 4
BaSO↓+2HO;
4 2
④Fe与CuSO 溶液反应生成FeSO 和Cu,离子方程式为Fe+Cu2+=Cu+Fe2+;
4 4
⑤NaCO 溶液与Ca(OH) 溶液反应生成CaCO 沉淀和NaOH,离子方程式为CO2-+Ca2+=CaCO ↓。
2 3 2 3 3 3
(2)①CO2-+2H+=CO ↑+HO可以表示碳酸钠与硝酸的反应,化学方程式为NaCO+2HNO=CO ↑+HO
3 2 2 2 3 3 2 2
+2NaNO ;
3
②Ag++Cl-=AgCl↓可以表示硝酸银溶液与氯化钠溶液的反应,化学方程式为AgNO+NaCl=AgCl↓+
3
NaNO ;
3
③Cu2++2OH-=Cu(OH) ↓可以表示硝酸铜溶液与氢氧化钠溶液的反应,化学方程式为Cu(NO )+
2 3 2
2NaOH=Cu(OH) ↓+2NaNO ;
2 3
④SO +2OH-=SO2-+HO可以表示SO 与强碱NaOH溶液的反应,化学方程式为SO +2NaOH=Na SO
2 3 2 2 2 2 3
+HO;
2
⑤Fe O+6H+=2Fe3++3HO可以表示氧化铁与强酸硝酸的反应,化学方程式为Fe O+6HNO=2Fe(NO)
2 3 2 2 3 3 3 3
+3HO;
2
⑥Ba2++2OH-+CO=BaCO ↓+HO可以表示氢氧化钡溶液与二氧化碳的反应,化学方程式为Ba(OH) +
2 3 2 2
CO=BaCO ↓+HO;
2 3 2
⑦Ba2++SO 2-=BaSO ↓可以表示硝酸钡溶液与硫酸钠溶液的反应,化学方程式为Ba(NO )+
4 4 3 2
NaSO =BaSO ↓+2NaNO ;
2 4 4 3
⑧Fe(OH) +3H+=Fe3++3HO可以表示氢氧化铁与硝酸溶液的反应,化学方程式为Fe(OH) +
3 2 3
3HNO=Fe(NO)+3HO。
3 3 3 2
12. 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和NaSO 溶液将这三种离子逐一沉淀分离。其
2 4
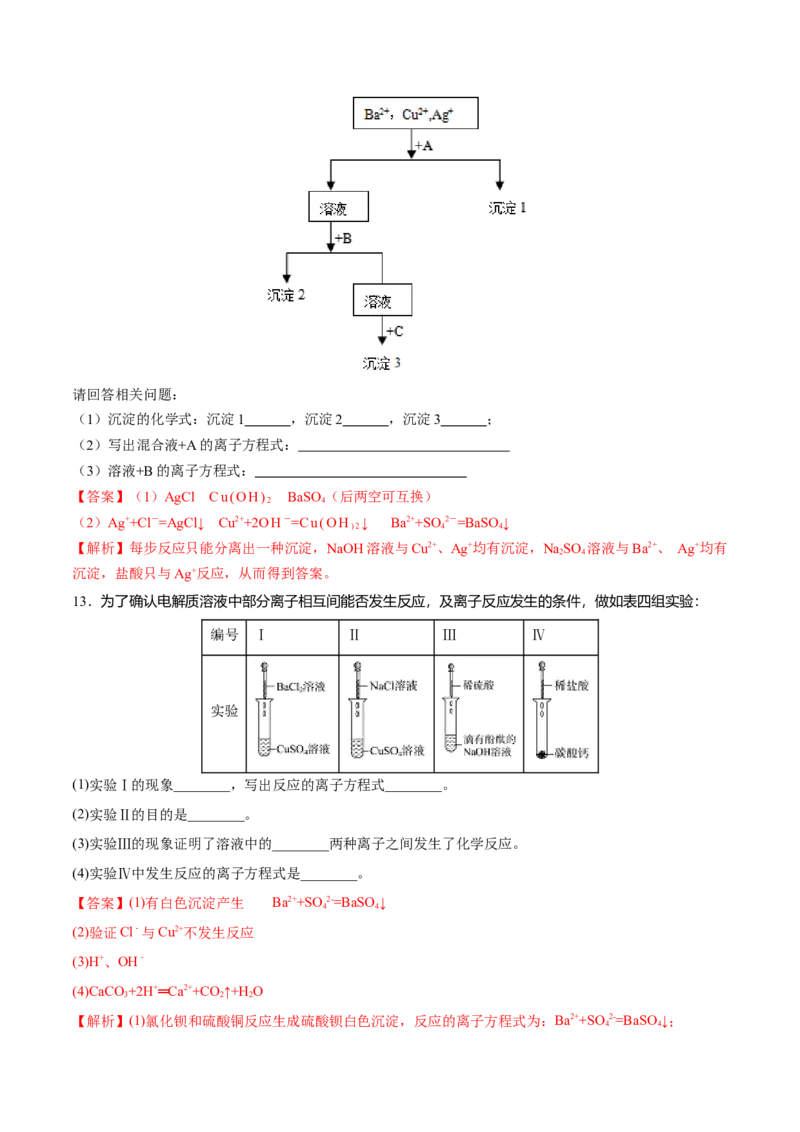
流程图如右图所示。请回答相关问题:
(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式:
(3)溶液+B的离子方程式:
【答案】(1)AgCl Cu(OH) BaSO(后两空可互换)
2 4
(2)Ag++Cl-=AgCl↓ Cu2++2OH-=Cu(OH ↓ Ba2++SO 2-=BaSO↓
)2 4 4
【解析】每步反应只能分离出一种沉淀,NaOH溶液与Cu2+、Ag+均有沉淀,NaSO 溶液与Ba2+、 Ag+均有
2 4
沉淀,盐酸只与Ag+反应,从而得到答案。
13.为了确认电解质溶液中部分离子相互间能否发生反应,及离子反应发生的条件,做如表四组实验:
编号 Ⅰ Ⅱ Ⅲ Ⅳ
实验
(1)实验Ⅰ的现象________,写出反应的离子方程式________。
(2)实验Ⅱ的目的是________。
(3)实验Ⅲ的现象证明了溶液中的________两种离子之间发生了化学反应。
(4)实验Ⅳ中发生反应的离子方程式是________。
【答案】(1)有白色沉淀产生 Ba2++SO2-=BaSO ↓
4 4
(2)验证Cl﹣与Cu2+不发生反应
(3)H+、OH﹣
(4)CaCO+2H+═Ca2++CO ↑+H O
3 2 2
【解析】(1)氯化钡和硫酸铜反应生成硫酸钡白色沉淀,反应的离子方程式为:Ba2++SO2-=BaSO ↓;
4 4(2)实验Ⅰ溶液中还存在氯离子和铜离子,实验Ⅱ可验证Cl-与Cu2+不发生反应;
(3)发生中和反应,溶液由红色变为无色,说明H+、OH-发生反应;
(4)盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,反应的离子方程式为CaCO +2H+═Ca2++CO ↑+H O。
3 2 2