文档内容
山东省名校联盟2024-2025学年高一下学期3月校际联考
化学试题(A)
一、单选题
1.人类对能源的利用正在向新能源方向高质量发展。下列有关能源的叙述错误的是
A.太阳能、风能均属于可再生能源 B.铝—空气海洋电池将化学能转化为电能
C.燃料电池将热能转化为电能 D.太阳能光解水可制氢
2.许多核素有重要的用途,下列对应正确的组合是
①考古中推断生物体的存在年代: ②相对原子质量的标准原子:
③核反应堆的燃料: ④确定磷在植物中的作用部位:
⑤制造氢弹: 、
A.①②③ B.①③④ C.①②③④ D.①②③④⑤
3.下列化学用语表述正确的是
A.次氯酸的电子式: B.氯原子的结构示意图:
C.甲烷分子的空间结构示意图: D.HCl的形成过程:
4.某物质结构式如图所示,其中短周期元素X、Y、Z、Q、W原子的半径依次增大,X、Q、W分别位于
不同的周期,X和W同主族但不相邻,Y和Q最外层电子数之和是Z原子L层电子数的二倍,下列说法正
确的是A.水玻璃是一种含有W元素的强电解质
B.Q的单质一定不导电
C.简单氢化物的稳定性和沸点均为:Y高于Q
D.与Y同主族下一周期元素的氧化物对应的水化物一定是强酸
5.下列实验装置正确且能达到对应实验目的的是
A.验证NaCO 固体遇水放热 B.H 和Cl 反应
2 3 2 2
C.将萃取碘水后的上层液体从下口流出 D.证明非金属性:Cl>C>Si
A.A B.B C.C D.D
6.“类比”是预测物质结构、性质与化学反应的重要方法之一,下列有关类比合理的是
A.铊(Tl)与铝同主族,其氢氧化物既能与盐酸反应又能与氢氧化钠溶液反应
B.Na在空气中加热能生成NaO,则Li在空气中加热也能生成LiO
2 2 2 2
C.CO 和强碱反应生成盐和水,则SiO 也能和强碱反应生成盐和水
2 2
D.向AlCl 溶液中滴加NaOH溶液先生成白色沉淀后沉淀溶解,则滴加浓氨水也能出现相同现象
3
7.工业上可用焦炭在电炉中还原二氧化硅得到粗硅,下列说法正确的是
A.SiO 既能与NaOH溶液反应又能与HF反应,属于两性氧化物
2
B.Si可用作半导体材料,SiO 可用来制造光导纤维
2
C.炼粗硅的化学方程式为
D.通过炼粗硅的化学反应可以证明非金属性:C>Si
8.氢气燃烧生成水蒸气的能量变化如图所示。下列说法正确的是A.H 燃烧放出能量是因为氢气的能量大于HO的能量
2 2
B.吸热反应都需要加热,放热反应都不需要加热
C.断开1molH-O键吸收930kJ的能量
D.H 和O 生成1molH O(l)释放的能量大于245kJ
2 2 2
9.X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层电子数之和为18,Y原子最外层的电子
数为4,Z和Q同族,Z的原子序数是Q的一半,W元素的焰色试验呈黄色。下列说法错误的是
A.Y、Z对应的单质都有同素异形体
B.X、Q两种元素组成的化合物有还原性
C.Z、W两种元素组成的化合物能与水反应
D.X可能为H或Li,它们所在族的元素称为碱金属元素
10.为早日实现“碳中和碳达峰”目标,科学家提出用钌(Ru)基催化剂催化CO(g)和H(g)反应生成
2 2
HCOOH。反应机理如图所示。
已知:生成46g液态HCOOH时放出31.2kJ的热量。
下列说法正确的是
A.反应历程中存在极性键、非极性键的断裂与形成
B.物质I为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.上述物质中HO和CO 都是直线形分子
2 2
D.通过CO(g)和H(g)反应制备液态HCOOH,每转移1mole-,放出31.2kJ的热量
2 2
11.为回收利用含I 的CCl 废液,某化学兴趣小组设计方案如下,下列说法错误的是
2 4A.萃取过程中放气的操作为
B.步骤I中,发生反应的离子方程式为
C.试剂X可用稀硫酸
D.可利用碘易升华的性质将I 和NH Cl固体分离
2 4
12.以氧化镁粗品(含有少量SiO、Fe O 和Al O 等)为原料制备耐火材料—轻质氧化镁的流程如下:
2 2 3 2 3
下列说法错误的是
A.滤渣I的主要成分是SiO
2
B.步骤Ⅱ利用了 是两性氢氧化物的特点将之分离
C.步骤V由 得到MgO的操作在蒸发皿中进行
D.步骤IV中发生反应的离子方程式为
二、多选题
13.下列实验方案设计、现象和结论均正确的是
实验方案 实验现象 实验结论
分别向MgCl 、AlCl 溶液中滴加足量 前者产生白色沉淀;后者先产生白色
A 2 3 金属性:Mg>Al
NaOH溶液 沉淀,后沉淀消失
B 用玻璃棒蘸取某样品进行焰色反应 观察到黄色火焰 该样品含钠元素HClO既有酸性又
C 将氯水点在pH试纸中央 试纸先变红后变白
有漂白性
向2mL0.1mol·L-1NaS的溶液中滴加几滴
D 2 产生淡黄色沉淀 氧化性:Br >S
溴水,振荡 2
A.A B.B C.C D.D
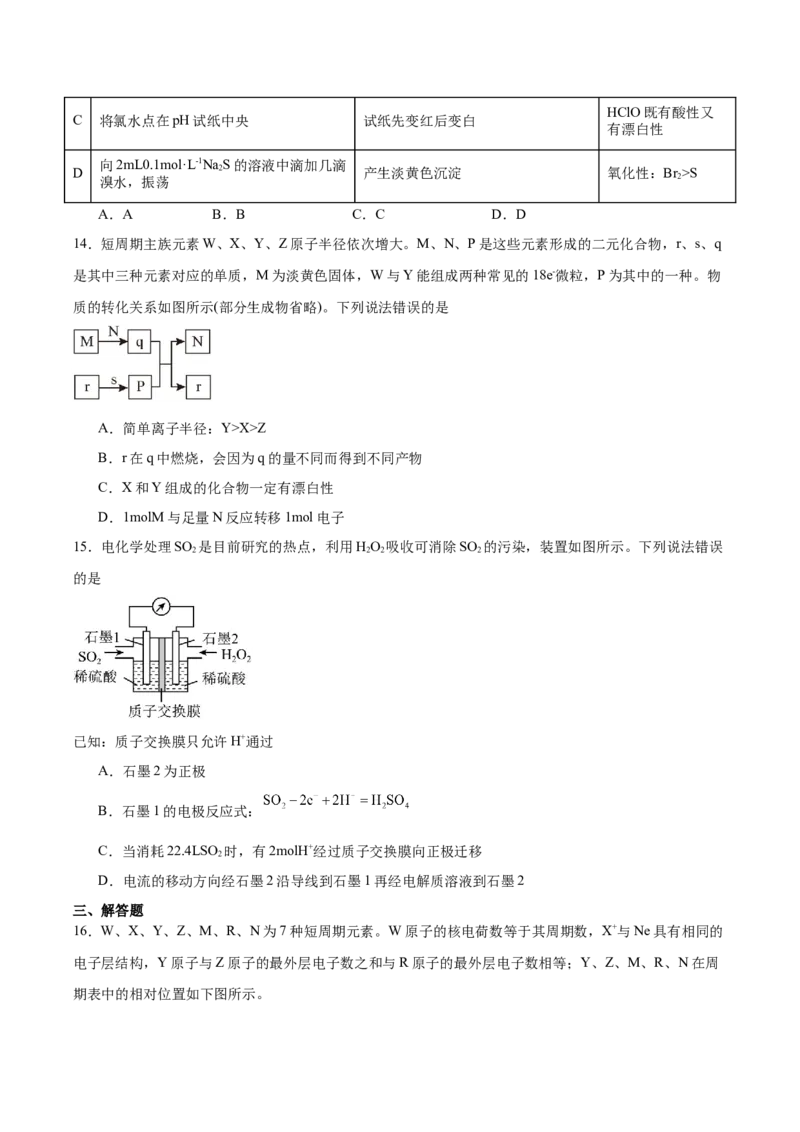
14.短周期主族元素W、X、Y、Z原子半径依次增大。M、N、P是这些元素形成的二元化合物,r、s、q
是其中三种元素对应的单质,M为淡黄色固体,W与Y能组成两种常见的18e-微粒,P为其中的一种。物
质的转化关系如图所示(部分生成物省略)。下列说法错误的是
A.简单离子半径:Y>X>Z
B.r在q中燃烧,会因为q的量不同而得到不同产物
C.X和Y组成的化合物一定有漂白性
D.1molM与足量N反应转移1mol电子
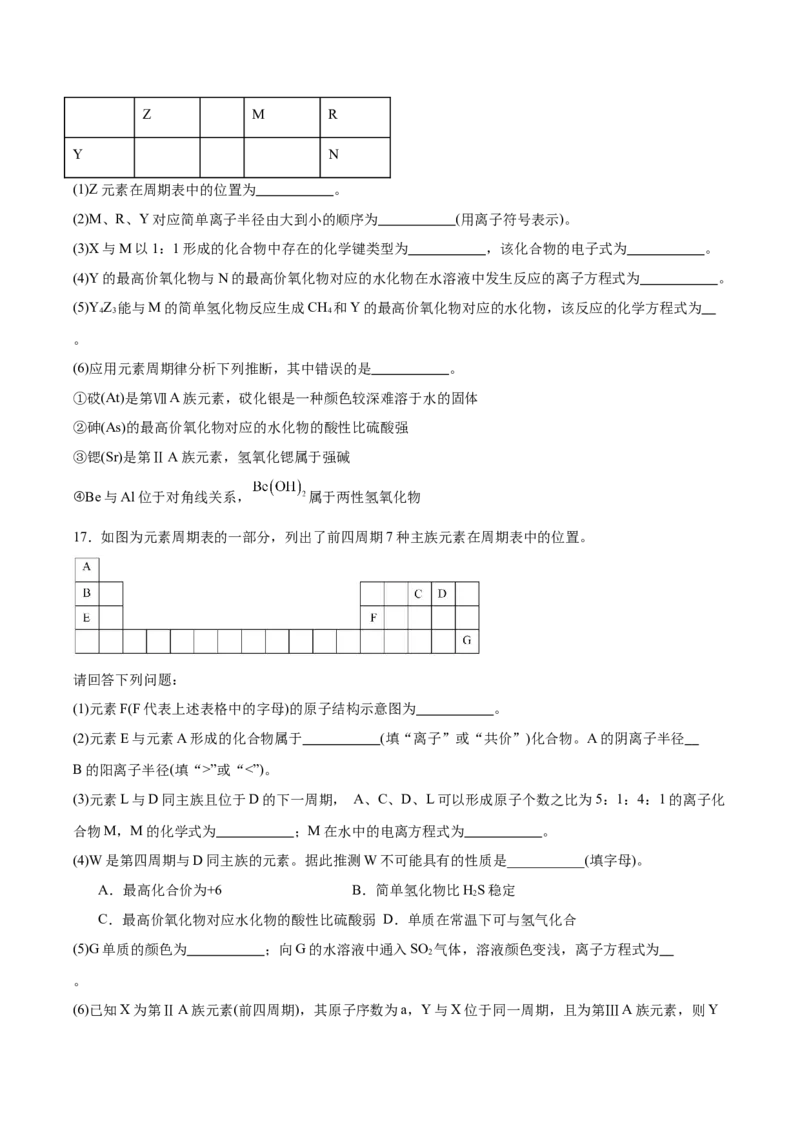
15.电化学处理SO 是目前研究的热点,利用HO 吸收可消除SO 的污染,装置如图所示。下列说法错误
2 2 2 2
的是
已知:质子交换膜只允许H+通过
A.石墨2为正极
B.石墨1的电极反应式:
C.当消耗22.4LSO 时,有2molH+经过质子交换膜向正极迁移
2
D.电流的移动方向经石墨2沿导线到石墨1再经电解质溶液到石墨2
三、解答题
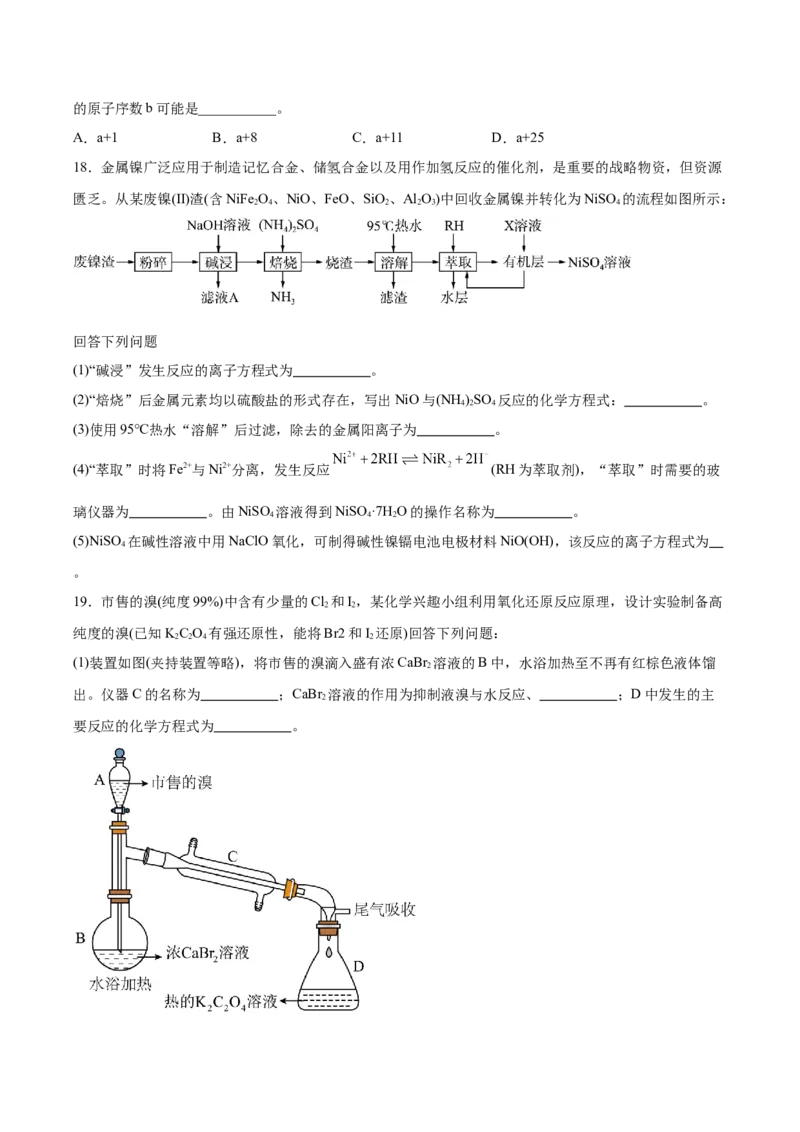
16.W、X、Y、Z、M、R、N为7种短周期元素。W原子的核电荷数等于其周期数,X+与Ne具有相同的
电子层结构,Y原子与Z原子的最外层电子数之和与R原子的最外层电子数相等;Y、Z、M、R、N在周
期表中的相对位置如下图所示。Z M R
Y N
(1)Z元素在周期表中的位置为 。
(2)M、R、Y对应简单离子半径由大到小的顺序为 (用离子符号表示)。
(3)X与M以1:1形成的化合物中存在的化学键类型为 ,该化合物的电子式为 。
(4)Y的最高价氧化物与N的最高价氧化物对应的水化物在水溶液中发生反应的离子方程式为 。
(5)Y Z 能与M的简单氢化物反应生成CH 和Y的最高价氧化物对应的水化物,该反应的化学方程式为
4 3 4
。
(6)应用元素周期律分析下列推断,其中错误的是 。
①砹(At)是第ⅦA族元素,砹化银是一种颜色较深难溶于水的固体
②砷(As)的最高价氧化物对应的水化物的酸性比硫酸强
③锶(Sr)是第ⅡA族元素,氢氧化锶属于强碱
④Be与Al位于对角线关系, 属于两性氢氧化物
17.如图为元素周期表的一部分,列出了前四周期7种主族元素在周期表中的位置。
请回答下列问题:
(1)元素F(F代表上述表格中的字母)的原子结构示意图为 。
(2)元素E与元素A形成的化合物属于 (填“离子”或“共价”)化合物。A的阴离子半径
B的阳离子半径(填“>”或“<”)。
(3)元素L与D同主族且位于D的下一周期, A、C、D、L可以形成原子个数之比为5:1:4:1的离子化
合物M,M的化学式为 ;M在水中的电离方程式为 。
(4)W是第四周期与D同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
A.最高化合价为+6 B.简单氢化物比HS稳定
2
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(5)G单质的颜色为 ;向G的水溶液中通入SO 气体,溶液颜色变浅,离子方程式为
2
。
(6)已知X为第ⅡA族元素(前四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b可能是___________。
A.a+1 B.a+8 C.a+11 D.a+25
18.金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源
匮乏。从某废镍(Ⅱ)渣(含NiFe O、NiO、FeO、SiO、Al O)中回收金属镍并转化为NiSO 的流程如图所示:
2 4 2 2 3 4
回答下列问题
(1)“碱浸”发生反应的离子方程式为 。
(2)“焙烧”后金属元素均以硫酸盐的形式存在,写出NiO与(NH )SO 反应的化学方程式: 。
4 2 4
(3)使用95℃热水“溶解”后过滤,除去的金属阳离子为 。
(4)“萃取”时将Fe2+与Ni2+分离,发生反应 (RH为萃取剂),“萃取”时需要的玻
璃仪器为 。由NiSO 溶液得到NiSO ·7H O的操作名称为 。
4 4 2
(5)NiSO 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiO(OH),该反应的离子方程式为
4
。
19.市售的溴(纯度99%)中含有少量的Cl 和I,某化学兴趣小组利用氧化还原反应原理,设计实验制备高
2 2
纯度的溴(已知KC O 有强还原性,能将Br2和I 还原)回答下列问题:
2 2 4 2
(1)装置如图(夹持装置等略),将市售的溴滴入盛有浓CaBr 溶液的B中,水浴加热至不再有红棕色液体馏
2
出。仪器C的名称为 ;CaBr 溶液的作用为抑制液溴与水反应、 ;D中发生的主
2
要反应的化学方程式为 。(2)将D中溶液转移至 (填仪器名称)中,边加热边向其中滴加酸化的KMnO 溶液至刚好出现红
4
棕色气体,继续加热将溶液蒸干得固体R。该过程中生成I 的离子方程式为 。
2
(3)利用图示相同装置,将R和KCr O,固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加
2 2
适量浓HSO ,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作
2 4
用为 和 。
(4)为保证溴的纯度,步骤(3)中KCr O 固体的用量按理论所需量的 计算,若固体R质量为m克(以KBr
2 2 7
计),则需称取 gKCr O(M=294g·mol-1)(用含m的代数式表示)。
2 2 7
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为:漏斗下端管口紧靠烧杯内壁,
转移溶液时用 ,滤液沿烧杯壁流下。
四、填空题
20.碳中和作为一种新型环保形式可推动全社会绿色发展。下图为科学家正在研究建立的一种二氧化碳新
循环体系。
(1)大气中存在温室气体CO,写出CO 的电子式 。碳有多种单质,一定条件下,1mol石墨转
2 2
化为金刚石吸收1.85kJ能量,则 (填“石墨”或“金刚石”)更稳定。碳与硅同族,制备纯硅的
一种中间产物SiHCl 遇水剧烈反应生成HSiO、HCl和另一种物质,写出该反应的化学方程式:
3 2 3
。
(2)过程I利用CO 制取甲醇的有关化学反应如下:
2
CO(g)+3H(g)=CH OH(g)+H O(g)
2 2 3 2
已知:i.断开1molCH OH(g)中的化学键共吸收2060kJ的能量;
3
1molCO 和3molH 完全反应生成1mol气态CHOH和1mol气态HO放出178kJ热量。
2 2 3 2
ii.反应中部分化学键键能数据如下:
化学键 H—H H—O
键能/
436 463
(kJ·mol-1)
由此计算断开1molC=O需要吸收 kJ的能量
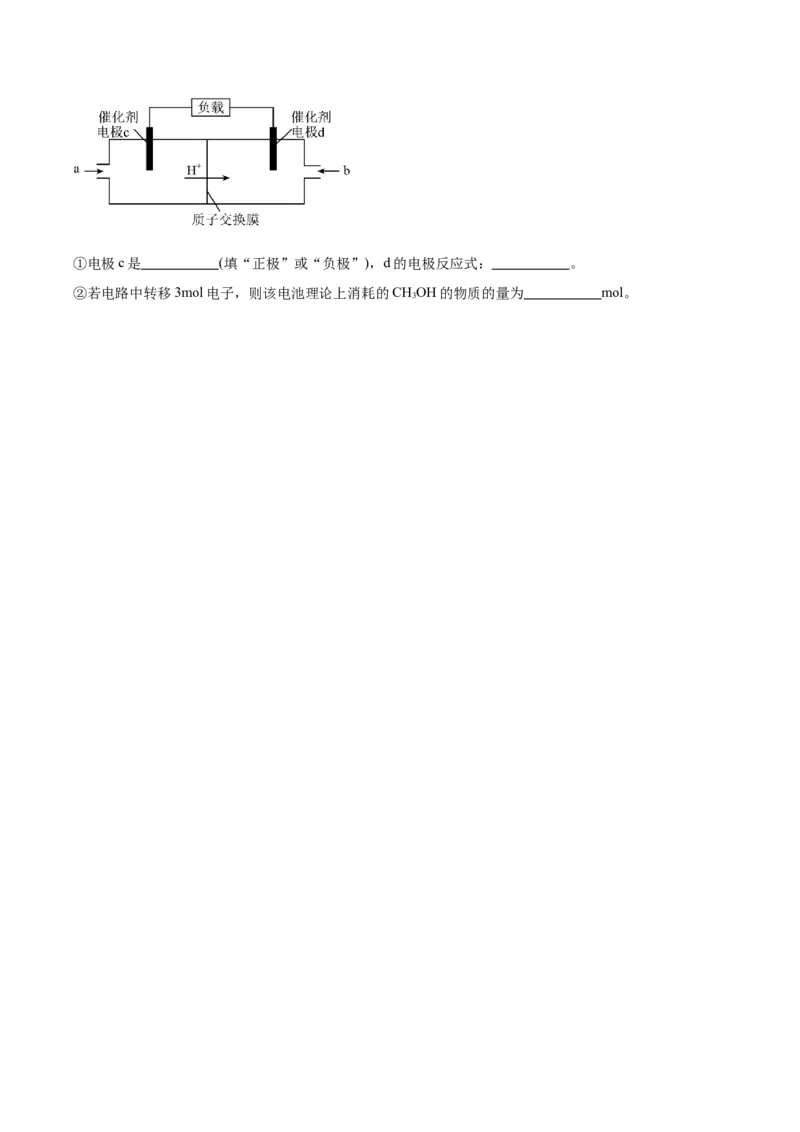
(3)利用过程Ⅲ的反应设计的一种原电池,工作原理如图所示。①电极c是 (填“正极”或“负极”),d的电极反应式: 。
②若电路中转移3mol电子,则该电池理论上消耗的CHOH的物质的量为 mol。
3题号 1 2 3 4 5 6 7 8 9 10
答案 C D C C A C B D D B
题号 11 12 13 14 15
答案 D C AD BC BC
16.(1)第二周期IVA族
(2)O2->F->Al3+
(3) 非极性共价键和离子键
(4)AlO+6H+ =2Al3++3H O
2 3 2
(5)AlC +12H O=4Al(OH) ↓+3CH ↑
4 3 2 3 4
(6)②
17.(1)
(2) 离子 >
(3) NH HSO
4 4
(4)BD
(5) 红棕色
(6)AC
18.(1)AlO+2OH-+3H O=2 、SiO+2OH-= +H O
2 3 2 2 2
(2)NiO+(NH )SO NiSO +2NH↑+H O
4 2 4 4 3 2
(3)Fe(OH)
3
(4) 分液漏斗、烧杯(或锥形瓶) 蒸发浓缩、冷却结晶、过滤、洗涤、干燥
(5)
19.(1) 直形冷凝管 除去市售的溴中少量的Cl Br +K C O 2KBr+2CO↑
2 2 2 2 4 2
(2) 蒸发皿 2 +10I-+16H+ 2Mn2++5I +8H O
2 2(3) 液封 降低温度
(4)0.31m
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处
20.(1) 石墨 SiHCl +3H O=HSiO+3HCl+H ↑
3 2 2 3 2
(2)750