文档内容
第三章 第三节 第2课时 盐类水解的影响因素及应用 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 生活中处处有化学,下列有关说法正确的是( )
A.天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子
B.焊接时用NH Cl溶液除锈与盐类水解无关
4
C.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理
D.在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐褪去
2 3 2
2. 下列应用与盐类水解无关的是( )
A.泡沫灭火器 B.氯化铵和消石灰制备氨气
C.明矾净水 D.草木灰不宜与铵态氮肥混合使用
3.下列说法正确的是( )
A.将AlCl 溶液和Al (SO ) 溶液分别加热、蒸干、灼烧,所得固体成分相同
3 2 4 3
B.配制FeSO 溶液时,将FeSO 固体溶于稀盐酸中,然后稀释至所需浓度
4 4
C.用加热的方法可以除去KCl溶液中的Fe3+
D.洗涤油污常用热的碳酸钠溶液
4. 实验室有下列试剂:①NaOH溶液、②水玻璃、③NaS溶液、④NaCO 溶液、⑤NH Cl溶液、
2 2 3 4
⑥澄清石灰水、⑦浓硫酸,其中必须用带橡胶塞的试剂瓶保存的是( )
A.①⑥ B.①②③④⑥
C.①②③⑥ D.①②③④⑦
5. 下列根据反应原理设计的应用,不正确的是( )
A.CO+HO HCO+OH- 热的纯碱溶液清洗油污
2
B.Al3++3HO Al(OH) +3H+ 明矾净水
2 3
C.TiCl +(x+2)H O(过量) TiO·xHO↓+4HCl 制备TiO·xHO
4 2 2 2 2 2
D.SnCl +HO Sn(OH)Cl+HCl 配制氯化亚锡溶液时加入稀HSO
2 2 2 4
6. 在水溶液中,因发生水解反应而不能大量共存的离子组是( )
A.SO、OH-、Na+、H+ B.H+、Na+、AlO、Cl-
C.Ba2+、HCO、NO、Fe3+ D.S2-、Cl-、SO、Cu2+
7. 下列说法不正确的是 ( )
A.明矾能水解生成Al(OH) 胶体,可用作净水剂
3
B.水解反应NH++HO NH ·H O+H+达到平衡后,升高温度平衡逆向移动
4 2 3 2
C.制备AlCl 、FeCl 、CuCl 均不能采用将溶液直接蒸干的方法
3 3 2
D.盐类水解反应的逆反应是中和反应
8. 向三份0.1 mol·L-1的CHCOONa溶液中分别加入少量NH NO 、NaSO 、FeCl 固体(忽略溶液
3 4 3 2 3 2
1
学科网(北京)股份有限公司体积变化),则CHCOO-浓度的变化依次为( )
3
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
9. 下列应用与碳酸钠或碳酸氢钠能发生水解的事实无关的是( )
A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞
B.泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将两者混合就可产生大量二氧化碳
泡沫
C.厨房中常用碳酸钠溶液洗涤餐具上的油污
D.可用碳酸钠与醋酸制取少量二氧化碳
10.下列应用与盐类水解有关的是( )
①明矾和FeCl 可作为净水剂 ②为保存FeCl 溶液,要在溶液中加少量盐酸 ③实验室配制
3 3
AlCl 溶液时,应先把它溶解在较浓的盐酸中,然后加水稀释 ④NH Cl与ZnCl 溶液可作为
3 4 2
焊接中的除锈剂 ⑤实验室盛放NaCO 溶液的试剂瓶应用橡皮塞,而不用玻璃塞 ⑥用
2 3
NaHCO 与Al (SO ) 两种溶液可作为泡沫灭火剂 ⑦长期使用硫酸铵,土壤酸性增强 ⑧草木
3 2 4 3
灰与铵态氮肥不能混合施用
A.①④⑦ B.②⑤⑦ C.③⑥⑦ D.全有关
11.已知某元素X的酸式盐(NaHX)溶液显碱性,下列说法正确的是( )
A.NaHX的电离方程式为NaHX===Na++H++X2-
B.HX-的电离程度小于HX-的水解程度
C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HX-)+c(X2-)
D.加水稀释,促进HX-水解,c(HX-)增大
12. 为了得到比较纯净的物质,使用的方法恰当的是
A.向NaCO 饱和溶液中,通入过量的CO 后,在加压、加热的条件下,蒸发得NaHCO 晶
2 3 2 3
体
B.加热蒸发AlCl 饱和溶液可得到纯净的AlCl 晶体
3 3
C.向FeBr 溶液中加入过量的氯水,加热蒸发得FeCl 晶体
2 3
D.向FeCl 溶液里加入足量的NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe O
3 2 3
13. 化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO水解
B.明矾水解形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
C.将饱和FeCl 溶液滴入沸水中可制备Fe(OH) 胶体,利用的是盐类水解原理
3 3
D.配制FeCl 溶液时加入少量的盐酸,抑制Fe3+水解
3
14.常温下,浓度均为0.1 mol·L-1的四种盐溶液,其pH如表所示,下列说法正确的是( )
2
学科网(北京)股份有限公司序号 ① ② ③ ④
溶液 CHCOONa NaHCO NaCO NaClO
3 3 2 3
pH 8.8 9.7 11.6 10.3
A.等浓度的CHCOOH和HClO溶液,pH小的是HClO
3
B.NaCO 和NaHCO 溶液中离子种类不同
2 3 3
C.溶液中水的电离程度:①>②>④>③
D.NaHCO 溶液中:c(Na+)=c(CO)+c(HCO)+c(H CO)
3 2 3
15.常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
A.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7,则该溶液的pH一定为14-
a
B.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度的大小关系一定是:
c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
C.pH=3的二元弱酸HR溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应
2
后的混合液:c(R2-)+c(HR-)=c(Na+)
D.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则
反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-)
二、填空题(本题包括3个小题,共40分)
16.(10分)试用离子方程式和简要文字表述以下事实:
(1)盛纯碱溶液的试剂瓶有玻璃塞,时间久了不易打开;
。
(2)盛NH F试剂要用塑料瓶而不用玻璃瓶;
4
。
(3)铵态氮肥不能与草木灰混用;
。
(4)实验室配制的CuSO 溶液,常常出现浑浊的原因是________________(写出离子方程式),可
4
采取在配制时加入少量________防止浑浊。
(5)某同学想把AlCl (aq)和NaS(aq)混合制取Al S ,但最后得到一种白色絮状沉淀,而且混合
3 2 2 3
液中有臭鸡蛋气味的气体放出。试解释造成此结果的原因,写出反应的离子方程式,并指出制
取硫化铝的正确方法;
。
17.(10分)FeCl 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
3
FeCl 高效,且腐蚀性小。请回答下列问题:
3
(1)FeCl 在溶液中分三步水解:
3
Fe3++HO Fe(OH)2++H+ K
2 1
Fe(OH)2++HO Fe(OH)+H+ K
2 2
3
学科网(北京)股份有限公司Fe(OH)+HO Fe(OH) +H+ K
2 3 3
以上水解反应的平衡常数K 、K 、K 由大到小的顺序是__________。通过控制条件,以上水解
1 2 3
产物聚合,生成聚合氯化铁,离子方程式为xFe3++yHO Fe(OH)+yH+,欲使平衡正向移
2 x
动可采用的方法是________(填字母)。
a.降温 b.加水稀释 c.加入NH Cl d.加入NaHCO
4 3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是__________。
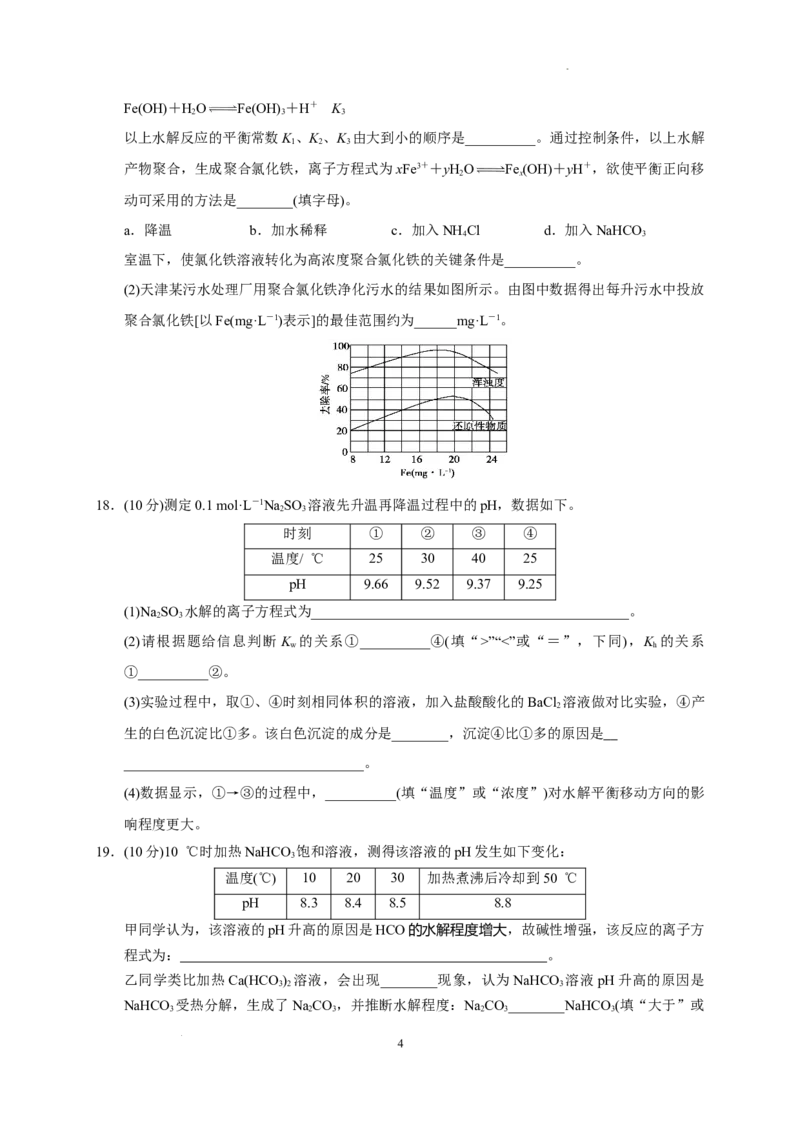
(2)天津某污水处理厂用聚合氯化铁净化污水的结果如图所示。由图中数据得出每升污水中投放
聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为______mg·L-1。
18.(10分)测定0.1 mol·L-1NaSO 溶液先升温再降温过程中的pH,数据如下。
2 3
时刻 ① ② ③ ④
温度/ ℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
(1)Na SO 水解的离子方程式为_____________________________________________。
2 3
(2)请根据题给信息判断 K 的关系①__________④(填“>”“<”或“=”,下同),K 的关系
w h
①__________②。
(3)实验过程中,取①、④时刻相同体积的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产
2
生的白色沉淀比①多。该白色沉淀的成分是________,沉淀④比①多的原因是
__________________________________。
(4)数据显示,①→③的过程中,__________(填“温度”或“浓度”)对水解平衡移动方向的影
响程度更大。
19.(10分)10 ℃时加热NaHCO 饱和溶液,测得该溶液的pH发生如下变化:
3
温度(℃) 10 20 30 加热煮沸后冷却到50 ℃
pH 8.3 8.4 8.5 8.8
甲同学认为,该溶液的pH升高的原因是HCO的水解程度增大,故碱性增强,该反应的离子方
程式为: 。
乙同学类比加热Ca(HCO ) 溶液,会出现________现象,认为NaHCO 溶液pH升高的原因是
3 2 3
NaHCO 受热分解,生成了NaCO ,并推断水解程度:NaCO________NaHCO (填“大于”或
3 2 3 2 3 3
4
学科网(北京)股份有限公司“小于”)。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,则说明________(填“甲”或
“乙”)判断正确。试剂X是________(填字母)。
A.Ba(OH) 溶液 B.BaCl 溶液
2 2
C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到 10 ℃,若溶液的 pH________(填“高于”、“低于”或“等
于”)8.3,则说明另一判断正确。
1.答案:D
解析:A项,天然硬水是因为其中含有较多的Mg2+、Ca2+等离子,错误;B项,NH Cl是强酸弱碱
4
盐,水解显酸性,因此能溶解铁锈,错误;C项,惰性电极电解食盐水生成物是H 、Cl 、NaOH,
2 2
Cl 与NaOH溶液反应可以制备漂白液,与水解无关,错误;D项,NaCO 溶液中存在水解平衡CO
2 2 3
+HO HCO+OH-,加入BaCl 溶液后生成BaCO 沉淀,c(CO)降低,溶液的碱性减弱,所以
2 2 3
红色逐渐褪去,正确。
2.答案:B
解析:A项,泡沫灭火器中Al3+与HCO相互促进水解;B项,NH Cl与Ca(OH) 反应制备NH 与水
4 2 3
解无关;C项,明矾可以净水是因为Al3+水解生成Al(OH) 胶体,胶体具有吸附性;D项,草木灰
3
不宜与铵态氮肥混合使用是因为CO与NH相互促进水解。
3.答案:D
解析:A项,氯化铝溶液蒸干、灼烧后得到氧化铝,而硫酸铝溶液蒸干、灼烧后得到的仍是硫酸铝,
不正确;B项,所加酸应是稀硫酸,不能引入新杂质;C项,加热法不能除去Fe3+。
4.答案:B
解析:水玻璃是矿物胶,能将玻璃瓶塞与瓶口黏结在一起;碱性溶液均会腐蚀玻璃,生成硅酸盐。
所以只有⑤⑦不用橡胶塞。
5.答案:D
解析:加入稀HSO 可以抑制Sn2+水解,但引入SO,D不正确。
2 4
6.答案:C
解析:A项,溶液中发生中和反应:H++OH-===H O,不能大量共存;B项,溶液中H+和AlO发
2
生反应,不是因水解而不共存;C项,溶液中Fe3+和HCO发生相互促进的水解反应生成沉淀,不
能大量共存;D项,溶液中发生反应:Cu2++S2-===CuS↓,不能大量共存。
7.答案:B
解析:水解过程一般为吸热过程,升高温度平衡右移。
8.答案:A
5
学科网(北京)股份有限公司解析:CHCOONa溶液中存在水解平衡CHCOO-+HO CHCOOH+OH-,加入的NH NO 和
3 3 2 3 4 3
FeCl 水解显酸性,故促进其平衡正向移动,则 CHCOO-浓度减小;加入的NaSO 水解显碱性,
2 3 2 3
对水解有抑制作用,故CHCOO-浓度增大。
3
9.答案:D
解析:NaCO 与CHCOOH反应制CO 是利用的酸性强弱,与NaCO 的水解无关。
2 3 3 2 2 3
10.答案:D
解析:①明矾和氯化铁水解生成氢氧化铝胶体、氢氧化铁胶体等,可吸附水中的杂质;②在氯化铁
溶液中加入盐酸,抑制Fe3+的水解;③AlCl 水解生成氢氧化铝和盐酸,先溶解在较浓的盐酸中可
3
以抑制水解;④氯化铵、氯化锌溶液水解呈酸性,利用酸溶解金属氧化物;⑤碳酸钠水解,溶液呈
碱性,与玻璃中的主要成分二氧化硅反应生成具有黏合性的硅酸钠;⑥碳酸氢钠和硫酸铝溶液混合,
发生双水解反应;⑦硫酸铵水解,溶液呈酸性,使土壤酸性增强;⑧铵态氮肥水解呈酸性,而草木
灰的主要成分是碳酸钾,水解呈碱性,混合后发生反应,使肥效降低。
11.答案:B
解析:酸式盐(NaHX)溶液显碱性,HX-水解程度大于电离程度,说明HX是弱酸,NaHX的电离
2
方程式为NaHX===Na++HX-,A错误;溶液显碱性,HX-的电离程度小于HX-的水解程度,B
正确;由电荷守恒可知离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HX-)+2c(X2-),C错误;加水
稀释,促进HX-水解,c(HX-)减小,D错误。
12.答案:D
解析:A不正确,因为NaHCO 加热要分解;B、C项也不正确, 因为AlCl 与FeCl 在加热蒸发的
3 3 3
情况下,水解趋于完全,分别发生下列反应:Al3++3H O Al(OH) +3H+,2Al(OH)
2 3 3
Al O+3H O,Fe3++3H O Fe(OH) +3H+,2Fe(OH) Fe O+3H O。
2 3 2 2 3 3 2 3 2
13.答案:A
解析:正常的雨水由于溶解了二氧化碳,其pH约为5.6,pH小于5.6为酸雨,某雨水样品的pH由
4.68变为4.28,主要是雨水中溶解的二氧化硫生成亚硫酸,亚硫酸被氧化为硫酸,由弱酸转化为强
酸,溶液酸性增强,故A错误;明矾净水的原理是:Al3++3HO Al(OH) (胶体)+3H+,利用
2 3
Al(OH) (胶体)的吸附性进行净水,故B正确;三价铁离子结合水电离出的氢氧根离子生成氢氧化铁,
3
水解是吸热过程,升温促进水解且饱和氯化铁浓度较大,有利于胶体的生成,故C正确;FeCl 溶
3
液中存在水解平衡:Fe3++3HO Fe(OH) +3H+,配制FeCl 溶液时加入少量的盐酸,增加了氢
2 3 3
离子浓度,抑制了铁离子的水解,故D正确。
14.答案:D
6
学科网(北京)股份有限公司解析:等浓度的CHCOONa和NaClO溶液相比,前者的pH小于后者,说明ClO-的水解程度大于
3
CHCOO-的水解程度,根据盐类“越弱越水解”的规律推知,酸性:CHCOOH>HClO,故等浓度
3 3
的CHCOOH和HClO溶液,pH小的是CHCOOH溶液,A错误;NaCO 和NaHCO 溶液中均含有
3 3 2 3 3
两种阳离子(Na+、H+)和三种阴离子(OH-、HCO、CO),B错误;盐的水解促进了水的电离,等浓
度的四种盐溶液,盐的水解程度越大,溶液的 pH 越大;由表可知,水解程度:
NaCO>NaClO>NaHCO >CH COONa,则水的电离程度:③>④>②>①,C错误;NaHCO 溶液中,
2 3 3 3 3
根据物料守恒可得:c(Na+)=c(CO)+c(HCO)+c(H CO),D正确。
2 3
15.答案:D
解析:本题考查电解质溶液有关知识,意在考查考生综合分析问题的能力。常温时,某溶液中由水
电离出的c(H+)=1×10-a mol/L,若a>7,说明水的电离受到抑制,可能为酸溶液也可能为碱溶液,
若为酸溶液,则pH=a,若为碱溶液,则pH=14-a,A项错误;当溶质为硫化钠时,浓度大小关
系符合,当溶质为硫氢化钠和硫化氢,且溶液呈酸性时,浓度大小关系不符合,B项错误;由电荷
守恒知,2c(R2-)+c(HR-)+c(OH-)=c(Na+)+c(H+),混合液的pH等于7,故c(OH-)=c(H+),应
有2c(R2-)+c(HR-)=c(Na+),C项错误;根据电荷守恒知,c(OH-)+c(A-)=c(H+)+c(Na+),根据
物料守恒知,c(A-)+c(HA)=2c(Na+),二者联立可得:2c(OH-)+c(A-)=2c(H+)+c(HA),D项正
确。
16.答案:(1)CO+HO HCO+OH-、SiO+2OH-===SiO+HO,NaCO 水解生成的NaOH与
2 2 2 2 3
玻璃的主要成分SiO 反应生成黏性的NaSiO,会把瓶塞与瓶口黏在一起
2 2 3
(2)NH+F-+HO HF+NH ·H O,由于F-与NH的水解互相促进,生成较高浓度的氢氟酸,
2 3 2
使HF与SiO 反应而将玻璃腐蚀4HF+SiO===SiF ↑+2HO
2 2 4 2
(3)CO+HO===HCO+OH-、NH+HO NH ·H O+H+、H++OH-===H O,草木灰的主要
2 2 3 2 2
成分KCO 与铵态氮肥中的NH水解相互促进,生成NH ·H O分解而挥发,降低了氮肥的肥效
2 3 3 2
(4)Cu2++2HO Cu(OH) +2H+ HSO
2 2 2 4
(5)因为S2-和Al3+水解相互促进,使反应较彻底2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑,因
2 3 2
生成HS逸出,闻到臭鸡蛋气味。用硫粉与铝粉的混合物在干态时共热制Al S 2Al+3S=====Al S
2 2 3, 2 3
17.答案: (1)K >K >K bd 调节溶液的pH (2)18~20
1 2 3
解析:(1)铁离子的水解分为三步,且水解程度逐渐减弱,所以水解平衡常数逐渐减小,则
K1>K2>K3;使平衡正向移动,因为水解为吸热反应,所以降温,平衡逆向移动;加水稀释,则水
解平衡也正向移动;加入氯化铵,氯化铵溶液为酸性,氢离子浓度增大,平衡逆向移动;加入碳酸
氢钠,则消耗氢离子,所以氢离子浓度降低,平衡正向移动,所以答案选bd;从反应的离子方程
式中可知,氢离子的浓度影响高浓度聚合氯化铁的生成,所以关键步骤是调节溶液的pH。(2)由
图像可知,聚合氯化铁的浓度在18~20 mg·L-1时,去除率达到最大值,污水的浑浊度减小。
18.答案:(1)SO 2-+HO HSO -+OH- (2)= <
3 2 3
7
学科网(北京)股份有限公司(3)BaSO 升温过程中部分SO 2-被氧化为SO 2-
4 3 4
(4)浓度
解析:(1)Na SO 是强碱弱酸盐,SO水解使溶液显碱性,其离子方程式为SO 2-+HO HSO -+
2 3 3 2 3
OH-。(2)水的离子积常数K 只与温度有关,由于①和④的温度相同,故二者K 相同;盐的水解为
w w
吸热反应,升高温度,盐的水解平衡右移,K 增大,故K 的关系为①<②。(3)升高温度的过程中部
h h
分SO 2-被氧化为SO 2-,SO 2-与Ba2+反应生成BaSO 白色沉淀,且BaSO 不溶于稀盐酸,故④中产
3 4 4 4 4
生的白色沉淀比①中多。(4)①→③的过程中,温度升高,水解平衡右移,而升温过程中,部分
SO 2-被氧化为SO 2-,SO 2-浓度减小,水解平衡左移,由题表知,①→③溶液pH降低,说明浓度对
3 4 3
水解平衡移动方向的影响程度更大。
19.答案:HCO+HO HCO+OH- 浑浊 大于 (1)乙 B (2)等于
2 2 3
解析:(1)HCO水解方程式:HCO+HOH CO+OH-。
2 2 3
(2)加热煮沸后,若HCO分解成CO,加入BaCl 溶液则生成沉淀。不能选A、C、D,因为它
2
们均有OH-,能与HCO反应生成CO。
8
学科网(北京)股份有限公司9
学科网(北京)股份有限公司