文档内容
第三章 第四节 第1课时 难溶电解质的沉淀溶解平衡 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列说法正确的是( )
A.溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度的乘积
B.溶度积常数是不受任何条件影响的常数,简称溶度积
C.可用离子积Q 与溶度积K 的比较来判断沉淀溶解平衡进行的方向
c sp
D.所有物质的溶度积都是随温度的升高而增大的
2. 下列对沉淀溶解平衡的描述正确的是( )
A.沉淀开始溶解时,溶液中各离子浓度相等
B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变
D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
3. 某温度下向含AgCl固体的AgCl饱和溶液中加少量稀盐酸,下列说法正确的是( )
A.AgCl的溶解度、K 均减小
sp
B.AgCl的溶解度、K 均不变
sp
C.AgCl的溶解度减小、K 不变
sp
D.AgCl的溶解度不变、K 减小
sp
4. 把Ca(OH) 放入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下列
2 2
说法正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入NaCO 溶液,其中固体质量增加
2 3
D.向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
5. 在100 mL 0.01 mol·L-1的KCl溶液中,加入1 mL 0.01 mol·L-1的AgNO 溶液,下列说法正确
3
的是(已知AgCl的K =1.8×10-10)( )
sp
A.有AgCl沉淀析出 B.无AgCl沉淀析出
C.无法确定 D.有沉淀但不是AgCl
6. AgCl和Ag CrO 的溶度积分别为1.8×10-10和2.0×10-12,若用难溶盐在溶液中的浓度来表示其
2 4
溶解度,则下面的叙述中正确的是( )
A.AgCl和Ag CrO 的溶解度相等
2 4
B.AgCl的溶解度大于Ag CrO 的溶解度
2 4
C.两者类型不同,不能由K 的大小直接判断溶解能力的大小
sp
1
学科网(北京)股份有限公司D.都是难溶盐,溶解度无意义
7. 将一定量的硫酸钡放入水中,对此有关的叙述正确的是( )
A.硫酸钡不溶于水,硫酸钡固体质量不会改变
B.最终会得到BaSO 的极稀的饱和溶液
4
C.因为:Ba2++SO===BaSO ↓很容易发生,所以不存在
4
BaSO(s)===Ba2+(aq)+SO(aq)的反应
4
D.因为BaSO 难溶于水,所以改变外界条件也不会改变BaSO 的溶解性
4 4
8. 向盛有10滴AgNO 溶液的试管中滴加0.1 mol/L NaCl溶液,至不再有白色沉淀生成;继续向
3
试管中滴加0.1 mol/L KI溶液并振荡,沉淀变为黄色;再向试管中滴入0.1 mol/L Na S溶液并振
2
荡,沉淀又变成黑色。根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag S
2
B.AgClAgI>Ag S
2
D.AgI>AgCl>Ag S
2
9. 某温度时,BaSO 在水中的沉淀溶解平衡曲线如图所示, 下列说法正确
4
的是( )
A.加入NaSO 可使溶液由a点变到b点
2 4
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO 沉淀生成
4
D.a点对应的K 大于c点对应的K
sp sp
10.已知25 ℃时,K(HF)=3.6×10-4,K (CaF )=1.46×10-10。现向1 L 0.2 mol·L-1 HF溶液中加入
a sp 2
1 L 0.2 mol·L-1 CaCl 溶液。则下列说法中正确的是( )
2
A.25 ℃时,0.1 mol·L-1 HF溶液pH=1
B.K (CaF )随温度和浓度的变化而变化
sp 2
C.该体系中没有沉淀产生
D.该体系中HF与CaCl 反应产生沉淀
2
11.下表是五种银盐的溶度积常数(25 ℃),下列有关说法错误的是( )
化学式 AgCl Ag SO Ag S AgBr AgI
2 4 2
溶度积 1.8×10-10 1.4×10-5 6.3×10-50 5.4×10-13 8.5×10-16
A.五种物质在常温下溶解度最大的是Ag SO
2 4
B.将AgCl溶解于水后,向其中加入NaS,则可以生成黑色的Ag S沉淀
2 2
C.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
D.常温下,AgCl、AgBr和AgI三种物质的溶解度逐渐增大
12.某温度时,Ag SO 在水中的沉淀溶解平衡曲线如图所示,该温度下,下列说法正确的是( )
2 4
A.含有大量SO的溶液中肯定不存在Ag+
2
学科网(北京)股份有限公司B.0.02 mol·L-1的AgNO 溶液与0.02 mol·L-1的NaSO 溶液等体积混合不会生成沉淀
3 2 4
C.Ag SO 的溶度积常数(K )为1×10-3
2 4 sp
D.a点表示Ag SO 的不饱和溶液,蒸发可以使溶液由a点变到b点
2 4
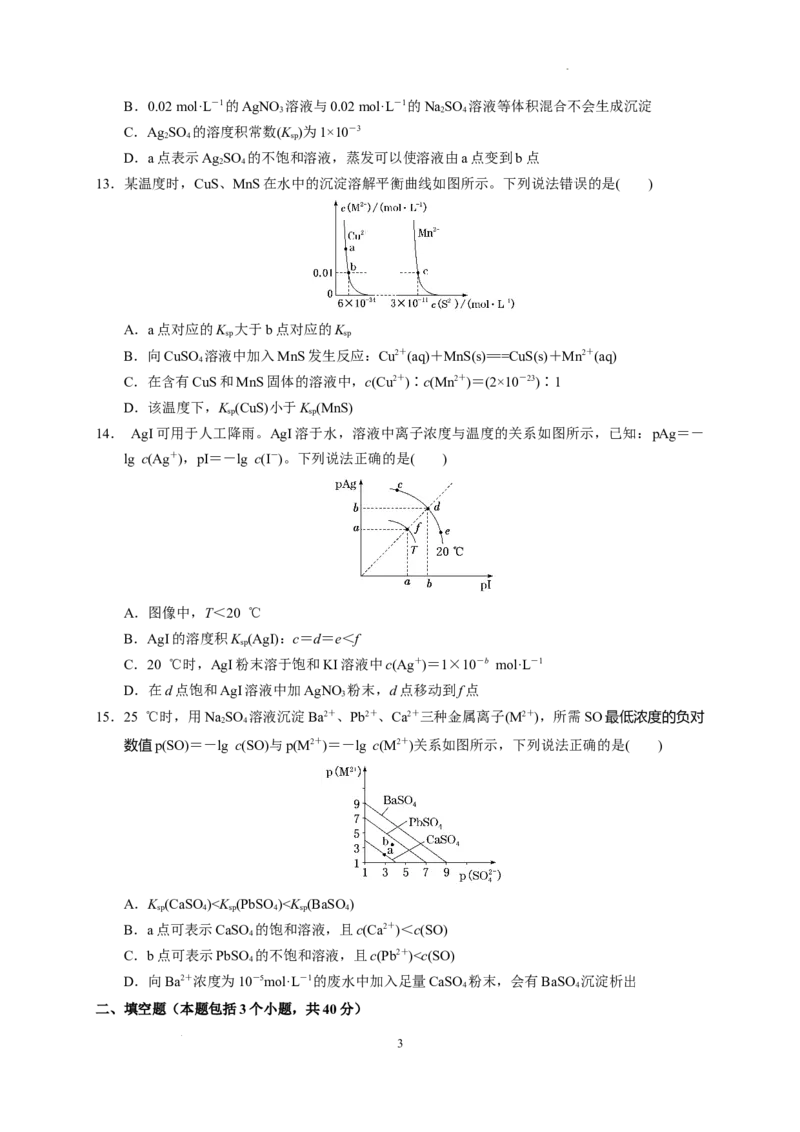
13.某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
A.a点对应的K 大于b点对应的K
sp sp
B.向CuSO 溶液中加入MnS发生反应:Cu2+(aq)+MnS(s)===CuS(s)+Mn2+(aq)
4
C.在含有CuS和MnS固体的溶液中,c(Cu2+)∶c(Mn2+)=(2×10-23)∶1
D.该温度下,K (CuS)小于K (MnS)
sp sp
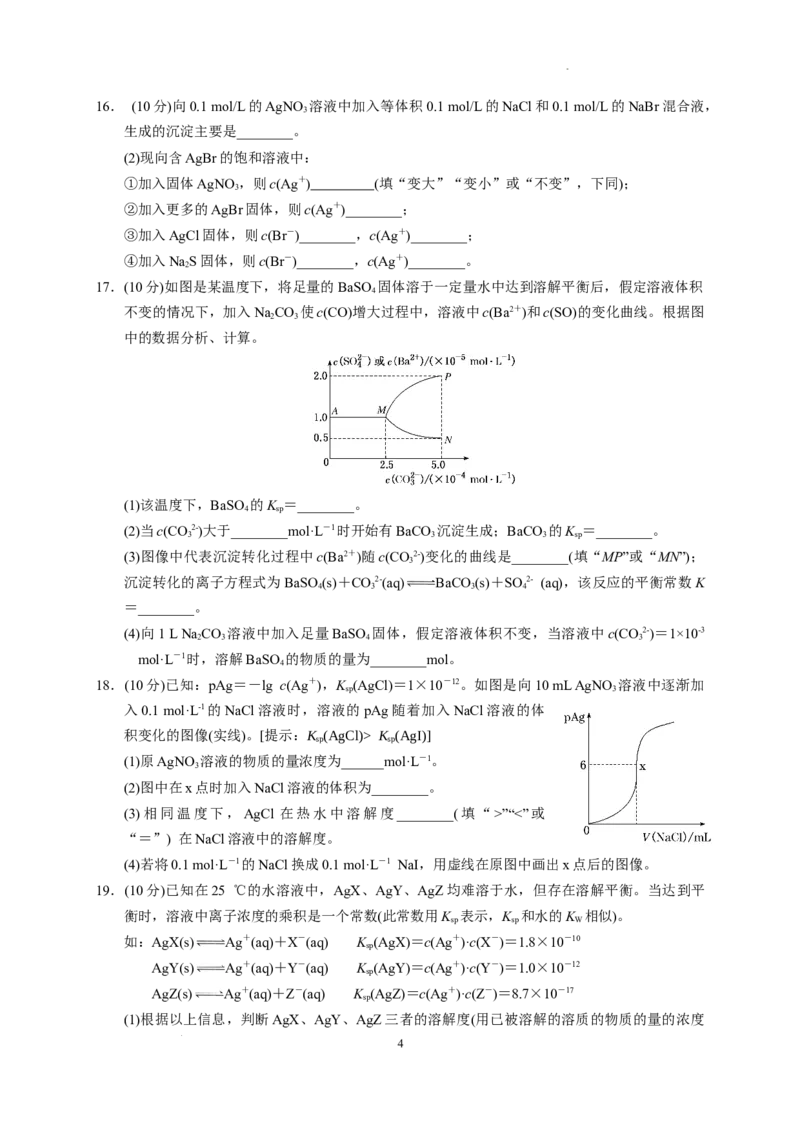
14. AgI可用于人工降雨。AgI溶于水,溶液中离子浓度与温度的关系如图所示,已知:pAg=-
lg c(Ag+),pI=-lg c(I-)。下列说法正确的是( )
A.图像中,T<20 ℃
B.AgI的溶度积K (AgI):c=d=e<f
sp
C.20 ℃时,AgI粉末溶于饱和KI溶液中c(Ag+)=1×10-b mol·L-1
D.在d点饱和AgI溶液中加AgNO 粉末,d点移动到f点
3
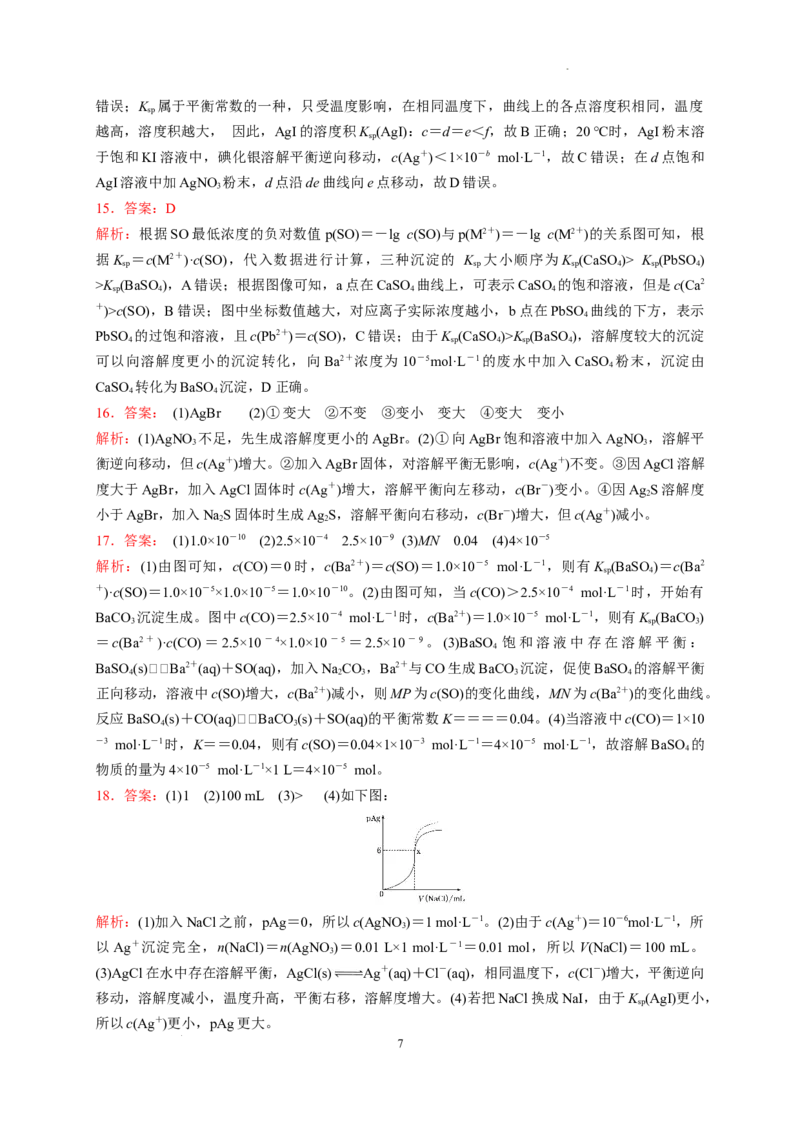
15.25 ℃时,用NaSO 溶液沉淀Ba2+、Pb2+、Ca2+三种金属离子(M2+),所需SO最低浓度的负对
2 4
数值p(SO)=-lg c(SO)与p(M2+)=-lg c(M2+)关系如图所示,下列说法正确的是( )
A.K (CaSO) K (AgI)]
sp sp
(1)原AgNO 溶液的物质的量浓度为______mol·L-1。
3
(2)图中在x点时加入NaCl溶液的体积为________。
(3)相同温度下,AgCl 在热水中溶解度________(填“>”“<”或
“=”) 在NaCl溶液中的溶解度。
(4)若将0.1 mol·L-1的NaCl换成0.1 mol·L-1 NaI,用虚线在原图中画出x点后的图像。
19.(10分)已知在25 ℃的水溶液中,AgX、AgY、AgZ均难溶于水,但存在溶解平衡。当达到平
衡时,溶液中离子浓度的乘积是一个常数(此常数用K 表示,K 和水的K 相似)。
sp sp W
如:AgX(s) Ag+(aq)+X-(aq) K (AgX)=c(Ag+)·c(X-)=1.8×10-10
sp
AgY(s) Ag+(aq)+Y-(aq) K (AgY)=c(Ag+)·c(Y-)=1.0×10-12
sp
AgZ(s) Ag+(aq)+Z-(aq) K (AgZ)=c(Ag+)·c(Z-)=8.7×10-17
sp
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量的浓度
4
学科网(北京)股份有限公司表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为__________________________。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)________(填“增大“减小”或“不
变”)。
(3)在25 ℃时,若取0.188 g的AgY(相对分子质量为188)固体放入100 mL水中(忽略溶液体积
的变化),则溶液中Y-的物质的量浓度为_____ ___。
(4)①由上述K 判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
sp
_________________________________________________________________________。
②在上述(3)体系中,能否实现AgY向AgX的转化?根据你的观点选答一项。
若不能,请简述理由:___________________________________________________________。
若能,则实现转化的必要条件是:_________________________________________________。
1.答案:C
解析:溶度积应是沉淀溶解平衡时难溶电解质在溶液中各离子浓度幂的乘积,A错。溶度积与温度
有关,B错。Ca(OH) 的K 随温度升高而减小,D错。答案:C
2 sp
2.答案:B
解析:A项沉淀开始溶解时,各离子的浓度没有必然的关系;B项正确;C项沉淀溶解达到平衡时,
溶液中溶质的离子浓度保持不变,但不一定相等;D项沉淀溶解达到平衡时,如果再加入难溶性的
该沉淀物,由于固体的浓度为常数,故平衡不发生移动。
3.答案:C
解析:在含AgCl固体的AgCl饱和溶液中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq),当加
入少量稀盐酸时,c(Cl-)增大,平衡逆向移动,c(Ag+)减小,溶解的氯化银质量减小,AgCl的溶解
度减小;AgCl的K 只受温度影响,温度不变,AgCl的K 不变,故选C。
sp sp
4.答案:C
解析:恒温下K 不变,加入CaO后,CaO与水反应生成Ca(OH) ,溶液仍为Ca(OH) 的饱和溶液,
sp 2 2
pH不变,A错误;加热,Ca(OH) 的溶解度减小,溶液的pH降低,B错误;加入NaCO 溶液,沉
2 2 3
淀溶解平衡向右移动,Ca(OH) 固体转化为少量CaCO 固体,固体质量增加,C正确;加入少量
2 3
NaOH固体,平衡向左移动,Ca(OH) 固体质量增加,D错误。
2
5.答案:A
解析:Q=c(Cl-)·c(Ag+)=0.01 mol·L-1×× mol·L-1≈9.8×10-7>1.8×10-10=K ,故有AgCl沉淀生成。
c sp
6.答案:C
解析:AgCl和Ag CrO 阴、阳离子比类型不同,不能直接利用K 来比较二者溶解能力的大小,所
2 4 sp
以只有C对;其余三项叙述均错误。比较溶解度大小,若用溶度积必须是同类型,否则不能比较。
7.答案:B
解析:BaSO 不溶于水并不是绝对不溶,它存在溶解平衡,当沉淀溶解和生成的速率相等时,得到
4
5
学科网(北京)股份有限公司了BaSO 的饱和溶液,即建立了动态平衡BaSO(s) Ba2+(aq)+SO(aq),A、C项错误,B项正确;
4 4
升高温度,BaSO 溶解度增大,D项错误。答案:B
4
8.答案:C
解析:一般来说,溶解度小的沉淀容易转化成溶解度更小的沉淀。由实验现象知,白色沉淀
(AgCl)→黄色沉淀(AgI)→黑色沉淀(Ag S),则溶解度为:AgCl>AgI>Ag S。答案:C
2 2
9.答案:C
解析:本题考查溶解平衡有关知识,意在考查考生的识图和运用所学知识解决问题的能力。BaSO
4
在水中存在着溶解平衡 BaSO(s) Ba2+(aq)+SO(aq),a点在平衡曲线上,加入 NaSO 会增大
4 2 4
c(SO),平衡左移,c(Ba2+)应降低,A项错误;d点时溶液不饱和,蒸发溶剂水,c(SO)、c(Ba2+)均
增大,B项错误;b点时溶液过饱和,有沉淀生成,C项正确;K 是一常数,温度不变K 不变,
sp sp
在曲线上的任意一点K 都相等,D项错误。答案:C
sp
10.答案:D
解析:若HF完全电离,则0.1 mol·L-1 HF溶液的pH=1,但由K (HF)=3.6×10-4可知,HF为弱
sp
电解质,不能完全电离,故0.1 mol·L-1 HF溶液的pH>1,A项错误。K 不随浓度变化而变化,B
sp
项错误。K(HF)===3.6×10-4,则c2(F-)=3.6×10-5,c(Ca2+)=0.1 mol·L-1,则Q=c2(F-)·c(Ca2+)
a c
=3.6×10-6>1.46×10-10,体系中有CaF 沉淀析出,C项错误,D项正确。答案:D
2
11.答案:D
解析:由溶度积常数可以看出,卤化银中AgCl的溶解度最大,Ag SO 和Ag S相比,Ag SO 的溶
2 4 2 2 4
解度较大,AgCl达到沉淀溶解平衡时,c(Ag+)≈1.34×10-5 mol·L-1,由计算得溶解度最大的是
Ag SO ,A项正确;AgCl比Ag S的溶度积常数大很多,则Ag S更难溶,所以将AgCl溶解于水后,
2 4 2 2
向其中加入NaS可以生成黑色的Ag S沉淀,B项正确;沉淀溶解平衡的建立是有条件的,外界条
2 2
件改变时,平衡也会发生移动,C项正确;从溶度积常数可以看出,AgCl、AgBr、AgI溶度积常数
逐渐减小,所以AgCl、AgBr、AgI三种物质在常温下的溶解度逐渐减小,D项错误。
12.答案:B
解析:A项,由于沉淀与溶解是一个平衡,故即使SO浓度再大,也有少量的Ag+存在,不正确;
B项,根据图像,K [Ag SO ]=(2×10-2)2×5×10-2=2×10-5,而0.02 mol/L AgNO 溶液与0.02 mol/L
sp 2 4 3
的NaSO 溶液等体积混合,离子积c2(Ag+)×c(SO)=(0.01)2×0.01=1×10-6<2×10-5,故没有沉淀生成,
2 4
正确;C项,由B项解析知不正确;D项,a点到b点,如果是蒸发的话,Ag+和SO的浓度均会增
大,而不是只增大SO的浓度。答案:B
13.答案:A
解析:因为 a 点和 b 点都在 CuS 的沉淀溶解平衡曲线上,K 是定值,A 错误;因为
sp
K (CuS) K (PbSO )
sp sp sp 4 sp 4
>K (BaSO),A错误;根据图像可知,a点在CaSO 曲线上,可表示CaSO 的饱和溶液,但是c(Ca2
sp 4 4 4
+)>c(SO),B错误;图中坐标数值越大,对应离子实际浓度越小,b点在PbSO 曲线的下方,表示
4
PbSO 的过饱和溶液,且c(Pb2+)=c(SO),C错误;由于K (CaSO)>K (BaSO),溶解度较大的沉淀
4 sp 4 sp 4
可以向溶解度更小的沉淀转化,向Ba2+浓度为10-5mol·L-1的废水中加入CaSO 粉末,沉淀由
4
CaSO 转化为BaSO 沉淀,D正确。
4 4
16.答案: (1)AgBr (2)①变大 ②不变 ③变小 变大 ④变大 变小
解析:(1)AgNO 不足,先生成溶解度更小的AgBr。(2)①向AgBr饱和溶液中加入AgNO ,溶解平
3 3
衡逆向移动,但c(Ag+)增大。②加入AgBr固体,对溶解平衡无影响,c(Ag+)不变。③因AgCl溶解
度大于AgBr,加入AgCl固体时c(Ag+)增大,溶解平衡向左移动,c(Br-)变小。④因Ag S溶解度
2
小于AgBr,加入NaS固体时生成Ag S,溶解平衡向右移动,c(Br-)增大,但c(Ag+)减小。
2 2
17.答案: (1)1.0×10-10 (2)2.5×10-4 2.5×10-9 (3)MN 0.04 (4)4×10-5
解析:(1)由图可知,c(CO)=0时,c(Ba2+)=c(SO)=1.0×10-5 mol·L-1,则有K (BaSO)=c(Ba2
sp 4
+)·c(SO)=1.0×10-5×1.0×10-5=1.0×10-10。(2)由图可知,当c(CO)>2.5×10-4 mol·L-1时,开始有
BaCO 沉淀生成。图中c(CO)=2.5×10-4 mol·L-1时,c(Ba2+)=1.0×10-5 mol·L-1,则有K (BaCO)
3 sp 3
=c(Ba2+)·c(CO)=2.5×10-4×1.0×10-5=2.5×10-9。(3)BaSO 饱和溶液中存在溶解平衡:
4
BaSO(s)Ba2+(aq)+SO(aq),加入NaCO ,Ba2+与CO生成BaCO 沉淀,促使BaSO 的溶解平衡
4 2 3 3 4
正向移动,溶液中c(SO)增大,c(Ba2+)减小,则MP为c(SO)的变化曲线,MN为c(Ba2+)的变化曲线。
反应BaSO(s)+CO(aq)BaCO (s)+SO(aq)的平衡常数K====0.04。(4)当溶液中c(CO)=1×10
4 3
-3 mol·L-1时,K==0.04,则有c(SO)=0.04×1×10-3 mol·L-1=4×10-5 mol·L-1,故溶解BaSO 的
4
物质的量为4×10-5 mol·L-1×1 L=4×10-5 mol。
18.答案:(1)1 (2)100 mL (3)> (4)如下图:
解析:(1)加入NaCl之前,pAg=0,所以c(AgNO)=1 mol·L-1。(2)由于c(Ag+)=10-6mol·L-1,所
3
以Ag+沉淀完全,n(NaCl)=n(AgNO)=0.01 L×1 mol·L-1=0.01 mol,所以 V(NaCl)=100 mL。
3
(3)AgCl在水中存在溶解平衡,AgCl(s) Ag+(aq)+Cl-(aq),相同温度下,c(Cl-)增大,平衡逆向
移动,溶解度减小,温度升高,平衡右移,溶解度增大。(4)若把NaCl换成NaI,由于K (AgI)更小,
sp
所以c(Ag+)更小,pAg更大。
7
学科网(北京)股份有限公司19.答案:(1)S(AgX)>S(AgY)>S(AgZ) (2)减小 (3)1.0×10-6 mol·L-1
(4)①能。K (AgY)=1.0×10-12>K (AgZ)=8.7×10-17
sp sp
②能。当溶液中c(X-)>1.8×10-4 mol·L-1时,可实现AgY向AgX的转化,若要实现AgY向
AgX的完全转化,必须保持溶液中的c(X-)>1.8×10-4 mol·L-1
解析:(1)根据各物质的K 可知其溶解度S(AgX)>S(AgY)>S(AgZ)。(2)由于AgY比AgX更难溶。则
sp
向AgY饱和溶液中加入AgX固体,则发生沉淀的转化:AgX(s)+Y-(aq)===AgY(s)+X-(aq),c(Y
-)减小。(3)25 ℃时。K (AgY)=1.0×10-12,即溶液达到饱和时,c(Ag+)=c(Y-)=1.0×10-12mol·L-
sp
1,可知100 mL水溶解AgY的质量约为:0.10 L×1.0×10-6 mol·L-1×188 g·mol-1=1.88×10-5 g<0.188
g,即0.188 g AgY固体放入100 mL水中,形成AgY的饱和溶液且固体还有剩余,则溶液中c(Y)=
1.0×10-6 mol·L-1。(4)①由于K (AgZ)K (AgY),但当c(X-)>=1.8×10-4 mol·L-1时,也可实现AgY
sp sp
向AgX的转化。
8
学科网(北京)股份有限公司9
学科网(北京)股份有限公司