第二章 第二节 第3课时 影响化学平衡因素 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列说法不正确的是( )
A.反应混合物各组分百分含量发生改变,化学平衡一定发生了移动
B.外界条件的改变引起浓度商或化学平衡常数改变,则平衡一定发生移动
C.平衡移动,反应物的浓度一定减小
D.外界条件发生变化,化学平衡不一定移动
2. 对于反应:2A(g)+B(g) 2C(g) ΔH<0,当温度升高时,平衡向逆反应方向移动,其原因
是( )
A.正反应速率增大,逆反应速率减小
B.逆反应速率增大,正反应速率减小
C.正、逆反应速率均增大,但是逆反应速率增大的程度大于正反应速率增大的程度
D.正、逆反应速率均增大,而且增大的程度一样
3. 下列可确认化学平衡一定发生移动的是( )
A.化学反应速率发生了改变
B.可逆反应达到平衡,使用了催化剂
C.有气态物质参加的可逆反应达到平衡后,改变了压强
D.由于某一条件的改变,使正、逆反应速率不再相等
4. 将NO 装入带活塞的密闭容器中,当反应2NO (g) NO(g)达到平衡后,改变下列一个条件,
2 2 2 4
其中叙述正确的是( )
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒容时,充入惰性气体,压强增大,平衡向右移动,混合气体的颜色变浅
5. 如图a曲线表示放热反应X(g)+Y(g) Z(g)+M(g)+N(g)进行过程中X的转化率随时间变
化的关系。若要改变某一起始条件,使反应过程按b曲线进行,可采取的措施是( )
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
6. 在一定条件下,发生反应CO(g)+NO (g) CO(g)+NO(g),达到化学平衡后,降低温度,
2 2
混合物的颜色变浅,下列有关该反应的说法中正确的是( )
1
学科网(北京)股份有限公司A.正反应为吸热反应
B.正反应为放热反应
C.降温后CO的浓度增大
D.降温后各物质的浓度不变
7.下列事实不能用平衡移动原理解释的是( )
A.开启啤酒瓶后, B.由H(g)、I(g)、 C.实验室制取乙酸
2 2
D.石灰岩受地下水
瓶中马上泛起大量泡 HI(g)组成的平衡体系 乙酯时,将乙酸乙酯
长期溶蚀形成溶洞
沫 加压后颜色变深 不断蒸出
8. 对密闭容器中进行的反应:X(g)+3Y(g) 2Z(g)绘制如下图像,下列说法错误的是( )
A.依据图甲可判断正反应为放热反应
B.在图乙中,虚线可表示使用了催化剂后X的转化率
C.图丙可表示减小压强,平衡向逆反应方向移动
D.依据图丁中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的ΔH<0
9. 向一容积为2 L的恒容密闭容器中充入1 mol N 和4 mol H ,在一定温度下发生反应:N(g)+
2 2 2
3H(g) 2NH (g) ΔH<0。10秒时达到平衡,c(NH )为0.4 mol·L-1。下列说法正确的是(
2 3 3
)
A.该反应达到平衡时H 的转化率为40%
2
B.降低温度能使混合气体的密度增大
C.向该容器中充入N,平衡正向移动
2
D.研发高效催化剂可大大提高NH 的产率
3
10.臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO (g)+O(g) NO(g)+O(g),若反应在
2 3 2 5 2
恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A B C D
2
学科网(北京)股份有限公司0~3 s内,反应速率
升高温度,平衡 t 时仅加入催化 达平衡时,仅改变
1
为:v(NO )=0.2 mol·L
2
常数减小 剂,平衡正向移动 x,则x为c(O )
2
-1
11.下列事实不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡:Br +HO HBr+HBrO,当加入少量AgNO 溶液后,溶液的颜色
2 2 3
变浅
B.对2HI(g) H(g)+I(g),缩小容器的容积可使平衡体系的颜色变深
2 2
C.反应CO(g)+NO (g) CO(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向移动
2 2
D.对于合成NH 反应,为提高NH 的产率,理论上应采取低温措施
3 3
12.已知某可逆反应mA(g)+nB(g) pC(g)在密闭容器中进行,如图表示在不同反应时间t时,
温度T和压强p与反应物B在混合气体中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判
断正确的是( )
A.T
p,m+n>p,放热反应
1 2 1 2
B.T>T,pp,吸热反应
1 2 1 2
C.Tp,m+nT,p0,不改变其他条件的情况下合理的说
2 2 2
法是( )
A.加入催化剂,反应途径将发生改变,ΔH也将随之改变
B.升高温度,正、逆反应速率都增大,HS分解率也增大
2
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注入一些H 后达新平衡,H 浓度将减小
2 2
14.在密闭容器中投入一定量反应物发生储氢反应:LaNi(s)+3H(g) LaNiH(s) ΔH=-301
5 2 5 6
kJ·mol-1。在某温度下,达到平衡状态,测得氢气压强为2 MPa。下列说法不正确的是( )
A.当LaNi 的浓度不再变化时,该反应达到平衡状态
5
B.若温度不变,缩小容器的容积至原来的一半,重新达到平衡时H 的压强仍为2 MPa
2
C.扩大容器的容积,重新达到平衡时n(H )增多
2
D.增大压强,降低温度,有利于储氢
15.已知2SO (g)+O(g) 2SO (g) ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分
2 2 3
别充入气体:(甲) 2 mol SO 和1 mol O ;(乙)1 mol SO 和0.5 mol O ;(丙) 2 mol SO 。恒温、
2 2 2 2 3
3
学科网(北京)股份有限公司恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强p:p =p >2p
甲 丙 乙
B.SO 的质量m:m =m >2m
3 甲 丙 乙
C.c(SO )与c(O )之比k:k =k >k
2 2 甲 丙 乙
D.反应放出或吸收热量的数值Q:Q =Q >2Q
甲 丙 乙
二、填空题(本题包括4个小题,共40分)
16.(10分)在一定条件下,可逆反应A+B mC变化如图所示。已知纵坐标表示在不同温度和
压强下生成物C在混合物中的质量分数,p为反应在T 温度时达到平衡后向容器加压的变化情
2
况,问:
(1)温度T________T(填“大于”“等于”或“小于”)。
1 2
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2 (填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强
________(填“增大”“减小”或“不变”),平衡________移动(填“向正反应方向”“向逆反
应方向”或“不”)。
17.(10分)已知NO 和NO 可以相互转化,反应:2NO (g) NO(g) ΔH=-57.2 kJ·mol-1。
2 2 4 2 2 4
(1)一定温度下,将1 mol N O 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡
2 4
状态的是________(填序号,下同)。
(2)在恒容容器中,该反应达到平衡后,若只改变一个条件,达到新平衡时,下列能使 NO 的
2
体积分数增大的是________。
A.充入一定量NO B.分离出一定量NO
2 2
C.充入一定量N D.降低温度
2
(3)若反应2NO (g) NO(g)在容积为1 L的恒容密闭容器中进行,保持温度不变,达到平衡
2 2 4
后,向反应容器中再充入少量NO ,平衡________移动(填“向左”“向右”或“不”),重新
2
达到平衡后,和原平衡相比,混合气体的颜色_____(填“变深”“变浅”或“不变”),NO
2
的转化率_____(填“增大”“减小”或“不变”)。
4
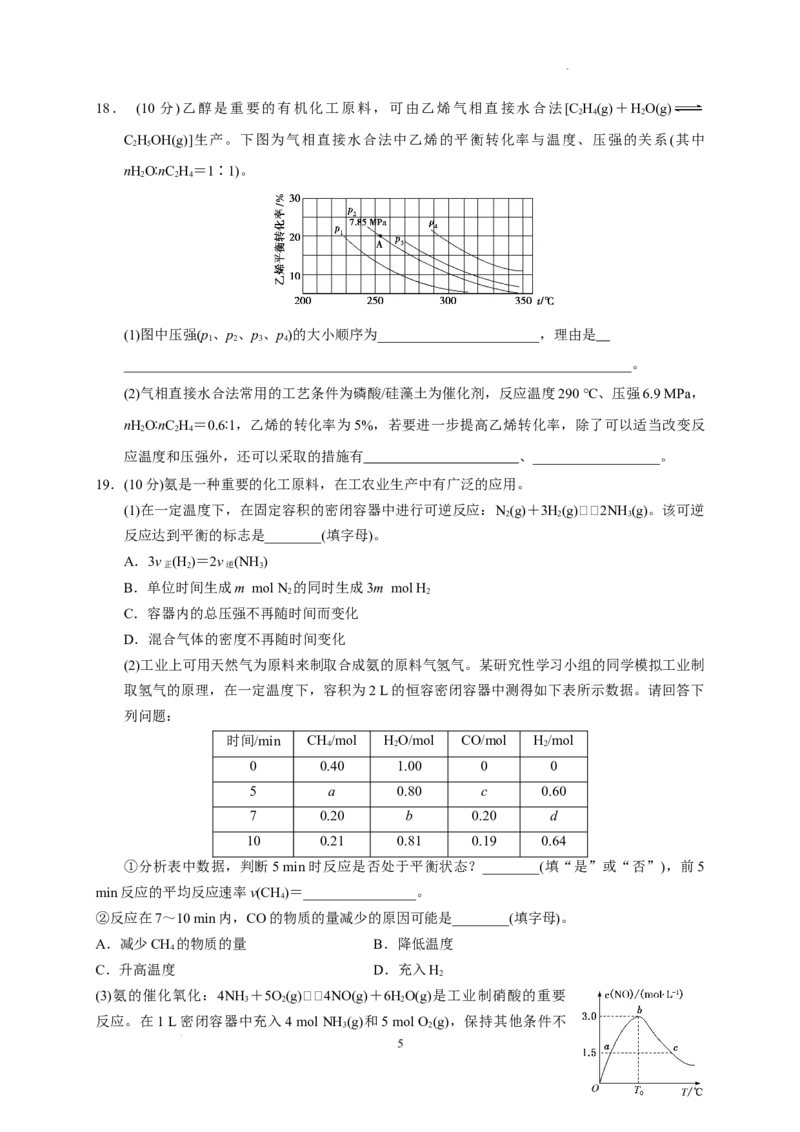
学科网(北京)股份有限公司18. (10 分)乙醇是重要的有机化工原料,可由乙烯气相直接水合法[C H(g)+HO(g)
2 4 2
C HOH(g)]生产。下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中
2 5
nHO∶nC H=1∶1)。
2 2 4
(1)图中压强(p、p、p、p)的大小顺序为_______________________,理由是
1 2 3 4
________________________________________________________________________。
(2)气相直接水合法常用的工艺条件为磷酸/硅藻土为催化剂,反应温度290 ℃、压强6.9 MPa,
nHO∶nC H =0.6∶1,乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反
2 2 4
应温度和压强外,还可以采取的措施有 、__________________。
19.(10分)氨是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定容积的密闭容器中进行可逆反应:N(g)+3H(g)2NH(g)。该可逆
2 2 3
反应达到平衡的标志是________(填字母)。
A.3v (H )=2v (NH )
正 2 逆 3
B.单位时间生成m mol N 的同时生成3m mol H
2 2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取合成氨的原料气氢气。某研究性学习小组的同学模拟工业制
取氢气的原理,在一定温度下,容积为2 L的恒容密闭容器中测得如下表所示数据。请回答下
列问题:
时间/min CH/mol HO/mol CO/mol H/mol
4 2 2
0 0.40 1.00 0 0
5 a 0.80 c 0.60
7 0.20 b 0.20 d
10 0.21 0.81 0.19 0.64
①分析表中数据,判断5 min时反应是否处于平衡状态?________(填“是”或“否”),前5
min反应的平均反应速率v(CH)=________________。
4
②反应在7~10 min内,CO的物质的量减少的原因可能是________(填字母)。
A.减少CH 的物质的量 B.降低温度
4
C.升高温度 D.充入H
2
(3)氨的催化氧化:4NH +5O(g)4NO(g)+6HO(g)是工业制硝酸的重要
3 2 2
反应。在1 L密闭容器中充入4 mol NH (g)和5 mol O (g),保持其他条件不
3 2
5
学科网(北京)股份有限公司变,测得c(NO)与温度的关系如图所示。该反应的ΔH______(填“>”“<”或“=”)0;T℃下,
0
NH 的转化率为________。
3
1.答案: C
解析:外界条件的改变使正、逆反应速率不相等或Q≠K时才能使化学平衡发生移动。增大反应物
浓度化学平衡移动时反应物的浓度增大。
2.答案: C
解析:外界条件的改变使正、逆反应速率不相等时才能使化学平衡发生移动,增大反应物浓度使化
学平衡移动时反应物的浓度增大。
3.答案: D
解析:化学平衡移动的实质是正、逆反应速率不相等。A中化学反应速率发生了改变,但可能正、
逆反应速率同等程度地改变,两者仍相等;B中对于反应前后气体体积相等的反应,压强的改变对
正、逆反应速率的影响相同;C中催化剂同等程度地改变正、逆反应速率。
4.答案: C
解析:升高温度,气体颜色加深,则平衡向左移动,该反应为放热反应,A错误;根据勒夏特列原
理,混合气体的颜色比原平衡深,压强小于原平衡的两倍,因此B错误,C正确;恒温恒容,充入
惰性气体,c(NO )和c(N O)均不变,平衡不移动,气体的颜色不变,D错误。
2 2 4
5.答案: C
解析:由图可知,a、b曲线所示反应平衡时,X的转化率相同,只是b曲线所示反应达到平衡所用
时间短,升高温度、增大X的浓度、增大体积时X的平衡转化率都不相同,A、B、D错误,C正
确。
6.答案: B
解析:降低温度,混合物颜色变浅,说明NO 浓度减小,平衡向右移动,正反应为放热反应,CO
2
浓度减小。
7.答案: B
解析:啤酒中存在平衡:HCO HO+CO ,开启啤酒瓶,瓶内压强降低,平衡向气体体积增
2 3 2 2
大的方向移动,即向生成二氧化碳气体的方向移动,故能用平衡移动原理解释,A不选;反应H+
2
I 2HI是一个反应前后气体分子数不变的反应,压强改变并不能使平衡发生移动,混合气体加
2
压后颜色变深,是因为I 的浓度增大,不能用平衡移动原理解释,B选;实验室制取乙酸乙酯时,
2
采用加热的方式将乙酸乙酯不断蒸出,从而使平衡向生成乙酸乙酯的方向移动,能用平衡移动原理
解释,C不选;石灰岩溶蚀发生反应:CaCO +CO +HO Ca(HCO ) ,能用平衡移动原理解释,
3 2 2 3 2
D不选。
6
学科网(北京)股份有限公司8.答案: C
解析:图甲中v 、v 曲线的交点是平衡点,升高温度,v 增大的程度小于v ,平衡逆向移动,
正 逆 正 逆
则该反应的正反应是放热反应,A正确;使用催化剂,可加快反应速率,缩短达到平衡的时间,但
平衡不移动,X的转化率不变,故图乙中虚线可表示使用催化剂后X的转化率,B正确;减小压强,
v 、v 均减小,且反应向气体分子总数增大的方向进行,即平衡逆向移动,与图丙不相符,C错
正 逆
误;X、Y、Z均为气体,混合气体的总质量不变,图丁中随温度升高而逐渐减小,说明升高温度,
平衡逆向移动,则正反应的ΔH<0,D正确。
9.答案: C
解析:A项,根据题中数据可知,NH 的生成量为0.8 mol,则H 的减少量为1.2 mol,α(H )=
3 2 2
×100%=30%;B项,降温,平衡正向移动,但气体总质量不变,容器容积不变,则密度不变;C
项,容积不变,充入N ,c(N )增大,平衡正向移动;D项,催化剂不能使平衡发生移动,因此各
2 2
物质的转化率不变、产率不变。
10.答案: A
解析:本题考查化学平衡原理,涉及图像分析、平衡常数、反应速率计算及反应物的转化率等内容。
A项正确,由图像可知,反应物的总能量高于生成物的总能量,说明此反应是放热反应,所以升高
温度,平衡将逆向移动,平衡常数减小;B项错误;v(NO )应等于0.2 mol·L-1·s-1;C项错误,加
2
入催化剂,平衡不发生移动;D项错误,达平衡时,增大c(O ),平衡逆向移动,NO 的转化率会减
2 2
小。
11.答案: B
解析:溴水中存在平衡:Br +HO HBr+HBrO,加入少量AgNO 溶液,HBr与AgNO 反应生
2 2 3 3
成AgBr沉淀,c(HBr)减小,平衡正向移动,溶液的颜色变浅,A可以用勒夏特列原理解释;2HI(g)
H(g)+I(g)的正反应是反应前后气体总分子数不变的反应,缩小容器的容积,压强增大,平
2 2
衡不移动,但c(I)增大,导致平衡体系的颜色变深,由于平衡不移动,故B不能用勒夏特列原理解
2
释;反应CO(g)+NO (g) CO(g)+NO(g)的ΔH<0,升高温度,为了减弱温度的改变,平衡逆向
2 2
移动,C可以用勒夏特列原理解释;合成氨的反应是放热反应,降低温度,平衡正向移动,有利于
生成NH ,D可以用勒夏特列原理解释。
3
12.答案: D
解析:通过①和②的比较,相同压强下,温度越高反应速率越快,到达平衡所用时间越短,
T>T ,且升高温度平衡正移,正反应为吸热反应;通过②和③的比较,相同温度下,压强越大反
1 2
应速率越快,到达平衡所用时间越短,p>p,且压强增大平衡逆向移动,m+n2m ;c(SO )与c(O )之比均相等;甲丙反应放出或吸收热量的数值 Q不一定相等,所以
甲 丙 乙 2 2
选B。
16.答案:(1)大于 (2)放热 (3)大于 (4)增大 不
解析:由图像知温度T 时到达平衡用时间少,则反应速率快,说明温度大于 T ;升高温度C的百
1 2
分含量降低,平衡逆移,则正反应放热;加压C的百分含量降低,平衡逆移,则正反应体积增大,
m大于2;当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强增大,
但对该反应体系来说,各物质浓度没有变化,平衡不移动。
17.答案:(1)ad (2)B (3)向右 变深 增大
解析:(1)恒压容器中充入1 mol N O 进行2NO (g)N O(g)反应,反应逆向进行,气体总物质的
2 4 2 2 4
量增大,则容器的容积增大,气体的密度变小,当气体密度不变时,该反应达到平衡状态,a正确;
ΔH取决于反应物和生成物具有的总能量,与反应进行的方向及程度无关,故不能根据 ΔH判断是
否达到平衡状态,b错误;图中只有NO 和NO 的v ,无法判断v 、v 是否相等,故无法判断是
2 2 4 正 正 逆
否达到平衡状态,c错误;NO 的转化率不变时,NO 的v 、v 相等,则该反应达到平衡状态,d
2 4 2 4 正 逆
正确。(2)恒容容器中,充入一定量NO ,相当于增大压强,平衡正向移动,达到新平衡时,NO 的
2 2
转化率增大,体积分数减小,同理,分离出一定量的NO ,相当于减小压强,平衡逆向移动,达到
2
新平衡时,NO 的转化率减小,体积分数增大,故A错误,B正确;充入一定量N,平衡不移动,
2 2
NO 的体积分数不变,C错误;该反应的ΔH<0,降低温度,平衡正向移动,NO 的体积分数减小,
2 2
D错误。(3)恒温恒容时,充入少量NO ,平衡向右移动,根据勒夏特列原理可知,重新达到平衡后,
2
和原平衡相比,c(NO )仍比原平衡大,故混合气体的颜色变深。恒温恒容时,充入少量NO ,相当
2 2
于保持n(NO )不变,缩小容器的容积,而缩小容积,增大压强,平衡正向移动,NO 的转化率增大。
2 2
18.答案:(1)p>p>p>p
4 3 2 1
8
学科网(北京)股份有限公司正反应为分子数减少的化学反应,相同温度下,压强增大,乙烯转化率提高
(2)将产物乙醇液化移去 增加nHO∶nC H 的比值
2 2 4
19.答案:答案:(1)C (2)①是 0.02 mol·L-1·min-1 ②D (3)< 75%
解析:(1)3v (NH )=2v (H )时反应达到平衡,A项错误;生成m mol N ,必生成3m mol H ,但
逆 3 正 2 2 2
反应不一定达到平衡,B项错误;此反应为反应前后气体分子数不相等的反应,压强不变可以说明
反应达到平衡状态,C项正确;混合气体总质量不变,容器容积不变,所以混合气体的密度始终不
变,故混合气体的密度不变不能说明反应达到平衡状态,D项错误。(2)①根据反应:CH(g)+
4
HO(g)CO(g)+3H(g),结合表中数据 5 min 时 H 为 0.60 mol,可知 CO 为 0.20 mol,即 c=
2 2 2
0.20,则a=0.20,7 min时,各物质的物质的量与5 min时相同,所以5 min时反应达到平衡状态;
v(CH)==0.02 mol·L-1·min-1。②10 min时,只有CO的物质的量减少,其他物质的物质的量都增
4
加,所以原因只能是充入氢气,使平衡逆向移动,故选D。(3)由图像可知,NO的浓度达到最大值
后,随温度升高,NO的浓度又逐渐减小,所以该反应的ΔH<0;T ℃时,c(NO)=3.0 mol·L-1,
0
则反应消耗的n(NH )=3.0 mol,NH 的转化率为×100%=75%。
3 3
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司