文档内容
第五章 单元过关检测
时间:90分钟 满分:100分
一、选择题(本题共14小题,每小题3分,共42分)
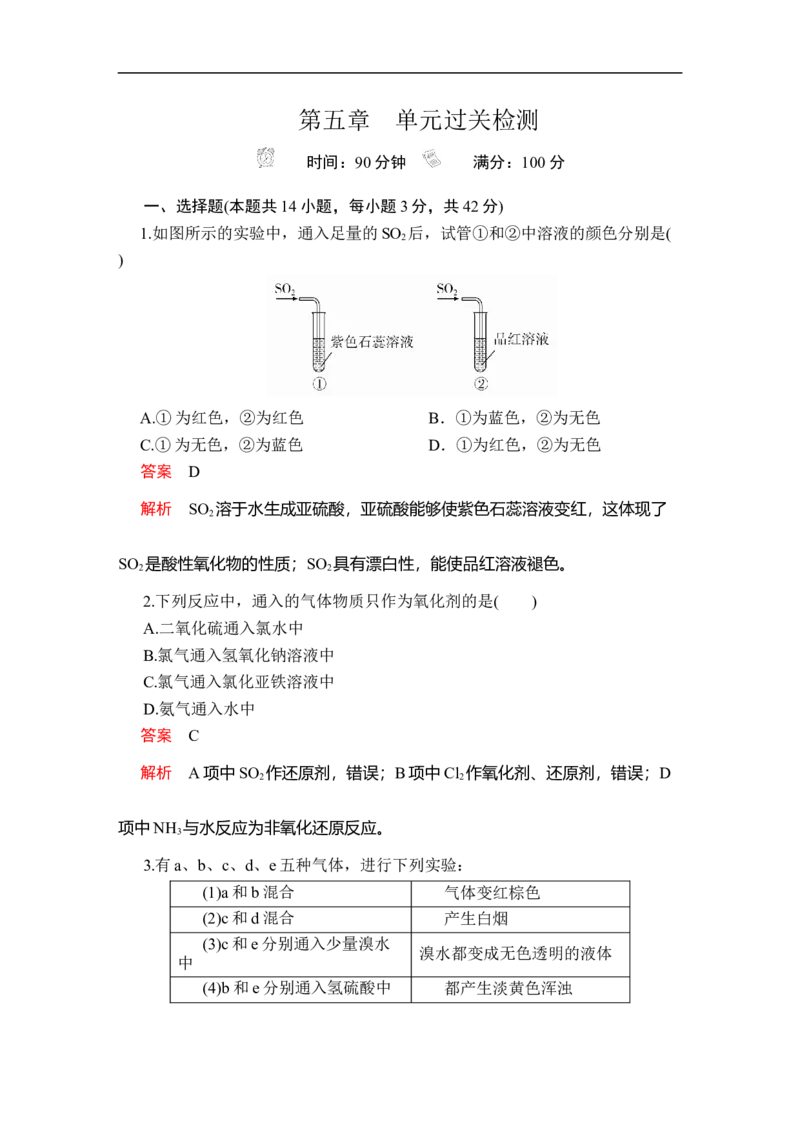
1.如图所示的实验中,通入足量的SO 后,试管①和②中溶液的颜色分别是(
2
)
A.①为红色,②为红色 B.①为蓝色,②为无色
C.①为无色,②为蓝色 D.①为红色,②为无色
答案 D
解析 SO 溶于水生成亚硫酸,亚硫酸能够使紫色石蕊溶液变红,这体现了
2
SO 是酸性氧化物的性质;SO 具有漂白性,能使品红溶液褪色。
2 2
2.下列反应中,通入的气体物质只作为氧化剂的是( )
A.二氧化硫通入氯水中
B.氯气通入氢氧化钠溶液中
C.氯气通入氯化亚铁溶液中
D.氨气通入水中
答案 C
解析 A项中SO 作还原剂,错误;B项中Cl 作氧化剂、还原剂,错误;D
2 2
项中NH 与水反应为非氧化还原反应。
3
3.有a、b、c、d、e五种气体,进行下列实验:
(1)a和b混合 气体变红棕色
(2)c和d混合 产生白烟
(3)c和e分别通入少量溴水
溴水都变成无色透明的液体
中
(4)b和e分别通入氢硫酸中 都产生淡黄色浑浊a、b、c、d、e依次可能是( )
A.O 、NO、HCl、NH 、CO
2 3 2
B.O 、NO、NH 、HCl、SO
2 3 2
C.NO、O 、NH 、HCl、SO
2 3 2
D.HCl、CO 、NH 、H S、CH
2 3 2 4
答案 C
解析 a和b混合后气体变成红棕色,可知a和b分别为NO、O 中的一种;b
2
通入氢硫酸中产生淡黄色浑浊,则b为O ,a为NO;c和d混合产生白烟,则c
2
和d分别为NH 、HCl中的一种;c通入少量溴水中使溴水变成无色透明液体,
3
则c为NH ,d为HCl;e通入少量溴水中,溴水变成无色透明的液体,e通入氢
3
硫酸中产生淡黄色浑浊,则e为SO 。
2
4.人类的生产生活离不开化学,下列关于生活中的化学知识说法错误的是(
)
A.用氯气与石灰乳反应能制得漂白粉
B.常温下,可用铝槽车装运浓硝酸
C.二氧化碳、二氧化硫是形成酸雨的主要原因
D.不需要通过化学反应就能从海水中获得食盐和淡水
答案 C
解析 A项,氯气与石灰乳反应生成氯化钙和次氯酸钙,能制得漂白粉,正
确;B项,常温下,铝遇浓硝酸钝化,可用铝槽车装运浓硝酸,正确;C项,二
氧化硫和氮氧化物是形成酸雨的主要原因,而二氧化碳不能形成酸雨,错误;D
项,可通过蒸发海水获得食盐和淡水,此方法为物理变化,正确。
5.除去下列气体中的杂质(括号内是杂质)所用试剂不正确的是( )
A.CO [HCl]:用饱和的NaHCO 溶液
2 3
B.CO [SO ]:用饱和酸性KMnO 溶液
2 2 4
C.Cl [HCl]:用饱和的NaCl溶液
2D.SO [HCl]:用饱和的Na SO 溶液
2 2 3
答案 D
解析 D选项不仅除去了氯化氢,二氧化硫也会被吸收,错误。
6.关于非金属元素Si、N、S的叙述,正确的是( )
A.通常情况下,它们的单质均为气体
B.它们在自然界中都存在游离态形式
C.它们都有对应的含氧酸
D.每种元素都只有一种氧化物
答案 C
解析 A项,Si、S的单质常温下为固体,而N的单质为气体,故不选A;B
项,Si在自然界中以化合态存在,故不选B;C项,均为非金属,存在对应的酸
性氧化物,则都有对应的含氧酸,故选C;D项,N和S的氧化物有多种,故不
选D。
7.在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻
轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终充满烧瓶,
则a和b分别是( )
答案 A
解析 B选项不能充满;C选项Cl 几乎不溶于饱和食盐水;D选项氮气不溶
2
于盐酸。8.按如图进行实验,试管内装有12 mL NO,然后间歇而缓慢地通入8 mL
O ,下面有关实验最终状态的描述正确的是( )
2
A.试管内气体呈红棕色
B.试管内气体为无色的NO
C.试管内气体为无色的O
2
D.试管内充满了液体
答案 B
解析 据题意在装有NO的试管内通入O 时依次发生反应2NO+
2
O ===2NO 3NO +H O===2HNO +NO,二者相加得总反应为4NO+3O +
2 2, 2 2 3 2
2H O===4HNO ,由于==>,即NO过量,试管内剩余气体为无色的NO,液体
2 3
未充满试管。
9.下列说法正确的是( )
A.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓
硝酸
B.在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应
C.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中含
SO
D.将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
答案 A
解析 A项,浓硝酸光照下发生分解生成NO ,NO 溶于浓硝酸中使浓硝酸
2 2
呈黄色;B项,Cl 氧化I-生成I ,淀粉遇I 变蓝色;C项,溶液中若存在Ag+或
2 2 2SO也会产生相同的实验现象;D项,常温时,Cu与浓硫酸不发生反应。
10.甲和乙两种物质混合反应(反应可加热),将所得气体通入适量的丙中,丙
中不能产生明显化学现象的是( )
答案 B
解析 A项,C与浓硫酸在加热条件下反应生成CO 、SO 和H O,澄清石灰
2 2 2
水能与CO 、SO 反应产生白色沉淀;B项,MnO 与稀盐酸不反应,加热时也得
2 2 2
不到Cl ,所以品红溶液不褪色;C项,浓氨水与碱石灰作用可得NH ,NH 溶
2 3 3
于水与AlCl 溶液反应产生白色沉淀;D项,Cu与浓硝酸反应产生NO ,NO 溶
3 2 2
于水生成HNO 和NO,HNO 能将HSO氧化为SO,从而产生BaSO 白色沉淀。
3 3 4
11.下列由相关实验现象所推出的结论正确的是( )
A.Cl 、SO 均能使品红溶液褪色,说明二者均有氧化性
2 2
B.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有SO
3 2
C.Fe与稀HNO 、稀H SO 反应均有气泡产生,说明Fe与两种酸均发生置换
3 2 4
反应
D.分别充满HCl、NH 的烧瓶倒置于水中后液面均迅速上升,说明二者易溶
3
于水
答案 D
解析 A项,Cl 溶于水生成的HClO具有氧化性,能使品红溶液褪色,SO
2 2能使品红溶液褪色体现了SO 的漂白性,错误;B项,溶液中也可能含有SO,
2
SO与酸化的Ba(NO ) 溶液反应,被其中的H+和NO氧化为SO,SO与Ba2+结
3 2
合为BaSO 沉淀,错误;C项,铁与硝酸发生的不是置换反应,错误。
4
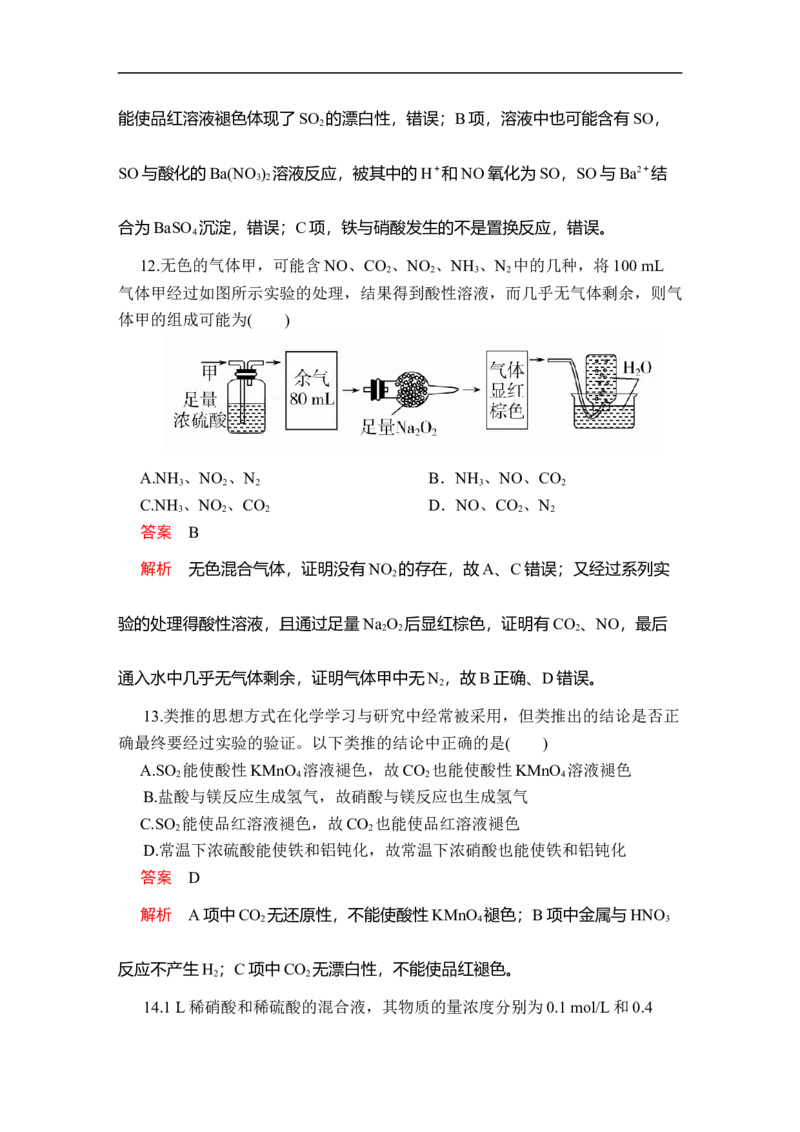
12.无色的气体甲,可能含NO、CO 、NO 、NH 、N 中的几种,将100 mL
2 2 3 2
气体甲经过如图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,则气
体甲的组成可能为( )
A.NH 、NO 、N B.NH 、NO、CO
3 2 2 3 2
C.NH 、NO 、CO D.NO、CO 、N
3 2 2 2 2
答案 B
解析 无色混合气体,证明没有NO 的存在,故A、C错误;又经过系列实
2
验的处理得酸性溶液,且通过足量Na O 后显红棕色,证明有CO 、NO,最后
2 2 2
通入水中几乎无气体剩余,证明气体甲中无N ,故B正确、D错误。
2
13.类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正
确最终要经过实验的验证。以下类推的结论中正确的是( )
A.SO 能使酸性KMnO 溶液褪色,故CO 也能使酸性KMnO 溶液褪色
2 4 2 4
B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气
C.SO 能使品红溶液褪色,故CO 也能使品红溶液褪色
2 2
D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化
答案 D
解析 A项中CO 无还原性,不能使酸性KMnO 褪色;B项中金属与HNO
2 4 3
反应不产生H ;C项中CO 无漂白性,不能使品红褪色。
2 2
14.1 L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1 mol/L和0.4mol/L。若向该混合液中加入足量的铜粉,则最多能溶解铜粉的质量为( )
A.2.4 g B.3.2 g C.6.4 g D.9.6 g
答案 D
解析 混合溶液中n(NO)=0.1 mol,n(H+)=0.9 mol,3Cu+8H++2NO===3Cu2
++2NO↑+4H O,NO的量不足,按其来进行计算,最多溶解Cu:0.15
2
mol×64 g/mol=9.6 g。
二、非选择题(本题共4小题,共58分)
15.(13分)X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三
种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的
产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是
硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚
酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1∶1在水溶液中能发生反应,离子方程式
为____________________________________。
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填
化学式)________;该反应是氧化还原反应,则其中的氧化剂是(填化学
式)________。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为________。
(4)检验W气体的方法是________________________________________。
答案 (1)Cl +SO +2H O===4H++2Cl-+SO
2 2 2
(2)N NO
2 2
(3)1∶2
(4)将湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝,证明该气体为NH (合
3
理即可)
解析 X、Y、Z、W是中学化学中常见的四种气体,X、Y、Z三种气体都能
对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,
是形成酸雨的物质,则X是二氧化硫;Y是一种单质,它的水溶液具有漂白作用,则Y是氯气;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应,则
Z是二氧化氮;W气体的水溶液滴入酚酞变红色,说明W气体为碱性气体,则
为氨气。
16.(15分)(1)SiO 在自然界中广泛存在,它是制备现代通讯材料________(写该
2
材料名称)的主要原料;以SiO 为原料,在工业上制备单质硅的化学方程式为
2
________________________;在常温下,SiO 可与一种酸发生反应,该反应的化
2
学方程式为______________________。该反应的重要应用是______________。
(2)在一定体积的18 mol/L的浓硫酸加入过量铜片,加热使之反应,被还原的
硫酸为0.9 mol。则浓硫酸的实际体积________(填“大于”“小于”或“等
于”)100 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO 溶
3
液),则该反应的离子方程式________________________________________。
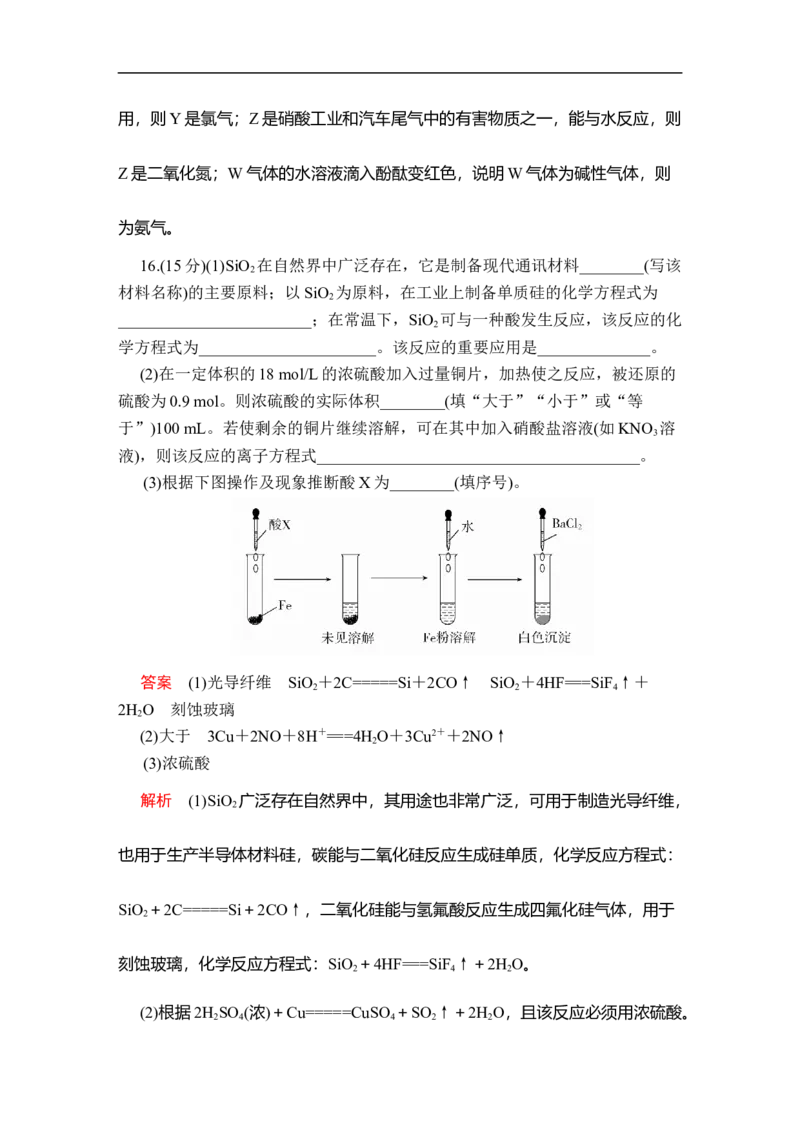
(3)根据下图操作及现象推断酸X为________(填序号)。
答案 (1)光导纤维 SiO +2C=====Si+2CO↑ SiO +4HF===SiF ↑+
2 2 4
2H O 刻蚀玻璃
2
(2)大于 3Cu+2NO+8H+===4H O+3Cu2++2NO↑
2
(3)浓硫酸
解析 (1)SiO 广泛存在自然界中,其用途也非常广泛,可用于制造光导纤维,
2
也用于生产半导体材料硅,碳能与二氧化硅反应生成硅单质,化学反应方程式:
SiO +2C=====Si+2CO↑,二氧化硅能与氢氟酸反应生成四氟化硅气体,用于
2
刻蚀玻璃,化学反应方程式:SiO +4HF===SiF ↑+2H O。
2 4 2
(2)根据2H SO (浓)+Cu=====CuSO +SO ↑+2H O,且该反应必须用浓硫酸。
2 4 4 2 2所以还原0.9 mol的硫酸所需硫酸大于1.8 mol。即所需体积大于100 mL;铜片
不与稀硫酸反应,加入硝酸盐后相当于组成了稀硝酸。离子方程式为3Cu+2NO
+8H+===4H O+3Cu2++2NO↑。
2
(3)由图中铁未见溶解,则酸一定不是盐酸或稀硫酸、稀硝酸,则加入酸可能
为浓硫酸或浓硝酸,而加水溶解,则浓酸变为稀酸,最后生成白色沉淀为硫酸钡,
所以推断加入酸为浓硫酸。
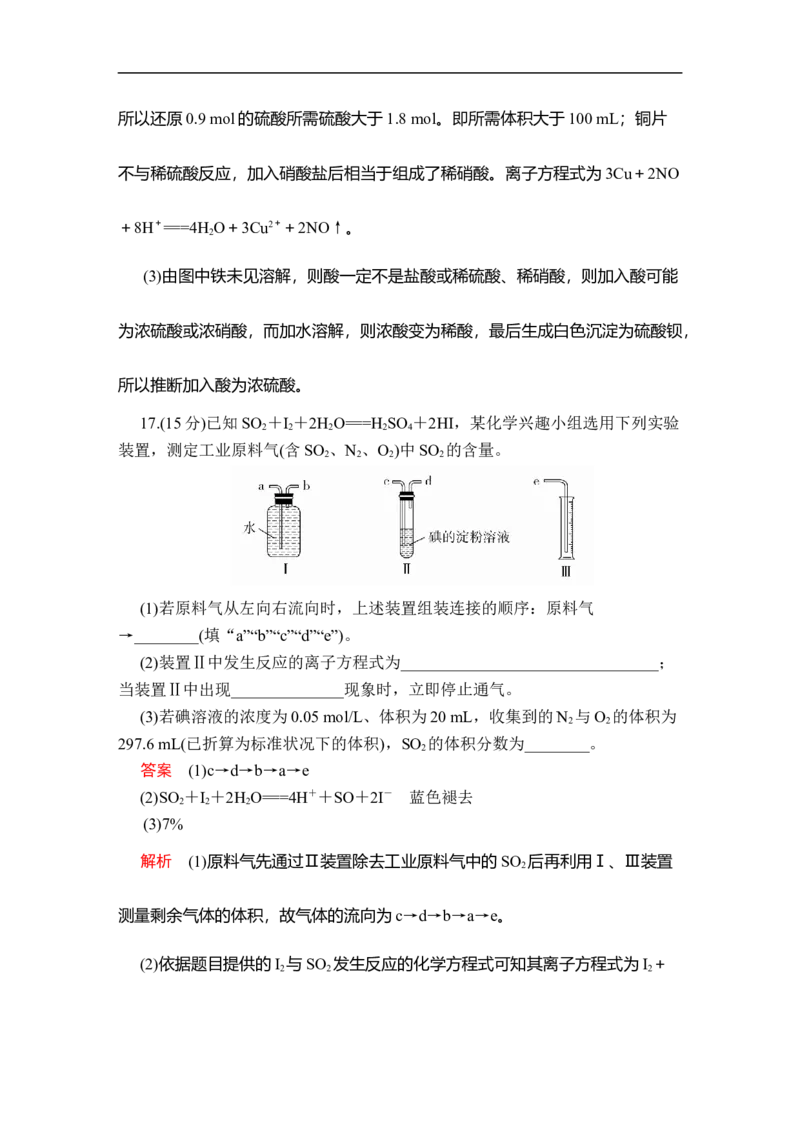
17.(15分)已知SO +I +2H O===H SO +2HI,某化学兴趣小组选用下列实验
2 2 2 2 4
装置,测定工业原料气(含SO 、N 、O )中SO 的含量。
2 2 2 2
(1)若原料气从左向右流向时,上述装置组装连接的顺序:原料气
→________(填“a”“b”“c”“d”“e”)。
(2)装置Ⅱ中发生反应的离子方程式为________________________________;
当装置Ⅱ中出现______________现象时,立即停止通气。
(3)若碘溶液的浓度为0.05 mol/L、体积为20 mL,收集到的N 与O 的体积为
2 2
297.6 mL(已折算为标准状况下的体积),SO 的体积分数为________。
2
答案 (1)c→d→b→a→e
(2)SO +I +2H O===4H++SO+2I- 蓝色褪去
2 2 2
(3)7%
解析 (1)原料气先通过Ⅱ装置除去工业原料气中的SO 后再利用Ⅰ、Ⅲ装置
2
测量剩余气体的体积,故气体的流向为c→d→b→a→e。
(2)依据题目提供的I 与SO 发生反应的化学方程式可知其离子方程式为I +
2 2 2SO +2H O===4H++SO+2I-,当溶液中蓝色褪去时,表明I 与SO 恰好完全反
2 2 2 2
应。
(3)由反应方程式可知:
SO ~ I
2 2
22400 mL 1 mol
V 0.05 mol/L×0.020 L
V=22.4 mL
则SO 的体积分数为×100%=7%。
2
18.(15分)大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含
有下列离子:Na+、Ba2+、NH、Al3+、Cl-、SO、SO、NO等。某研究小组取该
地一定量的酸雨,浓缩后将所得澄清试液分成三份,进行如下实验:
请回答下列问题:
(1)根据实验判断该酸雨中肯定不存在的离子是__________________________,
不能确定的离子有________________。
(2)写出第一份试液滴加淀粉KI溶液时发生反应的离子方程式:______________________。
(3)第三份试液滴加NaOH溶液,加热,整个过程中发生了多个反应,写出其
中两个反应的离子方程式:________________________、
________________________。
(4)设计实验方案,检验该酸雨中是否存在Cl-:
________________________________________。
(5)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量
NO的SO 气体,再慢慢通入O ,发生化学反应后,再喷洒适量蒸馏水即得硫酸
2 2
型酸雨,则NO在上述反应中的作用是______________。
答案 (1)SO、Ba2+ Na+、Cl-
(2)6I-+2NO+8H+===2NO↑+3I +4H O
2 2
(3)H++OH-===H O
2
NH+OH-=====NH ↑+H O
3 2
Al3++3OH-===Al(OH) ↓
3
Al(OH) +OH-===AlO+2H O(任写两个)
3 2
(4)取少量试液滴加足量的Ba(NO ) 溶液,静置,取上层澄清液,加HNO 酸
3 2 3
化的AgNO 溶液,若有白色沉淀生成,则证明存在Cl-
3
(5)催化剂
解析 (1)由第一份试液产生的现象知该酸雨中含有NO,因酸性条件下SO不
能与NO共存,故试液中没有SO;由第二份试液产生的现象知该酸雨中含有
SO,没有Ba2+;由第三份试液产生的现象知该酸雨中含有Al3+、NH。故该酸雨
中肯定不存在的离子是SO、Ba2+,不能确定的离子有Na+、Cl-。
(2)滴加淀粉KI溶液时,I-被氧化为I ,NO被还原为NO。
2
(3)第三份试液中OH-分别与H+、Al3+、NH、Al(OH) 发生反应。
3
(4)检验Cl-时,需要先用足量的Ba(NO ) 溶液将SO除去以排除干扰,然后
3 2
用HNO 酸化的AgNO 溶液进行检验。
3 3(5)通入O 后,2NO+O ===2NO ,NO +SO ===NO+SO ,喷水后SO +
2 2 2 2 2 3 3
H O===H SO ,故NO起催化作用。
2 2 4