文档内容
课时作业
A篇·知识对点训练
1.下列关于硫的说法不正确的是( )
A.试管内壁附着的硫可用二硫化碳溶解除去
B.游离态的硫存在于火山口附近或地壳的岩层里
C.单质硫既有氧化性,又有还原性
D.硫在过量纯氧中的燃烧产物是三氧化硫
答案 D
解析 硫和氧气反应生成物为二氧化硫。
2.下列化合物能由两种单质直接化合生成的是( )
A.Fe S B.CuS C.SO D.SO
2 3 3 2
答案 D
3.某研究小组成员设计鉴别浓硫酸和稀硫酸的如下方案,不合理的是(
)
答案 B
解析 向稀H SO 中加入金属铝片后,产生无色无味气体,B错误。
2 4
4.下列关于浓硫酸与Cu反应的叙述正确的是( )
A.在反应中,浓硫酸只表现出氧化性
B.此反应属于氧化还原反应
C.在反应中,浓硫酸只表现出氧化性D.每1 mol铜参加反应就有2 mol H SO 被还原,同时生成2 mol SO
2 4 2
答案 B
解析 该反应的化学方程式为 2H SO (浓)+Cu=====CuSO +2H O+
2 4 4 2
SO ↑,反应中硫元素的化合价既有降低又有不变,浓硫酸既表现出氧化性,又
2
表现出酸性。该反应属于氧化还原反应,1 mol铜参加反应有1 mol H SO 被还原,
2 4
同时生成1 mol SO 。
2
5.在加热条件下,木炭与浓H SO 反应,产生的气体所具有的性质是( )
2 4
A.能使BaCl 溶液变浑浊
2
B.能使酸性KMnO 溶液或品红溶液褪色
4
C.只用澄清石灰水即可判断某种气体一定存在
D.能使灼热的氧化铜变为亮红色
答案 B
解析 木炭与浓H SO 在加热条件下发生反应:C+2H SO (浓)=====CO ↑
2 4 2 4 2
+2SO ↑+2H O,所得的气体为SO 和CO 的混合物,通入BaCl 溶液中时,不
2 2 2 2 2
发生反应,故不会出现浑浊,A错误;SO 具有还原性和漂白性,B正确;SO
2 2
与CO 都能与Ca(OH) 溶液反应出现浑浊,故不能判断某一种气体一定存在,C
2 2
错误;SO 、CO 都不与灼热的氧化铜反应,D错误。
2 2
6.下列各组物质,常温下能持续发生反应的是( )
A.铁跟浓硫酸 B.碳跟稀硫酸
C.铜跟稀盐酸 D.铁跟稀硫酸
答案 D
解析 铁在浓H SO 中钝化,不能持续反应,A错误;碳与稀H SO 不反应,
2 4 2 4
B错误;铜跟稀盐酸不反应,C错误;Fe可与稀H SO 持续反应,D正确。
2 4
7.下列事实与原因(括号中)对应关系正确的是( )A.在空气中敞口久置的浓硫酸,溶液质量增大(浓硫酸具有难挥发性)
B.向某样品溶液中先滴加过量的稀盐酸无现象,再滴加 BaCl 溶液后出现
2
白色沉淀(样品溶液中含有SO)
C.蔗糖与浓硫酸反应中有海绵状的炭生成(浓硫酸具有吸水性)
D.浓硫酸可与铜反应(只显示浓硫酸的强氧化性)
答案 B
解析 在空气中敞口久置的浓硫酸,溶液质量增大是因为浓硫酸的吸水性;
向样品溶液中加入稀盐酸,没有任何现象,说明一定没有 Ag+,再加入少量
BaCl 溶液,生成白色沉淀,此时溶液为酸性,而 BaSO 既不溶于水也不溶于酸,
2 4
则白色沉淀为BaSO ,溶液中含有SO;蔗糖与浓硫酸反应中有海绵状的炭生成
4
主要是利用了浓硫酸的脱水性;浓硫酸与金属铜的反应中既表现浓硫酸的强氧化
性又显示浓硫酸的酸性。
8.大约4000年前,埃及人已经用硫燃烧所形成的二氧化硫漂白布匹。在古
罗马著名诗人荷马的著作里也讲到硫燃烧有消毒和漂白作用。下列物质漂白原理
相同的是( )
①潮湿的氯气 ②二氧化硫 ③活性炭 ④过氧化钠
A.①③ B.②③ C.①④ D.②④
答案 C
解析 潮湿的氯气和过氧化钠都是由于具有强氧化性而能漂白,二氧化硫为
化合作用,活性炭是吸附作用,故选C。
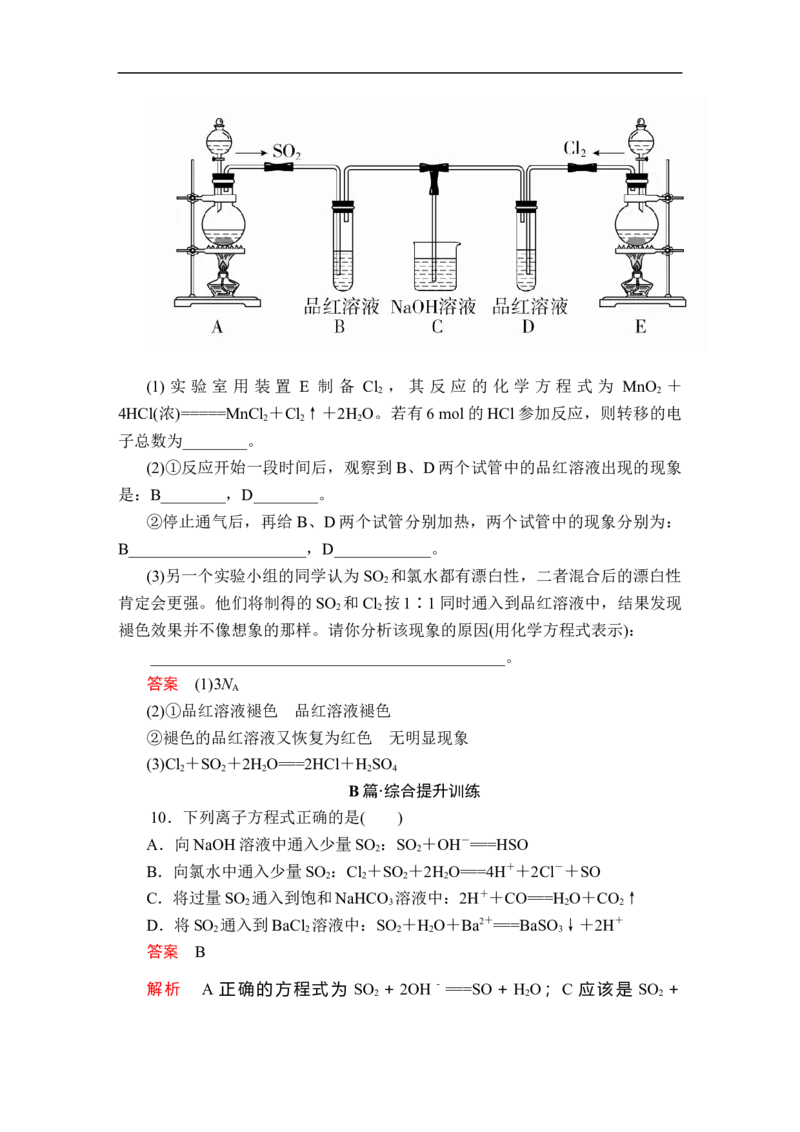
9.某化学实验小组的同学为探究和比较 SO 和氯水的漂白性,设计了如下
2
的实验装置。(1) 实 验 室 用 装 置 E 制 备 Cl , 其 反 应 的 化 学 方 程 式 为 MnO +
2 2
4HCl(浓)=====MnCl +Cl ↑+2H O。若有6 mol的HCl参加反应,则转移的电
2 2 2
子总数为________。
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象
是:B________,D________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:
B______________________,D____________。
(3)另一个实验小组的同学认为SO 和氯水都有漂白性,二者混合后的漂白性
2
肯定会更强。他们将制得的SO 和Cl 按1∶1同时通入到品红溶液中,结果发现
2 2
褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示):
____________________________________________。
答案 (1)3N
A
(2)①品红溶液褪色 品红溶液褪色
②褪色的品红溶液又恢复为红色 无明显现象
(3)Cl +SO +2H O===2HCl+H SO
2 2 2 2 4
B篇·综合提升训练
10.下列离子方程式正确的是( )
A.向NaOH溶液中通入少量SO :SO +OH-===HSO
2 2
B.向氯水中通入少量SO :Cl +SO +2H O===4H++2Cl-+SO
2 2 2 2
C.将过量SO 通入到饱和NaHCO 溶液中:2H++CO===H O+CO ↑
2 3 2 2
D.将SO 通入到BaCl 溶液中:SO +H O+Ba2+===BaSO ↓+2H+
2 2 2 2 3
答案 B
解析 A 正确的方程式为 SO +2OH-===SO+H O;C 应该是 SO +
2 2 2HCO===CO ↑+HSO;D不发生化学反应。
2
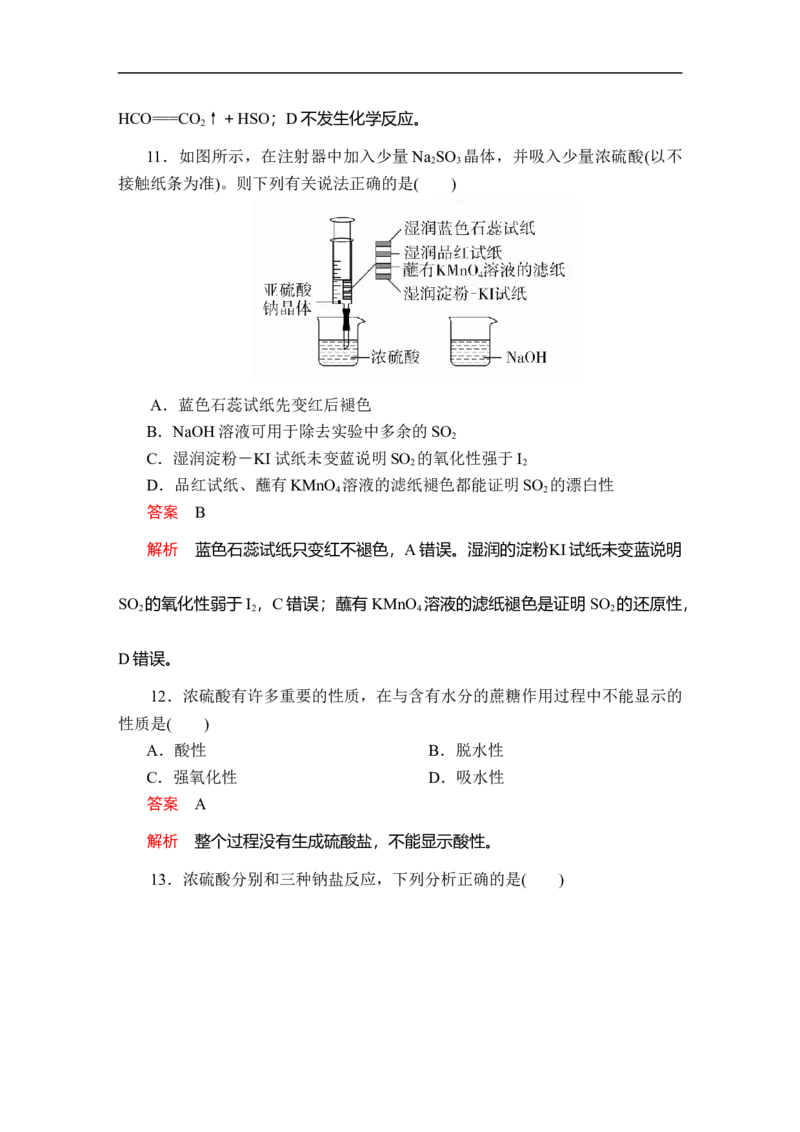
11.如图所示,在注射器中加入少量Na SO 晶体,并吸入少量浓硫酸(以不
2 3
接触纸条为准)。则下列有关说法正确的是( )
A.蓝色石蕊试纸先变红后褪色
B.NaOH溶液可用于除去实验中多余的SO
2
C.湿润淀粉-KI试纸未变蓝说明SO 的氧化性强于I
2 2
D.品红试纸、蘸有KMnO 溶液的滤纸褪色都能证明SO 的漂白性
4 2
答案 B
解析 蓝色石蕊试纸只变红不褪色,A错误。湿润的淀粉KI试纸未变蓝说明
SO 的氧化性弱于I ,C错误;蘸有KMnO 溶液的滤纸褪色是证明SO 的还原性,
2 2 4 2
D错误。
12.浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的
性质是( )
A.酸性 B.脱水性
C.强氧化性 D.吸水性
答案 A
解析 整个过程没有生成硫酸盐,不能显示酸性。
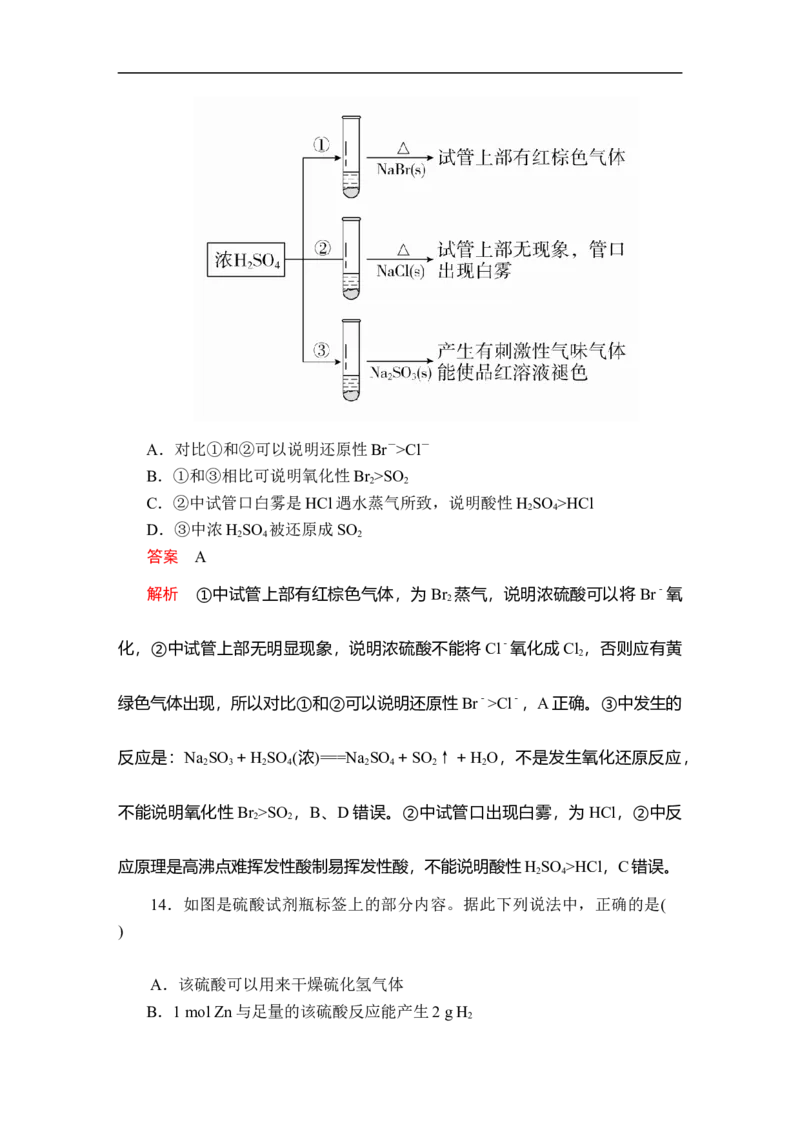
13.浓硫酸分别和三种钠盐反应,下列分析正确的是( )A.对比①和②可以说明还原性Br->Cl-
B.①和③相比可说明氧化性Br >SO
2 2
C.②中试管口白雾是HCl遇水蒸气所致,说明酸性H SO >HCl
2 4
D.③中浓H SO 被还原成SO
2 4 2
答案 A
解析 ①中试管上部有红棕色气体,为 Br 蒸气,说明浓硫酸可以将 Br-氧
2
化,②中试管上部无明显现象,说明浓硫酸不能将 Cl-氧化成Cl ,否则应有黄
2
绿色气体出现,所以对比①和②可以说明还原性Br->Cl-,A正确。③中发生的
反应是:Na SO +H SO (浓)===Na SO +SO ↑+H O,不是发生氧化还原反应,
2 3 2 4 2 4 2 2
不能说明氧化性Br >SO ,B、D错误。②中试管口出现白雾,为 HCl,②中反
2 2
应原理是高沸点难挥发性酸制易挥发性酸,不能说明酸性H SO >HCl,C错误。
2 4
14.如图是硫酸试剂瓶标签上的部分内容。据此下列说法中,正确的是(
)
A.该硫酸可以用来干燥硫化氢气体
B.1 mol Zn与足量的该硫酸反应能产生2 g H
2C.配制200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D.若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗
答案 C
解析 该试剂瓶中所盛试剂为浓硫酸。浓硫酸有强氧化性,不能干燥硫化氢
气体,A错误;浓硫酸与金属反应时还原产物为二氧化硫,不生成氢气,B错误;
浓硫酸和氢氧化钠都具有强烈的腐蚀性,D错误。
15.一定条件下,下列各组物质混合后,两种反应物最有可能恰好反应完的
是( )
A.盐酸与MnO 共热制Cl
2 2
B.铜片、浓硫酸
C.大理石块、硫酸
D.铁粉与稀盐酸
答案 D
解析 MnO 只能和浓盐酸反应;铜片只与浓硫酸反应;大理石与硫酸反应
2
生成的CaSO 是微溶的,它覆盖在大理石块上会将两种反应物隔离开,反应终止。
4
16.某化学小组同学依据化学反应 Zn+2H SO (浓)=====ZnSO +SO ↑+
2 4 4 2
2H O制取22.4 L(标准状况)SO 气体。取65.0 g锌粒与110 mL 98%的浓H SO 充
2 2 2 4
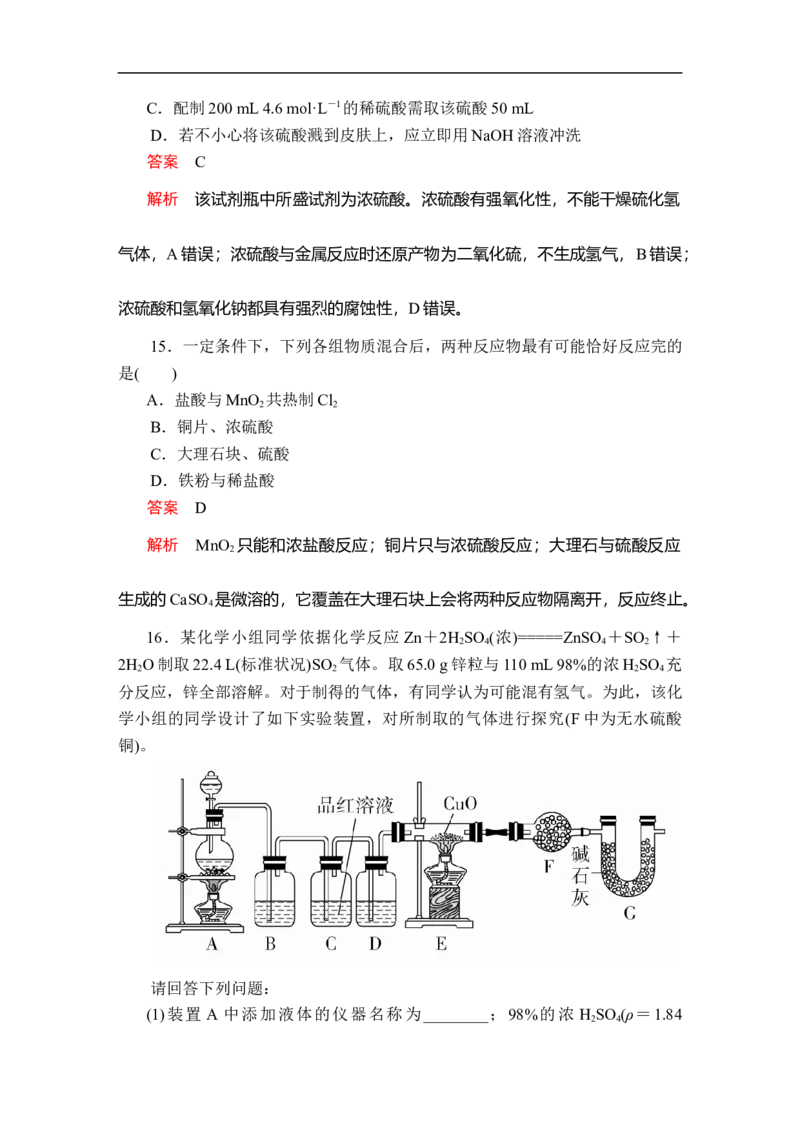
分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,该化
学小组的同学设计了如下实验装置,对所制取的气体进行探究(F中为无水硫酸
铜)。
请回答下列问题:
(1)装置 A 中添加液体的仪器名称为________;98%的浓 H SO (ρ=1.84
2 4g/cm3)的物质的量浓度是________。
(2)装置B是为了吸收SO ,则不能选用下列试剂中的________(填序号)。
2
A.NaOH溶液 B.浓H SO
2 4
C.KMnO 溶液
4
(3)装置D的作用是________。
(4)可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的
实验现象是________________________________。
答案 (1)分液漏斗 18.4 mol/L
(2)B
(3)干燥气体
(4)E中黑色固体变红,F中白色固体变蓝
解析 (1)98%的浓H SO (ρ=1.84 g/cm3)的物质的量浓度是=18.4 mol/L。
2 4
(2)二氧化硫为酸性氧化物,能够与氢氧化钠溶液反应被吸收,故 A不选;
浓硫酸与二氧化硫不反应,不能用来吸收二氧化硫,故 B选;高锰酸钾具有强
氧化性,能够氧化二氧化硫,可以用高锰酸钾溶液吸收二氧化硫,故C不选。
(3)E为加热装置,所以为防止硬质试管炸裂,进入的气体不能含有水蒸气,
所以D的作用为干燥气体。
(4)氢气具有还原性,能将黑色的CuO还原为红色的Cu,且生成水,水能使
无水硫酸铜变蓝色,所以如果有氢气,看到的现象是:装置 E中黑色粉末变红
色,F中无水硫酸铜变蓝色。