文档内容
5.2氮及其化合物—2022-2023学年高一化学人教版(2019)必修第二
册同步课时训练
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1、燃油车易产生 等污染性气体。下列有关这两种氮氧化物的说法正确的是( )
A.NO为红棕色气体
B.NO易溶于水
C. 和水反应生成
D.NO可用排空气法收集
2、下列过程中不属于氮的固定的是( )
A.雷雨天有NO生成
B.植物的根从土壤中吸收铵根离子和硝酸盐
C.工业上用氢气与氮气合成氨
D.豆科植物的根瘤菌把空气巾的氮气转化为硝酸盐
3、下列有关浓硝酸的说法不正确的是( )
A.实验室常用浓硝酸与金属锌反应制备氢气
B.常温下,浓硝酸能使金属铝钝化
C.浓硝酸不稳定,见光易分解,需要避光保存
D.浓硝酸易挥发,打开瓶塞,瓶口有白雾产生
4、下列关于铵盐的说法中正确的是( )
A.所有铵盐受热均可以分解,其产物中都有氨
B.所有铵盐都易溶于水,且其中的N元素均呈-3价
C.向氯化铵溶液中加入浓烧碱溶液共热时反应的离子方程式为
D.氯化铵和氯化钠的固体混合物可用升华法分离
5、下列离子方程式中书写正确的是( )
A.氯化铵固体和熟石灰混合加热:
B.NaOH溶液与 溶液混合加热:
C.向氨水中加入盐酸:
D.向氯化铝溶液中加入过量的氨水:6、只用一种试剂,将 这4种物质的溶液区分开(可加热),
这种试剂是( )
A.NaOH溶液
B. 溶液
C. 溶液
D. 溶液
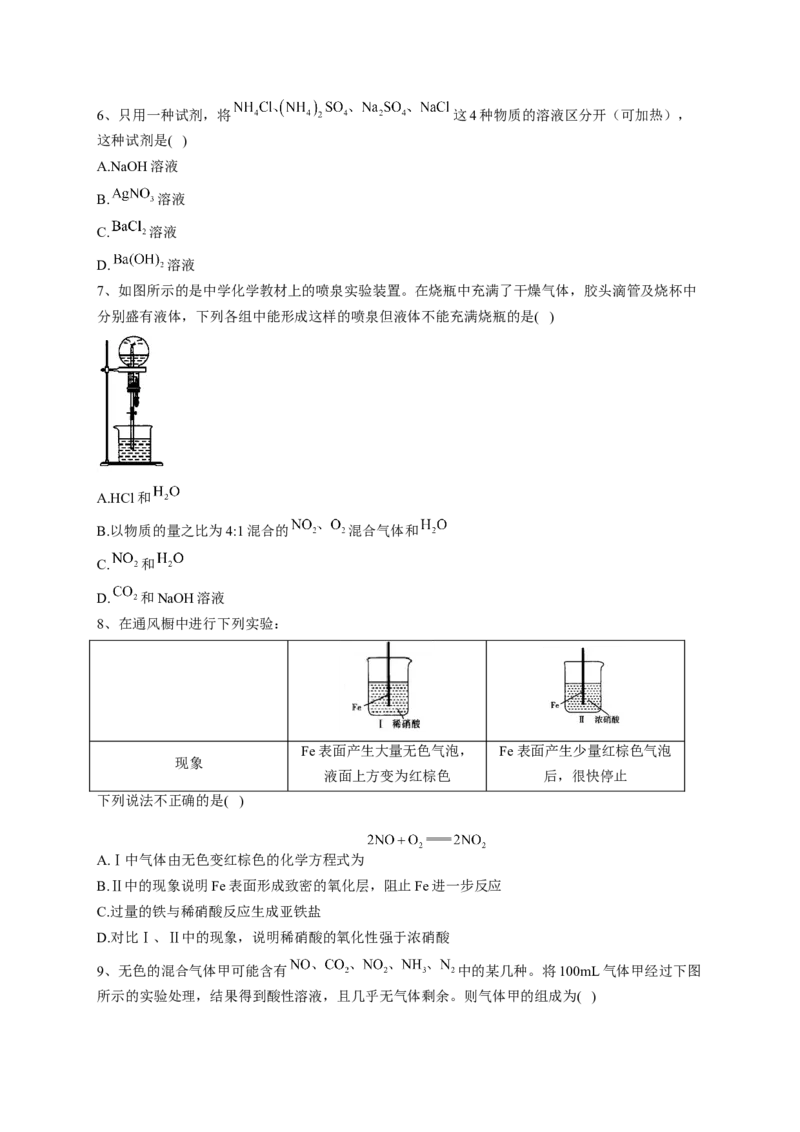
7、如图所示的是中学化学教材上的喷泉实验装置。在烧瓶中充满了干燥气体,胶头滴管及烧杯中
分别盛有液体,下列各组中能形成这样的喷泉但液体不能充满烧瓶的是( )
A.HCl和
B.以物质的量之比为4:1混合的 混合气体和
C. 和
D. 和NaOH溶液
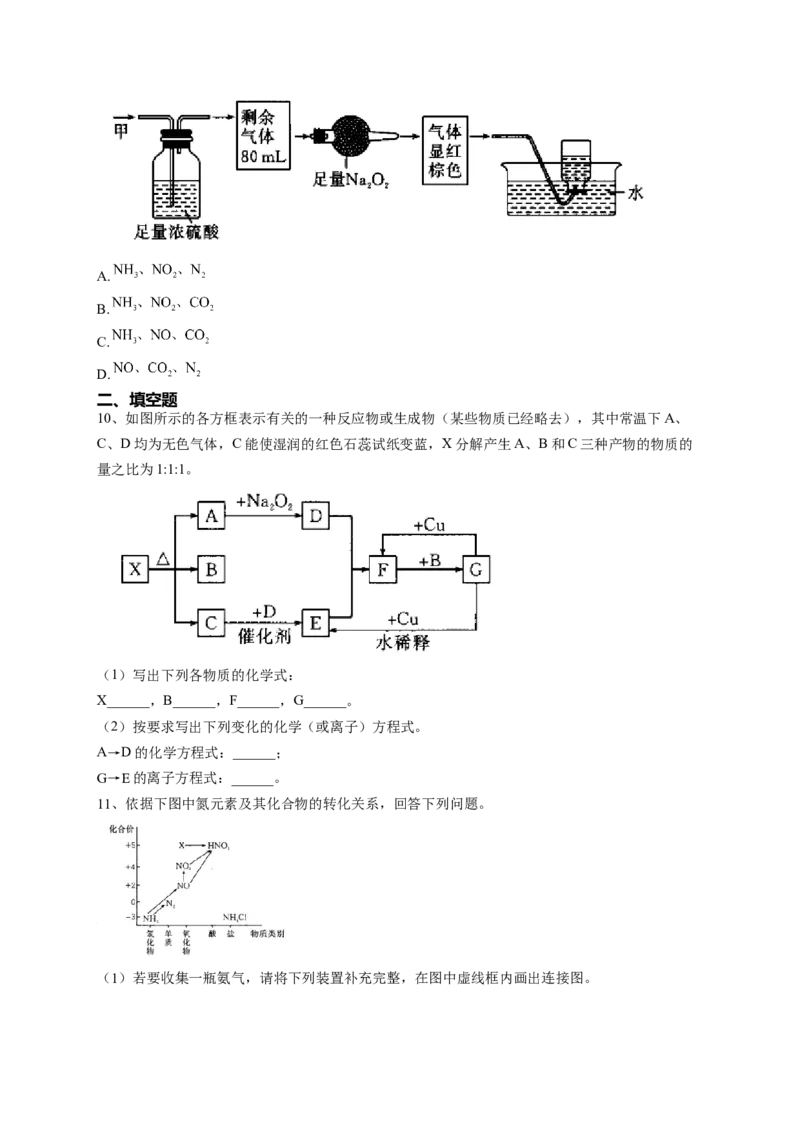
8、在通风橱中进行下列实验:
Fe表面产生大量无色气泡, Fe表面产生少量红棕色气泡
现象
液面上方变为红棕色 后,很快停止
下列说法不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.过量的铁与稀硝酸反应生成亚铁盐
D.对比Ⅰ、Ⅱ中的现象,说明稀硝酸的氧化性强于浓硝酸
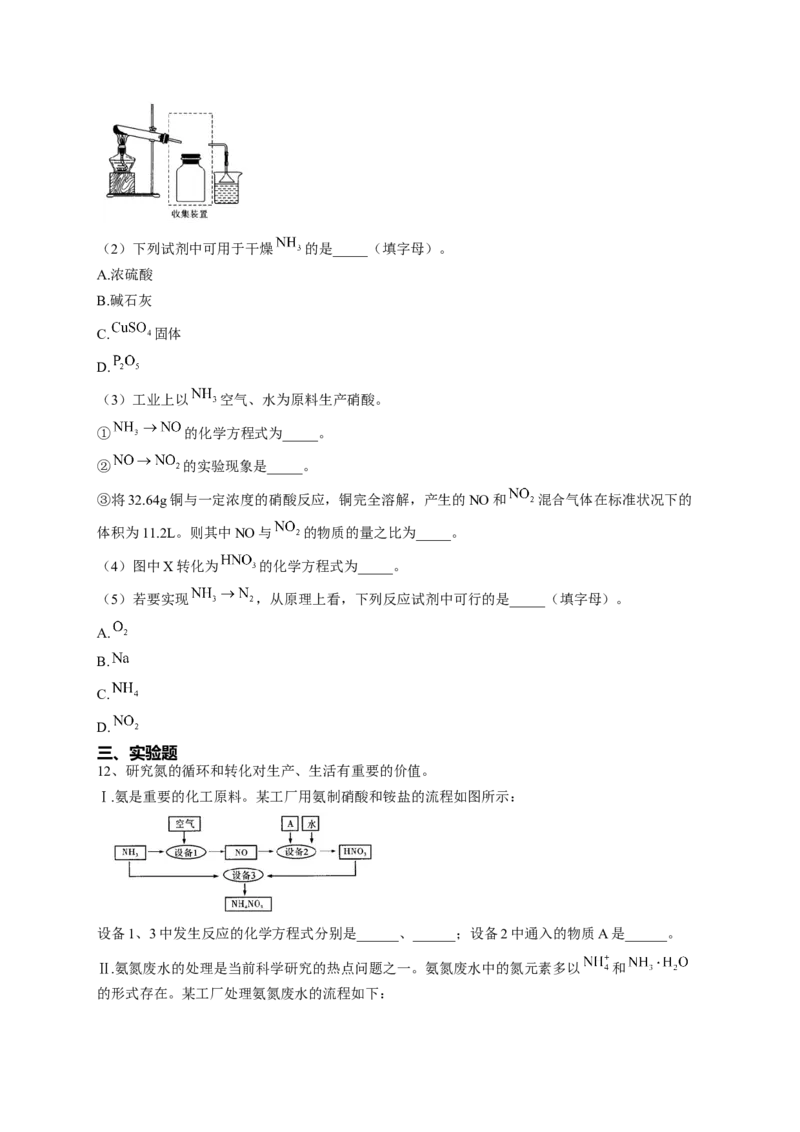
9、无色的混合气体甲可能含有 中的某几种。将100mL气体甲经过下图
所示的实验处理,结果得到酸性溶液,且几乎无气体剩余。则气体甲的组成为( )A.
B.
C.
D.
二、填空题
10、如图所示的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、
C、D均为无色气体,C能使湿润的红色石蕊试纸变蓝,X分解产生A、B和C三种产物的物质的
量之比为1:1:1。
(1)写出下列各物质的化学式:
X______,B______,F______,G______。
(2)按要求写出下列变化的化学(或离子)方程式。
A→D的化学方程式:______;
G→E的离子方程式:______。
11、依据下图中氮元素及其化合物的转化关系,回答下列问题。
(1)若要收集一瓶氨气,请将下列装置补充完整,在图中虚线框内画出连接图。(2)下列试剂中可用于干燥 的是_____(填字母)。
A.浓硫酸
B.碱石灰
C. 固体
D.
(3)工业上以 空气、水为原料生产硝酸。
① 的化学方程式为_____。
② 的实验现象是_____。
③将32.64g铜与一定浓度的硝酸反应,铜完全溶解,产生的NO和 混合气体在标准状况下的
体积为11.2L。则其中NO与 的物质的量之比为_____。
(4)图中X转化为 的化学方程式为_____。
(5)若要实现 ,从原理上看,下列反应试剂中可行的是_____(填字母)。
A.
B.
C.
D.
三、实验题
12、研究氮的循环和转化对生产、生活有重要的价值。
Ⅰ.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:
设备1、3中发生反应的化学方程式分别是______、______;设备2中通入的物质A是______。
Ⅱ.氨氮废水的处理是当前科学研究的热点问题之一。氨氮废水中的氮元素多以 和
的形式存在。某工厂处理氨氮废水的流程如下:(1)过程①的目的是将 转化为 ,并通过鼓入大量热空气将氨气吹出,写出 转化为
的离子方程式:______。
(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质
的化学式分别为______、______。
(3)图中含余氯废水中含有NaClO,则X可选用______(填序号)的溶液达到去除余氯的目的。
a.KOH
b.
c.
d.
13、某课外活动小组在实验室用如图所示装置快速制取 并验证 的某些性质,同时还收集
到少量纯净的氮气。
(1)用生石灰和浓氨水制取 的原理为__________。
(2)实验进行一段时间后,观察到装置C中黑色氧化铜粉末变为红色,装置F中无水硫酸铜变为
蓝色,并且在最后的出气导管口处收集到纯净、干燥的氮气。根据这些现象,写出装置C中发生
反应的化学方程式:__________,该反应说明 具有__________(填序号)。
A.碱性
B.还原性
C.氧化性
D.不稳定性
(3)装置D中浓硫酸的作用是__________。
(4)欲在最后的出气导管口处收集到干燥、纯净的氮气,收集方法是__________(填序号)。
A.排空气法
B.排水法
C.用气囊收集
(5)装置E的作用是__________,装置F的作用主要是__________。参考答案
1、答案:C
解析:NO为无色气体, 为红棕色气体,A项错误;NO不溶于水,B项错误; 和水反应
生成 和NO,C项正确;NO可与氧气反应生成 ,不能用排空气法收集,其不溶于水,
可用排水法收集,D项错误。
2、答案:B
解析:氮的固定是指将大气中游离态的氮转化为氮的化合物,雷雨天在闪电(自然放电)的作用
下,空气中的 与 反应生成NO,属于氮的固定,A不符合题意;含有 或 的物质属于
氮的化合物,即植物的根从土壤中吸收铵根离子和硝酸盐,吸收的对象是氮的化合物,故不属于
氮的固定,B符合题意; 与 反应生成 ,是将游离态的氮转化为氮的化合物,属于氮的固
定,C不符合题意;豆科植物的根瘤菌将空气中的 转化为氮的化合物硝酸盐,属于氮的固定,
D不符合题意。
3、答案:A
解析:浓硝酸的氧化性很强,与金属反应时一般不生成氢气而生成氮氧化物,所以实验室中不能
使用浓硝酸制备氢气,故A不正确;在常温下,铁、铝遇浓硝酸会被氧化,在表面产生一层致密
的氧化物薄膜,对内层的金属起到了保护作用,这种现象叫钝化,故B正确;浓硝酸不稳定,见
光容易分解: ,所以应避光保存,故C正确;浓硝酸易挥发,
打开瓶塞,瓶口有白雾产生,故D正确。
4、答案:C
解析:有的铵盐(如 )受热分解产生氨,有的铵盐受热分解不产生氨,如硝酸铵分解不生
成氨: ,故A错误;铵盐都易溶于水,但不是所有铵盐中的氮元素均
呈-3价,如硝酸铵中硝酸根离子中的氮元素是+5价,故B错误;向氯化铵溶液中加入浓烧碱溶液
共热时反应生成氨气和水,离子方程式为 ,故C正确;可用加热法分
离 和某些固体(不分解、不升华的固体)的混合物,但其过程为先受热分解,再降温化合,
而不是升华,故D错误。
5、答案:C
解析:A项,该反应属于固体间的加热反应,不能写成离子形式,错误;B项,加热条件下
应分解为 和 ,离子方程式应为 ,错误;C项,符
合反应原理及离子方程式的书写要求,正确;D项,一水合氨是弱碱,不能完全电离,向氯化铝溶液中加入过量的氨水应生成 沉淀,离子方程式应为
,错误。
6、答案:D
解析:加热时氢氧化钠溶液能与硫酸铵溶液或氯化铵溶液反应产生有刺激性气味的气体,氢氧化
钠溶液与硫酸钠溶液或氯化钠溶液混合均无明显现象,无法区分,A项不符合题意;硝酸银溶液与
这四种溶液混合均会产生白色沉淀,现象相同,无法区分,B项不符合题意;氯化钡溶液能与硫酸
铵溶液或硫酸钠溶液反应产生白色沉淀,氯化钡溶液与氯化铵溶液或氯化钠溶液混合均无明显现
象,无法区分,C项不符合题意;加热时氢氧化钡溶液与氯化铵溶液反应产生有刺激性气味的气体,
加热时氢氧化钡溶液与硫酸铵溶液反应产生白色沉淀和有刺激性气味的气体,氢氧化钡溶液与硫
酸钠溶液反应产生白色沉淀,氢氧化钡溶液与氯化钠溶液混合无明显现象,可以区分,D项符合题
意。
7、答案:C
解析:喷泉实验产生的根本原因是烧瓶内外产生气压差,当把胶头滴管内的液体挤入烧瓶时,题
中四个选项的物质均可产生气压差形成喷泉。HCl能完全溶于水,液体能充满烧瓶,A错误;以物
质的量之比为4:1混合的 混合气体能恰好与水发生反应: ,
故液体能充满烧瓶,B错误; 与 反应时有NO生成,液体不能充满烧瓶,C正确;
可与NaOH溶液完全反应,液体能充满烧瓶,D错误。
8、答案:D
解析:无色的NO遇氧气生成红棕色气体 ,I中气体由无色变红棕色的化学方程式为
,A项正确;Ⅱ中现象说明Fe在浓硝酸中钝化,B项正确;铁被稀硝酸氧化生
成硝酸铁,过量的铁把硝酸铁还原为硝酸亚铁,C项正确;硝酸越浓,氧化性越强,则浓硝酸的氧
化性强于稀硝酸,D项错误。
9、答案:C
解析:二氧化氮是红棕色的气体,所以无色的混合气体甲中一定不存在二氧化氮,硫酸和碱性气
体能反应,所以100mL气体甲经过足量的浓疏酸,剩余气体为80mL,说明气体甲中一定有
存在且体积为20mL,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为
,一氧化氮无色,可与氧气立即反应变为红棕色的二氧化氮,通
过足量的过氧化钠后气体显红棕色,说明气体甲中有NO、 ,排水法收集气体,且几乎没有气
体剩余,说明气体甲中没有 。综上所述可知,C项符合题意。
10、答案:(1) ; ; ;(2) ;
解析:C能使湿润的红色石蕊试纸变蓝,说明C应该是 ,因此X是铵盐,A能与 反应,
说明A是 或 ,因此D应该是 ,所以E应该是NO,F是 ,则G是 ,B是
,A是 ,由于X分解产生A、B、C三种产物的物质的量之比为1:1:1,因此X是
。
(1)根据以上分析可知,X为 ,B为 ,F为 ,G为 。
(2)A→D的化学方程式是 ;G→E的离子方程式为
。
11、答案:(1)
(2)B
(3)① ;②气体由无色变成红棕色;③13:12
(4)
(5)AD
解析:(1)氨气极易溶于水,且密度比空气的小,收集氨气的方法只能用向下排空气法,集气瓶
中导气管位置应“短进长出”。
(2)因为氨气为碱性气体,需要用碱性干燥剂来干燥,浓硫酸与五氧化二磷为酸性干燥剂,会与
氨气发生反应,不能起到干燥的目的,A、D项错误;碱石灰为碱性干燥剂,可以干燥氨气,B项
正确;硫酸铜只能检验水的存在,不能作为干燥剂,C项错误。
(3)① 为氨气的催化氧化,其化学方程式为 ;②
的实验现象是无色气体变为红棕色气体;③设生成的NO为 mol, 为 mol,
则 0.5mol,铜的物质的量为 ,根据电子守恒规律可知,失电子总数等于得电子总数,即 ,结合上面两式可得
,则NO与 的物质的量之比为0.26mol:0.24mol=13:12。
(4)由题图分析可知,X为氧化物且与 均对应+5价,则X的化学式为 ,X转化为
的化学方程式为 。
(5)若要实现 ,N元素的化合价由-3价变为0价, 作还原剂被氧化,应选择具有
氧化性的物质。 具有氧化性,故A正确;Na具有还原性,故B错误; 与氨气不反应,
故C错误; 具有氧化性,故D正确。
12、答案:Ⅰ. ; ;空气(或 )
Ⅱ.(1)
(2) ;
(3)b
解析:Ⅰ.设备1中 和 发生反应,化学方程式为 ;设备3
中 和 发生反应,化学方程式为 ;设备2中发生的反应为
,所以通入的物质A是 或空气。
Ⅱ.(1)过程①的目的是将 转化为 ,并通过鼓入大量热空气将氨气吹出, 转化为
的离子方程式为 。
(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应的化学方程式为
,所以含氮元素、氯元素的物质的化学式分别为 、
NaCl。
(3)含余氯废水中含有NaClO,要除去NaClO需加入还原性物质 。
13、答案:(1)生石灰与浓氨水中的水反应放出大量的热,使 受热分解生成 ,又
由于温度升高, 的溶解度减小,从溶液中逸出(2) ;B
(3)干燥 ,并吸收多余的氨气,防止其污染空气
(4)C
(5)干燥 ;检验装置C中是否有水生成
解析:分析实验过程如下:
(1)CaO与浓氨水中的水反应生成 ,同时放出大量的热,使 受热分解生成
,又由于温度升高, 的溶解度减小,从溶液中逸出。
(2)装置C中的CuO与 发生反应,CuO转化为Cu, 转化为 ,同时有 生成,在
该反应中CuO得到电子, 失去电子,表现出 的还原性。
(3)多余的 被装置D中的浓硫酸吸收,防止其逸出而污染环境,同时浓硫酸能干燥 。
(4) 的密度与空气相近,不能用排空气法进行收集,排水法收集到的 中有水蒸气,故只有
用气囊收集才能得到干燥、纯净的 。
(5)装置E中盛放的是碱石灰,其作用是吸收 中的水蒸气,干燥 。装置F中盛放的无水
硫酸铜与 作用变为蓝色,所以装置F的作用主要是检验装置C中是否有 生成。