文档内容
课时作业
A篇·知识对点训练
知识点1 硝酸的性质
1.关于硝酸的说法正确的是( )
A.硝酸电离出的H+,能被Zn、Fe等金属还原成H
2
B.浓HNO 与浓HCl按3∶1的体积比所得的混合物叫王水
3
C.硝酸与金属反应时,主要是+5价的氮元素得电子
D.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
答案 C
解析 A项,硝酸能电离出 H+,但氧化性NO(H+)>H+,H+不能被Zn、Fe
等金属还原成H ,错误;B项,浓HNO 与浓HCl按1∶3的体积比所得的混合
2 3
物叫王水,错误;C项,硝酸与金属反应时,主要是+5价的氮元素得电子,正
确;D项,常温下,向浓HNO 中投入Fe片,发生钝化,不会产生大量的红棕
3
色气体,错误。
2.从经济效益和环境保护的观点出发,由铜制取硝酸铜最适宜的方法是(
)
A.Cu与浓HNO ―→Cu(NO )
3 3 2
B.Cu与稀HNO ―→Cu(NO )
3 3 2
C.Cu――→CuO――→Cu(NO )
3 2
D.Cu+AgNO ―→Cu(NO )
3 3 2
答案 C
解析 A项,生成的NO 会造成大气污染,不正确;B项,生成的NO也会
2
造成大气污染,不正确;C项,生成等量的硝酸铜所用的原料少比较经济,又不
会对环境造成污染,正确;D项,硝酸银成本较高,同时硝酸银会对环境造成一
定的污染,主要是重金属污染,不正确。3.将铜粉放入稀硫酸中,加热无明显反应,但加入某盐后,发现铜粉质量
逐渐减少,该盐是( )
A.硫酸亚铁 B.硫酸锌
C.硝酸钾 D.氯化钠
答案 C
解析 在酸性溶液中,硝酸盐具有氧化性,能把铜氧化生成硝酸铜和 NO,
选项C符合题意。
4.0.3 mol Cu和含1.2 mol HNO 的浓硝酸,充分反应后,生成 NO 的量为(
3 2
)
A.0.2 mol B.0.6 mol
C.小于0.6 mol D.大于0.6 mol
答案 C
解析 因铜与浓硝酸反应:Cu+4HNO (浓)===
3
Cu(NO ) +2NO ↑+2H O,随着反应的进行,浓硝酸变稀,稀硝酸与铜反
3 2 2 2
应:3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O,所以放出的 NO 小于 0.6
3 3 2 2 2
mol。
5.将 1.92 g 铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体
1.12 L(标准状况下)。则所消耗硝酸的物质的量是( )
A.0.12 mol B.0.11 mol
C.0.09 mol D.0.08 mol
答案 B
解析 铜与HNO 反应时,消耗的HNO 转变为
3 3
Cu(NO ) 和氮的氧化物(NO 或 NO)。n(Cu)==0.03 mol;n(气体)==0.05
3 2 2
mol;所以共耗HNO 的物质的量n(HNO )=0.03 mol×2+0.05 mol=0.11 mol。
3 3
6.在浓硝酸中放入铜片:
(1)开始反应的化学方程式为__________________________,实验现象为
____________________________。(2)若铜有剩余,则反应将要结束时的反应方程式为______________。
(3)待反应停止后,再加入少量 25%的稀硫酸,这时铜片上又有气泡产生,
其原因是______________________________________________。
(4)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生 5.6 L(标准状
况)气体。则所消耗的 HNO 的物质的量为________,其中显氧化性的硝酸的物
3
质的量为________。
答案 (1)Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O 铜片逐渐变小,溶
3 3 2 2 2
液颜色变成蓝色,并有红棕色气体产生
(2)3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O
3 3 2 2
(3)溶液中有硝酸根离子,加入稀硫酸后增加了溶液中氢离子的浓度,发生反
应:3Cu+8H++2NO===3Cu2++2NO↑+4H O
2
(4)0.65 mol 0.25 mol
解析 随着反应的进行,硝酸的浓度不断减小,反应结束前实质上是铜与稀
硝酸的反应。反应停止后再加稀H SO ,溶液中的NO在酸性条件下,又相当于
2 4
稀HNO 与铜反应。
3
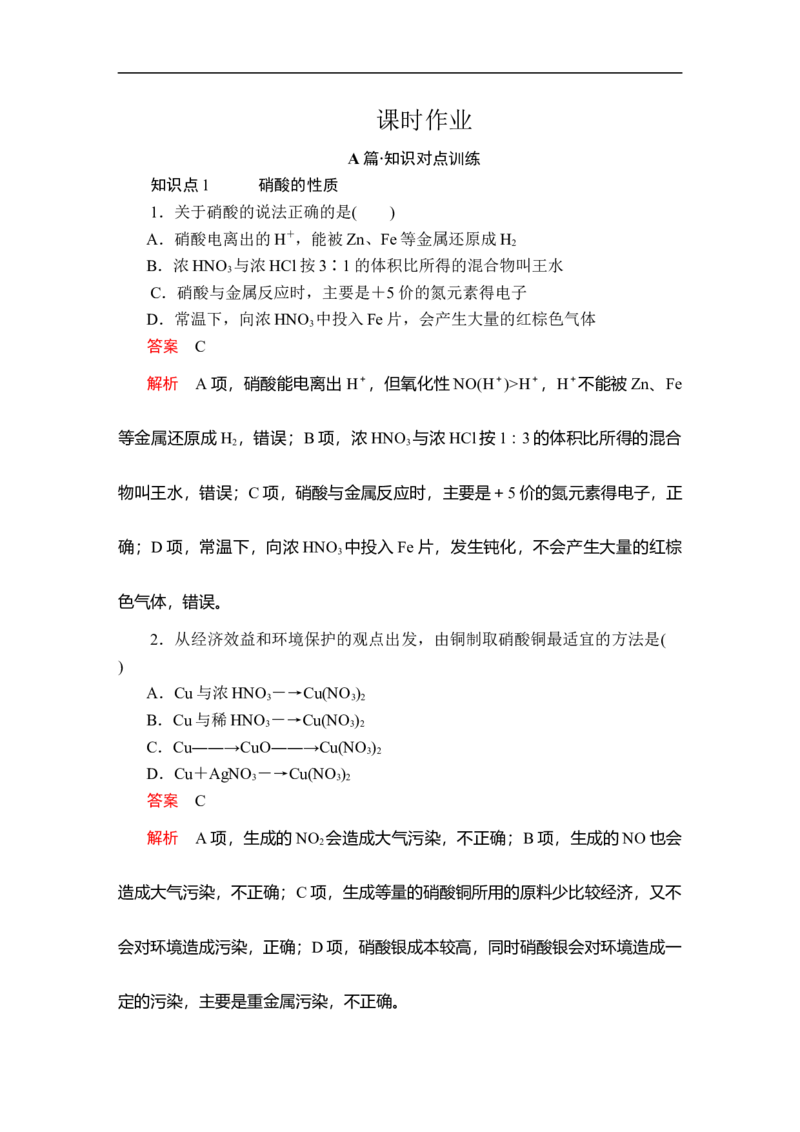
7.为了证明稀硝酸与铜反应的气体产物是 NO,某同学设计了如下实验装
置和实验方案。
实验步骤:
(1)关闭K ,打开K ,向试管中加石灰石,通过分液漏斗向其中加入一定的
1 2
稀硝酸,则加入石灰石的作用是________________________________,反应的化
学方程式是________________________________________。
(2)将铜丝插入稀硝酸中,微热大试管。该步反应的离子方程式是__________________________________。
(3)充分反应后,打开开关 K ,通过气囊鼓入空气,可以观察到烧瓶中
1
______________________,证明稀硝酸与铜反应的气体产物是NO。
(4)NaOH溶液的作用________________________。
答案 (1)石灰石与稀硝酸生成 CO ,把装置中的氧气排尽 CaCO +
2 3
2HNO ===Ca(NO ) +CO ↑+H O
3 3 2 2 2
(2)3Cu+8H++2NO===3Cu2++2NO↑+4H O
2
(3)无色气体变成红棕色气体
(4)尾气处理,以免气体污染环境
知识点2 酸雨及防治
8.“保护环境,就是保护人类自己。”下列环境问题与产生的主要原因不
相符的是( )
①“臭氧空洞”主要是大量使用氟氯代烃等引起的 ②“光化学烟雾”主要
是由NO 等引起的
2
③“酸雨”主要是由空气中CO 浓度增大引起的
2
④“白色污染”主要是由聚乙烯塑料等引起的
⑤“厄尔尼诺”现象由空气中CO 浓度增大引起的
2
⑥“温室效应”主要是由空气中CO 浓度增大引起的
2
⑦“赤潮”主要是由水体中P、N等元素过量引起的
A.只有①② B.只有②③⑤
C.全部 D.只有③
答案 D
解析 “酸雨”的形成主要是SO 及NO 引起,故③不正确。
2 x
B篇·综合提升训练
9.1.92 g Cu投入到一定量的浓硝酸中,铜完全溶解,生成的气体的颜色越
来越浅,共收集到672 mL的气体(气体体积已折算为标准状况下)。将盛有此气
体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于
水,则通入的氧气的体积为( )
A.168 mL B.224 mL
C.336 mL D.504 mL
答案 C
解析 此题首先要理清电子的转移情况,然后找出关系式:,整个过程相当于 Cu失的
e-转移给O ,由此得出Cu和O 的关系式:2Cu~O ,计算出O 的体积。
2 2 2 2
10.各取0.1 mol Cu分别投入足量的下列酸中(必要时可加热):①浓硫酸,
②浓硝酸,③稀硝酸。充分反应后在相同的条件下得到的气体体积由大到小的顺
序是( )
A.②③① B.②①③
C.①②③ D.③①②
答案 B
解析 由于Cu的用量一样,电子转移数目相等,产生 1 mol 气体需要获得
的电子:浓H SO →SO 2 mol e-;浓HNO →NO 1 mol e-;稀HNO →NO,3 mol
2 4 2, 3 2, 3
e-。故产生的气体的体积由大到小的顺序为②>①>③。
11.将红热的木炭与浓硝酸共热产生的气体等分为①和②两份,第①份先通
过适量蒸馏水,再通入足量澄清石灰水中;第②份直接通入少量澄清石灰水中。
则澄清石灰水的变化最可能为( )
A.①不变浑浊,②变乳白色
B.①变乳白色,②不变浑浊
C.①变乳白色,②变乳白色
D.①不变浑浊,②不变浑浊
答案 B
解析 碳与浓硝酸反应产生CO 和NO 的混合气体,而NO 可与水反应生成
2 2 2
硝酸,故将混合气体直接通入少量澄清石灰水中,会产生 Ca(NO ) 溶液,难以
3 2
得到 CaCO 沉淀;将混合气体先通过适量蒸馏水,NO 与水反应生成硝酸和
3 2
NO,则NO和CO 的混合气体再通入足量澄清石灰水中会产生CaCO 沉淀。
2 3
12.将0.1 mol铜与40 mL 10 mol·L-1 HNO 充分反应后,溶液中含 a mol H
3+,由此可知( )
A.生成的气体在标准状况下的体积为4.48 L
B.生成的气体在标准状况下的体积为1.49 L
C.被还原的硝酸的物质的量为(0.2-a) mol
D.反应后溶液中所含NO的物质的量为0.2 mol
答案 C
解析 溶液中含有H+,则HNO 过量。在反应过程中HNO 逐渐变稀,实际
3 3
上发生了两个反应:①Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O、②3Cu+
3 3 2 2 2
8HNO (稀)===3Cu(NO ) +2NO↑+4H O。反应消耗的HNO 包括起酸性作用和
3 3 2 2 3
氧化剂作用两部分,前者反应后以 Cu(NO ) 形式存在,后者被还原后生成
3 2
NO 、NO 气体,从两反应式看出:Cu~2HNO (酸)~Cu(NO ) ,HNO (氧化
2 3 3 2 3
剂)~NO (或NO),作酸用的硝酸为0.2 mol,生成的气体为NO、NO 的混合气
2 2
体,溶液中有a mol的HNO 过量,则被还原的HNO 的物质的量=生成的气体
3 3
的物质的量=(0.4-a-0.2) mol=(0.2-a) mol,溶液中的NO由过量的HNO 和
3
Cu(NO ) 中的NO组成,为(a+0.2) mol。
3 2
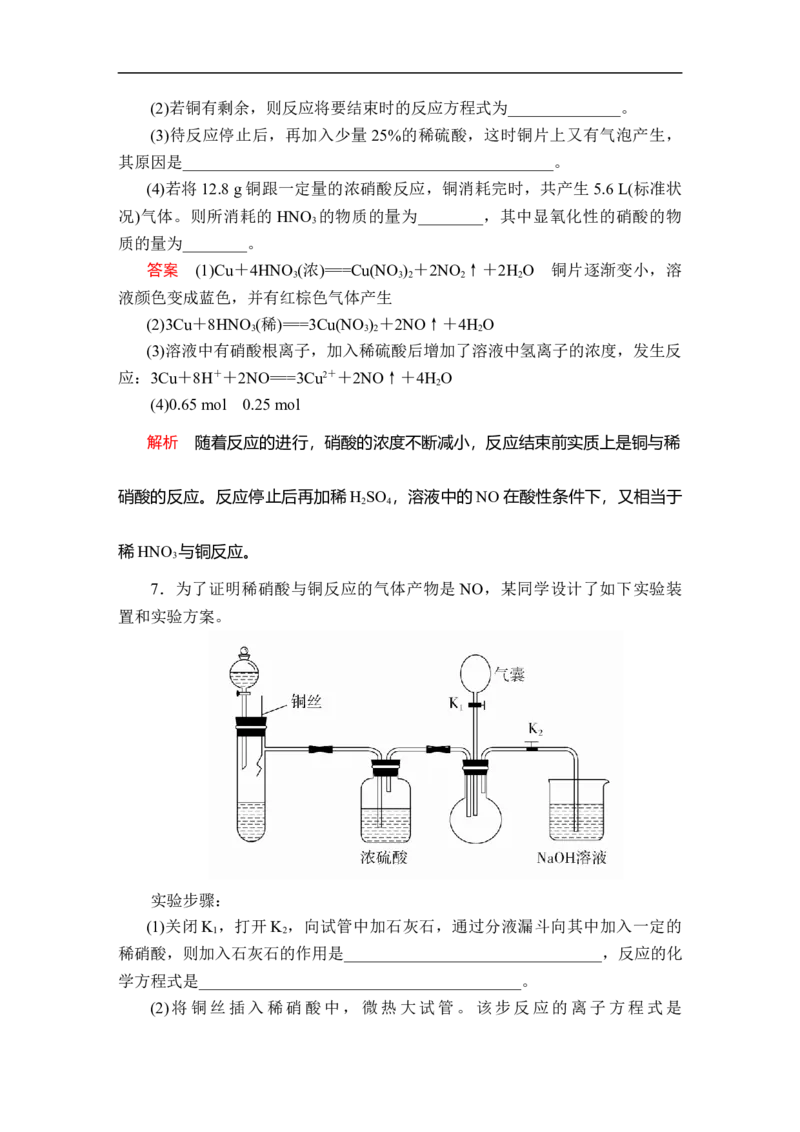
13.(1)实验室用金属铜和稀硝酸制取NO的化学方程式为______________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易
的、能随开随用、随关随停的NO气体发生装置,如图甲所示。①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝
状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填
选项编号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色
的,原因是________________________________(填化学方程式)。
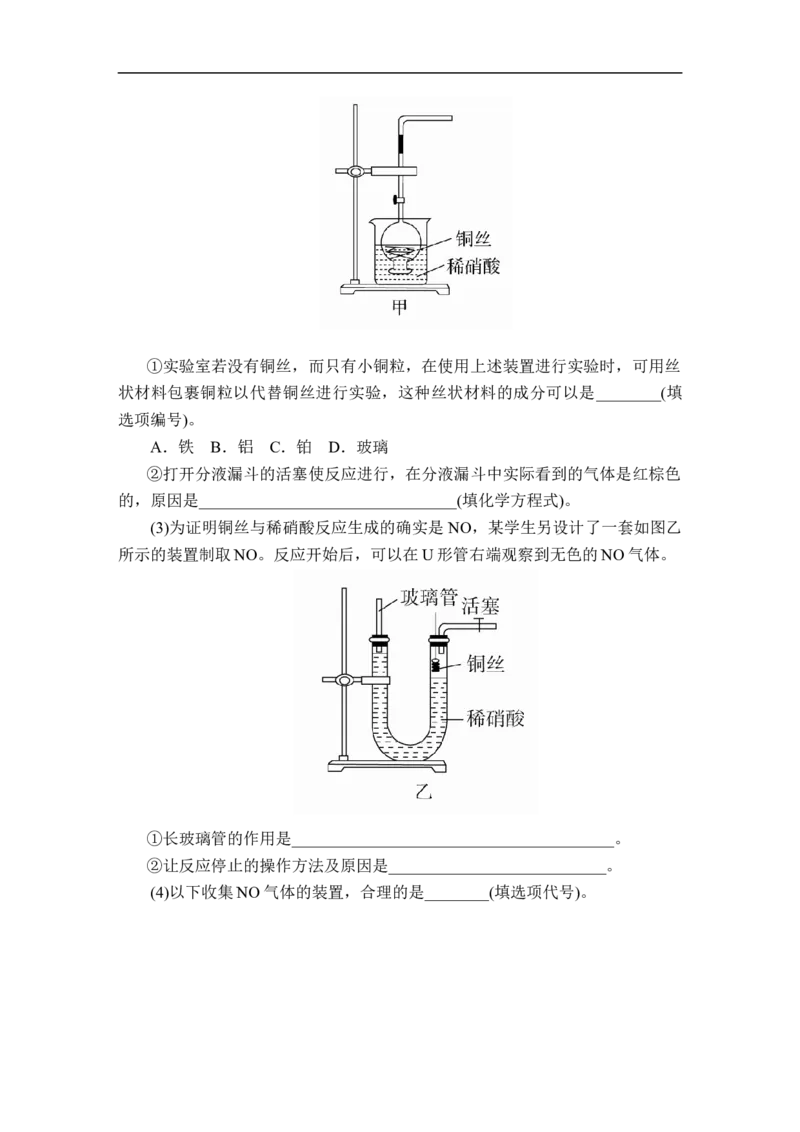
(3)为证明铜丝与稀硝酸反应生成的确实是 NO,某学生另设计了一套如图乙
所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是________________________________________。
②让反应停止的操作方法及原因是___________________________。
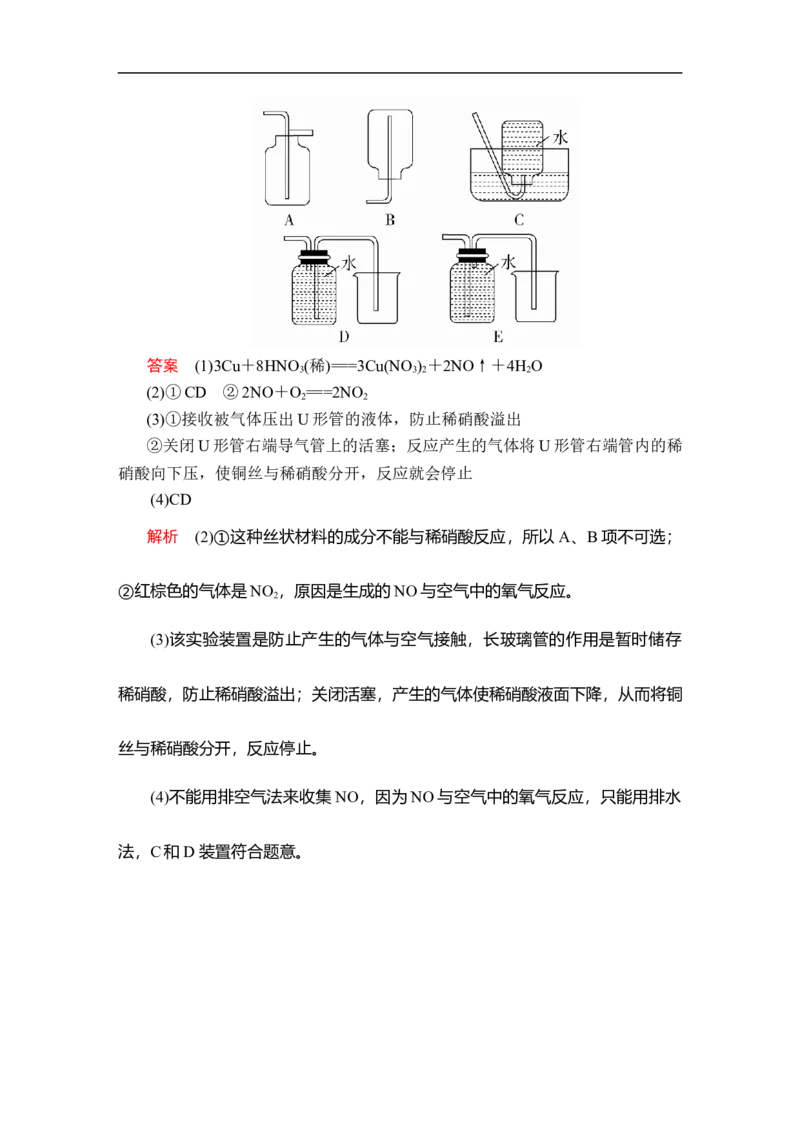
(4)以下收集NO气体的装置,合理的是________(填选项代号)。答案 (1)3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O
3 3 2 2
(2)①CD ②2NO+O ===2NO
2 2
(3)①接收被气体压出U形管的液体,防止稀硝酸溢出
②关闭U形管右端导气管上的活塞;反应产生的气体将U形管右端管内的稀
硝酸向下压,使铜丝与稀硝酸分开,反应就会停止
(4)CD
解析 (2)①这种丝状材料的成分不能与稀硝酸反应,所以 A、B项不可选;
②红棕色的气体是NO ,原因是生成的NO与空气中的氧气反应。
2
(3)该实验装置是防止产生的气体与空气接触,长玻璃管的作用是暂时储存
稀硝酸,防止稀硝酸溢出;关闭活塞,产生的气体使稀硝酸液面下降,从而将铜
丝与稀硝酸分开,反应停止。
(4)不能用排空气法来收集 NO,因为NO与空气中的氧气反应,只能用排水
法,C和D装置符合题意。