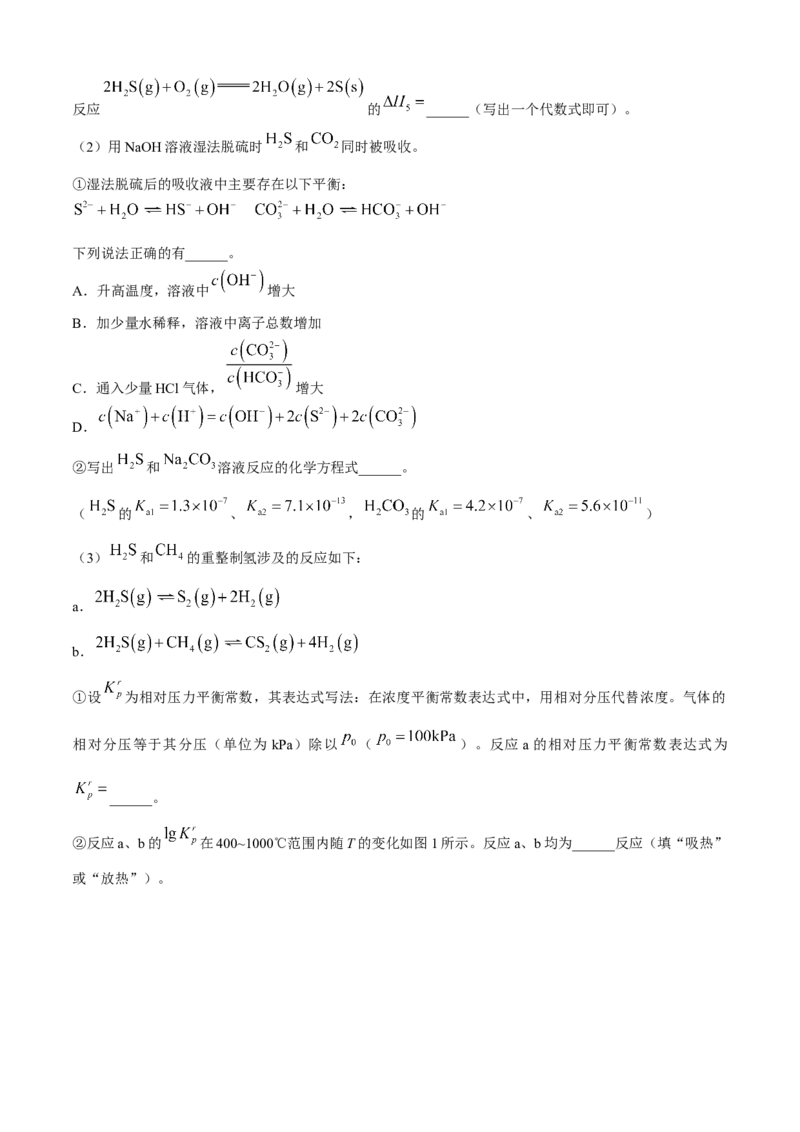文档内容
★启用前注意保密 试卷类型:B
2024 年广州市普通高中毕业班综合测试(二)
化 学
本试卷共8页,20小题,满分100分。考试用时75分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考生号、试室号
和座位号填写在答题卡上。用2B铅笔将试卷类型(B)填涂在答题卡相应位置上。并在化学
答题卡相应位置上填涂考生号。
2.作答选择题时,选出每小题答案后,用 2B铅笔把答题卡对应题目选项的答案信息点涂黑;
如需改动,用橡皮擦干净后,再选涂其他答案。答案不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相
应位置上;如需改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液。不
按以上要求作答无效。
4.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、单项选择题:本题共16小题,共4分。第1~10小题,每小题2分;第11~16小题,每小
题4分。每小题只有一个选项符合题意。
1.我国古代的容器充分展现工艺之美。下列容器主要由合金材料制成的是( )
A.人面鱼纹彩陶盆 B.玛瑙梅花耳杯 C.青铜敦 D.彩漆木雕鸳鸯形盒
2.化学推动科技进步。下列说法正确的是( )
A.我国科学家首次合成了新核素 , 和 互为同位素
B.中国空间站机械臂采用铝合金材料,Al是第ⅢA族元素
C.鹊桥号中继卫星的天线由镀金钼丝织成,镀金钼丝是无机非金属材料
D.中国天眼主镜面的防腐膜中含有聚苯乙烯,聚苯乙烯是天然高分子材料
3.广东的非物质文化遗产丰富多彩。下列说法正确的是( )
A.绘有金色花纹的广彩瓷器含有硅单质
B.使用蚕丝制作粤绣,蚕丝的主要成分是蛋白质
C.龙舟表面所涂红色颜料的主要成分是氧化亚铁
D.广东剪纸所用纸张的氧化漂白过程不涉及化学变化
4.下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 用氢氟酸刻蚀玻璃器皿 氢氟酸是弱酸
B 用草木灰对农作物施肥 草木灰含有钾元素
学科网(北京)股份有限公司C 利用铝热反应焊接钢轨 高温下铝能还原氧化铁
D 将锌块镶嵌在轮船底部防腐 锌的金属性比铁强
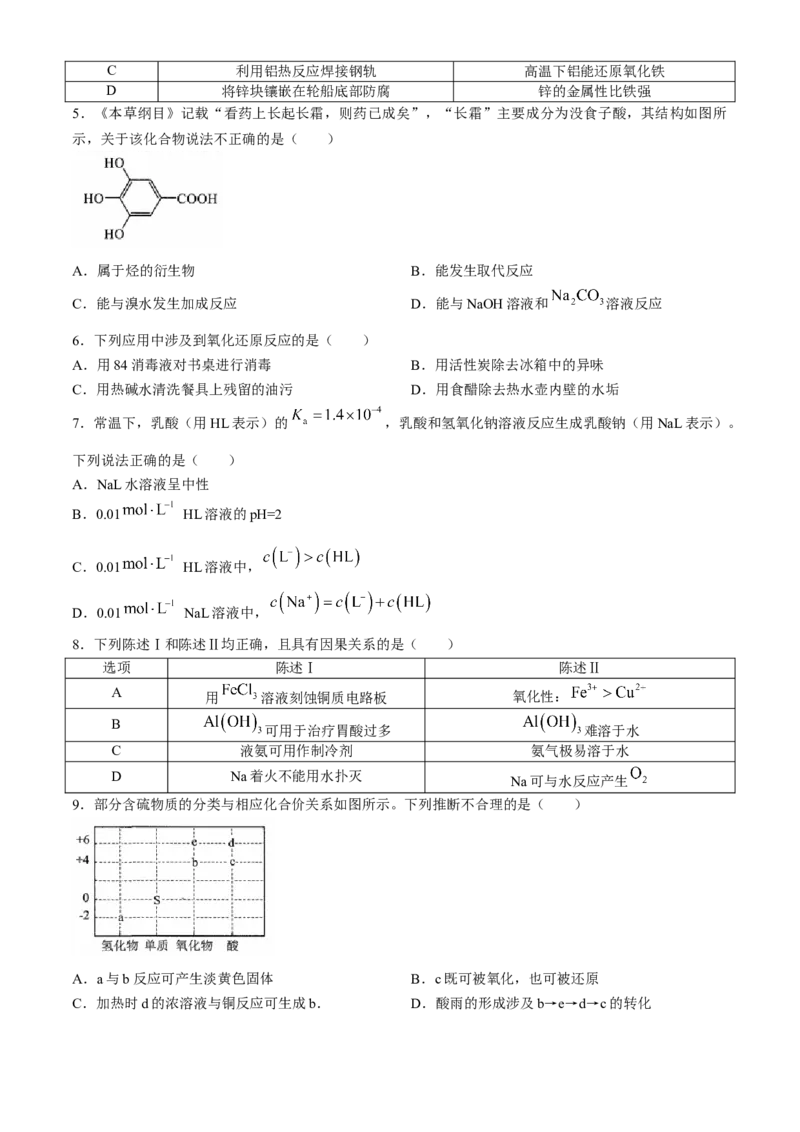
5.《本草纲目》记载“看药上长起长霜,则药已成矣”,“长霜”主要成分为没食子酸,其结构如图所
示,关于该化合物说法不正确的是( )
A.属于烃的衍生物 B.能发生取代反应
C.能与溴水发生加成反应 D.能与NaOH溶液和 溶液反应
6.下列应用中涉及到氧化还原反应的是( )
A.用84消毒液对书桌进行消毒 B.用活性炭除去冰箱中的异味
C.用热碱水清洗餐具上残留的油污 D.用食醋除去热水壶内壁的水垢
7.常温下,乳酸(用HL表示)的 ,乳酸和氢氧化钠溶液反应生成乳酸钠(用NaL表示)。
下列说法正确的是( )
A.NaL水溶液呈中性
B.0.01 HL溶液的pH=2
C.0.01 HL溶液中,
D.0.01 NaL溶液中,
8.下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 用 溶液刻蚀铜质电路板 氧化性:
B
可用于治疗胃酸过多 难溶于水
C 液氨可用作制冷剂 氨气极易溶于水
D Na着火不能用水扑灭
Na可与水反应产生
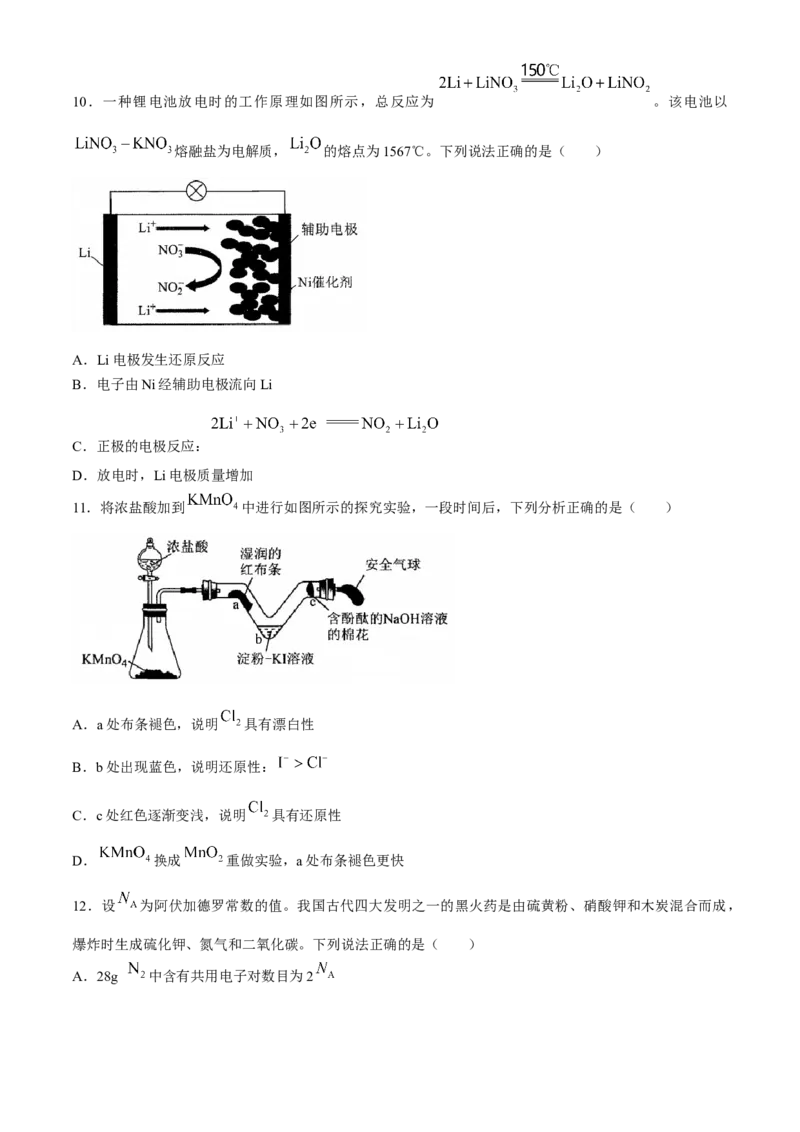
9.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a与b反应可产生淡黄色固体 B.c既可被氧化,也可被还原
C.加热时d的浓溶液与铜反应可生成b. D.酸雨的形成涉及b→e→d→c的转化
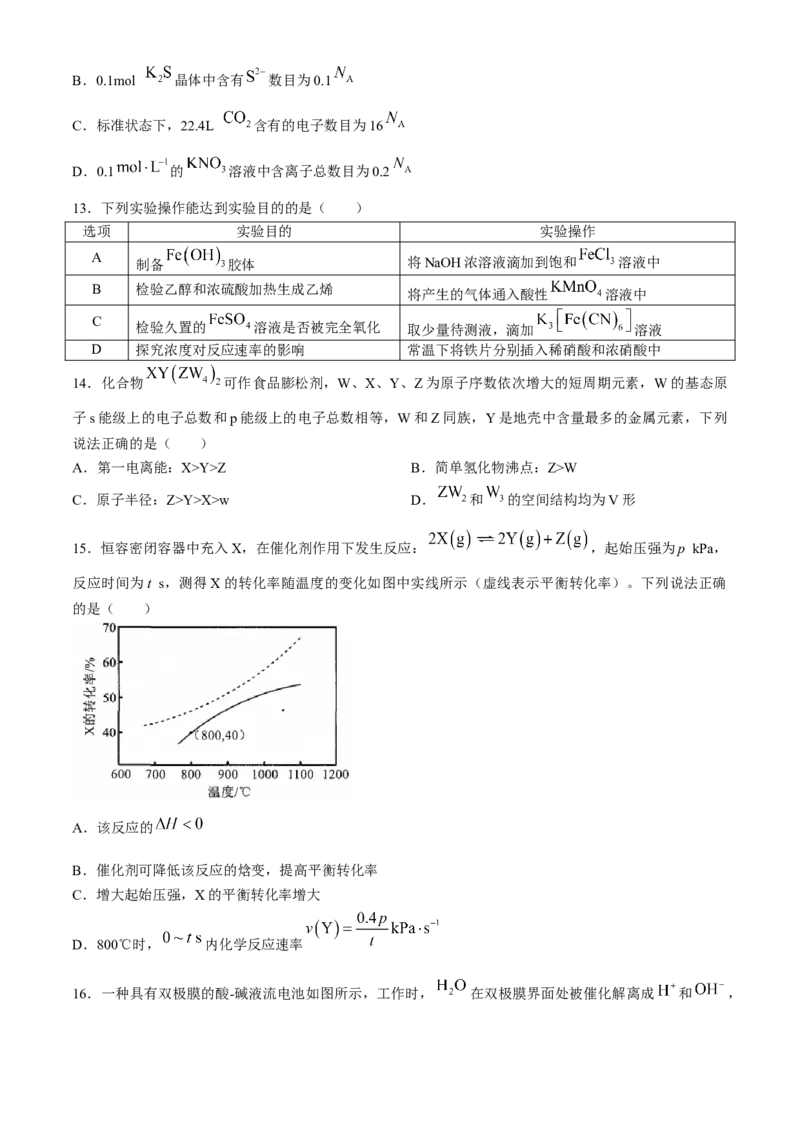
学科网(北京)股份有限公司10.一种锂电池放电时的工作原理如图所示,总反应为 。该电池以
熔融盐为电解质, 的熔点为1567℃。下列说法正确的是( )
A.Li电极发生还原反应
B.电子由Ni经辅助电极流向Li
C.正极的电极反应:
D.放电时,Li电极质量增加
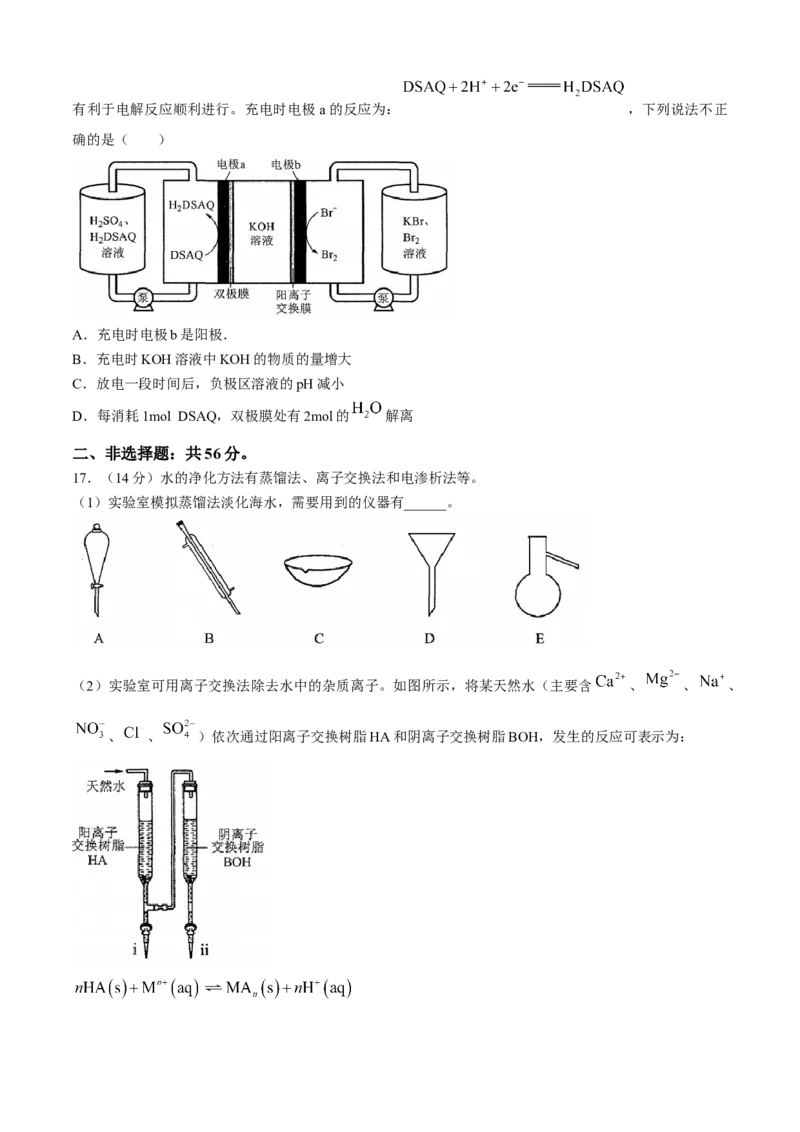
11.将浓盐酸加到 中进行如图所示的探究实验,一段时间后,下列分析正确的是( )
A.a处布条褪色,说明 具有漂白性
B.b处出现蓝色,说明还原性:
C.c处红色逐渐变浅,说明 具有还原性
D. 换成 重做实验,a处布条褪色更快
12.设 为阿伏加德罗常数的值。我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭混合而成,
爆炸时生成硫化钾、氮气和二氧化碳。下列说法正确的是( )
A.28g 中含有共用电子对数目为2
学科网(北京)股份有限公司B.0.1mol 晶体中含有 数目为0.1
C.标准状态下,22.4L 含有的电子数目为16
D.0.1 的 溶液中含离子总数目为0.2
13.下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A
制备 胶体 将NaOH浓溶液滴加到饱和 溶液中
B 检验乙醇和浓硫酸加热生成乙烯
将产生的气体通入酸性 溶液中
C
检验久置的 溶液是否被完全氧化 取少量待测液,滴加 溶液
D 探究浓度对反应速率的影响 常温下将铁片分别插入稀硝酸和浓硝酸中
14.化合物 可作食品膨松剂,W、X、Y、Z为原子序数依次增大的短周期元素,W的基态原
子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含量最多的金属元素,下列
说法正确的是( )
A.第一电离能:X>Y>Z B.简单氢化物沸点:Z>W
C.原子半径:Z>Y>X>w D. 和 的空间结构均为V形
15.恒容密闭容器中充入X,在催化剂作用下发生反应: ,起始压强为p kPa,
反应时间为t s,测得X的转化率随温度的变化如图中实线所示(虚线表示平衡转化率)。下列说法正确
的是( )
A.该反应的
B.催化剂可降低该反应的焓变,提高平衡转化率
C.增大起始压强,X的平衡转化率增大
D.800℃时, 内化学反应速率
16.一种具有双极膜的酸-碱液流电池如图所示,工作时, 在双极膜界面处被催化解离成 和 ,
学科网(北京)股份有限公司有利于电解反应顺利进行。充电时电极a的反应为: ,下列说法不正
确的是( )
A.充电时电极b是阳极.
B.充电时KOH溶液中KOH的物质的量增大
C.放电一段时间后,负极区溶液的pH减小
D.每消耗1mol DSAQ,双极膜处有2mol的 解离
二、非选择题:共56分。
17.(14分)水的净化方法有蒸馏法、离子交换法和电渗析法等。
(1)实验室模拟蒸馏法淡化海水,需要用到的仪器有______。
(2)实验室可用离子交换法除去水中的杂质离子。如图所示,将某天然水(主要含 、 、 、
、 、 )依次通过阳离子交换树脂HA和阴离子交换树脂BOH,发生的反应可表示为:
学科网(北京)股份有限公司①取ⅰ处流出液,其中主要含有的离子有______。
②工作一段时间后,离子交换树脂失去交换能力。证明阴离子交换树脂已失去交换能力的操作及现象是:
取ⅰ处流出液,加入______(填试剂),观察到______(填实验现象)。
(3)某小组使用离子交换法测定 的溶度积常数 ,实验方案如下:
步骤 实验操作
Ⅰ
往 固体加入蒸馏水,过滤,得到 饱和溶液。
Ⅱ
将25.00mL 饱和溶液分批通过阳离子交换树脂HA,得到流出液。
Ⅲ 用蒸馏水洗涤阳离子交换树脂至流出液呈中性。
Ⅳ 合并步骤Ⅱ和Ⅲ中的流出液,……,计算得到H的物质的量为a mol。
①步骤Ⅱ发生反应的离子方程式为______。
②将步骤Ⅳ的实验方案补充完整:______。
③ 的 ______(写出含a的计算式)。
④若省略步骤Ⅲ,測得 的 ______(填“偏大”、“偏小”或“不变”)。
18.(14分)
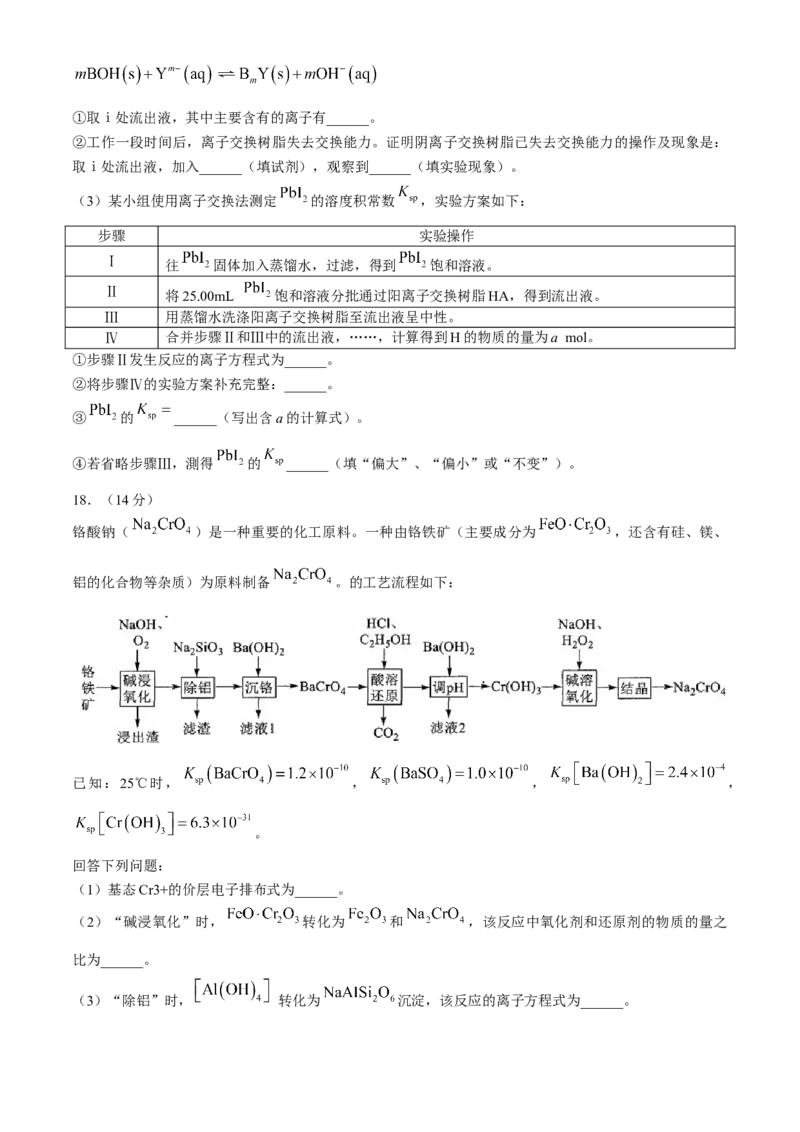
铬酸钠( )是一种重要的化工原料。一种由铬铁矿(主要成分为 ,还含有硅、镁、
铝的化合物等杂质)为原料制备 。的工艺流程如下:
已知:25℃时, , , ,
。
回答下列问题:
(1)基态Cr3+的价层电子排布式为______。
(2)“碱浸氧化”时, 转化为 和 ,该反应中氧化剂和还原剂的物质的量之
比为______。
(3)“除铝”时, 转化为 沉淀,该反应的离子方程式为______。
学科网(北京)股份有限公司(4)“沉铬”中,常温下,往“除铝”所得滤液中加入过量 固体,充分搅拌,当溶液中
沉淀完全( )时,滤液1中 为______ 。滤液1经浓缩后可循环至
______工序重复使用。(已知: )
(5)“酸溶还原”所得溶液中的溶质除HCl外,还含有______(填化学式)。
(6)“碱溶氧化”中,生成 ,反应的化学方程式为______。
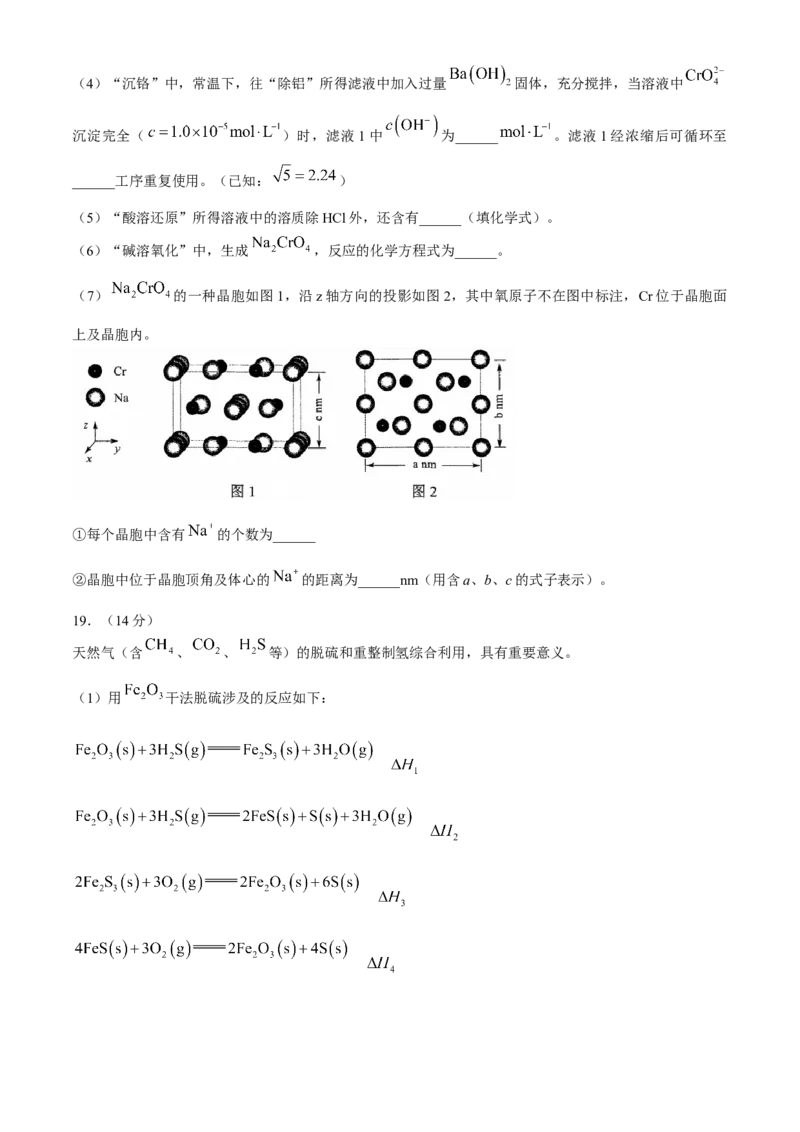
(7) 的一种晶胞如图1,沿z轴方向的投影如图2,其中氧原子不在图中标注,Cr位于晶胞面
上及晶胞内。
①每个晶胞中含有 的个数为______
②晶胞中位于晶胞顶角及体心的 的距离为______nm(用含a、b、c的式子表示)。
19.(14分)
天然气(含 、 、 等)的脱硫和重整制氢综合利用,具有重要意义。
(1)用 干法脱硫涉及的反应如下:
学科网(北京)股份有限公司反应 的 ______(写出一个代数式即可)。
(2)用NaOH溶液湿法脱硫时 和 同时被吸收。
①湿法脱硫后的吸收液中主要存在以下平衡:
下列说法正确的有______。
A.升高温度,溶液中 增大
B.加少量水稀释,溶液中离子总数增加
C.通入少量HCl气体, 增大
D.
②写出 和 溶液反应的化学方程式______。
( 的 、 , 的 、 )
(3) 和 的重整制氢涉及的反应如下:
a.
b.
①设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的
相对分压等于其分压(单位为 kPa)除以 ( )。反应a的相对压力平衡常数表达式为
______。
②反应a、b的 在400~1000℃范围内随T的变化如图1所示。反应a、b均为______反应(填“吸热”
或“放热”)。
学科网(北京)股份有限公司③在恒压100kPa下按组成为 通入混合气体,测得平衡状态下H2、S2
的收率和 的转化率随温度的变化曲线如图2所示。
Ⅰ.计算 温度下 的收率,写出计算过程。
已知: 的收率= , 的收率=
Ⅱ.从800℃升温到1000℃过程中,反应a平衡向______反应方向移动。
20.(14分)
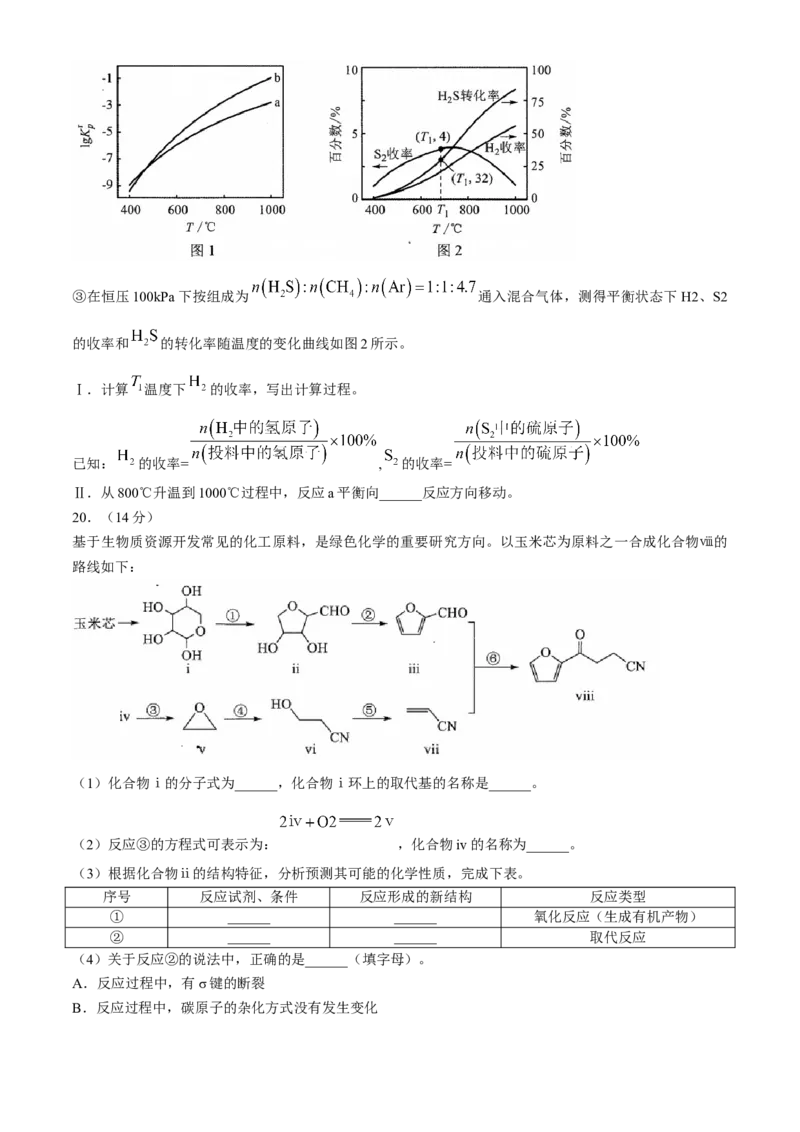
基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以玉米芯为原料之一合成化合物ⅷ的
路线如下:
(1)化合物ⅰ的分子式为______,化合物ⅰ环上的取代基的名称是______。
(2)反应③的方程式可表示为: ,化合物iv的名称为______。
(3)根据化合物ⅱ的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
① ______ ______ 氧化反应(生成有机产物)
② ______ ______ 取代反应
(4)关于反应②的说法中,正确的是______(填字母)。
A.反应过程中,有σ键的断裂
B.反应过程中,碳原子的杂化方式没有发生变化
学科网(北京)股份有限公司C.化合物ⅱ的分子中含有2个手性碳原子
D.化合物ⅱ能溶于水,原因是ⅱ能与水分子形成氢键
(5)芳香化合物y是ⅷ的同分异构体,y含有氰基( ),遇 溶液显紫色,核磁共振氢谱有3
组峰,峰面积之比为3∶2∶2,则y的结构有______种,写出其中一种的结构简式______。
(6)以 和 为原料,参考上述信息,写出制备化合物 的合成路线
______。
学科网(北京)股份有限公司