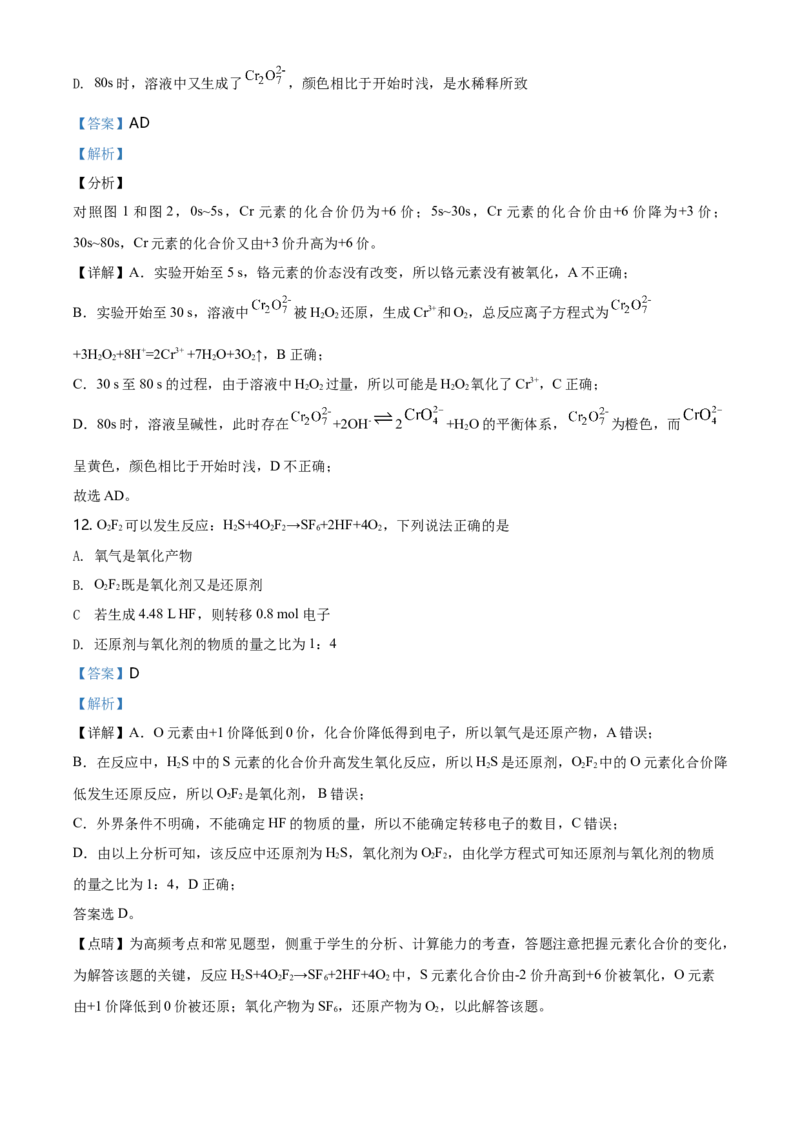文档内容
天津一中高一年级化学学科期中质量调查试卷
本试卷分为第I卷(选择题)、第II卷(非选择题)两部分,共100分,考试用时60分钟。
考生务必将答案涂写规定的位置上,答在试卷上的无效。
相对原子质量: H 1; O 16; C 12; N 14
第I卷(本卷共12道题,每题3分,共36分)
一、选择题(每题只有一个正确选项)
1. 2008年北京奥运会主体育场一“鸟巢”,被《泰晤士报》评为全球“最强悍”工程。“鸟巢”运用了高强度、
高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料。夜幕降临,北京
奥运会主会场“鸟巢”内灯火辉煌、鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。
鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色。有关说法正确的是( )
A. 合金的熔点通常比组分金属高,硬度比组分金属小
B. 所用材料从物质分类属于金属单质
C. 用金属铝与VO 反应冶炼钒,VO 作还原剂
2 5 2 5
D. 火焰利用了部分金属元素特征的焰色试验,该反应属于物理变化
【答案】D
【解析】
【分析】
【详解】A.合金的熔点通常比组分金属低,硬度比组分金属高,故A错误;
B.钒氮合金为金属材料,ETFE膜为有机高分子合成材料,故B错误;
C.用金属铝与VO 反应冶炼钒,VO 作氧化剂,故C错误;
2 5 2 5
D.焰色反应可检验金属元素的特性,是物理变化,故D正确;
故答案为D。
2. 2020 年春节前后,世界各地爆发了新型冠状病毒疫情。在疫情面前,我国人民众志成城,奋力战疫。下
列防疫物品的主要成分属于无机物的是( )A. 聚丙烯 B. 聚碳酸酯
C. 二氧化氯 D. 丁腈橡胶
【答案】C
【解析】
【分析】
【详解】A.聚丙烯为有机合成高分子化合物,故A错误;
B.聚碳酸酯是分子链中含有碳酸酯基的高分子聚合物,为有机合成高分子化合物,故B错误;
C.二氧化氯为氧化物,是无机化合物,故C正确;
D.丁腈橡胶为有机合成高分子化合物,故D错误;
故答案为C。
3. 中国传统文化对人类文明贡献巨大,下列各文献中所记载的古代化学研究过程或成果不涉及分离提纯操
作的的是
A. 《本草纲目》“(烧酒)自元时始创其法,用浓酒和精入甑,燕令气上……其清如水,味极浓烈,盖酒露
也。”
B. (齐民要术》“凡酿酒失所味者,或初好后动未压者,皆宜翅(同“回”)作醋。”
C. 《开宝本草》“(消石)所在山泽,冬月地上有霜扫取,以水淋汁,后乃煎炼而成。”
D. 《本草行义》“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖
长者为胜,平短者次之。”
【答案】B
【解析】
【分析】
【详解】A.由“浓酒和精入甑,燕令气上”可知,该过程中所采用的是蒸馏法提高酒精浓度,涉及分离提
纯操作;
B.由“酿酒”、“皆宜翅(同“回”)作醋”可知,其所描述的是酒精转化为醋酸,未涉及分离提纯操作;C.由“有霜扫取,以水淋汁,后乃煎炼而成”可知,该过程中所涉及溶解、蒸发结晶分离提纯操作;
D.该过程所描述的是将生砒加热升华,然后砒烟在容器上凝华,涉及升华、凝华分离提纯操作;
综上所述,涉及分离提纯操作的是B项,故答案为:B。
4. 某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡不亮;按照图乙连接好线路,
发现灯泡亮了。由此得出的以下结论中正确的是
A. NaCl为非电解质
B. NaCl溶液是电解质
C. 在NaCl溶液中,水电离出了大量的离子
D. NaCl在水溶液中电离出了可以自由移动的离子
【答案】D
【解析】
【分析】
由实验可知,固体NaCl不导电,NaCl溶液可以导电,即说明NaCl溶于水后可以电离出自由移动的离子,
从而导电,所以NaCl属于电解质。
【详解】A. NaCl溶于水能够导电,恰恰能证明其属于电解质,故A错误;
B.电解质指在溶于水或熔融状态下能够导电的化合物,NaCl溶液是混合物,不属于电解质,故B错误;C.NaCl溶液可以导电,是NaCl在水中发生了电离,产生了大量自由移动的离子,不是水电离出大量的
离子,故C错误;
D.NaCl溶液可以导电,是NaCl在水中发生了电离,产生了大量自由移动的离子,故D正确;
本题答案 D 。
5. 下列实验操作与观察目的一致的是( )
实验操作 观察目的
A 用小刀切开金属钠 钠的熔点较低
B 将钠放置在煤油中 钠有强还原性
C 将钠放在坩埚中加热 钠有较小的硬度
D 将一小块钠放入盛水的烧杯中 钠的密度比水小
A. A B. B C. C D. D
【答案】D
【解析】
【分析】
【详解】A.钠质软,可以用刀切,与熔点无关,故A错误;
B.将钠放置在煤油中,下沉,是钠的密度比煤油小,无法判断钠有强还原性,故B错误;
C.将钠放在坩埚中加热,钠熔化,说明钠的熔点低,故C错误;
D.将一小块钠放入盛水的烧杯中,钠浮在水面上,说明钠的密度比水小,故D正确;
故答案为D。
6. 下列离子在溶液中能大量共存,加入(NH )Fe(SO )·6H O 晶体后,仍能大量共存的是( )
4 2 4 2 2
A. Na+、H+、Cl-、NO B. Na+、 Mg2+、 Cl-、SO
C. K+、Ba2+、 OH-、I- D. Cu2+、CO 、 Br-、ClO-
【答案】B
【解析】
【分析】
【详解】(NH )Fe(SO )·6H O 晶体溶于水能电离出Fe2+、 、 ;
4 2 4 2 2
A.NO 在酸性条件下有强氧化性,能氧化Fe2+,不能大量共存,故A错误;B.Na+、 Mg2+、 Cl-、SO 彼此间不发生离子反应,且能与Fe2+、 大量共存,故B正确;
C.Ba2+与 能发生离子反应生成BaSO,且OH-与Fe2+和 均能发生离子反应,不能大量共存,故
4
C错误;
D.铜离子与碳酸根离子不能大量共存,且ClO-有强氧化性,能氧化Fe2+,Fe2+也能与CO 发生离子反应,
不能大量共存,故D错误;
故答案为B。
7. 下列说法正确的是( )
①钠燃烧时发出黄色的火焰
②过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
③过氢化钠能与水反应,所以过氧化钠可以作气体的干燥剂
④过氧化钠中阴阳离子个数比为1:1
⑤钠是一种很强的还原剂,钠可以把锆、铌等金属从它们的化合物的水溶液中置换出来
⑥NaO 分别与水及CO 反应产生相同量的O 时,需要水和CO 的质量相等
2 2 2 2 2
⑦可用水来确定某NaO粉末中是否含有NaO
2 2 2
⑧将足量的NaO、NaO分别加到酚酞试液中,最终溶液均为红色
2 2 2
A. ①②⑤⑦ B. ①⑧ C. ①②⑤⑧ D. ①⑦
【答案】D
【解析】
【分析】
【详解】①钠的焰色反应为黄色,钠燃烧时发出黄色的火焰,故①正确;
②与酸反应不仅生成盐和水,还生成O,故NaO 不 是碱性氧化物,故②错误;
2 2 2
③NaO 与水反应生成O,会引入新的杂质,故③错误;
2 2 2
④过氧化钠中含有阳离子为Na+、阴离子为 ,则过氧化钠中阴阳离子比1:2,故④错误;
⑤钠和钛锆等金属盐溶液的反应是先和其中的水反应置换出氢气,不会置换出金属,故⑤错误;
⑥NaO 分别与水及CO 反应产生相同量的O 时,消耗的水和二氧化碳的物质的量相同,水和CO 的质量
2 2 2 2 2
不同,故⑥错误;
⑦氧化钠和水反应生成氢氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,粉末放入水中有气泡生成,可
确定NaO粉末中含有NaO,故⑦正确;
2 2 2
⑧氧化钠加入酚酞试液中,反应生成的氢氧化钠是可溶性碱,溶液变红色,而过氧化钠加入酚酞溶液中,
生成氢氧化钠和氧气,氢氧化钠是碱使酚酞变红色,过氧化钠具有强氧化性能使红色溶液褪去,即溶液先变红色后褪色,故⑧错误;
①⑦正确,故答案为D。
8. 在实验室用下列装置制取氯气并验证氯气的某些化学性质,其中不能达到实验目的是( )
A. 闻氯气的气味
B. 实验室制取氯气
C. 回收固体二氧化锰
D. 验证氯气能支持H 燃烧
2
【答案】B
【解析】
【分析】
【详解】A.闻气味时,可用手在瓶口轻轻扇动,使少量氯气飘进鼻孔,以避免中毒,故A正确;
B.浓盐酸和二氧化锰在加热条件下反应,常温下不反应,故B错误;
C.MnO 不溶于水,利用过滤操作可回收固体MnO ,故C正确;
2 2
D.点燃条件下,氢气在氯气中安静燃烧,可验证氯气能支持H 燃烧,故D正确;
2
故答案为B。
9. 二氧化氯、铁酸钠以及臭氧是饮用水的“三净客”,用铁酸钠(Na FeO)处理来自河流湖泊的水,以作
2 4
为人们生活饮用水,是一项较新的技术。以下叙述中正确的是( )
①二氧化氯对水具有消毒、净化双效功能 ②臭氧可消除水洗物中残留的农药残留,杀灭水中的细菌病毒
③臭氧、明矾净水原理相同 ④用NaFeO 净水具消毒和净化双效功能
2 4A. ②④ B. ③④ C. ①③ D. ①④
【答案】A
【解析】
【分析】
【详解】①二氧化氯对水具有消毒功能,但不能净水,①错误;
②臭氧可消除水洗物中残留的农药残留,杀灭水中的细菌病毒,②正确;
③明矾中铝离子发生水解生成氢氧化铝胶体,吸附水中的杂质净水,而臭氧具有强氧化性,杀菌消毒,净
水原理不同,③错误;
④Na FeO 是可溶于水的强氧化剂,在水中有杀菌消毒的作用,其还原产物主要是 Fe3+,会水解形成
2 4
Fe(OH) 胶体,则Na FeO 净水具消毒和净化双效功能,④正确;
3 2 4
综上,②④正确,答案选A。
10. N 为阿伏伽德罗常数,下列叙述错误的是( )
A
A. 18g H O中含的质子数为10 N
2 A
B. HO+Cl= 2HC1+O 反应中,每生成32gO,转移2N 个电子
2 2 2 2 2 A
C. 3.6gCO和N 的混合气体含质子数为1.8 N
2 A
D. 1mol 冰醋酸溶于水中,所得溶液中H+数为N
A
【答案】D
【解析】
【分析】
【详解】A.每个HO分子含有10个质子,18gHO的物质的量为1mol,含质子数为10 N ,故A正确;
2 2 A
B.在HO+Cl═2HCl+O 反应中,氧元素由-1价变为0价,故生成32g氧气即1mol氧气时,转移2N 个
2 2 2 2 A
电子,故B正确;
C.氮气和CO的摩尔质量均为28g/mol,故3.6g混合物的物质的量为 = mol,且两者均含14
个质子,故 mol混合物中含 mol×14×N mol-1=1.8N 个质子,故C正确;
A A
D.醋酸是弱酸,不能完全电离,则1mol 冰醋酸溶于水中,所得溶液中H+数小于N ,故D错误;
A
故答案为D。
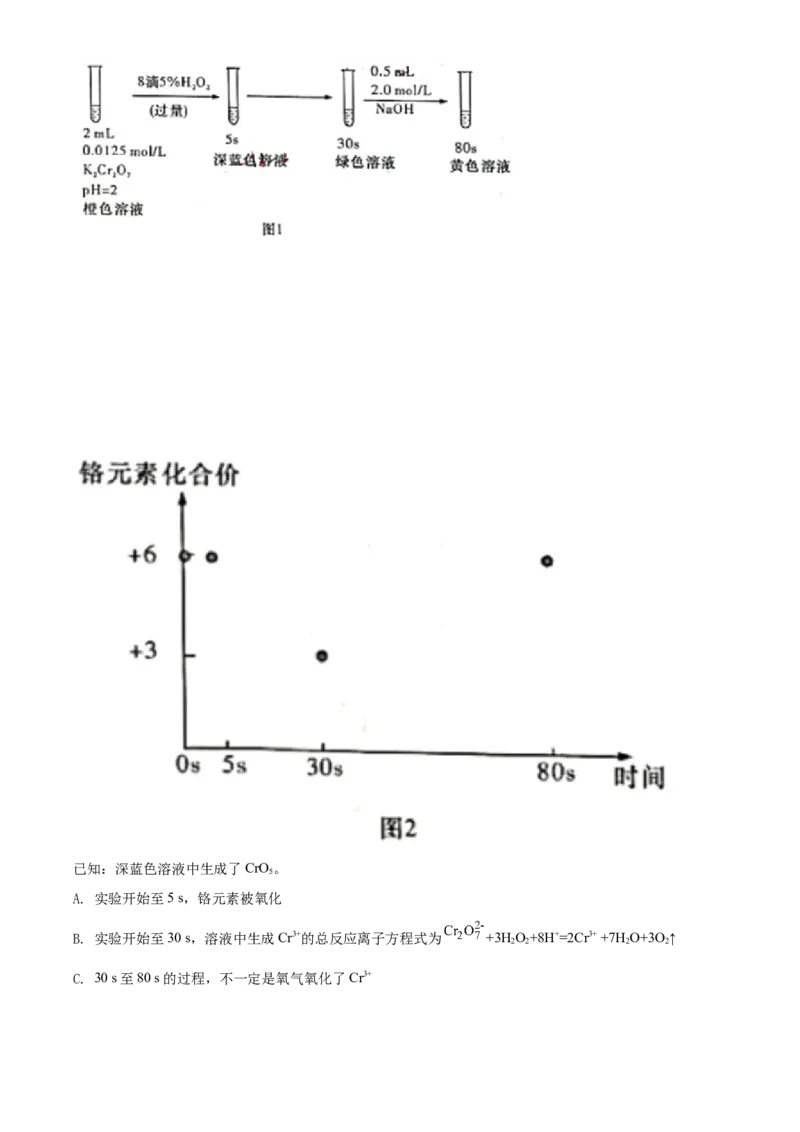
11. 实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2。下列说法
不正确的是已知:深蓝色溶液中生成了CrO。
5
A. 实验开始至5 s,铬元素被氧化
B. 实验开始至30 s,溶液中生成Cr3+的总反应离子方程式为 +3H O+8H+=2Cr3+ +7H O+3O↑
2 2 2 2
C. 30 s至80 s的过程,不一定是氧气氧化了Cr3+D. 80s时,溶液中又生成了 ,颜色相比于开始时浅,是水稀释所致
【答案】AD
【解析】
【分析】
对照图 1 和图 2,0s~5s,Cr 元素的化合价仍为+6 价;5s~30s,Cr 元素的化合价由+6 价降为+3 价;
30s~80s,Cr元素的化合价又由+3价升高为+6价。
【详解】A.实验开始至5 s,铬元素的价态没有改变,所以铬元素没有被氧化,A不正确;
B.实验开始至30 s,溶液中 被HO 还原,生成Cr3+和O,总反应离子方程式为
2 2 2
+3H O+8H+=2Cr3+ +7H O+3O↑,B正确;
2 2 2 2
C.30 s至80 s的过程,由于溶液中HO 过量,所以可能是HO 氧化了Cr3+,C正确;
2 2 2 2
D.80s时,溶液呈碱性,此时存在 +2OH- 2 +H O的平衡体系, 为橙色,而
2
呈黄色,颜色相比于开始时浅,D不正确;
故选AD。
12. OF 可以发生反应:HS+4OF→SF +2HF+4O,下列说法正确的是
2 2 2 2 2 6 2
A. 氧气是氧化产物
B. OF 既是氧化剂又是还原剂
2 2
.
C 若生成4.48 L HF,则转移0.8 mol电子
D. 还原剂与氧化剂的物质的量之比为1:4
【答案】D
【解析】
【详解】A.O元素由+1价降低到0价,化合价降低得到电子,所以氧气是还原产物,A错误;
B.在反应中,HS中的S元素的化合价升高发生氧化反应,所以HS是还原剂,OF 中的O元素化合价降
2 2 2 2
低发生还原反应,所以OF 是氧化剂, B错误;
2 2
C.外界条件不明确,不能确定HF的物质的量,所以不能确定转移电子的数目,C错误;
D.由以上分析可知,该反应中还原剂为HS,氧化剂为OF,由化学方程式可知还原剂与氧化剂的物质
2 2 2
的量之比为1:4,D正确;
答案选D。
【点晴】为高频考点和常见题型,侧重于学生的分析、计算能力的考查,答题注意把握元素化合价的变化,
为解答该题的关键,反应HS+4OF→SF +2HF+4O 中,S元素化合价由-2价升高到+6价被氧化,O元素
2 2 2 6 2
由+1价降低到0价被还原;氧化产物为SF ,还原产物为O,以此解答该题。
6 2第II卷(本卷共4道题,共64分)
13. 填空。
(1)有以下几种物质:①空气;②液态氧;③硝酸钾溶液;④硫酸铜晶体(CuSO ·5H O);⑤二氧化碳;⑥氧
4 2
化铜;⑦金刚石;⑧甲烷;⑨氢氧化铜。其中:
属于纯净物的是_____________________________________(填序号,下同);
属于混合物的是_____________________________________;
属于氧化物的是____________________________________;
属于盐 的是___________________________________________;
属于有机物的是_________________________________________;
属于碱的是____________________________________________;
属于单质的是__________________________________________。
(2)金属钠着火,应用________________灭火;过氧化钠可做呼吸面具的供氧剂,有关化学方程式
_____________________________________________________________________;除去NaHCO 溶液中的NaCO 的
3 2 3
有关化学方程式为____________________________________________________________________;
(3)我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb O 可写成2PbO·PbO,结合氧化物 的分类可
3 4 2
知PbO是碱性氧化物,而PbO 不是碱性氧化物。写出PbO (难溶于水)与盐酸反应的离子方程式
2
__________________________________________________________________;已知PbO 与浓盐酸混合后可得到
2
PbCl 、黄绿色气体等物质,请写出相应的化学方程式
2
_____________________________________________________________________。
【答案】 (1). ②④⑤⑥⑦⑧⑨ (2). ①③ (3). ⑤⑥ (4). ④ (5). ⑧ (6). ⑨ (7). ②⑦ (8). 干
燥 的 沙 子 (9). 2NaO+2H O=4NaOH+O ↑ 、 2NaO+2CO =2Na CO+O (10).
2 2 2 2 2 2 2 2 3 2
CO+H O+Na CO=2NaHCO (11). PbO+2H+=Pb2++H O (12). PbO +4HCl=PbCl +Cl↑+2H O
2 2 2 3 3 2 2 2 2 2
【解析】
【分析】
结合各类物质的概念和分类标准分析;结合钠及其化合物的性质分析;结合碱性氧化物的性质、PbO 和浓
2
盐酸反应的产物书写化学方程式。
【详解】(1)②液态氧、④硫酸铜晶体(CuSO ·5H O)、⑤二氧化碳、⑥氧化铜、⑦金刚石、⑧甲烷、⑨氢氧
4 2
化铜均只有一种物质组成,为纯净物,故属于纯净物的是②④⑤⑥⑦⑧⑨;
①空气、③硝酸钾溶液是由两种或两种以上不同物质组成的物质组成,为混合物,故属于混合物的是①③;
⑤二氧化碳和⑥氧化铜是由两种元素组成且其中一种为氧元素的纯净物,是氧化物,故属于氧化物的是
⑤⑥;④硫酸铜晶体(CuSO ·5H O)是结晶水合物,其中硫酸铜由Cu2+和 组成,是盐,故属于盐的是④;
4 2
⑧甲烷是碳氢化合物,是最简单的有机物,故属于有机物的是⑧;
⑨氢氧化铜电离的阴离子全部是OH-,是碱,故属于碱的是⑨;
②液态氧和⑦金刚石均为一种元素组成的纯净物,是单质,故属于单质的是②⑦;
(2)Na能与水反应,且燃烧产物NaO 能与水和CO 反应生成氧气,则金属钠着火,应用干燥的沙子灭火;
2 2 2
过氧化钠能与水和CO 反应生成氧气,可做呼吸面具的供氧剂,有关化学方程式为
2
2NaO+2H O=4NaOH+O ↑、2NaO+2CO =2Na CO+O ;除去NaHCO 溶液中的NaCO,可通入过量CO
2 2 2 2 2 2 2 2 3 2 3 2 3 2
气体即可,发生反应的化学方程式为CO+H O+Na CO=2NaHCO;
2 2 2 3 3
(3)PbO 是碱性氧化物,与盐酸反应的离子方程式为PbO+2H+=Pb2++H O;PbO 与浓盐酸混合后可得到
2 2
PbCl 、黄绿色气体等物质,则发生反应的化学方程式为PbO +4HCl=PbCl +Cl↑+2H O。
2 2 2 2 2
【点睛】注意把握钠及其化合物的性质,常见物质有钠、碳酸钠、碳酸氢钠、过氧化钠的性质,特别注意
NaO 有强氧化性,不是碱性氧化物,可做供氧剂。
2 2
14. 碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料。请根据题意回答下列问题:
I.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法。其流程如下:
(1)流程II的反应分步进行: a. Na SO +4C NaS +4CO↑ b. Na S与石灰石发生复分解反应,总反应
2 4 2 2
方程式可表示为_______________________________
II.1862 年,比利时人索尔维( ErnestSolvay)用氨碱法生产碳酸钠。反应原理如下:
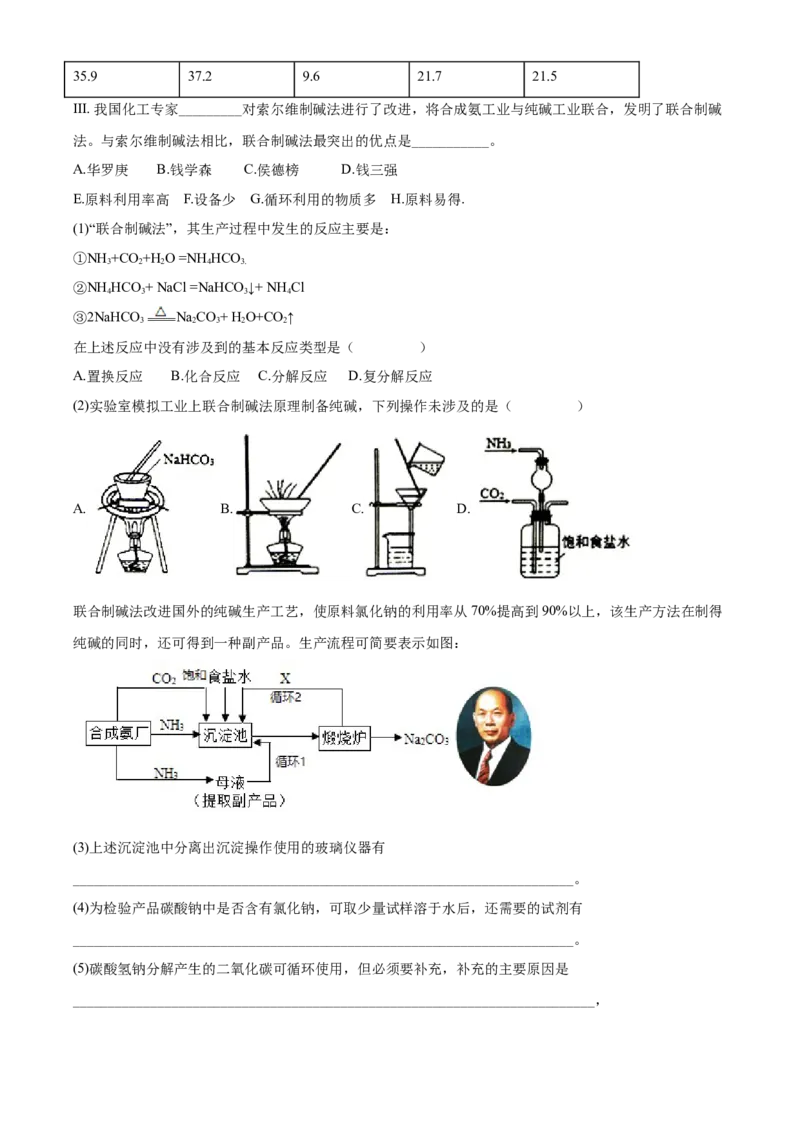
20℃时一些物质在水中的溶解度/g·( 100gH O)
2
NaCl NH Cl NaHCO NH HCO NaCO
4 3 4 3 2 335.9 37.2 9.6 21.7 21.5
III. 我国化工专家_________对索尔维制碱法进行了改进,将合成氨工业与纯碱工业联合,发明了联合制碱
法。与索尔维制碱法相比,联合制碱法最突出的优点是___________。
A.华罗庚 B.钱学森 C.侯德榜 D.钱三强
E.原料利用率高 F.设备少 G.循环利用的物质多 H.原料易得.
(1)“联合制碱法”,其生产过程中发生的反应主要是:
①NH +CO +H O =NHHCO
3 2 2 4 3.
②NH HCO + NaCl =NaHCO ↓+ NH Cl
4 3 3 4
③2NaHCO NaCO+ H O+CO↑
3 2 3 2 2
在上述反应中没有涉及到的基本反应类型是( )
A.置换反应 B.化合反应 C.分解反应 D.复分解反应
(2)实验室模拟工业上联合制碱法原理制备纯碱,下列操作未涉及的是( )
A. B. C. D.
联合制碱法改进国外的纯碱生产工艺,使原料氯化钠的利用率从70%提高到90%以上,该生产方法在制得
纯碱的同时,还可得到一种副产品。生产流程可简要表示如图:
(3)上述沉淀池中分离出沉淀操作使用的玻璃仪器有
_______________________________________________________________________。
(4)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,还需要的试剂有
_______________________________________________________________________。
(5)碳酸氢钠分解产生的二氧化碳可循环使用,但必须要补充,补充的主要原因是
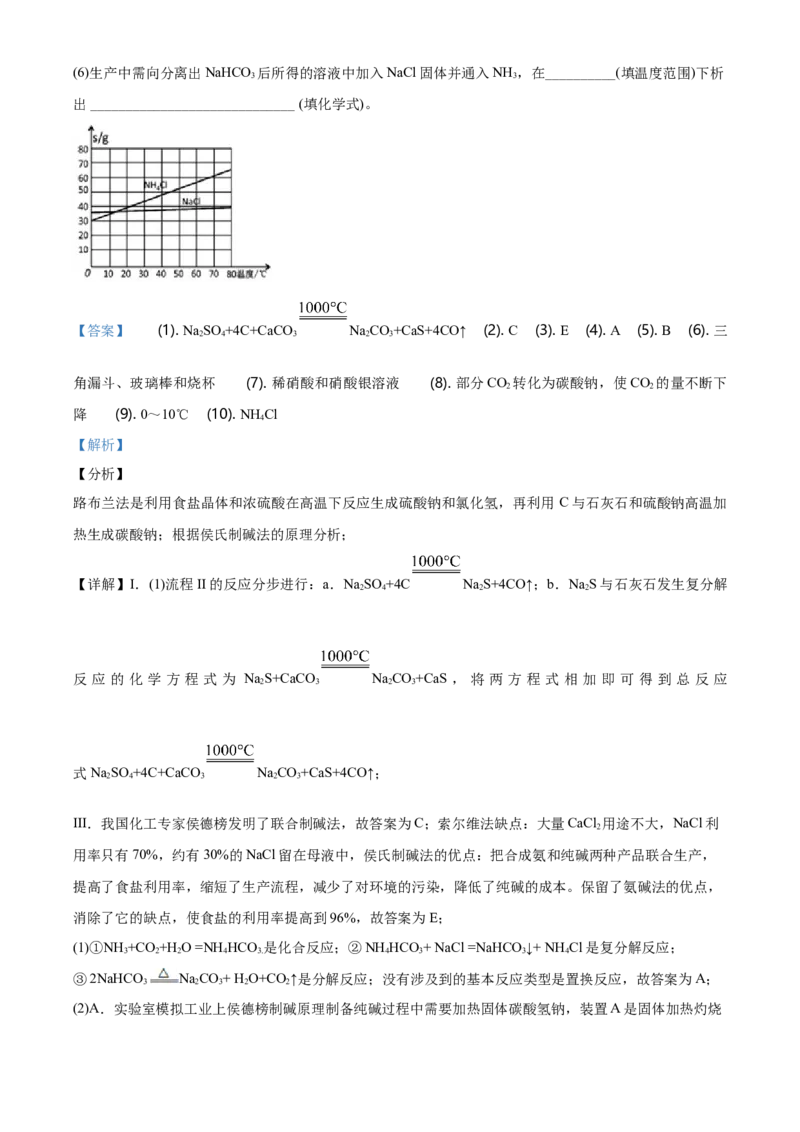
__________________________________________________________________________,(6)生产中需向分离出NaHCO 后所得的溶液中加入NaCl固体并通入NH ,在__________(填温度范围)下析
3 3
出 _____________________________ (填化学式)。
【答案】 (1). NaSO +4C+CaCO NaCO+CaS+4CO↑ (2). C (3). E (4). A (5). B (6). 三
2 4 3 2 3
角漏斗、玻璃棒和烧杯 (7). 稀硝酸和硝酸银溶液 (8). 部分CO 转化为碳酸钠,使CO 的量不断下
2 2
降 (9). 0~10℃ (10). NH Cl
4
【解析】
【分析】
路布兰法是利用食盐晶体和浓硫酸在高温下反应生成硫酸钠和氯化氢,再利用 C与石灰石和硫酸钠高温加
热生成碳酸钠;根据侯氏制碱法的原理分析;
【详解】I.(1)流程II的反应分步进行:a.NaSO +4C NaS+4CO↑;b.NaS与石灰石发生复分解
2 4 2 2
反 应 的 化 学 方 程 式 为 NaS+CaCO NaCO+CaS , 将 两 方 程 式 相 加 即 可 得 到 总 反 应
2 3 2 3
式 NaSO +4C+CaCO NaCO+CaS+4CO↑;
2 4 3 2 3
III.我国化工专家侯德榜发明了联合制碱法,故答案为C;索尔维法缺点:大量CaCl 用途不大,NaCl利
2
用率只有70%,约有30%的NaCl留在母液中,侯氏制碱法的优点:把合成氨和纯碱两种产品联合生产,
提高了食盐利用率,缩短了生产流程,减少了对环境的污染,降低了纯碱的成本。保留了氨碱法的优点,
消除了它的缺点,使食盐的利用率提高到96%,故答案为E;
(1)①NH +CO +H O =NHHCO 是化合反应;②NH HCO + NaCl =NaHCO ↓+ NH Cl是复分解反应;
3 2 2 4 3. 4 3 3 4
③2NaHCO NaCO+ H O+CO↑是分解反应;没有涉及到的基本反应类型是置换反应,故答案为A;
3 2 3 2 2
(2)A.实验室模拟工业上侯德榜制碱原理制备纯碱过程中需要加热固体碳酸氢钠,装置A是固体加热灼烧的装置,涉及此操作,故A正确;
B.装置B是蒸发溶液得到晶体的过程,侯德榜制碱原理中不需要蒸发溶液操作,故B错误;
C.装置未过滤操作,溶液中析出碳酸氢钠晶体需要过滤得到晶体,涉及此操作,故C正确;
D.装置工业上侯德榜制碱原理制备纯碱,向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢钠,
涉及此操作,故D正确;
故答案为B;
(3)沉淀池中分离出沉淀操作是过滤,使用的玻璃仪器有三角漏斗、玻璃棒和烧杯;
(4)Cl-与Ag+反应生成不溶于硝酸的AgCl沉淀,所以检验Cl-方法为:取少量试样溶于水后,再滴加硝酸酸
化的硝酸银溶液,看是否产生白色沉淀,则还需要的试剂有稀硝酸和硝酸银溶液;
(5)碳酸氢钠分解生成CO、碳酸钠和水,其中CO 可循环利用,因部分CO 转化为碳酸钠,使CO 的量不
2 2 2 2
断下降,则仍需要不断补充CO;
2
(6)在含有氯化铵的滤液中,加入氯化钠并通NH ,可提高溶液中Cl-和NH +的浓度,促进NH Cl(s) NH +
3 4 4 4
(aq)+Cl-(aq)溶解平衡逆向移动,析出晶体氯化铵;因NH Cl低温下溶解度比较小,低温更易NH Cl⇌晶体析
4 4
出,并以防止析出其他晶体。
【点睛】探究三种不同情况制备纯碱碳酸钠的实验原理,涉及反应原理、溶解度及混合物的分离操作,难
点为反应原理的分析,其中侯德榜制碱的原理:向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢
钠,加热分解碳酸氢钠来制备碳酸钠。
15. 为了减少“84”消毒液对物品的腐蚀,天津一中高三师生给教室消毒使用的是二氧化氯泡腾片:
二氧化氯(ClO )是一种黄绿色有刺激性气味的气体,其熔点为一59°C,沸点为11.0°C;易溶于水。是目前
2
国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。
与Cl 相比,ClO 不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
2 2
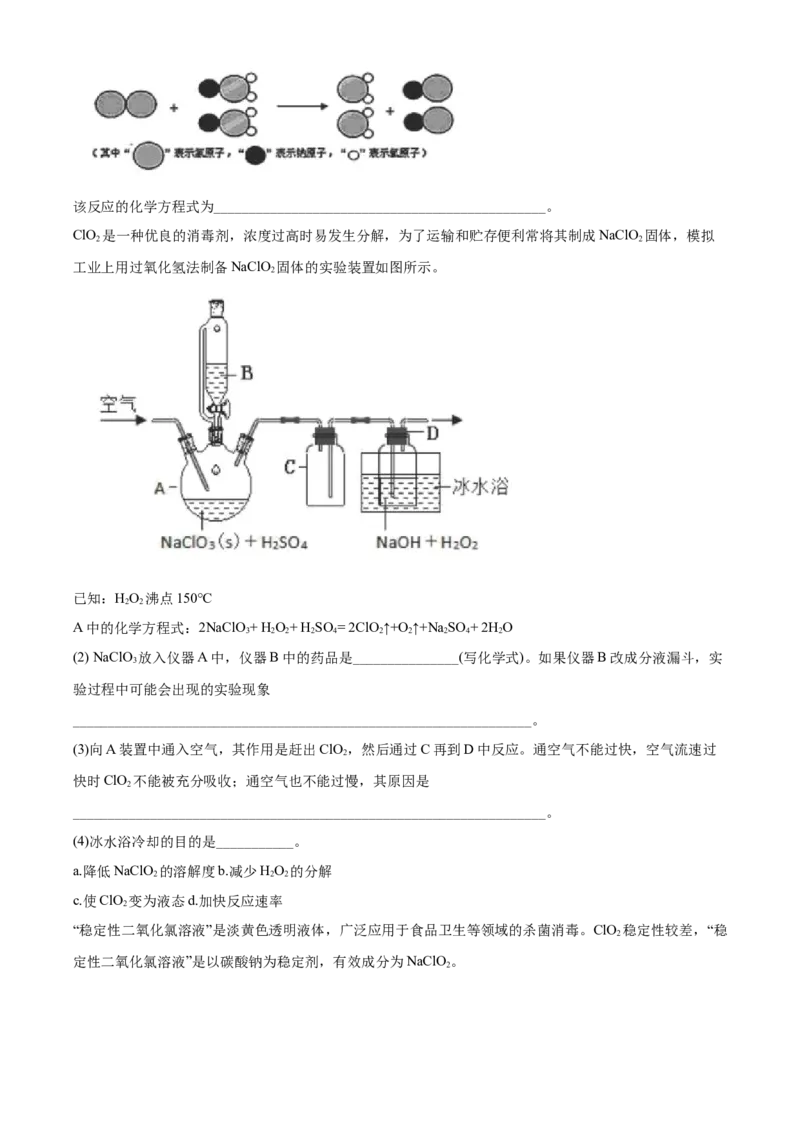
(1)我国最近成功研制出制取ClO 的新方法,其反应的微观过程如图所示:
2该反应的化学方程式为_______________________________________________。
ClO 是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成NaClO 固体,模拟
2 2
工业上用过氧化氢法制备NaClO 固体的实验装置如图所示。
2
已知:HO 沸点150°C
2 2
A中的化学方程式:2NaClO+ H O+ H SO = 2ClO ↑+O ↑+Na SO + 2H O
3 2 2 2 4 2 2 2 4 2
(2) NaClO 放入仪器A中,仪器B中的药品是_______________(写化学式)。如果仪器B改成分液漏斗,实
3
验过程中可能会出现的实验现象
_________________________________________________________________。
(3)向A装置中通入空气,其作用是赶出ClO ,然后通过C再到D中反应。通空气不能过快,空气流速过
2
快时ClO 不能被充分吸收;通空气也不能过慢,其原因是
2
___________________________________________________________________。
(4)冰水浴冷却的目的是___________。
a.降低NaClO 的溶解度b.减少HO 的分解
2 2 2
c.使ClO 变为液态d.加快反应速率
2
“稳定性二氧化氯溶液”是淡黄色透明液体,广泛应用于食品卫生等领域的杀菌消毒。ClO 稳定性较差,“稳
2
定性二氧化氯溶液”是以碳酸钠为稳定剂,有效成分为NaClO。
2某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量
与样品质量的比值来衡量)。请回答下列问题:
(5)为证实“稳定性二氧化氯溶液”中含有钠离子,方法是:
_______________________________________________________________________。
(6)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右)试样,置于烧瓶中,
向分液漏斗中加入10mL盐酸溶液:②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶
液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产
生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴
淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I+2S O =2I-+S O ),共用去VmL硫代硫酸钠
2 2 4
溶液。NaClO 与盐酸反应生成ClO (还原产物为Cl-),该反应的化学方程式为:
2 2
_____________________________________________________________________。ClO 通入锥形瓶与酸性
2
碘化钾溶液反应,二氧化氯被还原为氯离子,该反应的离子方程为:
___________________________________________________________________。
【答案】 (1). 2NaClO+Cl=2NaCl+2ClO (2). HO (3). 液体无法顺利滴落 (4). 空气流速过慢时,
2 2 2 2 2
ClO 不能及时被移走,浓度过高导致分解 (5). abc (6). 焰色反应或焰色试验 (7).
2
5NaClO+4HCl=4ClO +5NaCl+2H2O (8). 2ClO +10I-+8H+=2C1-+5I +4H O
2 2 2 2 2
【解析】
【分析】
根据微观结构分析得出反应的化学方程式。利用反应 2NaClO+H O+H SO =2ClO ↑+O ↑+Na SO +2H O
3 2 2 2 4 2 2 2 4 2
制得ClO ,利用空气将生成的ClO 吹出与氢氧化钠、双氧水反应生成NaClO ,利用冰水浴将ClO 变为液
2 2 2 2
体,降低双氧水分解,利于生成NaClO ,将NaClO 与盐酸反应生成ClO ,ClO 与KI反应生成单质碘,
2 2 2 2
淀粉作指示剂用硫代硫酸钠进行滴定,据此解答。
【详解】(1)根据微观结构分析反应的化学方程式为 2NaClO+Cl=2NaCl+2ClO ,故答案为:
2 2 22NaClO+Cl=2NaCl+2ClO ;
2 2 2
(2)根据A中反应物,得出仪器B中的药品是HO,如果仪器B改成分液漏斗,分液漏斗和三颈烧瓶中
2 2
的压强不相同,因此实验过程中可能会出现的实验现象液体无法顺利滴,故答案为:HO;液体无法顺利
2 2
滴落;
(3)向A装詈中通入空气,其作用是赶出ClO 然后通过C再到D中反应。通空气不能过快的,空气流速
2
过快时ClO 不能被充分吸收;通空气也不能过慢,根据题中信息ClO 是种优良的消毒剂,浓度过高时易
2 2
发生分解,因此空气流速过慢时,ClO 不能及时被移走,浓度过高导致分解,故答案为:空气流速过慢时,
2
ClO 不能及时被移走,浓度过高导致分解;
2
(4)根据题中信息二氧化氯(ClO )沸点为11.0℃,易溶于水,因此冰水浴冷却的目的是使ClO 变为液
2 2
态,更充分的反应生成的NaClO,减少HO 的分解,提高利用率,降低NaClO 的溶解度,使的更利于生
2 2 2 2
成NaClO,故答案为:abc;
2
(5)为证实稳定性二氧化氯溶液中含有钠离子,方法是:焰色反应或焰色试验,故答案为:焰色反应或
焰色试验;
(6)NaClO 与盐酸反应生成ClO 、NaCl和水,该反应的化学方程式为:
2 2
5NaClO+4HCl=4ClO +5NaCl+2H2O,故答案为:5NaClO+4HCl=4ClO +5NaCl+2H2O;ClO 通入锥形瓶与
2 2 2 2 2
酸性碘化钾溶液反应,二氧化氯被还原为氯离子,碘离子变为单质碘,反应的离子方程式为:2ClO +10I-
2
+8H+=2C1-+5I +4H O,故答案为:2ClO +10I-+8H+=2C1-+5I +4H O。
2 2 2 2 2
【点睛】ClO 是一种优良的消毒剂,浓度过高时易发生分解,因此空气流速过慢时,ClO 不能及时被移走,
2 2
浓度过高导致分解,对于新物质的性质,要关注题目提供的信息。
16. 在CaCO 、CO、CO、NaCO、NaHCO 、Cl 物质中
3 2 2 3 3 2
⑴大气中过多会造成温室效应的是_______________.
⑵俗名是小苏打,且是制糕点发酵粉的主要成分的是________
⑶能和血液中血红蛋白结合而使人中毒的是_________________
⑷是水垢的主要成分_______________
⑸能用于制造漂白粉的是__________________
⑹俗名是纯碱,工业上用于造纸业的是___________
【答案】 (1). CO (2). NaHCO (3). CO (4). CaCO (5). Cl (6). Na CO
2 3 3 2 2 3
【解析】
【分析】
(1)产生温室效应的气体是二氧化碳;
(2)碳酸氢钠的俗名是水苏打;
(3)CO易与血液中血红蛋白结合而难与血液中血红蛋白分离;(4)是水垢的主要成分CaCO 和Mg(OH) ;
3 2
(5)氯气与石灰乳反应,制取漂白粉;
(6)NaCO 俗名是苏打.
2 3
【详解】(1)产生温室效应的气体是二氧化碳,则大气中含量过多会造成温室效应的是CO;
2
(2)碳酸氢钠的俗名是水苏打,且是制糕点发酵粉的主要成分;
(3)易与血液中血红蛋白结合而难与血液中血红蛋白分离而使人中毒的是CO;
(4)是水垢的主要成分CaCO 和Mg(OH) ;
3 2
(5)氯气与石灰乳反应,制取漂白粉;
(6)NaCO 俗名是苏打,名是纯碱,工业上用于造纸业。
2 3