文档内容
常州市教育学会学业水平监测
高三化学 2024 年 1 月
注意事项:
1.本试卷分为选择题和非选择题两部分,共100分,考试时间75分钟。
2.将选择题的答案填涂在答题卡的对应位置上,非选择题的答案写在答题卡的指定栏目内。
可能用到的相对原子质量:H-1 Li-7 O-16 Al-27 S-32 Cl-35.5 K-39 Br-80 I-127
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.核酸因其最早在细胞核中发现,且有酸性而得名。下列不属于核酸水解产物的是( )
A.核苷酸 B.碳酸 C.戊糖 D.碱基
2.反应 应用于石油开采。下列说法正确的是( )
A.基态N原子的轨道表示式为
B. 的结构示意图为
C. 中N原子杂化类型为
D. 的空间填充模型为
3.元素F、Cl、Br、I位于周期表ⅦA族。下列事实不能通过比较元素电负性解释的是( )
A. 键的键能小于 键的键能
B. 与水发生反应的产物是 和HIO
C. 比 更易形成
D.气态氟化氢中存在 ,而气态氯化氢中是HCl分子
4.下列有关配制一定物质的量浓度溶液时的操作(图中箭头表示运动方向)正确的是( )A.转移 B.振荡 C.定容 D.摇匀
阅读下列材料,完成5~8题: 的综合利用具有重要意义。 的捕集方法众多,可以形成 、
、尿素 等重要化合物, 还可以催化转化为高附加值化学品 CO、 、
、HCOOH等。如用镍基催化剂催化电解 可得到 , 和 反应生成1 mol
和3 mol 可放出221.6 kJ的热量。
5.下列说法不正确的是( )
A. 与 属于同素异形体
B. 属于含有极性共价键的非极性分子
C.基态Ni原子的电子排布为
D.可通过X射线衍射实验比较 和 的键角大小
6.下列有关反应原理表述正确的是( )
A.侯氏制碱法中制备 :
B.碱性条件下催化电解 制 的阴极反应:
C.使用催化剂可降低 与 合成 的活化能,从而增大反应的
D.载人飞船中常用LiOH固体吸收 而不用KOH固体是由于LiOH碱性更强
7.下列物质结构与性质或物质性质与用途具有对应关系的是( )
A. 受热易分解,可用作化肥
B. 性质稳定,可作为燃料电池的燃料C. 与水分子之间形成氢键,医用酒精可使蛋白质变性
D.CO可与血红蛋白中的 以配位键结合,CO会引起人体中毒
8.固载Ru基催化剂催化反应 是实现 资源化的重要途径。将一定
比例的 和 的混合气体以一定流速通过装有催化剂的反应器,在反应器出口处检测到大量CO,其选择
性高达90%以上。下列说法不正确的是( )
A.HCOOH既有酸性,又有还原性
B.该反应的平衡常数
C.该反应中每消耗1 mol ,转移电子的数目约为
D.该反应可能经历了以下过程:① 、② ,且反应①
的活化能大于反应②
9.氮及其化合物的转化具有重要应用。下列说法正确的是( )
A.固氮菌能把空气中的 转化为 或铵态氮肥作为自身的养料
B.升高温度、增大压强,并使用合适催化剂,可使合成氨反应完全进行
C.“雷雨发庄稼”涉及的物质转化: 硝酸盐
D.用稀 处理做过银镜反应的试管:
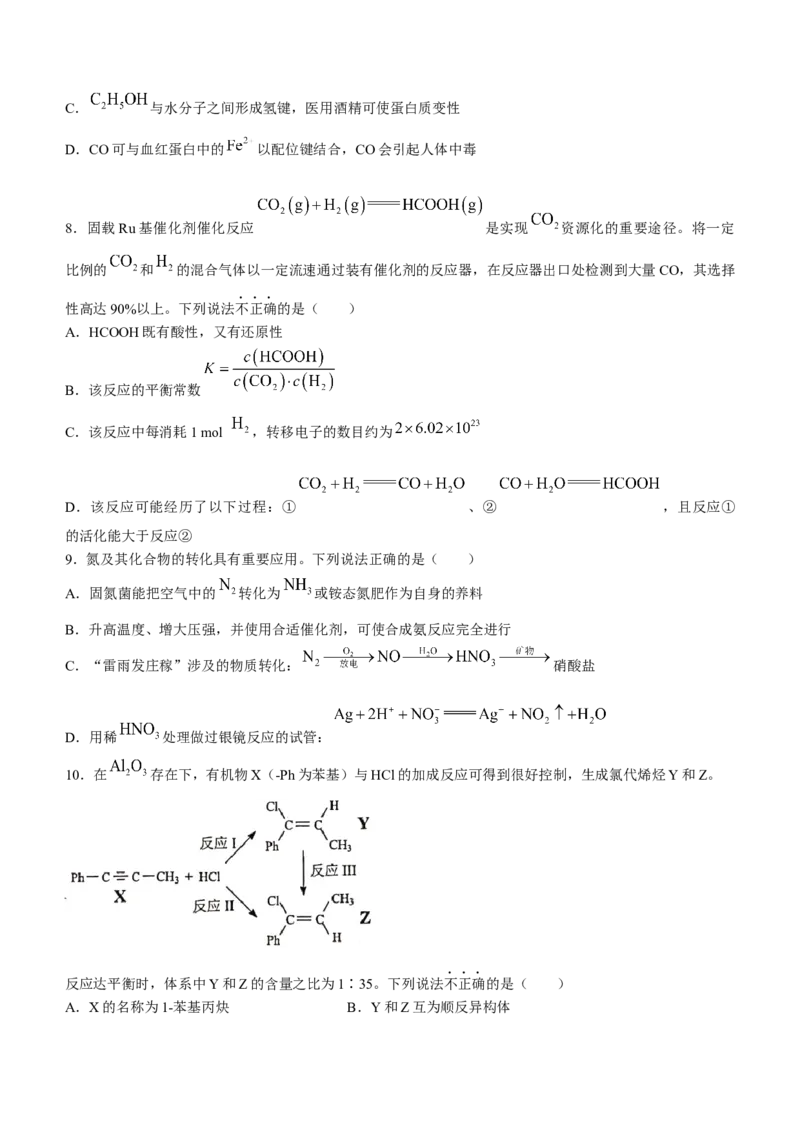
10.在 存在下,有机物X(-Ph为苯基)与HCl的加成反应可得到很好控制,生成氯代烯烃Y和Z。
反应达平衡时,体系中Y和Z的含量之比为1∶35。下列说法不正确的是( )
A.X的名称为1-苯基丙炔 B.Y和Z互为顺反异构体C.反应Ⅲ的 D.Y和Z不易与NaOH溶液反应
11.下列实验探究方案设计能达到相应探究目的的是( )
选项 探究方案 探究目的
A
室温下,用电导率传感器分别测定 溶液和盐酸的 判断 是否为弱电解质
电导率,比较溶液的导电性强弱
B
向1.00 mol·L 溶液中通入 气体,观察是否有黑 比较 与 的酸性强弱
色沉淀(CuS)生成
C 判断氯气与水的反应是否存在限
取两份新制氯水,分别滴加 溶液和淀粉KI溶液,观察
度
实验现象
D
向 的 溶液中加入等体积浓KI溶液,振荡后静置,观察 比较 在浓KI溶液与 中的
两层溶液颜色变化 溶解能力
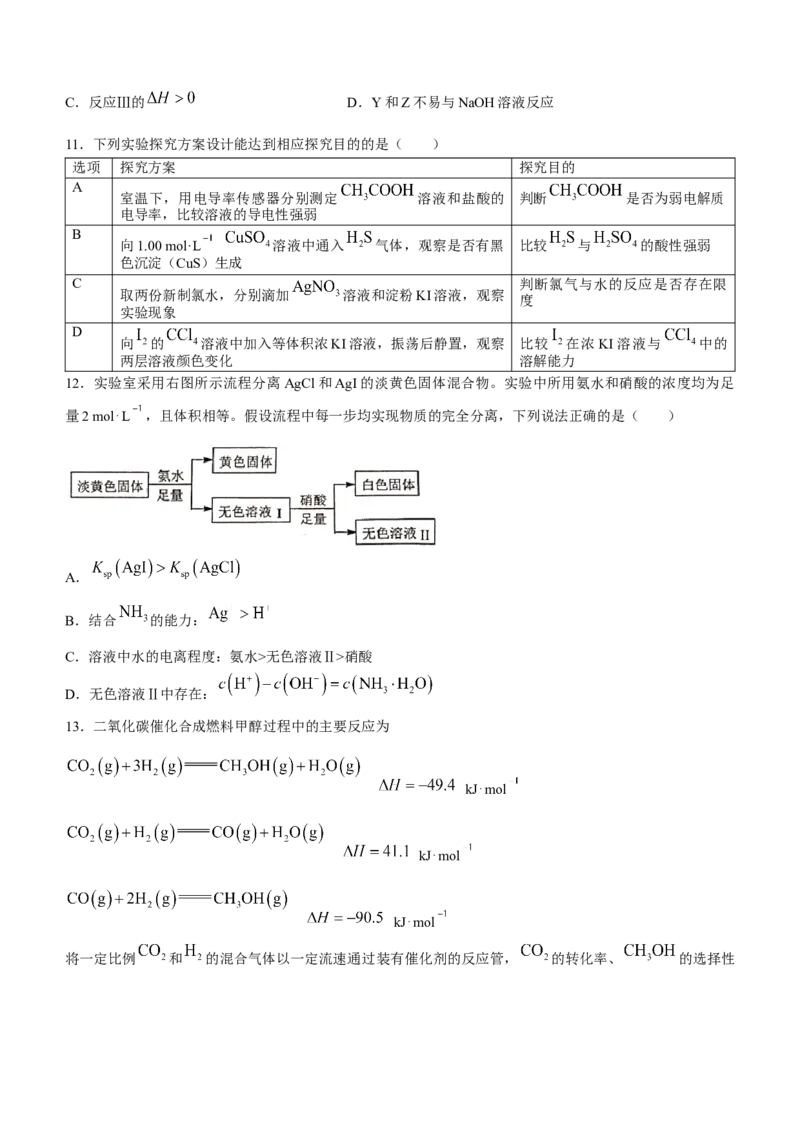
12.实验室采用右图所示流程分离AgCl和AgI的淡黄色固体混合物。实验中所用氨水和硝酸的浓度均为足
量2 mol⋅L ,且体积相等。假设流程中每一步均实现物质的完全分离,下列说法正确的是( )
A.
B.结合 的能力:
C.溶液中水的电离程度:氨水>无色溶液Ⅱ>硝酸
D.无色溶液Ⅱ中存在:
13.二氧化碳催化合成燃料甲醇过程中的主要反应为
kJ⋅mol
kJ⋅mol
kJ⋅mol
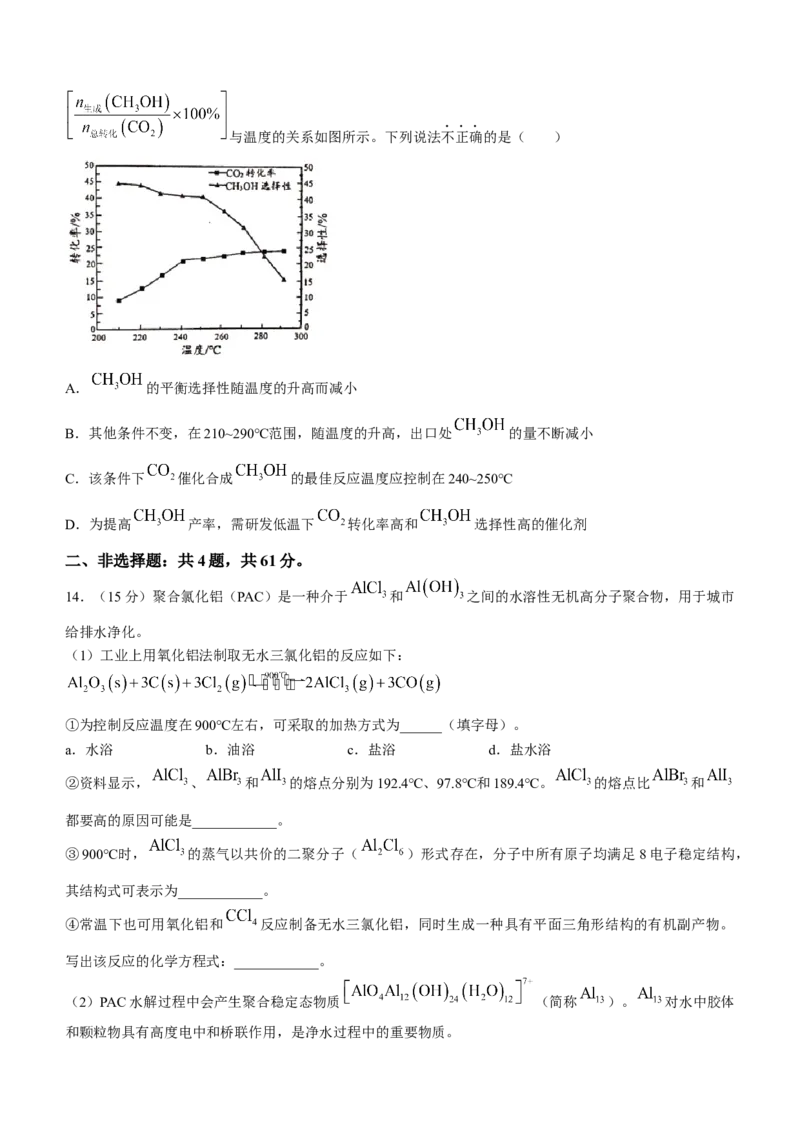
将一定比例 和 的混合气体以一定流速通过装有催化剂的反应管, 的转化率、 的选择性与温度的关系如图所示。下列说法不正确的是( )
A. 的平衡选择性随温度的升高而减小
B.其他条件不变,在210~290℃范围,随温度的升高,出口处 的量不断减小
C.该条件下 催化合成 的最佳反应温度应控制在240~250℃
D.为提高 产率,需研发低温下 转化率高和 选择性高的催化剂
二、非选择题:共4题,共61分。
14.(15分)聚合氯化铝(PAC)是一种介于 和 之间的水溶性无机高分子聚合物,用于城市
给排水净化。
(1)工业上用氧化铝法制取无水三氯化铝的反应如下:
①为控制反应温度在900℃左右,可采取的加热方式为______(填字母)。
a.水浴 b.油浴 c.盐浴 d.盐水浴
②资料显示, 、 和 的熔点分别为192.4℃、97.8℃和189.4℃。 的熔点比 和
都要高的原因可能是____________。
③900℃时, 的蒸气以共价的二聚分子( )形式存在,分子中所有原子均满足8电子稳定结构,
其结构式可表示为____________。
④常温下也可用氧化铝和 反应制备无水三氯化铝,同时生成一种具有平面三角形结构的有机副产物。
写出该反应的化学方程式:____________。
(2)PAC水解过程中会产生聚合稳定态物质 (简称 )。 对水中胶体
和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。① 在水解过程中会产生 、 等产物。写出 水解产生 的离子方
程式:__________________。
② 溶液与NaOH溶液反应时,若参与反应的 最终全部转化生成 ,则理论上参与反应的 与
OH⁻物质的量之比为______。
③使用 净水时应控制pH在6.80~8.02之间,否则净水效果不佳。在强酸性和强碱性环境时净水效果差的
原因是____________。
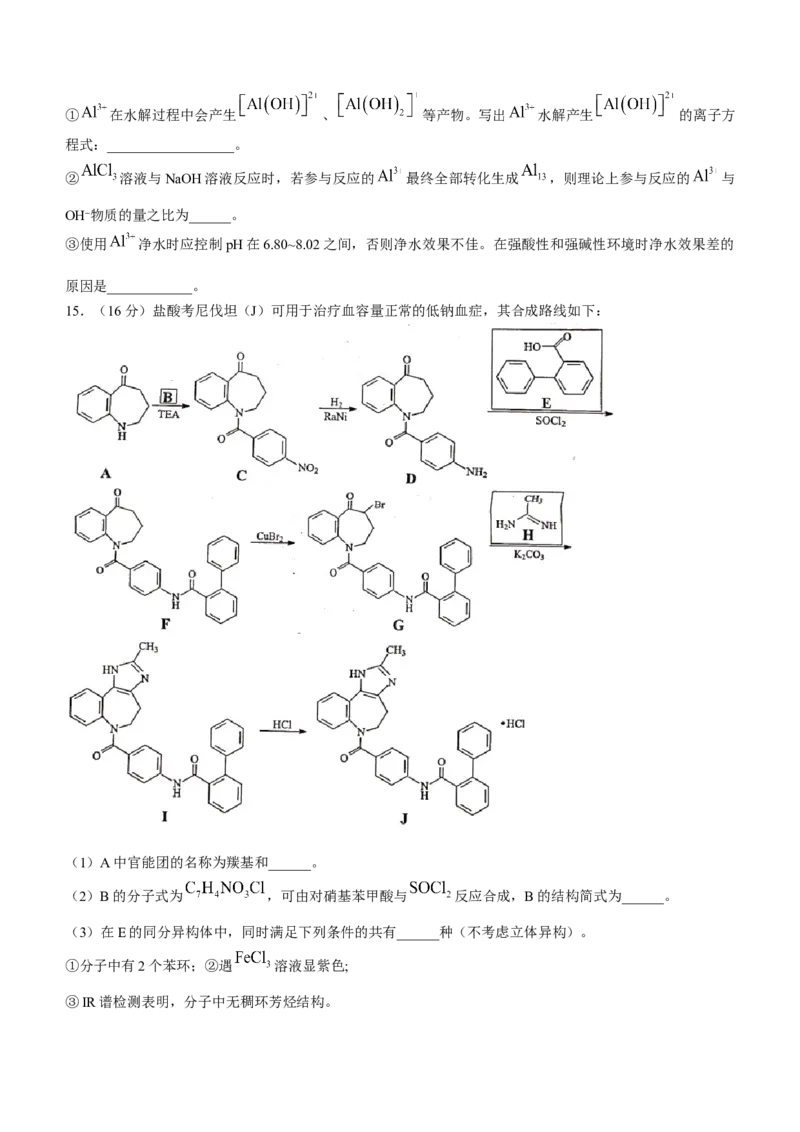
15.(16分)盐酸考尼伐坦(J)可用于治疗血容量正常的低钠血症,其合成路线如下:
(1)A中官能团的名称为羰基和______。
(2)B的分子式为 ,可由对硝基苯甲酸与 反应合成,B的结构简式为______。
(3)在E的同分异构体中,同时满足下列条件的共有______种(不考虑立体异构)。
①分子中有2个苯环;②遇 溶液显紫色;
③IR谱检测表明,分子中无稠环芳烃结构。(4) 的反应中,羰基相邻碳原子上的 键容易断裂的原因是____________。
(5) 的反应需经历 的过程。中间体X中无溴原子, 的过程中有π
键的断裂,则 的反应类型为______。
(6)将考尼伐坦(I)制成盐酸盐(J)的目的是____________。
(7)麻黄碱是治疗硬脊膜外麻醉引起低血压的常用药物,有机物K( )是生产麻黄碱的重
要中间体。写出以 和 为原料制备有机物K的合成路线流程图______(无机试剂和有机
溶剂任用,合成路线流程图示例见本题题干)。
16.(15分)实验室以废旧磷酸铁锂( )电极粉末为原料回收 ,其实验过程可表示为
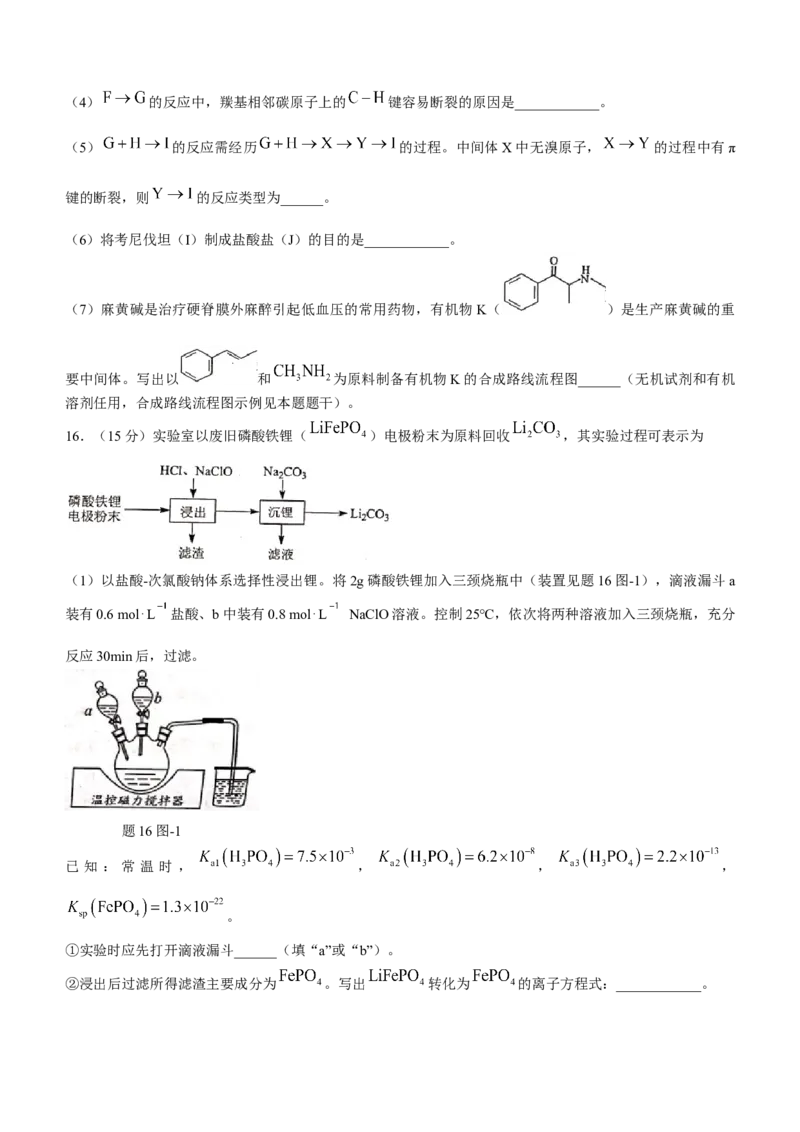
(1)以盐酸-次氯酸钠体系选择性浸出锂。将2g磷酸铁锂加入三颈烧瓶中(装置见题16图-1),滴液漏斗a
装有0.6 mol⋅L 盐酸、b中装有0.8 mol⋅L NaClO溶液。控制25℃,依次将两种溶液加入三颈烧瓶,充分
反应30min后,过滤。
题16图-1
已 知 : 常 温 时 , , , ,
。
①实验时应先打开滴液漏斗______(填“a”或“b”)。
②浸出后过滤所得滤渣主要成分为 。写出 转化为 的离子方程式:____________。③控制原料 ,锂的浸出率为95.59%。若提高盐酸用量,可使
锂浸出率达99%以上,但同时可能存在的缺陷有______。
(2)用碳酸钠作沉淀剂从浸出液中回收碳酸锂。有同学建议用“侯氏制碱法”的原理制备 。查阅资
料发现文献对常温下的 有不同的描述:
ⅰ.白色固体;ⅱ.尚未从溶液中分离出来。
为探究 的性质,将饱和LiCl溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变
浑浊并伴有气泡冒出,最终生成白色沉淀。
①上述现象说明,在该实验条件下 ______(填“稳定”或“不稳定”)。
②实验中发生反应的离子方程式为____________。
(3)盐湖提盐后的浓缩卤水(含 、 、 和少量 、 )也常用作制备 的重要原料。
已知:常温时 的溶解度为: 34.8g, , ,
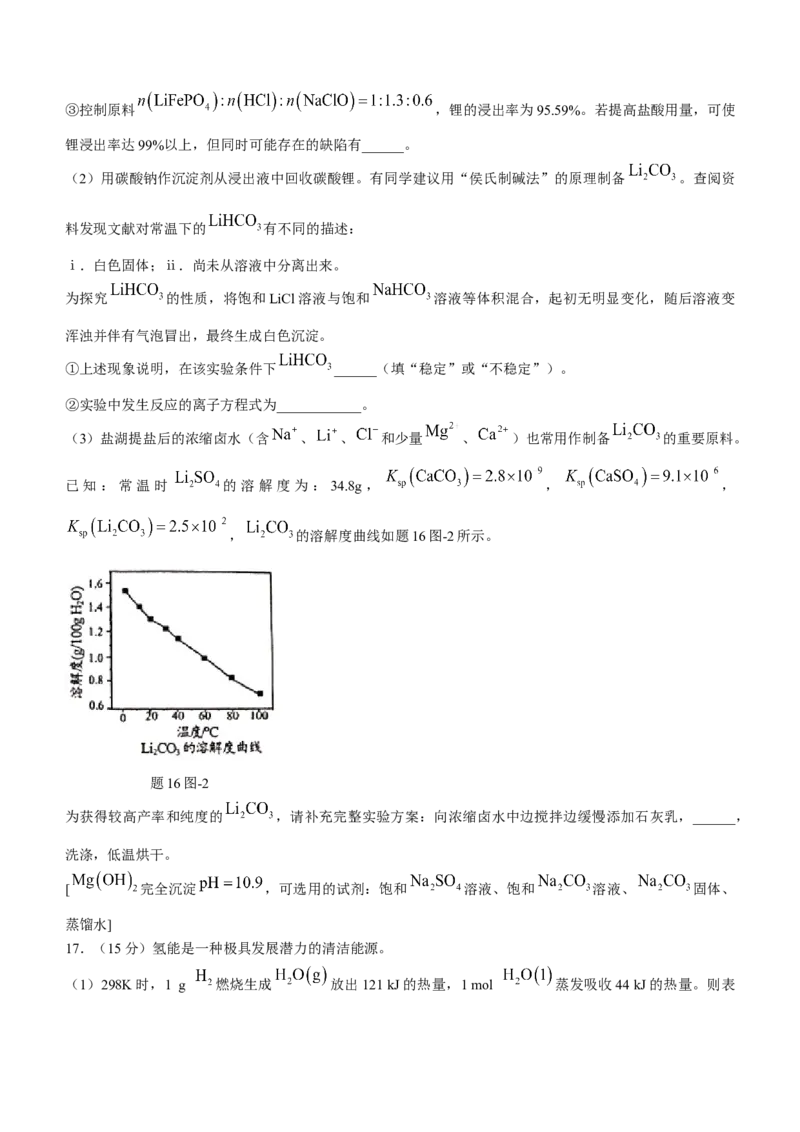
, 的溶解度曲线如题16图-2所示。
题16图-2
为获得较高产率和纯度的 ,请补充完整实验方案:向浓缩卤水中边搅拌边缓慢添加石灰乳,______,
洗涤,低温烘干。
[ 完全沉淀 ,可选用的试剂:饱和 溶液、饱和 溶液、 固体、
蒸馏水]
17.(15分)氢能是一种极具发展潜力的清洁能源。
(1)298K时,1 g 燃烧生成 放出121 kJ的热量,1 mol 蒸发吸收44 kJ的热量。则表示 燃烧热的热化学方程式为____________。
(2)工业上常用水煤气反应 制备氢气。生产水煤气时,通常交替通
入合适量的空气和水蒸气与煤炭反应,其原因是____________。
(3)一氧化碳变换反应 也可用于生产氢气。
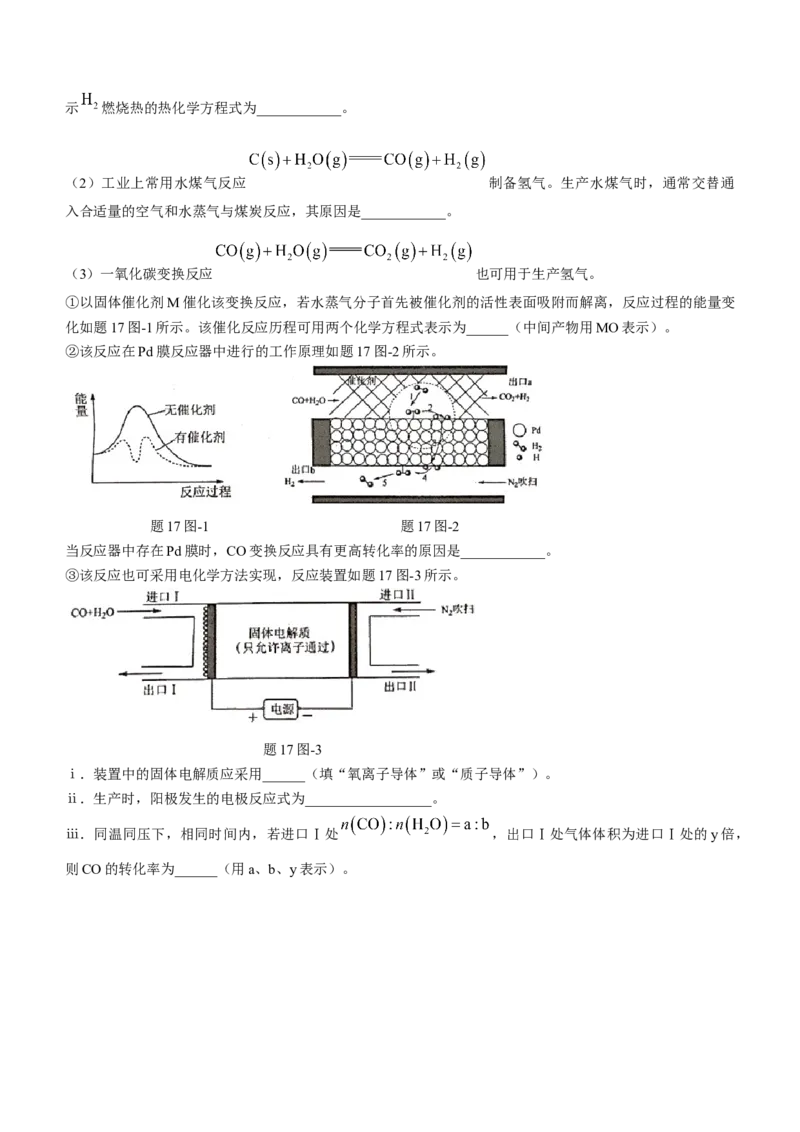
①以固体催化剂M催化该变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,反应过程的能量变
化如题17图-1所示。该催化反应历程可用两个化学方程式表示为______(中间产物用MO表示)。
②该反应在Pd膜反应器中进行的工作原理如题17图-2所示。
题17图-1 题17图-2
当反应器中存在Pd膜时,CO变换反应具有更高转化率的原因是____________。
③该反应也可采用电化学方法实现,反应装置如题17图-3所示。
题17图-3
ⅰ.装置中的固体电解质应采用______(填“氧离子导体”或“质子导体”)。
ⅱ.生产时,阳极发生的电极反应式为__________________。
ⅲ.同温同压下,相同时间内,若进口Ⅰ处 ,出口Ⅰ处气体体积为进口Ⅰ处的y倍,
则CO的转化率为______(用a、b、y表示)。常州市教育学会学业水平监测
高三化学参考答案 2024 年 1 月
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.B 2.C 3.A 4.A 5.A 6.B 7.D 8.D 9.A 10.C 11.D 12.D 13.B
二、非选择题:共4题,共61分。
14.(15分)
(1)①c(2分)
② 的化学键中离子键成分的百分数高于 和 ,具有一定的离子晶体的特征(2分)
③ (2分)
④ (2分)
(2)① (2分)
②13∶32(3分)
③强酸性环境,抑制 的水解,主要以 形式存在;强碱性环境,Al元素主要以 形式存在(2
分)
15.(16分)
(1)(亚)氨基(1分)
(2) (2分)
(3)22(2分)
(4)羰基为强吸电子基团,使得相邻碳原子上的C-H共用电子对更偏向羰基碳原子,C-H键的极性增强(2
分)
(5)消去反应(2分)
(6)增加药物的水溶性和稳定性(2分)(7) (5分)
16.(15分)
(1)①a(2分)
② (2分)
③过量的盐酸溶解 ,Fe元素也随Li一起浸出,导致产品纯度下降;产生 ,污染环境;后阶段消
耗更多的 ,增加试剂成本(3分)
(2)①不稳定(1分)
② (2分)
(3)调节溶液pH略大于10.9,(过滤,)边搅拌边往滤液中缓慢加入饱和 溶液至沉淀不再增加,
过滤,用蒸馏水洗涤固体2~3次,将洗涤滤液与滤液合并,加热溶液并保持100℃,边搅拌边添加
固体至沉淀不再增加,趁热过滤(5分)
17.(15分)
(1) kJ⋅mol (3分)
(2)水煤气反应吸热,煤炭与氧气反应放出的热量为水煤气反应供热。交替通入空气
和水蒸气,有利于维持体系处于较高温度,加快氢气的生成速率(2分)
(3)① 、 (2分)
②Pd膜能选择性分离出 ,促进反应正向进行(2分)
③i.质子导体(1分)
ⅰ. (2分)ⅱ. (3分)