文档内容
4.根据下列实验操作、现象得到的解释或结论错误的是
吉林省普通高中 G8 教考联盟 2024-2025 学年下学期期末考试
选项 实验操作 现象 解释或结论
高二年级 化学
向蛋白质溶液中加入适量的硫酸铜溶液并 溶液中有沉 可用硫酸铜溶液分
A.
本试卷共8页。考试结束后,将答题卡交回。
充分混合 淀析出 离、提纯蛋白质
注意事项:1.答卷前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在考生
信息条形码粘贴区。 向卤代烃CH 3 CH 2 CH 2 X中加入NaOH溶液
有淡黄色沉 该卤代烃中含有溴
2.答题时请按要求用笔。 B. 并加热,冷却后取上层液体,滴加过量稀
淀生成 元素
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案 硝酸,再加入几滴AgNO 溶液
3
无效;在草稿纸、试卷上答题无效。
溴的四氯化 该有机物中存在
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
C. 向丙烯醛中滴加溴的四氯化碳溶液
碳溶液褪色 碳碳双键
5.保持卡面清洁,不要折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量: H 1 C 12 N 14 O 16
向淀粉溶液中加入几滴稀硫酸,水浴加热,
D. 无蓝色出现 淀粉完全水解
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
冷却后加入几滴碘水,加热
符合题目要求。
1.化学是现代生产、生活与科技的中心学科之一。下列与化学有关的说法错误的是 5.下列离子方程式书写正 . 确 . 的是
A.羊毛织品水洗后会变形与氢键有关
A.过量铁粉与稀硝酸反应:
B.聚乙炔属于有机高分子材料,能导电
C.网状结构的聚丙烯酸钠是高吸水性树脂
D.淀粉、蛋白质和油脂都是有机高分子化合物
2.下列化学用语或表述正确的是
A.月壤成分中所含羟基的电子式:[ ]-
B.CH +的电子式为:
3
C.四氯化碳的空间填充模型:
D.反−2−丁烯分子的球棍模型;
3.分类是科学研究的重要方法,下列物质分类错误的是
..
A.非电解质:乙醇、NH 、CO B.同素异形体:石墨、C 、金刚石
3 2 60
C.碱性氧化物:氧化钠、氧化铁、氧化镁 D.酸性氧化物:干冰、二氧化硫、二氧化氮
化学试题 第1页 (共8页) 化学试题 第2页 (共8页)
F e + 4 H + + N O −3 = F e 3 + + N O + 2 H
2
O
B.新制氯水中加入少量CaCO :2Cl +H O+CaCO =Ca2++2Cl−+CO +2HClO
3 2 2 3 2
C.NaHSO 溶液与Ba(OH) 溶液混合至呈中性:
4 2
B a 2 + + O H − + S O 24 − + H + = B a S O
4
+ H
2
O
D.向FeBr 溶液中通入过量Cl :
2 2
2 F e 2 + + C l
2
= 2 F e 3 + + 2 C l −
6.除去下列物质中的杂质(括号内的物质),所使用的试剂和主要操作正确的是
选项 物质(杂质) 使用的试剂 主要操作
A 乙炔(硫化氢) 高锰酸钾溶液 洗气
B 苯(苯酚) 浓溴水 过滤
C 乙醇 (水) 生石灰 蒸馏
D 乙酸乙酯(乙酸) 氢氧化钠溶液 分液
A. A B. B C. C D . D
{#{QQABIYQoxggQghSACY5KVwFqCUoQsIKhJeoEAUAbKAQKCJFIBIA=}#}7.实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色溶液,且在溶液中四种离子
的数目相同。下列四个离子组能达到要求的是
A.
化学试题 第3页 (共8页) 化学试题 第4页 (共8页)
N a +、 K +、 S O 2−、
4
C −l B. C u 2 +、 K +、 S O 24 −、 N O −3
C. N H +、
4
N a +、 C l −、 H C O −3
11.将H S和空气的混合气体通入含 2
D.Al3+、K+、CO 2-、SO 2-
3 4
8.阿斯巴甜是一种常见的合成甜味剂,其结构如图所示,下列说法中正确的是
A.阿斯巴甜分子中含有4种官能团
B.阿斯巴甜可以与碱反应,与酸不反应
C.阿斯巴甜分子完全水解生成4种产物
D.1mol阿斯巴甜分子最多消耗6molH
2
9.高铁酸钠(Na FeO )具有很强的氧化性,能有效地杀灭水中的细菌和病毒,同时被还原成
2 4
Fe(OH) 能高效地除去水中的悬浮物,是一种新型高效水处理剂。其制备方法如下:
3
2Fe(OH) +3NaClO+aNaOH=2Na FeO +3NaCl+bH O。下列说法错误的是
3 2 4 2 ..
A.在水处理中,Na FeO 兼具消毒和净水两种功能
2 4
B.反应式中化学计量数a、b的值分别为4、5
C.碱性条件下NaClO氧化性强于Na FeO
2 4
D.含1molNa FeO 的溶液中含有阳离子的数目为2N
2 4 A
10.利用下列实验装置进行的相应实验,能达到实验目的的是
a b c d
A.用a装置制取硝基苯
B.用b装置验证酸性:醋酸>碳酸>苯酚
C.用c装置验证有HBr生成
D.用d装置检验乙醇发生消去反应的产物是乙烯
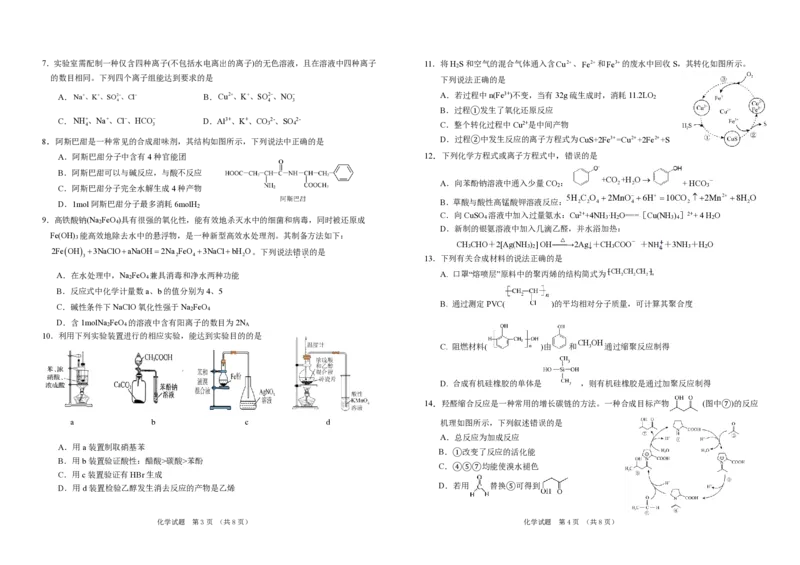
C u 2 + 、Fe2+和Fe3+的废水中回收S,其转化如图所示。
下列说法正确的是
A.若过程中n(Fe3+)不变,当有32g硫生成时,消耗11.2LO 2
B.过程①发生了氧化还原反应
C.整个转化过程中Cu2+是中间产物
D.过程②中发生反应的离子方程式为 C u S + 2 F e 3 + = C u 2 + + 2 F e 2 + + S
12.下列化学方程式或离子方程式中,错误的是
A.向苯酚钠溶液中通入少量CO : 2
+ C O
2
+ H
2
O →
+ HCO - 3
B.草酸与酸性高锰酸钾溶液反应:
5 H
2
C
2
O
4
+ 2 M n O −4 + 6 H + = 1 0 C O
2
+ 2 M n 2 + + 8 H
2
O
C.向CuSO 溶液中加入过量氨水:Cu2++4NH ·H O===[Cu(NH ) ]2++ 4 H O
4 3 2 3 4 2
D.新制的银氨溶液中加入几滴乙醛,并水浴加热:
CH CHO+2[Ag(NH ) ] OH―― △ →2Ag↓+CH COO- + +3NH +H O
3 3 2 3 3 2
13.下列有关合成材料的说法正确的是
A.
口罩“熔喷层”原料中的聚丙烯的结构简式为[CH
2
CH
2
CH
2
]
n
B. 通过测定PVC( )的平均相对分子质量,可计算其聚合度
C. 阻燃材料( )由 和
C H
3
O H
通过缩聚反应制得
D. 合成有机硅橡胶的单体是 ,则有机硅橡胶是通过加聚反应制得
14.羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物 (图中⑦)的反应
机理如图所示,下列叙述错误的是
A.总反应为加成反应
B.①改变了反应的活化能
C.④⑤⑦均能使溴水褪色
D.若用 替换⑤可得到
{#{QQABIYQoxggQghSACY5KVwFqCUoQsIKhJeoEAUAbKAQKCJFIBIA=}#}15.抗肿瘤药物盐酸苯达莫司汀的合成工艺中,其中一步的转化过程如图所示,已知该转化过
程中化合物a需经过两步反应才可成环。下列叙述正确的是
化学试题 第5页 (共8页) 化学试题 第6页 (共8页)
⎯ C⎯H H 2S2 ⎯5O O
4
H/ ⎯→
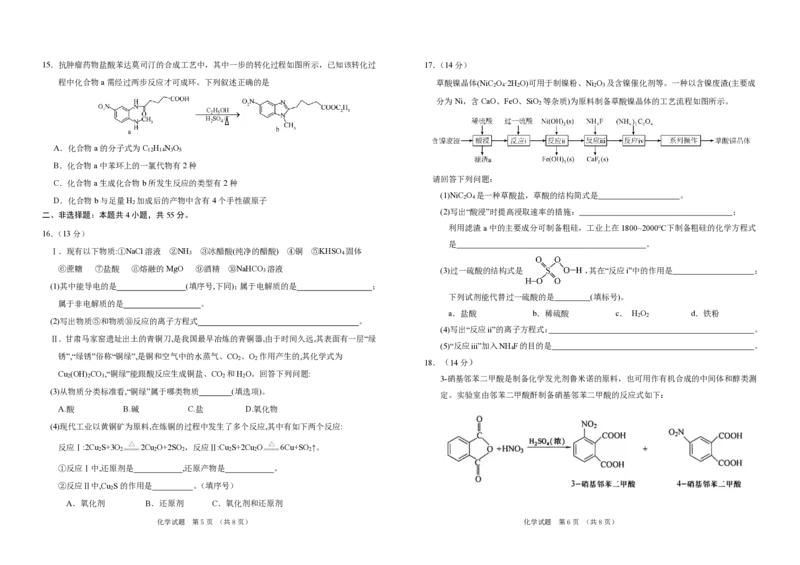
17.(14分)
草酸镍晶体(NiC O ·2H O)可用于制镍粉、Ni O 及含镍催化剂等。一种以含镍废渣(主要成
2 4 2 2 3
分为Ni,含CaO、FeO、SiO 等杂质)为原料制备草酸镍晶体的工艺流程如图所示。
2
A.化合物a的分子式为C H N O
12 14 3 5
B.化合物a中苯环上的一氯代物有2种
请回答下列问题:
C.化合物a生成化合物b所发生反应的类型有2种
(1)NiC O 是一种草酸盐,草酸的结构简式是 。
D.化合物b与足量H 加成后的产物中含有4个手性碳原子 2 4
2
(2)写出“酸浸”时提高浸取速率的措施: ;
二、非选择题:本题共4小题,共55分。
利用滤渣a中的主要成分可制备粗硅,工业上在1800~2000℃下制备粗硅的化学方程式
16.(13分)
是 。
Ⅰ.现有以下物质:①NaCl溶液 ②NH ③冰醋酸(纯净的醋酸) ④铜 ⑤KHSO 固体
3 4
⑥蔗糖 ⑦盐酸 ⑧熔融的MgO ⑨酒精 ⑩NaHCO 3 溶液 (3)过一硫酸的结构式是 ,其在“反应i”中的作用是 ;
(1)其中能导电的是 (填序号,下同);属于电解质的是 ;
下列试剂能代替过一硫酸的是 (填标号)。
属于非电解质的是 。
a.盐酸 b.稀硫酸 c. H O d.铁粉
2 2
(2)写出物质⑤和物质⑩反应的离子方程式 。
(4)写出“反应ii”的离子方程式: 。
Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿
(5)“反应iii”加入NH F的目的是 。
4
锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO 、O 作用产生的,其化学式为
2 2 18.(14分)
Cu (OH) CO ,“铜绿”能跟酸反应生成铜盐、CO 和H O。回答下列问题:
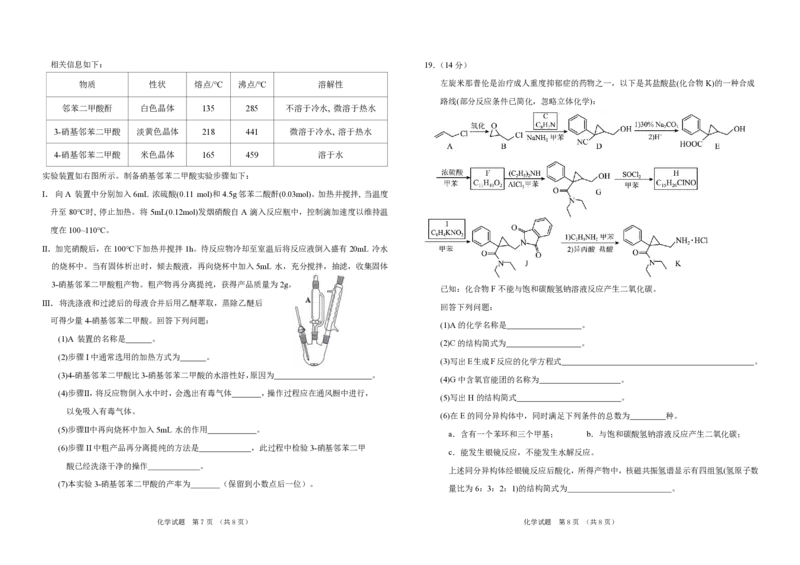
2 2 3 2 2 3-硝基邻苯二甲酸是制备化学发光剂鲁米诺的原料,也可用作有机合成的中间体和醇类测
(3)从物质分类标准看,“铜绿”属于哪类物质 (填选项)。
定。实验室由邻苯二甲酸酐制备硝基邻苯二甲酸的反应式如下:
A.酸 B.碱 C.盐 D.氧化物
(4)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
反应Ⅰ:2Cu S+3O 2Cu O+2SO ,反应Ⅱ:Cu S+2Cu O 6Cu+SO ↑。
2 2 2 2 2 2 2
①反应Ⅰ中,还原剂是 ,还原产物是 。
②反应Ⅱ中,Cu S的作用是 。(填序号)
2
A.氧化剂 B.还原剂 C.氧化剂和还原剂
{#{QQABIYQoxggQghSACY5KVwFqCUoQsIKhJeoEAUAbKAQKCJFIBIA=}#}相关信息如下: 19.(14分)
物质 性状 熔点/℃ 沸点/℃ 溶解性 左旋米那普伦是治疗成人重度抑郁症的药物之一,以下是其盐酸盐(化合物K)的一种合成
路线(部分反应条件已简化,忽略立体化学):
邻苯二甲酸酐 白色晶体 135 285 不溶于冷水, 微溶于热水
3-硝基邻苯二甲酸 淡黄色晶体 218 441 微溶于冷水, 溶于热水
4-硝基邻苯二甲酸 米色晶体 165 459 溶于水
实验装置如右图所示。制备硝基邻苯二甲酸实验步骤如下:
I. 向A 装置中分别加入6mL 浓硫酸(0.11 mol)和4.5g邻苯二酸酐(0.03mol)。加热并搅拌, 当温度
升至 80℃时, 停止加热。将 5mL(0.12mol)发烟硝酸自 A 滴入反应瓶中,控制滴加速度以维持温
度在100~110℃。
Ⅱ.加完硝酸后,在100℃下加热并搅拌1h。待反应物冷却至室温后将反应液倒入盛有20mL 冷水
的烧杯中。当有固体析出时,倾去酸液,再向烧杯中加入5mL 水,充分搅拌,抽滤,收集固体
3-硝基邻苯二甲酸粗产物。粗产物再分离提纯,获得产品质量为2g。
已知:化合物F不能与饱和碳酸氢钠溶液反应产生二氧化碳。
Ⅲ.将洗涤液和过滤后的母液合并后用乙醚萃取,蒸除乙醚后
回答下列问题:
可得少量4-硝基邻苯二甲酸。回答下列问题:
(1)A的化学名称是 。
(1)A 装置的名称是 。
(2)C的结构简式为 。
(2)步骤I中通常选用的加热方式为 。
(3)写出E生成F反应的化学方程式 。
(3)4-硝基邻苯二甲酸比3-硝基邻苯二甲酸的水溶性好,原因为 。
(4)G中含氧官能团的名称为 。
(4)步骤Ⅱ,将反应物倒入水中时,会逸出有毒气体 ,操作过程应在通风橱中进行,
(5)写出H的结构简式 。
以免吸入有毒气体。
(6)在E的同分异构体中,同时满足下列条件的总数为 种。
(5)步骤Ⅱ中再向烧杯中加入5mL 水的作用 。
a.含有一个苯环和三个甲基; b.与饱和碳酸氢钠溶液反应产生二氧化碳;
(6)步骤II中粗产品再分离提纯的方法是 ,此过程中检验3-硝基邻苯二甲
c.能发生银镜反应,不能发生水解反应。
酸已经洗涤干净的操作 。
上述同分异构体经银镜反应后酸化,所得产物中,核磁共振氢谱显示有四组氢(氢原子数
(7)本实验3-硝基邻苯二甲酸的产率为 (保留到小数点后一位)。
量比为6:3:2:1)的结构简式为 。
化学试题 第7页 (共8页) 化学试题 第8页 (共8页)
{#{QQABIYQoxggQghSACY5KVwFqCUoQsIKhJeoEAUAbKAQKCJFIBIA=}#}