文档内容
2024-2025 年度上学期河南省高二年级第一次联考
化学
本试卷满分100分,考试用时75分钟
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版选择性必修1第一章至第二章。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 古代典籍中蕴含丰富 化的学知识,下列古诗词的描述中存在吸热反应的是
A. 李白——日照香炉生紫烟 B. 王安石——爆竹声中一岁除
C. 李商隐——蜡炬成灰泪始干 D. 苏轼——投泥泼水愈光明
的
2. 生活中常采用一些措施,以改变化学反应速率,下列做法属于温度对化学反应速率影响 是
A. 肉制品放冰箱中保存
B. 洗衣粉加酶更易除奶渍、汗渍
C. 医用酒精通常比白酒燃烧更旺
D. 青皮香蕉中加一个熟苹果,可催熟香蕉
3. 已知:反应 。若反应速率分别用 、 、 、 表
示,则下列关系错误的是
A. B.
C. D.
第1页/共14页
学科网(北京)股份有限公司的
4. 乙烯是一种重要 基本化工原料,主要用于制造塑料、合成橡胶、合成纤维等。利用 氧化乙烷制
备乙烯的反应为 ,该反应达到平衡后,下列
措施不能提高 的平衡产率的是
A. 升高温度 B. 移除部分
C. 压缩容器体积 D. 增大 的浓度
5. 肼( )又称为联氨,在航空航天领域,可用作燃料和推进剂,它具有能量高、密度大、可贮存等优
点。下列能正确表示 燃烧热的热化学方程式的是
A.
B.
C.
D.
6. 下列说法正确的是
A. 放热反应均不需要加热
B. 活化分子间的碰撞均为有效碰撞
C. 能够自发进行的反应可能是吸热反应
D. 增大反应物浓度,容器内活化分子百分数增大
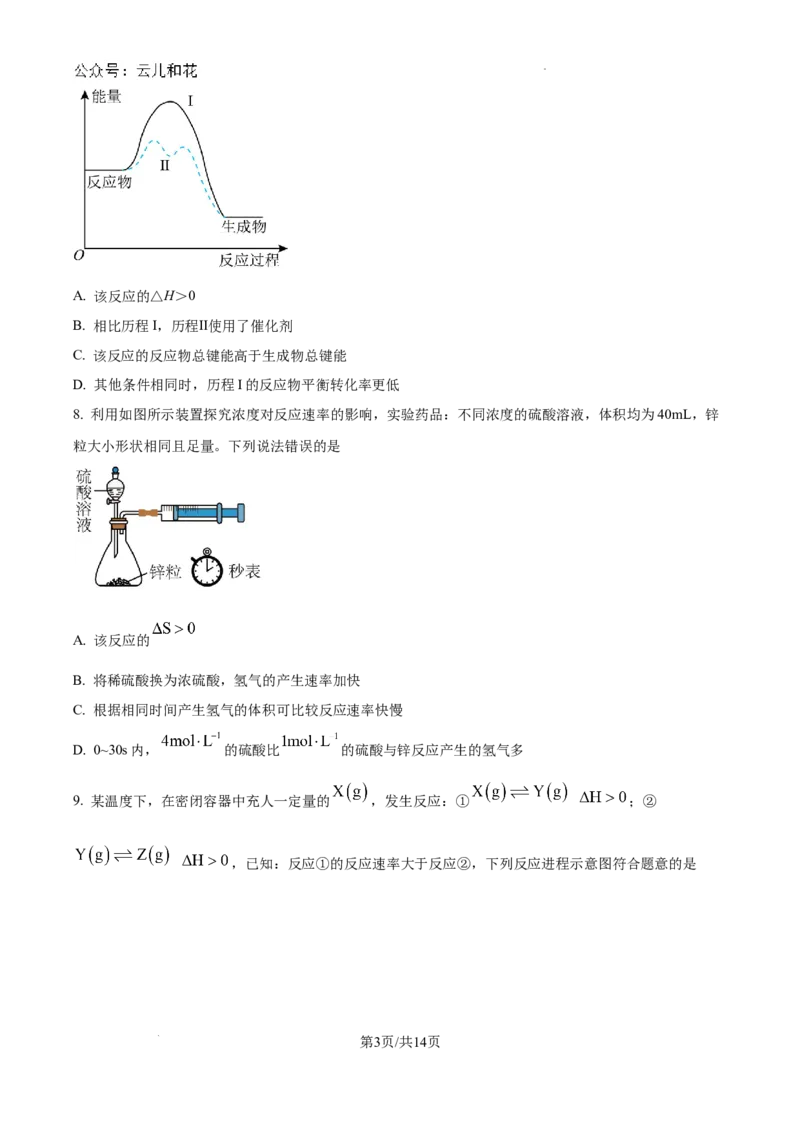
7. 某反应的反应过程与能量的关系如图所示,下列说法正确的是
第2页/共14页
学科网(北京)股份有限公司A. 该反应的△H>0
B. 相比历程I,历程Ⅱ使用了催化剂
C. 该反应的反应物总键能高于生成物总键能
D. 其他条件相同时,历程I的反应物平衡转化率更低
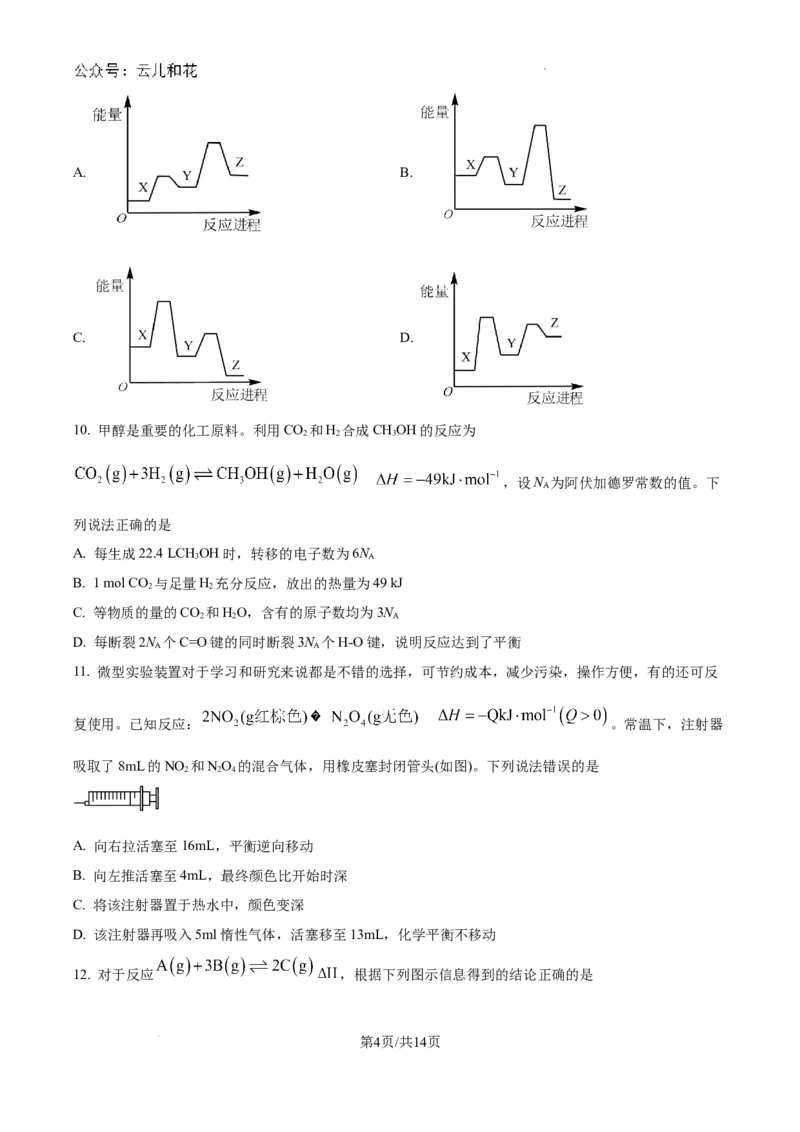
8. 利用如图所示装置探究浓度对反应速率的影响,实验药品:不同浓度的硫酸溶液,体积均为40mL,锌
粒大小形状相同且足量。下列说法错误的是
A. 该反应的
B. 将稀硫酸换为浓硫酸,氢气的产生速率加快
C. 根据相同时间产生氢气的体积可比较反应速率快慢
D. 0~30s内, 的硫酸比 的硫酸与锌反应产生的氢气多
9. 某温度下,在密闭容器中充人一定量的 ,发生反应:① ;②
,已知:反应①的反应速率大于反应②,下列反应进程示意图符合题意的是
第3页/共14页
学科网(北京)股份有限公司A. B.
C. D.
10. 甲醇是重要的化工原料。利用CO 和H 合成CHOH的反应为
2 2 3
,设N 为阿伏加德罗常数的值。下
A
列说法正确的是
A. 每生成22.4 LCH OH时,转移的电子数为6N
3 A
B. 1 mol CO 与足量H 充分反应,放出的热量为49 kJ
2 2
C. 等物质的量的CO 和HO,含有的原子数均为3N
2 2 A
D. 每断裂2N 个C=O键的同时断裂3N 个H-O键,说明反应达到了平衡
A A
11. 微型实验装置对于学习和研究来说都是不错的选择,可节约成本,减少污染,操作方便,有的还可反
复使用。已知反应: 。常温下,注射器
吸取了8mL的NO 和NO 的混合气体,用橡皮塞封闭管头(如图)。下列说法错误的是
2 2 4
A. 向右拉活塞至16mL,平衡逆向移动
B. 向左推活塞至4mL,最终颜色比开始时深
C. 将该注射器置于热水中,颜色变深
D. 该注射器再吸入5ml惰性气体,活塞移至13mL,化学平衡不移动
12. 对于反应 ,根据下列图示信息得到的结论正确的是
第4页/共14页
学科网(北京)股份有限公司A. 甲图: B. 乙图:
C. 丙图:点1对应的 D. 丁图:I对应的反应温度大于II对应的
13. 已知:通常状态下,由最稳定单质生成1mol某纯物质的热效应称为该物质的标准摩尔生成焓( ),
单质的标准摩尔生成焓为0。部分物质的标准摩尔生成焓如表所示:
物质
乙炔( )三聚化制苯( )是重要的有机合成反应,具有高效、快速等优点。下列说法错误的是
A. 的燃烧热 为
B.
C.
D.
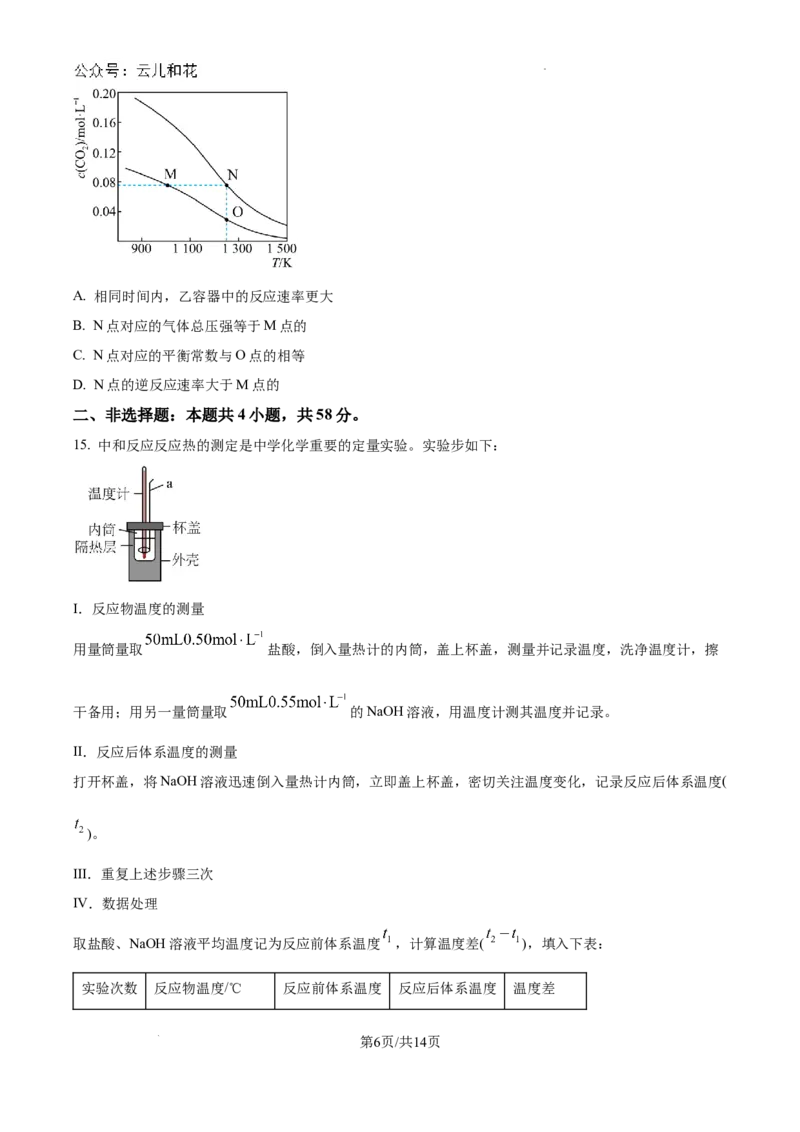
14. 在体积均为1L的甲、乙两个恒容密闭容器中分别加入足量的炭粉,再分别充入 和
,在不同温度下发生反应 ,反应达到平衡时, 的物质的量
浓度随温度的变化关系如图所示。下列说法错误的是
第5页/共14页
学科网(北京)股份有限公司A. 相同时间内,乙容器中的反应速率更大
B. N点对应的气体总压强等于M点的
C. N点对应的平衡常数与O点的相等
D. N点的逆反应速率大于M点的
二、非选择题:本题共4小题,共58分。
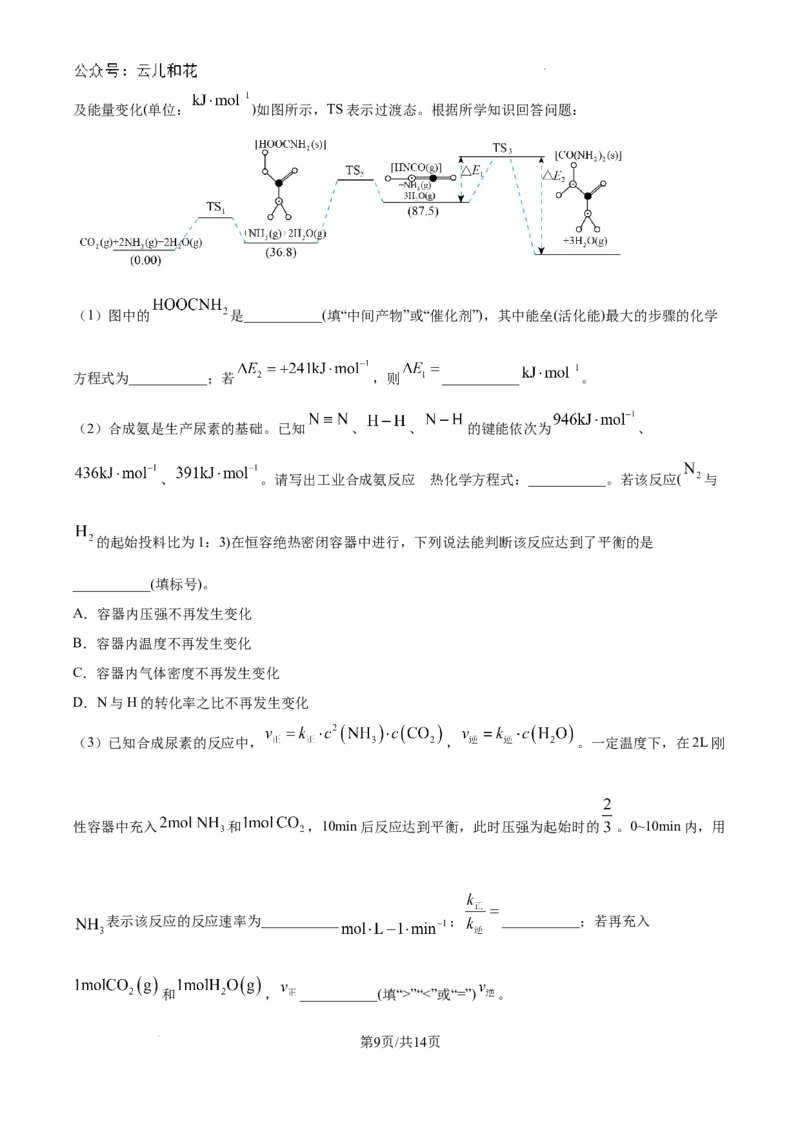
15. 中和反应反应热的测定是中学化学重要的定量实验。实验步如下:
I.反应物温度的测量
用量筒量取 盐酸,倒入量热计的内筒,盖上杯盖,测量并记录温度,洗净温度计,擦
干备用;用另一量筒量取 的NaOH溶液,用温度计测其温度并记录。
II.反应后体系温度的测量
打开杯盖,将NaOH溶液迅速倒入量热计内筒,立即盖上杯盖,密切关注温度变化,记录反应后体系温度(
)。
III.重复上述步骤三次
IV.数据处理
取盐酸、NaOH溶液平均温度记为反应前体系温度 ,计算温度差( ),填入下表:
实验次数 反应物温度/℃ 反应前体系温度 反应后体系温度 温度差
第6页/共14页
学科网(北京)股份有限公司盐
NaOH溶液 /℃ /℃ ( )/℃
酸
1 26.9 27.1 30.3
2 27.1 27.1 30.3
3 27.0 27.0 29.3
4 27.1 27.1 30.5
请回答下列问题:
(1)仪器a的名称是___________,搅拌的目的是___________;取反应时溶液的___________(填“最低温
度”“最高温度”或“平均温度”)作为反应后体系温度。
(2)量热计内筒与外壳上口相平且垫隔热层的原因是___________;若将盐酸浓度改为 ,
NaOH溶液浓度改为 ,测得的温度差___________(填“更大”“更小”或“相同”,下同),测
得的中和反应反应热 ___________。
(3)设实验所用的酸、碱溶液的密度均为 ,且比热容与水的相同,发生中和反应后溶液的比热
容 ,上述实验测得的中和反应反应热 ___________ [提示
];又知25℃、101kPa下,中和反应反应热 为 ,实验
值与理论值相差较大的原因可能是___________(任写一点)。
(4)进行中和反应反应热 的测定时,保持其他条件相同,使用下列酸碱组合:
①稀硫酸、 溶液 ②醋酸溶液、氨水 ③稀硫酸、NaOH溶液
理论上测得的中和反应反应热 由大到小的顺序为___________(填标号)。
16. 用目测法探究浓度、温度等对
的反应速率的影响,结果总不
尽如人意。某研究团队采用正交法,通过手持色度计和数据采集器,测定并记录溶液光透过率从开始到
100%所需的反应时间,确定反应快慢,实验数据及结果见下表:
第7页/共14页
学科网(北京)股份有限公司蒸
实
馏
验 反应
溶液体 溶液体 水 溶液体 反应时间
编 温度 溶液体积
体
号 积 积 积
积
1 25℃ 4mL 0.4mL 2mL 2滴 0
2 45℃ 4mL 0.4mL 2mL 2滴 0
.
3 25℃ 4mL 02mL 2mL V 0
4 25℃ 4mL 0.4mL 2mL 0 0.1mL
经查阅资料, 溶液与 溶液的浓度对反应速率影响不显著,在此不探究。
已知:1滴水的体积大约为0.05mL。
请回答下列问题:
(1) 溶液与 溶液反应的离子方程式为___________。
(2)实验1、实验4探究的影响因素是___________;探究 溶液浓度对反应速率影响的实验编号是
___________。
(3)实验3中, ___________mL;实验1中, 可能是___________(填标号)s;实验4中,0~30s内,
___________(保留两位有效数字) 。
A.11 B.22 C.68 D.153
(4)若反应温度每升高10℃,反应速率增加到原来的2~4倍。实验1中,若0~17s内
,实验2中,0~17s内, 最大为___________(用含a的式子表示)
。
17. “低碳经济”已成为全球研究重要课题。技术固碳主要是应用碳捕集、利用与封存的技术。 合成尿
素的反应为 ,合成尿素的机理
第8页/共14页
学科网(北京)股份有限公司及能量变化(单位: )如图所示,TS表示过渡态。根据所学知识回答问题:
(1)图中的 是___________(填“中间产物”或“催化剂”),其中能垒(活化能)最大的步骤的化学
方程式为___________;若 ,则 ___________ 。
(2)合成氨是生产尿素的基础。已知 、 、 的键能依次为 、
的
、 。请写出工业合成氨反应 热化学方程式:___________。若该反应( 与
的起始投料比为1:3)在恒容绝热密闭容器中进行,下列说法能判断该反应达到了平衡的是
___________(填标号)。
A.容器内压强不再发生变化
B.容器内温度不再发生变化
C.容器内气体密度不再发生变化
D.N与H的转化率之比不再发生变化
(3)已知合成尿素的反应中, , 。一定温度下,在2L刚
性容器中充入 和 ,10min后反应达到平衡,此时压强为起始时的 。0~10min内,用
表示该反应的反应速率为___________ ; ___________;若再充入
和 , ___________(填“>”“<”或“=”) 。
第9页/共14页
学科网(北京)股份有限公司18. 硅及其化合物在生活、生产中应用广泛。
(1)工业制备高纯硅的主要反应如下:
i.
ii.
iii.
则反应 的 ___________ ,
在___________(填“高温”“低温”或“任何温度”)下有利于该反应自发进行。
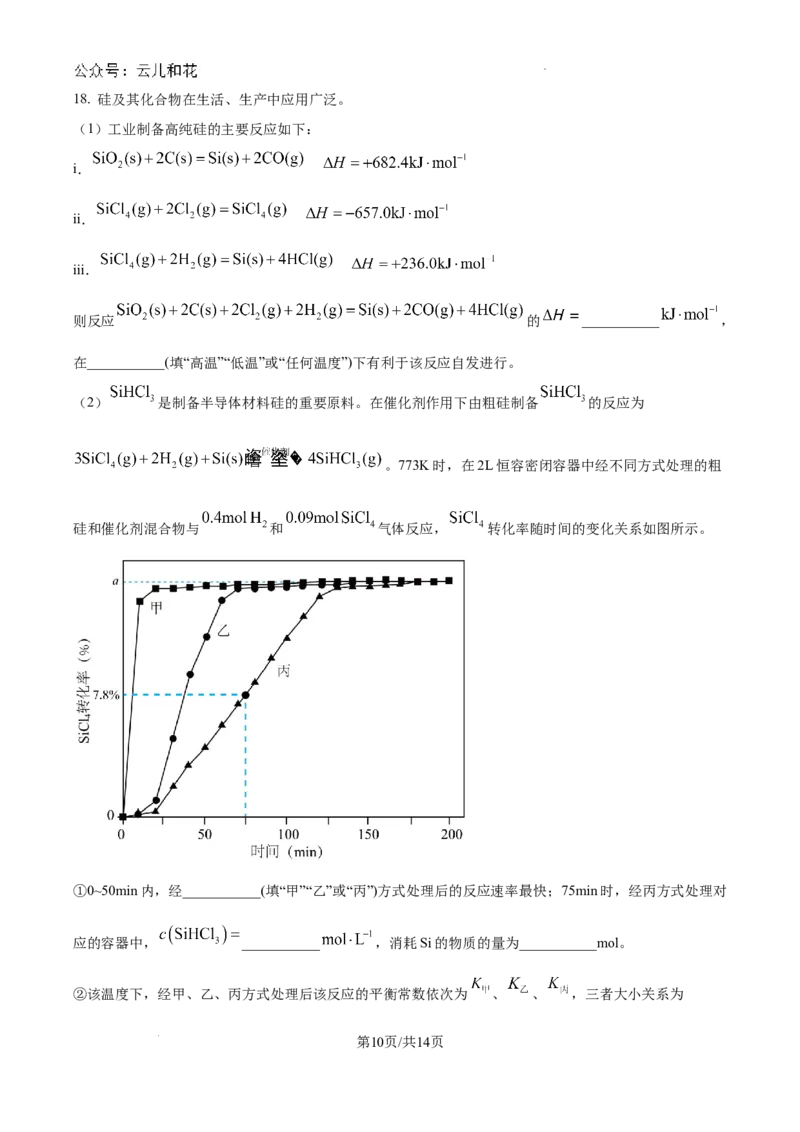
(2) 是制备半导体材料硅的重要原料。在催化剂作用下由粗硅制备 的反应为
。773K时,在2L恒容密闭容器中经不同方式处理的粗
硅和催化剂混合物与 和 气体反应, 转化率随时间的变化关系如图所示。
①0~50min内,经___________(填“甲”“乙”或“丙”)方式处理后的反应速率最快;75min时,经丙方式处理对
应的容器中, ___________ ,消耗Si的物质的量为___________mol。
②该温度下,经甲、乙、丙方式处理后该反应的平衡常数依次为 、 、 ,三者大小关系为
第10页/共14页
学科网(北京)股份有限公司___________, ___________(列出含a的计算式即可)。
③若保持温度不变,Si足量,再向上述已达平衡的容器中充入 气体,重新达到平衡后,
的转化率___________(填“增大”“减小”或“不变”)。
第11页/共14页
学科网(北京)股份有限公司2024-2025 年度上学期河南省高二年级第一次联考
化学
本试卷满分100分,考试用时75分钟
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版选择性必修1第一章至第二章。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
【1题答案】
【答案】D
【2题答案】
【答案】A
【3题答案】
【答案】A
【4题答案】
【答案】C
【5题答案】
【答案】B
【6题答案】
【答案】C
【7题答案】
【答案】B
【8题答案】
【答案】B
【9题答案】
第12页/共14页
学科网(北京)股份有限公司【答案】A
【10题答案】
【答案】D
【11题答案】
【答案】D
【12题答案】
【答案】C
【13题答案】
【答案】C
【14题答案】
【答案】B
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1) ①. 玻璃搅拌器 ②. 加快反应速率以减小误差 ③. 最高温度
(2) ①. 尽可能减少热量散失,以减小误差 ②. 更大 ③. 相同
(3) ①. ②. 实验装置保温、隔热效果差,热量损失大或未用水把温度计上的酸冲洗干
净
(4)
【16题答案】
【答案】(1)
(2) ①. 的催化作用 ②. 1、3
(3) ①. 0.3 ②. C ③.
(4)40a
【17题答案】
【答案】(1) ①. 中间产物 ②. ③.
(2) ①. ②. AB
(3) ①. 0.05 ②. 4 ③. =
第13页/共14页
学科网(北京)股份有限公司【18题答案】
【答案】(1) ①. ②. 高温
( 2 ) ① . 甲 ② . 0.00468 ③. 0.00234 ④. ⑤.
⑥. 减小
第14页/共14页
学科网(北京)股份有限公司