文档内容
化学参考答案及评分细则
一、命题指导思想
参考了 年河北省普通高中学业水平选择性考试化学试题的命制 特别关注
2021~2024 ,
了全国卷知识点和山东卷题型的变化 秉持了高考的核心功能 突出素养立意 较好地考查了
, , ,
学生的 必备知识 关键能力 学科素养及核心价值 重点选择了日常生活情境 生产环保情
“ 、 、 ”。 、
境 学术探索情境 为实现对高分段学生的有效区分奠定了基础 提升化学学科核心素养 本
、 , , 。
卷与 河北卷试卷结构基本保持一致 考向相仿 为学生适应 高考做好准备
2024 , , 2025 。
二、试题创作
引导学生关注社会热点问题
1.
提高学生的学习兴趣 感受化学知识的应用价值 如 第 题以 年政府工作报告为
, 。 : 3 2024
载体 让学生感受化学与社会热点的关联 培养科学态度与社会责任的化学学科核心素养
, , 。
体现学科应用
2.
第 题体现了化学知识在制药领域的应用 第 题体现了化学知识在工业生产
5、18 , 14、15
中的应用 让学生体验学习化学的重要性
, 。
突出知识融合
3.
第 题以含钴废渣中回收纯钴的工艺流程为载体 具体考查原料预处理 流程分析 试
16 , 、 、
剂选择 结合选择性必修 考查化学键 陌生方程式书写 与溶度积有关的计算 与高考题型
, 2 、 、 ,
保持一致
。
图像创新 提升化学学科核心素养
4. ,
第 题以工业废水中处理苯甲酸的不同 对树脂吸附苯甲酸的影响图像分析为载
13 pH
体 考查化学观念和运用科学思维分析问题的能力
, 。
注重基础 落实学业要求
5. ,
本卷难度系数约为 以基础题和中档题为主 特设置第 题 第 题回归教材 体
0.65, 。 2 、 11 ,
现阶段考试的特点 通过复习逐步拔高 达到复习目标 使学生最终取得理想的高考成绩
, , , 。
题号
1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
B A A B C A D C C B D C D C
解析:蒸馏在实验室用不到烧杯 应选 项
1.B , B 。
解析:酸性 溶液可腐蚀橡胶 项错误 钠在空气中会变质 其密度比煤油大 可保存在
2.A KMnO4 ,A ; , ,
煤油中 项正确 见光易分解 溶液应保存在棕色瓶中 并置于阴暗处 项正确 氢
,B ;AgNO3 ,AgNO3 , ,C ;
氟酸会腐蚀玻璃 可用塑料容器保存 项正确
, ,D 。
化学·调研卷 答案 第 页(共 页)
| Ⅱ 1 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}解析:工厂危废污泥中含有有害物质 应处理后再排放 不能制成有机肥 否则会对环境和人类生
3.A , , ,
存造成危害 项正确 将重质油裂解为轻质油并不能减少二氧化碳的排放量 达不到 碳中和 的目
,A ; , “ ”
标 项错误 有毒 不符合绿色化学减少或消除有害物质的理念 项错误 在汽油中加入含铅
,B ;HCN , ,C ;
化合物会造成重金属污染 含铅汽油已被禁用 项错误
, ,D 。
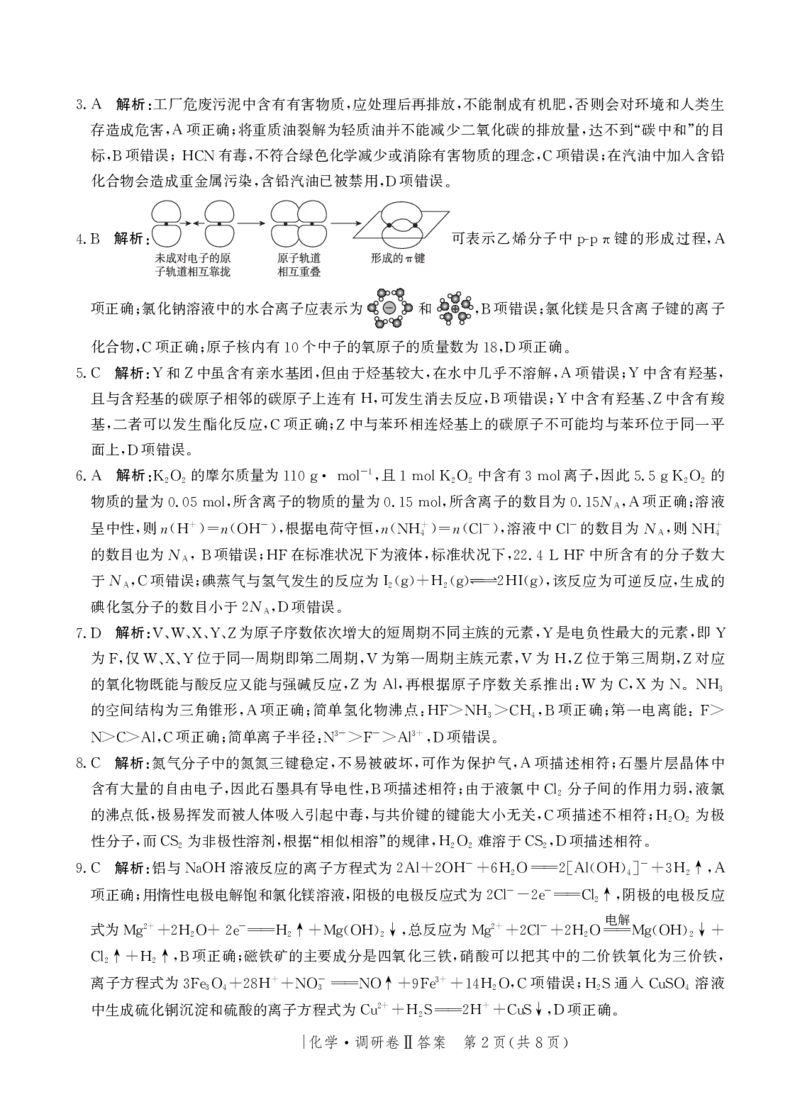
解析: 可表示乙烯分子中 键的形成过程
4.B p-pπ ,A
项正确 氯化钠溶液中的水合离子应表示为 和 项错误 氯化镁是只含离子键的离子
; ,B ;
化合物 项正确 原子核内有 个中子的氧原子的质量数为 项正确
,C ; 10 18,D 。
解析: 和 中虽含有亲水基团 但由于烃基较大 在水中几乎不溶解 项错误 中含有羟基
5.C Y Z , , ,A ;Y ,
且与含羟基的碳原子相邻的碳原子上连有 可发生消去反应 项错误 中含有羟基 中含有羧
H, ,B ;Y 、Z
基 二者可以发生酯化反应 项正确 中与苯环相连烃基上的碳原子不可能均与苯环位于同一平
, ,C ;Z
面上 项错误
,D 。
解析: 的摩尔质量为 且 中含有 离子 因此 的
-1
6.A K2O2 110g· mol , 1molK2O2 3mol , 5.5gK2O2
物质的量为 所含离子的物质的量为 所含离子的数目为 N 项正确 溶液
0.05mol, 0.15mol, 0.15 A,A ;
呈中性 则n + n - 根据电荷守恒n + n - 溶液中 - 的数目为N 则 +
, (H )= (OH ), ,(NH4)= (Cl), Cl A, NH4
的数目也为N 项错误 在标准状况下为液体 标准状况下 中所含有的分子数大
A,B ;HF , ,22.4LHF
于N 项错误 碘蒸气与氢气发生的反应为 该反应为可逆反应 生成的
A,C ; I2(g)+H2(g)2HI(g), ,
碘化氢分子的数目小于 N 项错误
2 A,D 。
解析: 为原子序数依次增大的短周期不同主族的元素 是电负性最大的元素 即
7.D V、W、X、Y、Z ,Y , Y
为 仅 位于同一周期即第二周期 为第一周期主族元素 为 位于第三周期 对应
F, W、X、Y ,V ,V H,Z ,Z
的氧化物既能与酸反应又能与强碱反应 为 再根据原子序数关系推出 为 为
,Z Al, :W C,X N。NH3
的空间结构为三角锥形 项正确 简单氢化物沸点 项正确 第一电离能
,A ; :HF>NH3>CH4,B ; :F>
项正确 简单离子半径 项错误
3- - 3+
N>C>Al,C ; :N >F >Al ,D 。
解析:氮气分子中的氮氮三键稳定 不易被破坏 可作为保护气 项描述相符 石墨片层晶体中
8.C , , ,A ;
含有大量的自由电子 因此石墨具有导电性 项描述相符 由于液氯中 分子间的作用力弱 液氯
, ,B ; Cl2 ,
的沸点低 极易挥发而被人体吸入引起中毒 与共价键的键能大小无关 项描述不相符 为极
, , ,C ;H2O2
性分子 而 为非极性溶剂 根据 相似相溶 的规律 难溶于 项描述相符
, CS2 , “ ” ,H2O2 CS2,D 。
解析:铝与 溶液反应的离子方程式为
- -
9.C NaOH 2Al+2OH +6H2O2[Al(OH)4]+3H2↑,A
项正确 用惰性电极电解饱和氯化镁溶液 阳极的电极反应式为 阴极的电极反应
- -
; , 2Cl-2e Cl2↑,
电解
式为 总反应为
2+ - 2+ -
Mg +2H2O+2e H2↑+Mg(OH)2↓, Mg +2Cl +2H2OMg(OH)2↓+
项正确 磁铁矿的主要成分是四氧化三铁 硝酸可以把其中的二价铁氧化为三价铁
Cl2↑+H2↑,B ; , ,
离子方程式为 项错误 通入 溶液
+ - 3+
3Fe3O4+28H +NO3 NO↑+9Fe +14H2O,C ;H2S CuSO4
中生成硫化铜沉淀和硫酸的离子方程式为 项正确
2+ +
Cu +H2S2H +CuS↓,D 。
化学·调研卷 答案 第 页(共 页)
| Ⅱ 2 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}解析:溶液变成红色的原因为 该可逆反应与 和 无关 其
3+ - 2- +
10.B Fe +3SCN Fe(SCN)3, SO4 K ,
浓度变化对该平衡无影响 不能得出 与 的反应不可逆的结论 项错误 根据实
, Fe2(SO4)3 KSCN ,A ;
验操作和现象 说明反应生成了 发生反应 证明氧化性
, I2, :2KI+Cl22KCl+I2, :Cl2>I2,Br2>I2,
项正确 向鸡蛋清溶液中加入少量浓硝酸 加热 生成黄色沉淀 说明蛋白质中的苯环发生了硝化
B ; , , ,
反应 项错误 含碘食盐中添加的是 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 说明没
,C ; KIO3, , ,
有碘单质 项错误
,D 。
解析: 不能用排空气法收集 项错误 碳和浓硝酸反应生成 和 所用试剂不合理
11.D NO ,A ; NO2 CO2, ,
且 的密度比空气大 应用向上排空气法收集 项错误 的密度比空气大 应用向上排空气
NO2 , ,B ;SO2 ,
法收集 项错误 可用浓氨水和 制备 且 的密度比空气的小 可用图中装置收集
,C ;NH3 CaO , NH3 , ,D
项正确
。
煅烧
解析:黄铁矿高温煅烧生成 反应原理为 当
12.C Fe2O3, 4FeS2+11O22Fe2O3+8SO2, 4molFeS2
参加反应时 转移 电子 被氧化时转移 电子 项正确 根据流程
, 44mol ,12gFeS2(0.1mol) 1.1mol ,A ;
图可知 反应 工序的化学方程式为 项正确 快速
,“ ” 2Na2S+4SO2+Na2CO33Na2S2O3+CO2,B ;
冷却得到的晶体颗粒较小 项错误 因 不溶于乙醇 故在冷却结晶后的固液混合
,C ; Na2S2O3·5H2O ,
物中加入乙醇 可析出更多的 晶体 项正确
, Na2S2O3·5H2O ,D 。
解析:苯甲酸不是强酸 电离方程式为 项错误 废水中苯甲酸的物质的量浓
+ -
13.D , HAH +A ,A ;
度约为 918
mol·L
-1
≈7.5×10
-3
mol·L
-1
,B
项错误
;
由题图可知
,
在
pH=1
和
pH=3
时
122×1000
两者的去除率几乎一致 处理倍数 倍时几乎都能去除全部苯甲酸 废水的 上升到 之后 处
, 50 , pH 5 ,
理倍数减小到 倍 而 上升到 处理能力急剧下降 低 有利于树脂吸附苯甲酸 在进行树脂
30 , pH 7 , pH ,
c c + -5
吸附前 不需要调节 项错误 当 为 时 废水中 (HA) (H ) 10
, pH,C ; pH 5 , c - = K = -5=0.16,D
(A ) a 6.25×10
项正确
。
解析:由晶胞结构可知 该晶胞中含有 个 个 个 化学式为 项正确 与
14.C , 1 Ca,1 Ti,3 O, CaTiO3,A ;
最近且距离相等的 的数目为 项正确 位于立方晶胞的体心 图 是沿晶胞任一体对角
Ca O 12,B ;Ti , 2
线的投影图 项错误 该晶体的密度为1.36×10
23
-3
项正确
,C ; a3N g·cm ,D 。
A
答案: 分 平衡压强 便于漏斗内液体顺利滴下 分
15. (15 )(1) , (2 )
球形冷凝管 分 冷凝回流 防止 损耗 分
(2) (1 ) , VOSO4 (2 )
△ 分
(3)V2O5+H2SO4(VO2)2SO4+H2O(2 )
分
(4)H2C2O4+(VO2)2SO4+H2SO42VOSO4+2CO2↑+2H2O(2 )
漏斗 烧杯 玻璃棒 分
(5) 、 、 (2 )
bc
分 81.5 分
(6)H2C2O4(2 ) a %(2 )
解析:()仪器 是恒压滴液漏斗,其中的导管可以平衡压强,便于漏斗内液体顺利滴下。
1 a
()仪器 的名称是球形冷凝 ,其作用是冷凝回流,防止 损耗。
2 b VOSO4
学·调研卷 答案 第 页(共 页)
Ⅱ 3 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}() 微溶于水,具有微弱碱性,能溶于强酸,反应的化学方程式为 △
3 V2O5 V2O5+H2SO4
( ) 。
VO2 2SO4+H2O
() 具有氧化性,在酸性条件下能被 还原为 ,该反应的反应物为 、
+ 2+
4VO2 H2C2O4 VO H2C2O4
( ) 、 ,产物为 、 、 ,化学方程式为 ( )
VO2 2SO4 H2SO4 VOSO4 CO2 H2O H2C2O4+ VO2 2SO4+H2SO4
。
2VOSO4+2CO2↑+2H2O
()“过滤”操作中用到的漏斗、烧杯和玻璃棒的材质为硅酸盐。
5
()据题意,用草酸还原( ) 所得 产品中含有草酸杂质,向产品中滴加酸性
6 VO2 2SO4 VOSO4 KMnO4
溶液可将草酸氧化为 除去。由题可得关系式: ,产品纯度为
2+ + 2+
CO2 Fe ~VO2 ~VO
b
mol
·
L
-1
×10
-3c
L×
100 mL
×163 g
·
mol
-1
bc
a
20mL
×100%=
81
a
.5
%
。
g
答案: 分 适当提高 酸浸 温度或适当提高稀硫酸浓度或粉碎含钴废渣 分 合理即可
16. (14 )(1) “ ” (1 , )
分
2+ + 3+
(2)H2O2+2Fe +2H 2H2O+2Fe (2 )
分 未开始 分
3+
完全沉淀时 此时理论上c
2+
最大为
5.4 -1
(3)AD(2 ) (1 ) Fe ,pH=3.0, (Zn ) 10 mol·L ,
远大于 分
5.4 -1 -1
10 mol·L 2.5mol·L (2 )
除去溶液中的 分
2+
(4) Zn (2 )
分 分
(5)2CoCO3+2H2+8COCo2(CO)8+2CO2+2H2O(2 ) B(2 )
解析:()适当提高“酸浸”温度,适当提高稀硫酸浓度,粉碎含钴废渣都可以提高酸浸速率。
1
()“酸浸”工序后溶液中的阳离子有 、 、 、 、 ,“氧化”的目的是使 转化为
3+ 2+ 2+ 2+ + 2+
2 Fe Zn Co Fe H Fe
,离子方程式为 。
3+ 2+ + 3+
Fe H2O2+2Fe +2H 2H2O+2Fe
()“试剂 ”可选用 ,消耗 ,且不引入杂质;“调 ”工序使铁元素恰好全部进入滤渣 时,
+
3 X AD H pH 2
,c(
-
)
-11 -1
,
2+
以 ( ) 完全沉淀时, ,c(
-
)
pH=3.0 OH =10 mol∙L Zn Zn OH 2 pH=8.2 OH
-5.8 -1
,K [ ( )]
-5 -5.8×2 -16.6
,理论上c(
2+
)最大为c(
2+
)
=10 mol∙L spZnOH 2 =10 ×10 =10 Zn Zn =
K s c p [ 2 Z ( n ( O - H ) ) 2 ] = 10 - - 1 1 1 6 × .6 2 mol ∙L -1 =10 5.4 mol ∙L -1 , 10 5.4 mol ∙L -1 远大于 2.5 mol ∙L -1 , Zn 2+
OH 10
未开始沉淀。
()根据前述分析可知,“萃取、分液”工序的目的是除去溶液中的 。
2+
4 Zn
()“气体 ”是 ,“合成”工序的化学方程式为 ( )
5 Y CO2 2CoCO3+2H2+8COCo2 CO8+2CO2+
; ( )的熔点为 ,可溶于多种有机溶剂,可知其为分子晶体,结合结构简式知其中
2H2OCo2 CO8 52℃
不含离子键,故选 。
B
答案: 分 分 分
-1
17. (15 )(1)-41kJ∙mol (1 ) 123(1 )
增大水蒸气的浓度 移出 分 合理即可
(2)① , CO2(2 , )
分
②ABC(2 )
增大 分 反应 和 的正反应都是吸热反应 温度升高平衡向正向移动 的平衡转化
(3) (2 ) Ⅰ Ⅱ , ,CH4
率随温度升高而增大 分
(2 )
化学·调研卷 答案 第 页(共 页)
Ⅱ 4 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}n m n
m n -1 -1 分 分 (3 +4 ) 分
(4)0.1( + )mol∙L ∙min (2 ) =(1 ) m . m n (2 )
(15- -2 )
解析:()H 反应物的总键能 生成物总键能
-1 -1
1Δ = - =1075kJ∙mol +2×463kJ∙mol -2×
-1 -1 -1 ;E逆 E正 H -1 ( -1 )
803kJ∙mol -436kJ∙mol =-41kJ∙mol a = a -Δ =82kJ∙mol - -41kJ∙mol =
。
-1
123kJ∙mol
() 恒温条件下,增大水蒸气的浓度,移出 都可使 的转化率和 的产率同时提高。
2① CO2 CO H2
的物质的量分数不再改变,说明反应已达到平衡状态, 项正确;对于绝热体系,体系温度不再
②H2 A
改变,说明反应已达到平衡状态, 项正确;因初始 ()和 ()的物质的量之比与反应过程消
B COg H2Og
耗二者的物质的量之比不同,故 ()和 ()的物质的量之比不变,可说明反应达到了平衡状
COg H2Og
态, 项正确;由于容器的容积不变,体系内物质全是气体,故混合气体的密度始终不改变,不能说明
C
反应达到平衡状态, 项错误。
D
()反应 和 的正反应都是吸热反应,且气体分子数增大,温度升高平衡向正向移动, 的平衡
3 Ⅰ Ⅱ CH4
转化率随温度升高而增大,压强增大平衡向逆向移动, ()的平衡转化率减小,故p、p、p 依
CH4 g 1 2 3
次增大。
c( )
()由反应 和 可知, 的化学反应速率为v( ) Δ CH4 (m n) -1 -1 ;反
4 Ⅰ Ⅱ CH4 CH4 = t =0.1 + mol∙L ∙min
Δ
应 为反应前后气体分子数不变的反应,压强平衡常数K 与浓度平衡常数K 数值大小关系为
Ⅲ p c
K K,设达到平衡时 在反应 中的变化浓度为a · -1 , 在反应 中的变化浓度为
p= c CH4 Ⅰ mol L CH4 Ⅱ
b · -1 , 在反应 中的变化浓度为c · -1 ,列出三个反应的变化浓度:
mol L CO Ⅲ mol L
() () () ()
CH4g+H2OgCOg+3H2g
变化浓度/( · -1 ) a a a a
mol L 3
() () () ()
CH4g+2H2OgCO2g+4H2g
变化浓度/( · -1 ) b b b b
mol L 2 4
() () () ()
COg+H2OgCO2g+H2g
变化浓度/( · -1 ) c c c c
mol L
由题意可知:c( )a · -1 c · -1 m · -1 ,c( )b · -1 c · -1
CO = mol L - mol L = mol L CO2 = mol L + mol L =
n · -1 ,c( ) a · -1 b · -1 c · -1 (m n) · -1 ,c( )
mol L H2 =3mol L +4 mol L + mol L = 3 +4 mol L H2O =
· -1 a · -1 b · -1 c · -1 ( m n) · -1 ,故K K
1.5mol L - mol L -2 mol L - mol L =1.5- -2 mol L p= c=
c( )·c( ) n(m n)
CO2 H2 3 +4 。
c( )·c( )=m(. m n)
CO H2O 15- -2
答案: 分 分
18. (14 )(1)C11H11O4Br(2 )
取代反应 分
(2) (1 )
催化剂
分
(3)2 +O2 →2 +2H2O(2 )
△
酯基 分
(4) (1 )
化学·调研卷 答案 第 页(共 页)
| Ⅱ 5 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}分
(5) (2 )
分 分
(6)5(2 ) (2 )
分
(7) (2 )
解析:() 的分子式为 。
1A C11H11O4Br
() 是卤代烃发生取代反应生成醇,醇再被氧化成醛,反应 的反应类型是取代反应。
2A→B→C A→B
催化剂
()醇的催化氧化反应为 。
3 2 +O2 →2 +2H2O
△
() 中含有的含氧官能团为酯基。
4E
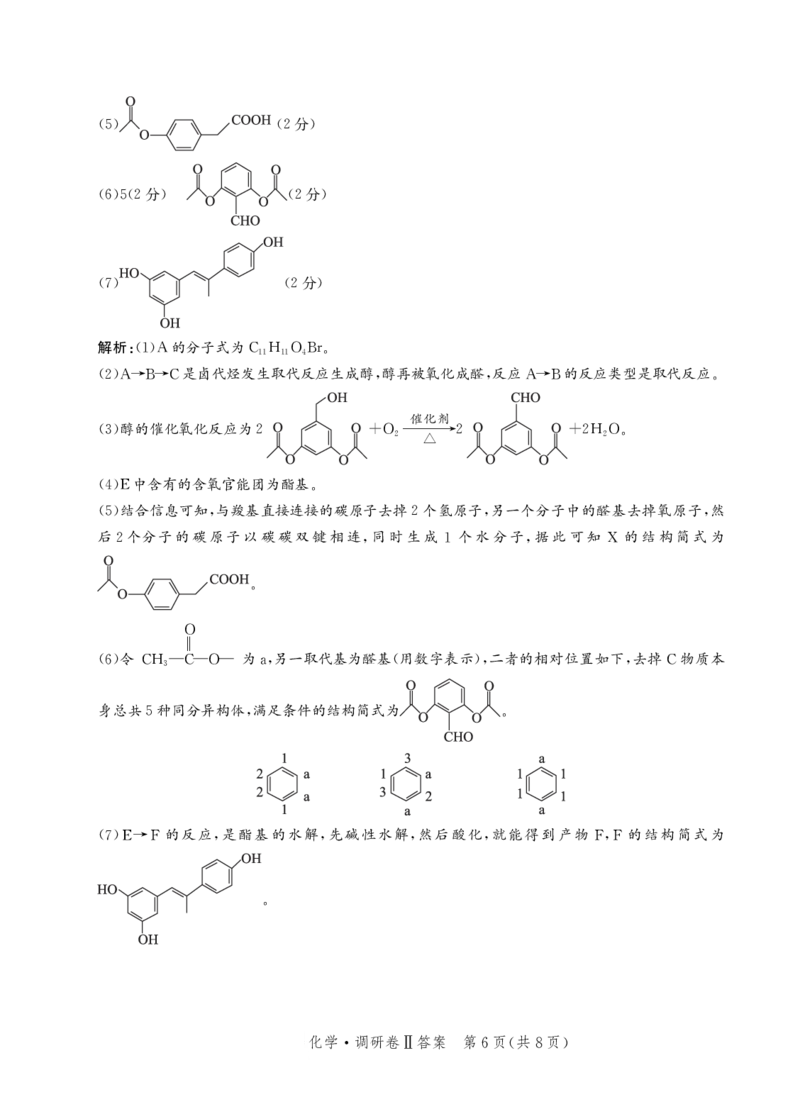
()结合信息可知,与羧基直接连接的碳原子去掉 个氢原子,另一个分子中的醛基去掉氧原子,然
5 2
后 个分子的碳原子以碳碳双键相连,同时生成 个水分子,据此可知 的结构简式为
2 1 X
。
O
()令
6 CH3 C
化学·调研卷 答案 第 页(共 页)
Ⅱ 6 8
为 ,另一取代基为醛基(用数字表示),二者的相对位置如下,去掉 物质本
O a C
身总共 种同分异构体,满足条件的结构简式为 。
5
() 的反应,是酯基的水解,先碱性水解,然后酸化,就能得到产物 , 的结构简式为
7E→F FF
。
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}编写细目表
能力要求
(1) :
接受 吸收 整合化学信息的能力 分析和解决化学问题的能力 化学实验与探究能力
Ⅰ. 、 、 Ⅱ. Ⅲ.
核心素养
(2) :
宏观辨识与微观探析 变化观念与平衡思想 证据推理与模型认知 实验探究与创新意识 科学
① ;② ;③ ;④ ;⑤
态度与社会责任
知识点 能力要求 核心素养 预估
题号 题型 分值
主题内容 难度
( )
Ⅰ Ⅱ Ⅲ ① ② ③ ④ ⑤
以古文献为载体考查化学基本操作
选择题 易
1 3 蒸馏 中的仪器选择 √ √ √
( )
考查化学试剂保存 涉及酸性
选择题 , KMnO4 易
2 3 溶液 溶液 氢氟酸 √ √
、Na、AgNO3 、
以社会热点为载体考查化学与环境
:
选择题 涉及危废污泥处理 石油裂解 绿色化 易
3 3 、 、 √ √
学 重金属污染
、
考查化学用语 涉及 键 水合离
: p-pπ 、
选择题 子 电子式表示的离子化合物的形成 中
4 3 、 √ √ √
过程等
考查三种有机化合物的转化 有机物
选择题 : 中
5 3 性质 反应类型 原子共平面等 √ √
、 、
考查N 固体混合物中粒子数目 盐
A: 、
选择题 类水解 气体摩尔体积的使用条件 可 易
6 3 、 、 √ √ √ √
逆反应
以陌生物质为载体考查元素推断 涉
,
选择题 及粒子的空间结构 第一电离能 简单 中
7 3 、 、 √ √ √
氢化物沸点 离子半径比较
、
以两栏表格的形式考查物质的性质与
选择题 结构的关系 涉及氮气 石墨 液氯 易
8 3 : 、 、 、 √ √ √
H2O2
考查离子方程式正误判断 具体考查
,
铝溶于 溶液 电解饱和
选择题 NaOH 、 MgCl2 中
9 3 溶液 磁铁矿溶于稀硝酸 通入 √ √
、 、H2S
溶液
CuSO4
以两栏表格的形式考查 实验操作及
“
现象 得出 结论 是否正确的分析 具
选择题 ” “ ” , 中
10 3 体考查可逆反应 氧化性比较 蛋白质 √ √ √
、 、
的显色反应 碘元素检验
、
给出装置图考查气体的制备和收集
选择题 , 中
11 3 具体考查 √ √ √
NO、NO2、SO2、NH3
化学·调研卷 答案 第 页(共 页)
| Ⅱ 7 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}续表
知识点 能力要求 核心素养 预估
题号 题型 分值
主题内容 难度
( )
Ⅰ Ⅱ Ⅲ ① ② ③ ④ ⑤
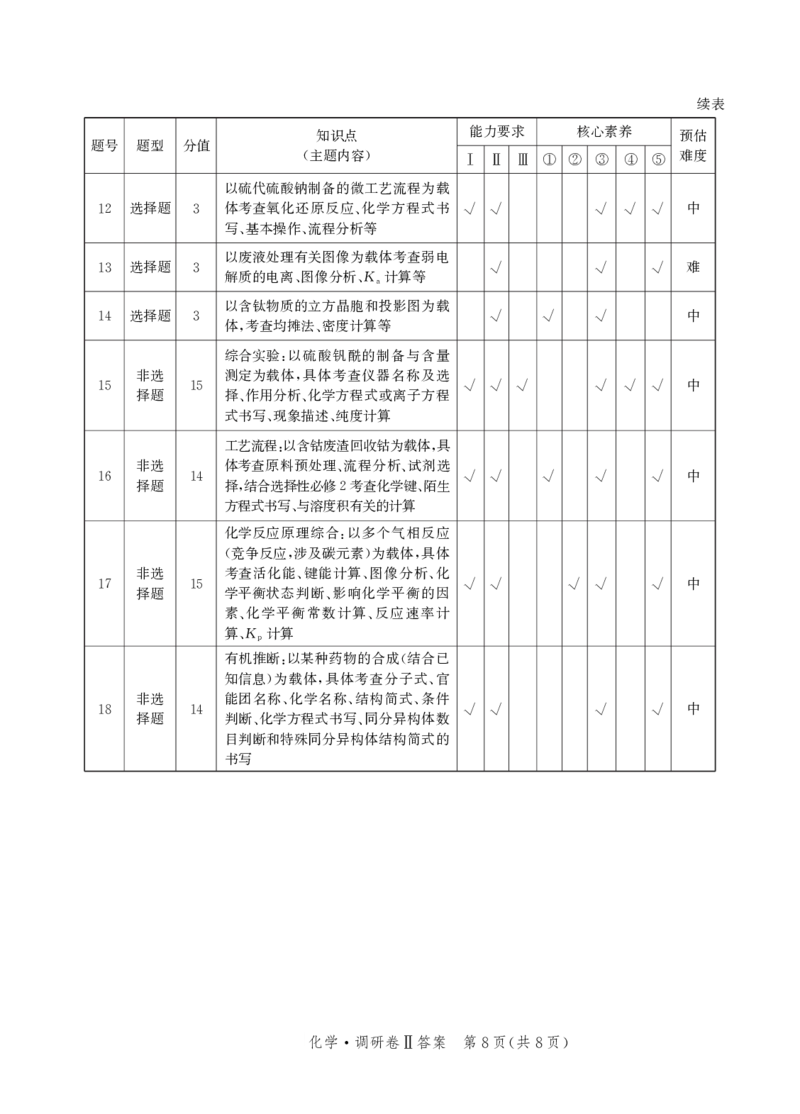
以硫代硫酸钠制备的微工艺流程为载
选择题 体考查氧化还原反应 化学方程式书 中
12 3 、 √ √ √ √ √
写 基本操作 流程分析等
、 、
以废液处理有关图像为载体考查弱电
选择题 难
13 3 解质的电离 图像分析K 计算等 √ √ √
、 、a
以含钛物质的立方晶胞和投影图为载
选择题 中
14 3 体 考查均摊法 密度计算等 √ √ √
, 、
综合实验 以硫酸钒酰的制备与含量
:
非选 测定为载体 具体考查仪器名称及选
, 中
15 择题 15 择 作用分析 化学方程式或离子方程 √ √ √ √ √ √
、 、
式书写 现象描述 纯度计算
、 、
工艺流程 以含钴废渣回收钴为载体 具
: ,
非选 体考查原料预处理 流程分析 试剂选
、 、 中
16 择题 14 择 结合选择性必修 考查化学键 陌生 √ √ √ √ √
, 2 、
方程式书写 与溶度积有关的计算
、
化学反应原理综合 以多个气相反应
:
竞争反应 涉及碳元素 为载体 具体
( , ) ,
非选 考查活化能 键能计算 图像分析 化
、 、 、 中
17 择题 15 学平衡状态判断 影响化学平衡的因 √ √ √ √ √
、
素 化学平衡常数计算 反应速率计
、 、
算K 计算
、p
有机推断 以某种药物的合成 结合已
: (
知信息 为载体 具体考查分子式 官
) , 、
非选 能团名称 化学名称 结构简式 条件
、 、 、 中
18 择题 14 判断 化学方程式书写 同分异构体数 √ √ √ √
、 、
目判断和特殊同分异构体结构简式的
书写
化学·调研卷 答案 第 页(共 页)
Ⅱ 8 8
{#{QQABJQCQggAAAgBAABhCAwUgCgMQkhACAQgOhAAEMAABSBNABAA=}#}