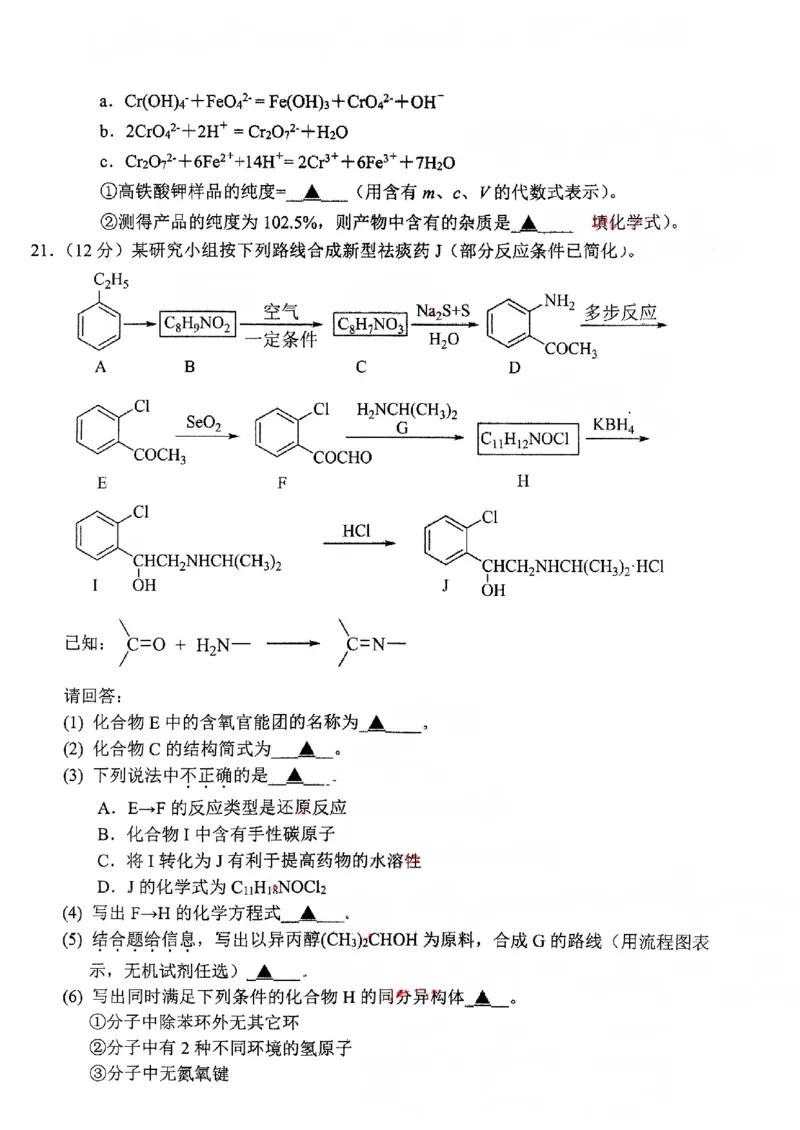
文档内容
一、选择题(本大题共16小题,每小题3分,共48分,每小题列出的四个备选项中只有一
个是符合题目要求的,不选、多选、错选均不得分)
1.浙江省博物馆收藏有一批蕴含区域文化特色的文物。下列文物主要成分是有机物的是
A.良渚遗址玉琮 B. 宁波朱金木雕
C.吴越鎏金纯银阿育王塔 D. 龙泉窑青瓷舟形砚滴
2.下列化学用语表示正确的是
A.乙烯中p-pπ键的电子云轮廓图: B. SOCl?的 VSEPR模型:
C. H?C=c-CH?-CH?加氢产物的名称:2-乙基丁烷 D. HCIl的电子式:H+[:C:」
3.下列关于物质的性质和用途说法不正确的是
A. SO?有还原性,食品中添加适量二氧化硫能起到抗氧化作用
B. SiC硬度大,可作砂纸磨料
C. BaSO?难溶于酸且不易被X射线透过,可做“钡餐”
D.纯铝的硬度和强度大,适合制造飞机零件
4.下列有关NH?的实验,合理的是
NH?Cl
NH?-
常 P?O?
煤油
棉花 稀H,SO?-
D.吸收氨气且
A.制取较多氨气 B.干燥氨气 C.收集氨气
防倒吸5.化学技术和化学物质可造福人类生活。下列说法不正确的是
A.利用液氮、液氢做火箭推进剂,可有效减少对环境的污染
B.硫酸亚铁可用作处理污水的混凝剂
C.丙三醇有吸水性,可用于配制化妆品
D.氯化镁、硫酸钙等可用作生产豆腐的凝固剂
6.六氟合铂酸氙(XePtF?,其中Pt为+5价)是人类发现的第一个稀有气体化合物,与水反
应方程式为;XePtF?+H?O→O?个+Xe个+PtO?-HF(未配平)。下列说法不正确的是
A.六氟合铂酸氙中Xe的化合价为+1价 B. XePtF?有强氧化性
C.每生成1mol O?,转移4mol电子 D. HF 是还原产物
7.从结构探析物质性质和用途是学习化学的有效方法。下列实例与解释不相符的是
选项 实例 解释
将95??醇加入 Cu(NH?)?SO?溶液中析出深 乙醇极性较小,降低了
A
蓝色晶体 Cu(NH?)?SO4的溶解性
铁原子核外电子在灼烧时
B
铁丝在酒精喷灯上灼烧,焰色无明显变化
没有发生跃迁
分子间氢键作用实现了超
C
DNA中碱基 A与T、G与C的互补配对
分子的分子识别
引入乙基减弱了离子间的
D
熔点:C?H?NH?NO?ZX? B.原子半径:M>Z>Y>X
C.最高价氧化物对应水化物的酸性:Z>M
D. 键角:Z?X?中的∠XZX>Y?X?中的∠XYX
化学试题卷 第 2 页 共8页11.1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,某种生产D方法的机理如下图所示。
CI
D
X M
G
以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对
应反应物的浓度。某温度下,恒容反应器中加入一定量的X,保持体系中氯气浓度恒
定,测定不同时刻相关物质的浓度,发现60min前,产物T可忽略不计。已知该温度
下,k:k?:k?:k4:ks=100:21:7:4:23。
下列说法不正确的是
A. 60min前,v?:v3=3:1 B.路径①→②→④中,④是决速步骤
C. 60min后,c(D)/c(G)逐渐减小
D.选择合适催化剂,控制反应时间,可提高D的产率
12.下列反应可以得到多卤化物:KI+I?=KI?、CsBr+IBr=CsIBr?。下列说法不正确的是
A. CsIBr?中阴阳离子个数比是1:1
B.苯与IBr在催化剂作用下发生取代反应可生成碘苯
C. CsIBr?受热分解生成的产物含有CsI
D. IBr能使湿润的淀粉-KI试纸变蓝色
13.利用丙烯腈(CH?=CHCN)制备己二腈[NC(CH?)?CN]的电有机合成装置如图所示。下列
说法不正确的是 电源
交换膜
A. 电极 a为阴极 能
B.四甲基溴化铵[(CH?)?NBr]可增加溶液导电性 化 位言收言
CH?=CHCN
期核心
C.交换膜为质子交换膜
SNC(CH??CN 2molL H?SO?
D. 电解过程中,右侧溶液的pH不变
(CHp?NBr水溶液
14.有机物1生o成酰胺的反应历程如图所示。
R-zR R njo
R
C
王
OH OH?
1 Ⅱ IV VVI
ll
已知:R、R'代表烷基。下列说法不正确的是
A. H+能加快反应速率 B.从图中历程可知,物质VI比V稳定
C.步骤Ⅱ→Ⅲ的历程中,C-R'键比C-R 键更容易断裂
o
D.mo(人
发生上述反应生成的主要产物是
化学试题卷 第 3 页 共 8 页15.工业锅炉需定期除水垢,其中的硫酸钙用纯碱溶液处理时,发生反应:
CaSO?(s)+CO23(aq)=— CaCO?(s)+SO24(aq)
将1.00g 硫酸钙(M=136g mol-1)加入100mL 0.100mol-L-1 Na?CO?溶液中,在25℃
和充分搅拌条件下,利用pH计测得体系pH 随时间t变化如图。
告
已知:Kai(H?CO?)=4.5×10-7,Ka2(H?CO?)=4.7×10-11,Ksp(CaCO?)
=3.5×10-9, Ksp(CaSO4)=4.9×10-?(不考虑 SO2-水解)。下列说
法不正确的是
A. t=0时,以上溶液中存在:c(CO3)>c(HCO?) 0 t? t/min
B.保持溶液中c(SO2-):c(CO3-)<1.4×104,可使水垢中的CaSO?
转化为CaCO?
C. t?时刻体系中CaSO?(s)+CO23(aq)=— CaCO?(s)+SO24(aq)已达平衡状态
D. t?时刻后向体系中加入少量 Na?SO4固体,溶液的pH 不变
16.为探究化学反应速率和化学平衡移动的影响因素,设计方案进行实验,观察到相关现
象。方案设计或结论不正确的是
影响
选项 方案设计 现象 结论
因素
向2 mL 0.1 mol/LNaCl溶液中 减小反应物浓度,平衡
先产生白色
加入2滴0.1 mol/LAgNO?溶 Ag*(aq)+Cl (aq)——
A 浓度 混浊,后出现
液,充分振荡后再滴加2滴 AgCl(s)向逆反应方向
黑色混浊
0.1 mol/LNa?S溶液 移动
增大压强,平衡
用注射器吸收20 mL Cl?和
氯水颜色 Cl?(aq)+H?O(1)
B 压强 20mL饱和氯水,封闭管口,
变深 →HCl(aq)+HClO(aq)
压缩注射器活塞
向逆反应方向移动
Fe Cu Fe Cu
左池Fe电极
附近的溶液
电化 负极 Fe的腐蚀速率快于
C
出现蓝色沉
学 阴极Fe的腐蚀速率
等浓度的食盐水 淀,右池溶液
一段时间后,同时取 Fe 电极 无明显现象
附近溶液,滴加铁氰化钾溶液
5?O?溶液 5?O?溶液
50℃水浴中
升高温度可以加快反应
D
温度 试管内产生
速率
气泡更快
冰水混合物 50℃水浴非选择题部分
二、非选择题(本大题共5小题,共52分)
17.(10分)N、O、F的化合物种类繁多,应用广泛,请回答:
(1)某化合物的晶胞如图所示。该化合物的化
Na
学式为 ▲ 已知图中虚线连接的 O
。
原子与Cu原子距离最近且相等,晶体中
0
距每个Cu原子最近的O原子有__▲ 个。
Cu
(2)下列说法不正确的是▲
A.基态铜原子的价电子排布式为3d?4s2
B. 第一电离能F>0>N
。
C.气态分子 NOCl中所有原子均满足8电子结构,则分子中存在双键
D. 离子键的百分数:MgO”、“<”、“=’)。
(5)弱电解质的电离一般是吸热,而HF(aq)—H+(aq)+F(aq)△H<0,结合F?的
结构说明原因 ▲
18.(10分)从炼铜副产物阳极泥(主要含Cu?Se、Ag?Se、Au等)中能提炼Se单质及许
多贵金属单质。
足量空气 CO?
稀硫酸
Na?CO?
溶液A Se
阳极泥
SO?
焙烧
水浸
固体 A
系列操作
固体 B Au、Ag、Cu
已知:固体 A中主要含CuO、Ag、Au、Na?SeO?等物质。请回答:
(1)固体B中单质 Au在酸性环境下与NaClO?、NaCl反应生成可溶性的Na[AuCl?],
写出该反应的离子方程式 ▲
(2)下列说法正确的是▲_。
A.加入 Na?CO?固体能促进 Ag?Se与O?反应生成 Ag
B.流程中 SO?主要体现氧化性
C.电解精炼铜的过程中,电能转化为化学能与热能
D.为简化操作,可将流程中的水浸改为稀硫酸浸取
(3)实验室中可以用NaHSO?代替流程中的 SO?。已知:NaHSO?+HCHO-X(NaOCh--0H)→Y (HOCn--0Na)
),上述转化
过程均可逆
。
①解释X最终转化为Y的原因
。
②验证Y中含有硫元素的实验操作如下:
步骤I:取少量Y于试管中,加入浓 NaOH溶液,充分加热;步骤Ⅱ:
写出步骤I的化学方程式_▲ ,将步骤Ⅱ的实验方案补充完整__▲
19.(10分)在天然气的开采净化过程中,往往会产生酸气(H?S与CO?)。将 H?S与CO?
协同转化,在减少碳排放的同时得到高附加值化学品。请回答:
(1)T℃时,H?S(g)+CO?(g)=COS(g)+H?O(g) K=6.7×10-6
①该反应逆过程△H__▲ 0(填“>”或“<”)。
②当原料 n(H?S):n(CO?)=1:4时,H?S的转化率≈ ▲ (保留一位有效数字)。
③相同条件下,H?S的转化率与反应时间的关系如图1所示。说法正确的是_率_。
A.分子筛具有催化作用,加快反应速率
B.分子筛可选择性吸附产物,促进反应正向进行
C.无分子筛时,增大 H?S和 CO?的投料比,H?S的平衡转化率升高
D.有分子筛时,温度升高,反应速率一定增太
70
H?S的转化率/100 有分子筛时 60
70
CO?转化率%50
n(H?S):n(CO?)
40 ×-30:5
30 -25:10
20 —-10:25
→-5:30
1 无分子筛时 10
0 1 2 3 4 L 5 6 0 20 40 60 80 100120
反应时间h
电场功率
第19题图 图1 第19题图 图2
(2)通过光伏-电催化可将 H?S与CO?协同转化为S、CO、CH?等产品。
FE???解过程中通过的总电子数。
已知:还原产物X的法拉第效率
当还原得到的CO和CH?的 FE?别为24? 8??,n(CO):n(CH?)= ▲_。
(3)等离子体催化 H?S与CO?协同转化可制得H?和CO等产品。在电场的激发下,部
分反应历程如下:
i. H?S→2H + S ii. CO?→CO + 0 iii.
iv.2H→H? v. HO + H→H?O
①补充步骤iii的反应历程:__▲。
。
②当保持通入气体的总物质的量和流速不变,改变电场功率和原料气的组成时,
CO?气体的转化率如图2所示。当电场功率不变时,在答卷图中画出CO?反应
速率v(CO2)随着H?S和CO?比例变化的示意图__▲
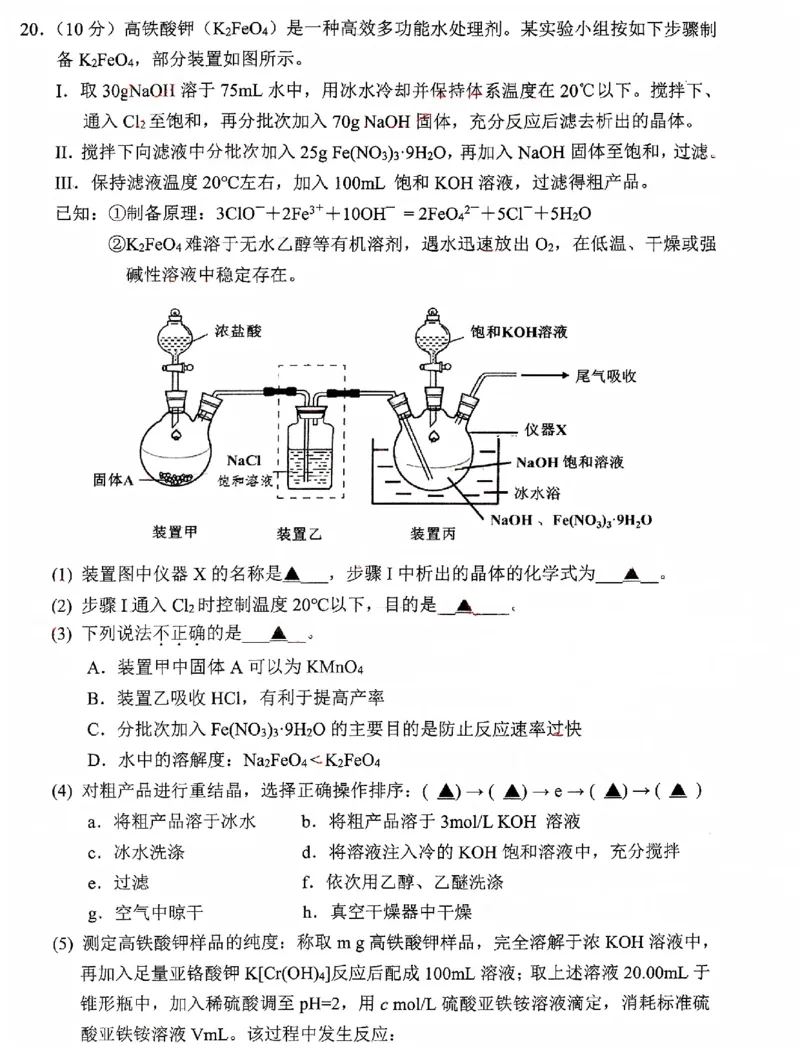
化学试题卷 第 6 页 共 8 页20.(10分)高铁酸钾(K?FeO?)是一种高效多功能水处理剂。某实验小组按如下步骤制
备K?FeO?,部分装置如图所示。
I.取30gNaOH溶于75mL 水中,用冰水冷却并保持体系温度在 20℃以下。搅拌下、
通入Cl?至饱和,再分批次加入70g NaOH 固体,充分反应后滤去析出的晶体。
II.搅拌下向滤液中分批次加入25g Fe(NO3)?·9H?O,再加入NaOH 固体至饱和,过滤。
II.保持滤液温度20℃左右,加入100mL 饱和 KOH溶液,过滤得粗产品。
已知:①制备原理:3ClO-+2Fe3++100H=2FeO?2-+5Cl~+5H?O
②K?FeO?难溶于无水乙醇等有机溶剂,遇水迅速放出 O?,在低温、干燥或强
碱性溶液中稳定存在。
浓盐酸 饱和KOH溶液
尾气吸收
仪器X
NaCl
NaOH 饱和溶液
固体A 野 饱和溶液
冰水浴
。
NaOH、Fe(NO?)?·9H?O
装置甲 装置乙 装置丙
(1)装置图中仪器X的名称是▲ 。 ,步骤I中析出的晶体的化学式为_ ▲
(2)步骤I通入 Cl?时控制温度20℃以下,目的是_▲
(3)下列说法不正确的是 ▲
A.装置甲中固体 A可以为KMnO?
B.装置乙吸收 HCl,有利于提高产率
C.分批次加入 Fe(NO?)?·9H?O的主要目的是防止反应速率过快
D.水中的溶解度:Na?FeO?