文档内容
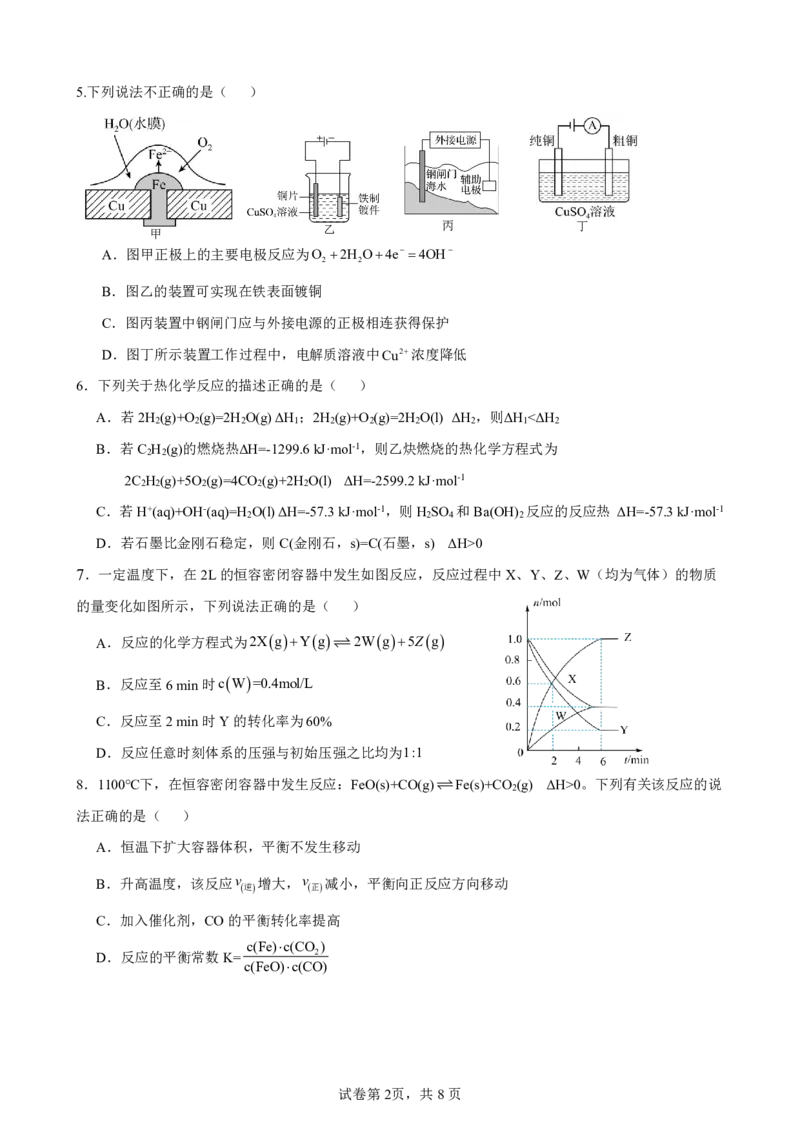
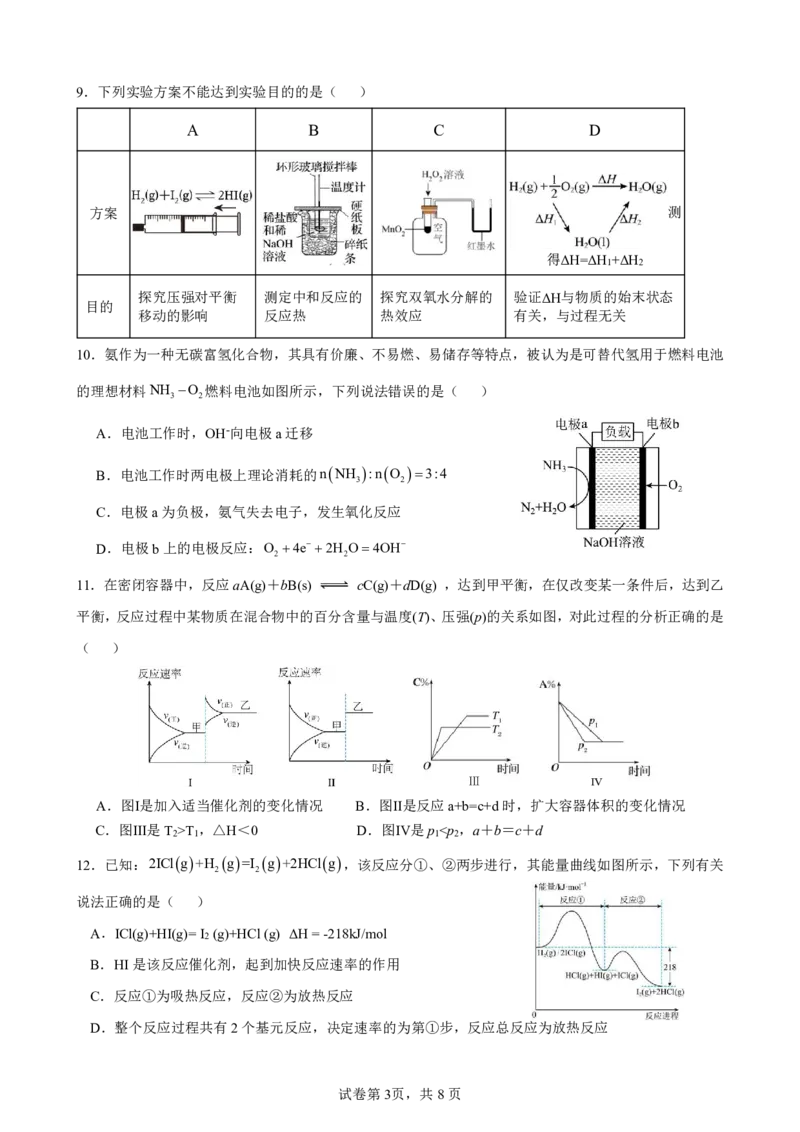
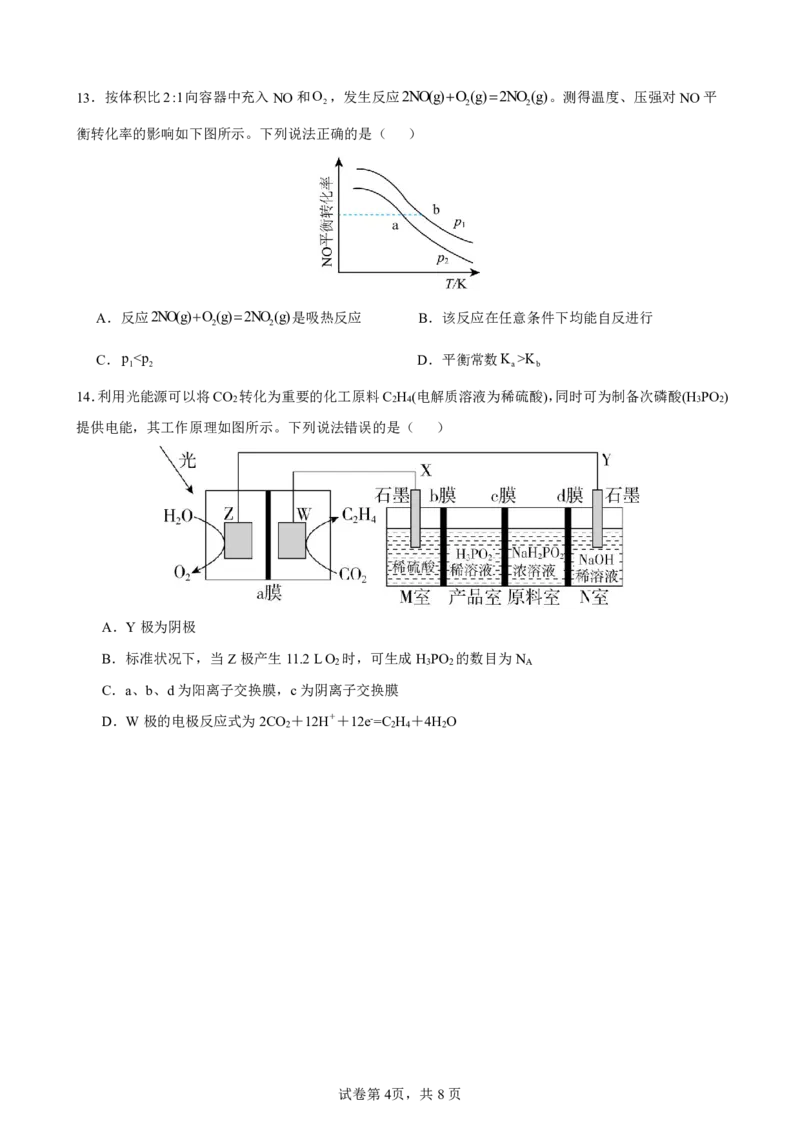
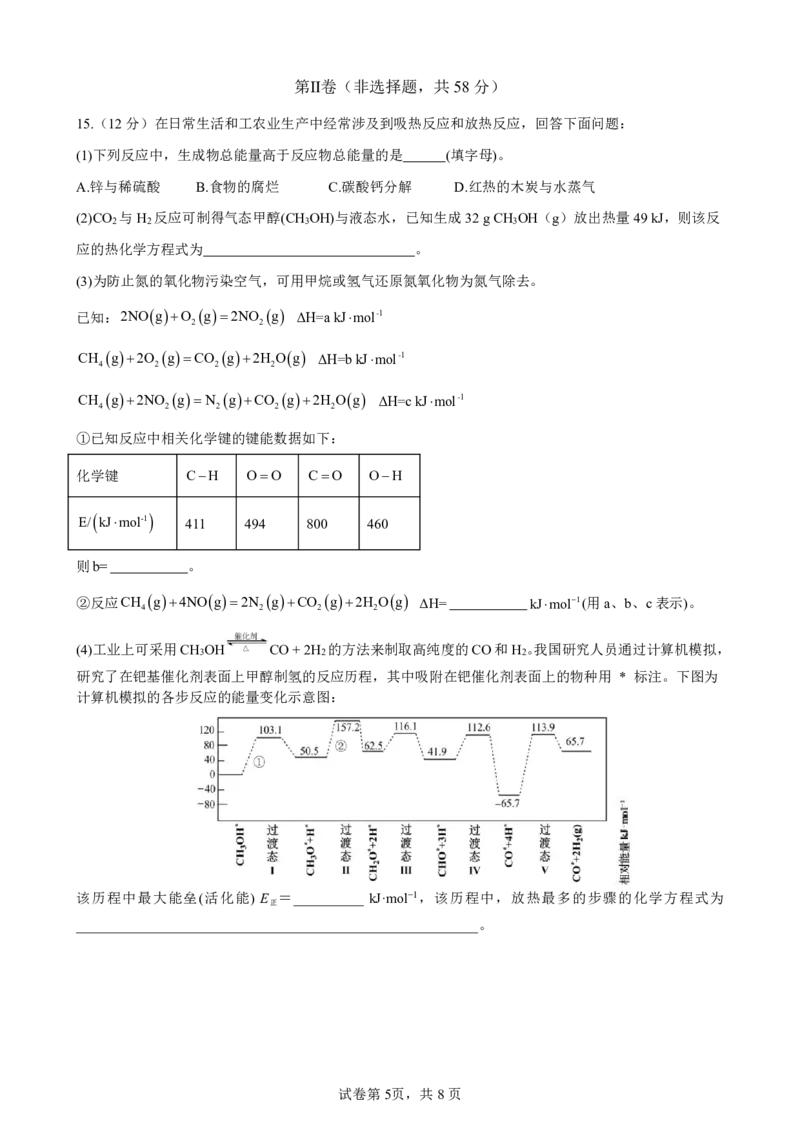
K 1 2 a b 14.利用光能源可以将CO 转化为重要的化工原料C H (电解质溶液为稀硫酸),同时可为制备次磷酸(H PO ) 2 2 4 3 2 提供电能,其工作原理如图所示。下列说法错误的是( ) A.Y极为阴极 B.标准状况下,当Z极产生11.2LO 时,可生成H PO 的数目为N 2 3 2 A C.a、b、d为阳离子交换膜,c为阴离子交换膜 D.W极的电极反应式为2CO +12H++12e-=C H +4H O 2 2 4 2 试卷第4页,共8页 {#{QQABZQ4AogioQJBAAAhCQQXQCgKYkACCCIgOAAAYIAAAQRFABCA=}#}第Ⅱ卷(非选择题,共58分) 15.(12分)在日常生活和工农业生产中经常涉及到吸热反应和放热反应,回答下面问题: (1)下列反应中,生成物总能量高于反应物总能量的是 (填字母)。 A.锌与稀硫酸 B.食物的腐烂 C.碳酸钙分解 D.红热的木炭与水蒸气 (2)CO 与H 反应可制得气态甲醇(CH OH)与液态水,已知生成32gCH OH(g)放出热量49kJ,则该反 2 2 3 3 应的热化学方程式为 。 (3)为防止氮的氧化物污染空气,可用甲烷或氢气还原氮氧化物为氮气除去。 已知:2NOgO g2NO g ΔH=akJmol-1 2 2 CH g2O gCO g2H Og ΔH=bkJmol-1 4 2 2 2 CH g2NO gN gCO g2H Og ΔH=ckJmol-1 4 2 2 2 2 ①已知反应中相关化学键的键能数据如下: 化学键 CH OO CO OH E/ kJmol-1 411 494 800 460 则b= 。 ②反应CH g4NOg2N gCO g2H Og ΔH= kJmol1(用a、b、c表示)。 4 2 2 2 (4)工业上可采用CH OH CO+2H 的方法来制取高纯度的CO和H 。我国研究人员通过计算机模拟, 3 2 2 研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为 计算机模拟的各步反应的能量变化示意图: 该历程中最大能垒(活化能) E =__________ kJ·mol−1,该历程中,放热最多的步骤的化学方程式为 正 _________________________________________________________。 试卷第5页,共8页 {#{QQABZQ4AogioQJBAAAhCQQXQCgKYkACCCIgOAAAYIAAAQRFABCA=}#}16.(12分)影响化学反应速率的因素有很多,某课外小组用实验的方法进行探究。 (1)实验一:取3mol·L-1的H O 溶液各10mL分别按下表进行实验。 2 2 实验序 V/mL(H O 溶 V/mL(FeCl 溶 MnO 质量 2 2 3 2 反应温度/℃ V(水)/mL 号 液) 液) /g 1 10 2 0 50 8 2 10 2 0 30 8 3 10 0 1 30 a ①实验1、2研究的是 对H O 分解速率的影响。 2 2 ②表中a为 ,如果实验3中30s时共收集到气体的体积为11.2mL(已折算成标准状况下),则 用过氧化氢表示的0~30s的平均反应速率为 。 (2)实验二:探究Co2+、Co3+能否催化H O 的分解,室温下进行了实验I~III。 2 2 实验I 实验II 实验III 溶液变为红色,伴有气 溶液变为墨绿色,并持续产生能使带火 无明显变化 泡产生 星木条复燃的气体 已知:CoH O 2+为粉红色、CoH O 3+为蓝色、CoCO 2-为红色、CoCO 3-为墨绿色。 2 6 2 6 3 2 3 3 回答下列问题: ①配制1.00molL-1的CoSO 溶液,需要用到下列仪器中的 (填标号)。 4 a. b. c. d. ②实验I表明CoH O 2+ (填“能”或“不能”)催化H O 的分解。实验II中发生反应的离子方 2 6 2 2 程式为 。 ③实验III初步表明CoCO 3-能催化H O 的分解。实验III中产生的气体为 。 3 3 2 2 试卷第6页,共8页 {#{QQABZQ4AogioQJBAAAhCQQXQCgKYkACCCIgOAAAYIAAAQRFABCA=}#}17.(16分)电池的发明和应用是化学家们对人类社会的重要贡献之一。每一次化学电池技术的突破,都 带来了电子设备革命性的发展。 (1)我国在甲烷燃料电池的相关技术上获得了新突破,原理如图1所示,甲烷燃料应从 (填字母)口通 入,发生的电极反应式为 。 图1 图2 (2)以石墨作电极电解饱和食盐水,如图2所示,电解开始后在 (填“阴极”或“阳极”)的周围先出现红 色,该极的电极反应式为 。 (3)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图3所示,该电池从浓缩 海水中提取LiCl的同时又获得了电能。该电池中电子的流向为 (填“a极到b极”或“b极到a极”); 当a极生成0.1molH 2 时,有 mol Li移向 (填“a”或“b”)极。 图3 图4 (4) 微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水 淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图4装置处理有机废水(以含CH COO的溶液为例)。 3 隔膜1为 (填“阴”或“阳”)离子交换膜,负极的电极反应式为 。当电路中 转移0.2mol电子时,模拟海水理论上除盐 g。 18.(18分)Ⅰ.氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。 已知:2CsO g 2COgK CsO g CO gK N gO g 2NOgK 2 1 2 2 2 2 2 3 (1)则2COg2NOg N g2CO g的平衡常数K,K (用K 、K 、K 表示)。在一 2 2 1 2 3 个恒温恒容的密闭容器中发生该反应,能表明该反应已达到平衡状态的标志有 (填字母)。 A.2v COv N B.混合气体的密度保持不变 正 逆 2 C.混合气体的平均相对分子质量保持不变 D.单位时间内生成2molN 同时消耗1molCO 2 E.气体的总质量保持不变 F.单位时间内生成1molCO同时消耗1molNO 试卷第7页,共8页 {#{QQABZQ4AogioQJBAAAhCQQXQCgKYkACCCIgOAAAYIAAAQRFABCA=}#}(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反Cs2NOg N gCO g, 2 2 NO和N 的物质的量变化如表所示。 2 条件 保持温度为T/℃ 时间 0 5min 10min 15min 20min 25min 30min NO物质的量/mol 2.0 1.8 1.4 1.1 0.90 0.80 0.80 N 物质的量/mol 0 0.10 0.30 0.45 0.55 0.60 0.60 2 平衡时NO的转化率a ,求该温度T℃下的平衡常数K ; 该温度达到平衡后,在容积不变的条件下再充入0.1molN 和0.1molNO,平衡 (填“正向”、“逆 2 向”或“不”)移动,理由是 。 (3) 若反应2CO+2NON 2 +2CO 2 ΔH<0,正、逆反应速率分别可表示为 v =k c2(CO)·c2(NO)、v =k c(N )·c(CO ),k 、k 分别表示正、逆反应速 正 正 逆 逆 2 2 正 逆 率常数,只与温度有关。下图所示的甲、乙、丙、丁四条直线中,有两条表示 lgk 和lgk 的随温度变化的直线,请选出其中表示lgk 随温度T变化关系的 正 逆 正 直线 (填“甲”或“乙”或“丙”或“丁”)。 Ⅱ.目前,常利用催化技术将汽车尾气的NO处理成无毒气体,发生的反应为C(s)+2NO(g) N (g) 2 +CO (g) ΔH=-34.0kJ·mol-1。在密闭容器中加入足量的C(s)和一定量的NO(g),保持恒压,测 2 得NO的转化率随温度的变化如图所示: (4)在1100K时,CO 的体积分数为________; 2 (5)由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为 ; 试卷第8页,共8页 {#{QQABZQ4AogioQJBAAAhCQQXQCgKYkACCCIgOAAAYIAAAQRFABCA=}#}一、选择题:(本题共 14小题,每小题 3分,共 42分) 题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 选项 D C A B C B D A A B C D D B 二、非选择题:(共 58分) 15.(12分,每空2分) (1)CD (2)CO (g)+3H (g)===CH OH(g)+H O(l) 2 2 3 2 (3)①-808 ②2a+2c-b (4)179.6 CHO*+3H*===CO*+4H* 16. (12分,除特殊说明外每空2分) (1) ①温度(1分); ②10(1分) 0.1 (2) ①bd ②不能 4HCOCo2 CoCO 2- 2CO 2H O 3 3 2 2 2 ③O 、CO 2 2 17. (16分,除特殊说明外每空2分) (1)b(1分); CH -8e-+2H O=CO +8H+ 4 2 2 (2)阴极(1分); 2H O+2e- = H ↑+2OH- 2 2 (3)b极到a极(1分); 0.2; a(1分) (4)阴; CH COO8e2H O2CO 7H ; 11.7 3 2 2 18. (18分,每空2分) (K )2 2 (1) K 1 K 3 ; CF 9 (2)60%; 或0.56 16 正向;充入物质后计算得到的浓度商Qc≈0.518小于K (3) 乙 (4) 20%;1050K前反应未达到平衡状态,随温度升高,反应速率加快,NO转化率增大。