文档内容
1
2024—2025 学年度上学期 2022 级
11 月月考化学试卷
考试时间:2024年11月26日
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.生活中蕴含着丰富的化学知识。下列相关解释错误的是
A.用过氧乙酸溶液对居住环境消毒:CHCOOOH具有较强氧化性
3
B.做豆腐时用石膏作凝固剂:CaSO·2HO是硫酸盐结晶水合物
4 2
C.制作腌菜、酱菜时添加食盐:高浓度的NaCl溶液使微生物脱水失活
D.果汁中添加维生素C:维生素C作抗氧化剂
2.材料的发展体现了“中国技术”和“中国力量”。下列说法正确的是
A.铁和氯气反应,实验室不能用钢瓶来装氯气
B.集成电路底板的酚醛树脂属于聚酯
C.铝锂合金材料强度大、密度小,可做航天材料
D.含碳量为3%的铁碳合金属于高碳钢
3.下列化学用语或图示正确的是
A.1-氯丙烯的结构简式:
B.基态 Cr原子的价层电子轨道表示式为
24
C.CO的电子式:
D.O 分子的球棍模型:
3
4.对于下列过程中发生的化学反应,相应化学或离子方程式错误的是
A.绿矾(FeSO ·7H O)处理酸性工业废水中的Cr O :6Fe2++Cr O +14H+=6Fe3++2Cr3++7H O
4 2 2 2 2
B.工业废水中的Pb2+用NaS去除:Pb2++S2-=PbS↓
2
C.海水提溴过程中将溴吹入SO 吸收塔:Br +SO+2H O=2Br-+SO +4H+
2 2 2 2
D.《天工开物》记载用炉甘石(ZnCO)火法炼锌:2ZnCO +C 2Zn+3CO ↑
3 3 2
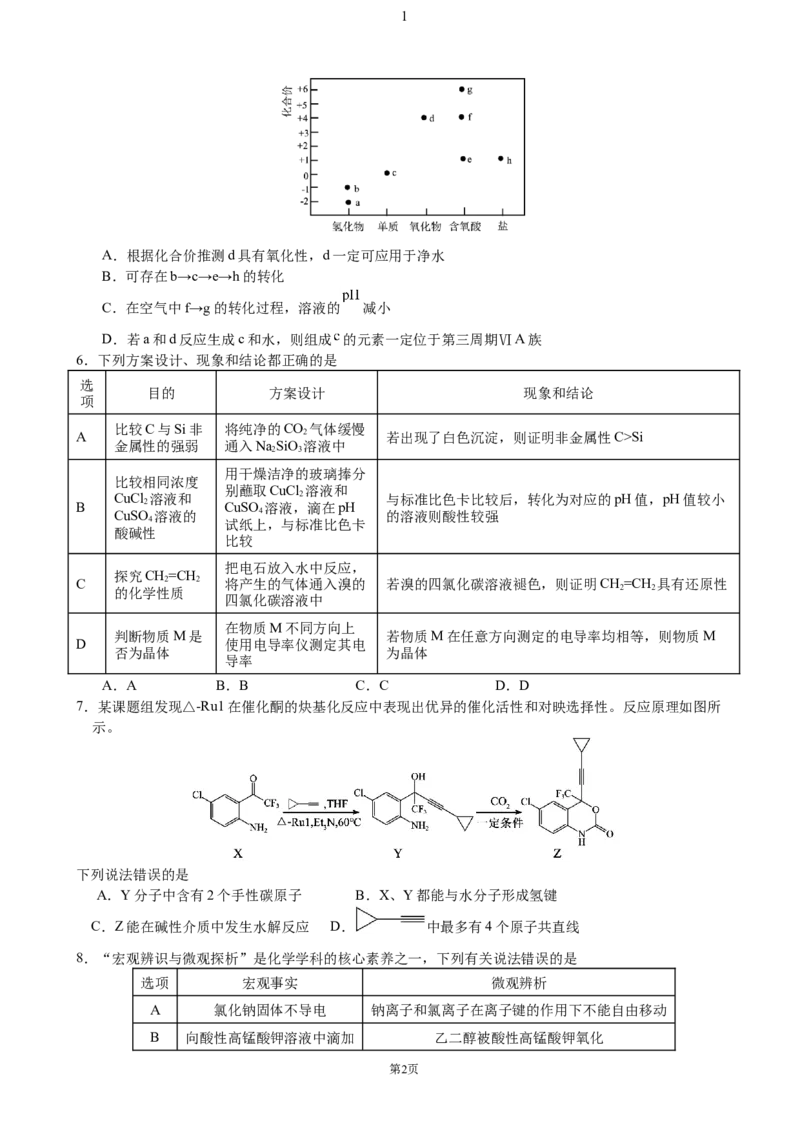
5.部分含氯或硫物质的分类与相应化合价关系如图所示。下列推断不合理的是
第1页1
A.根据化合价推测d具有氧化性,d一定可应用于净水
B.可存在b→c→e→h的转化
C.在空气中f→g的转化过程,溶液的 减小
D.若a和d反应生成c和水,则组成 的元素一定位于第三周期ⅥA族
6.下列方案设计、现象和结论都正确的是
选
目的 方案设计 现象和结论
项
比较C与Si非 将纯净的CO 气体缓慢
A 2 若出现了白色沉淀,则证明非金属性C>Si
金属性的强弱 通入NaSiO 溶液中
2 3
用干燥洁净的玻璃捧分
比较相同浓度
别蘸取CuCl 溶液和
CuCl 溶液和 2 与标准比色卡比较后,转化为对应的pH值,pH值较小
B 2 CuSO 溶液,滴在pH
CuSO 溶液的 4 的溶液则酸性较强
4 试纸上,与标准比色卡
酸碱性
比较
把电石放入水中反应,
探究CH=CH
C 2 2 将产生的气体通入溴的 若溴的四氯化碳溶液褪色,则证明CH=CH 具有还原性
的化学性质 2 2
四氯化碳溶液中
在物质M不同方向上
判断物质M是 若物质M在任意方向测定的电导率均相等,则物质M
D 使用电导率仪测定其电
否为晶体 为晶体
导率
A.A B.B C.C D.D
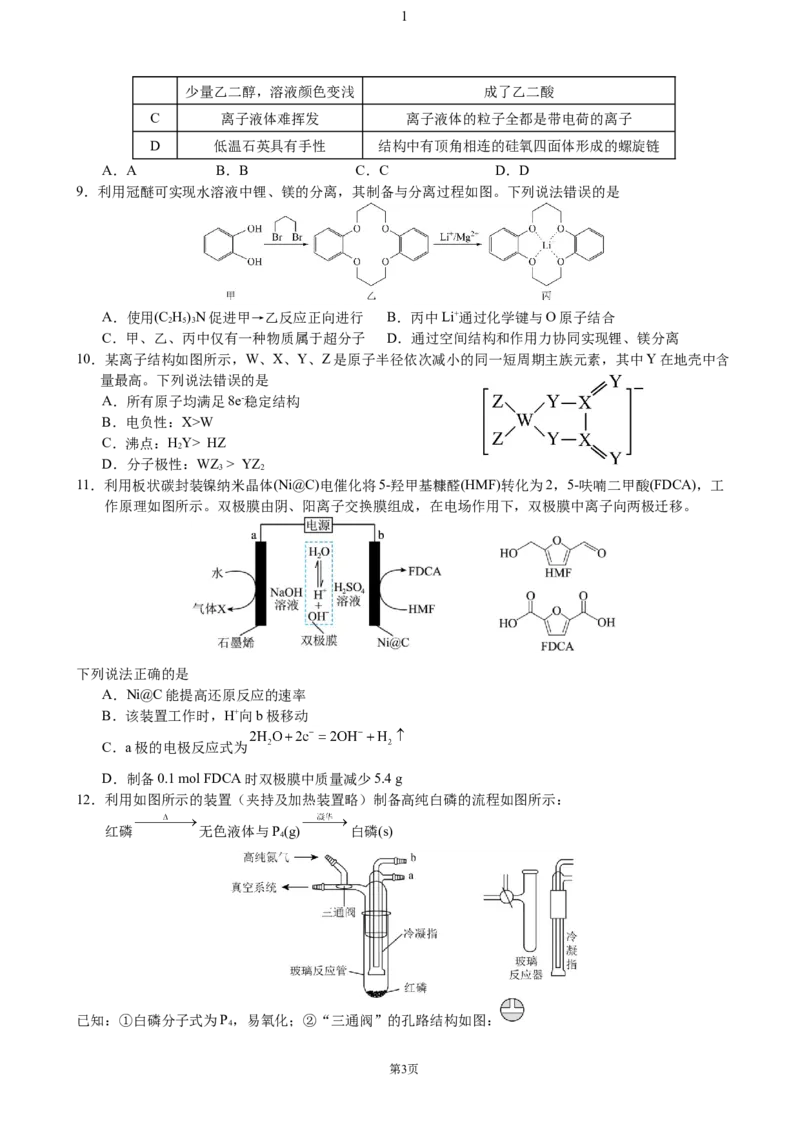
7.某课题组发现△-Ru1在催化酮的炔基化反应中表现出优异的催化活性和对映选择性。反应原理如图所
示。
下列说法错误的是
A.Y分子中含有2个手性碳原子 B.X、Y都能与水分子形成氢键
C.Z能在碱性介质中发生水解反应 D. 中最多有4个原子共直线
8.“宏观辨识与微观探析”是化学学科的核心素养之一,下列有关说法错误的是
选项 宏观事实 微观辨析
A 氯化钠固体不导电 钠离子和氯离子在离子键的作用下不能自由移动
B 向酸性高锰酸钾溶液中滴加 乙二醇被酸性高锰酸钾氧化
第2页1
少量乙二醇,溶液颜色变浅 成了乙二酸
C 离子液体难挥发 离子液体的粒子全都是带电荷的离子
D 低温石英具有手性 结构中有顶角相连的硅氧四面体形成的螺旋链
A.A B.B C.C D.D
9.利用冠醚可实现水溶液中锂、镁的分离,其制备与分离过程如图。下列说法错误的是
A.使用(C H)N促进甲→乙反应正向进行 B.丙中Li+通过化学键与O原子结合
2 5 3
C.甲、乙、丙中仅有一种物质属于超分子 D.通过空间结构和作用力协同实现锂、镁分离
10.某离子结构如图所示,W、X、Y、Z是原子半径依次减小的同一短周期主族元素,其中Y在地壳中含
量最高。下列说法错误的是
A.所有原子均满足8e-稳定结构
B.电负性:X>W
C.沸点:HY> HZ
2
D.分子极性:WZ > YZ
3 2
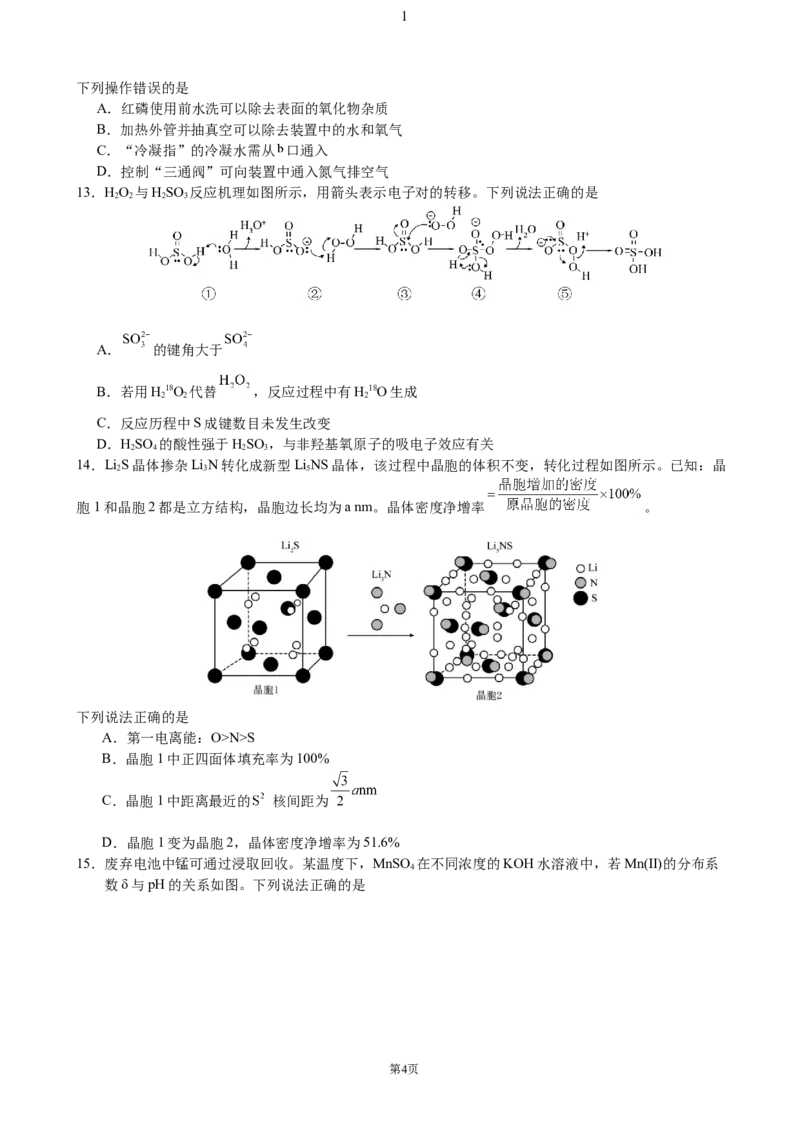
11.利用板状碳封装镍纳米晶体(Ni@C)电催化将5-羟甲基糠醛(HMF)转化为2,5-呋喃二甲酸(FDCA),工
作原理如图所示。双极膜由阴、阳离子交换膜组成,在电场作用下,双极膜中离子向两极迁移。
下列说法正确的是
A.Ni@C能提高还原反应的速率
B.该装置工作时,H+向b极移动
C.a极的电极反应式为
D.制备0.1 mol FDCA时双极膜中质量减少5.4 g
12.利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如图所示:
红磷 无色液体与P(g) 白磷(s)
4
已知:①白磷分子式为P,易氧化;②“三通阀”的孔路结构如图:
4
第3页1
下列操作错误的是
A.红磷使用前水洗可以除去表面的氧化物杂质
B.加热外管并抽真空可以除去装置中的水和氧气
C.“冷凝指”的冷凝水需从 口通入
D.控制“三通阀”可向装置中通入氮气排空气
13.HO 与HSO 反应机理如图所示,用箭头表示电子对的转移。下列说法正确的是
2 2 2 3
A. 的键角大于
B.若用H18O 代替 ,反应过程中有H18O生成
2 2 2
C.反应历程中S成键数目未发生改变
D.HSO 的酸性强于HSO ,与非羟基氧原子的吸电子效应有关
2 4 2 3
14.LiS晶体掺杂LiN转化成新型LiNS晶体,该过程中晶胞的体积不变,转化过程如图所示。已知:晶
2 3 5
胞1和晶胞2都是立方结构,晶胞边长均为a nm。晶体密度净增率 。
下列说法正确的是
A.第一电离能:O>N>S
B.晶胞1中正四面体填充率为100%
C.晶胞1中距离最近的 核间距为
D.晶胞1变为晶胞2,晶体密度净增率为51.6%
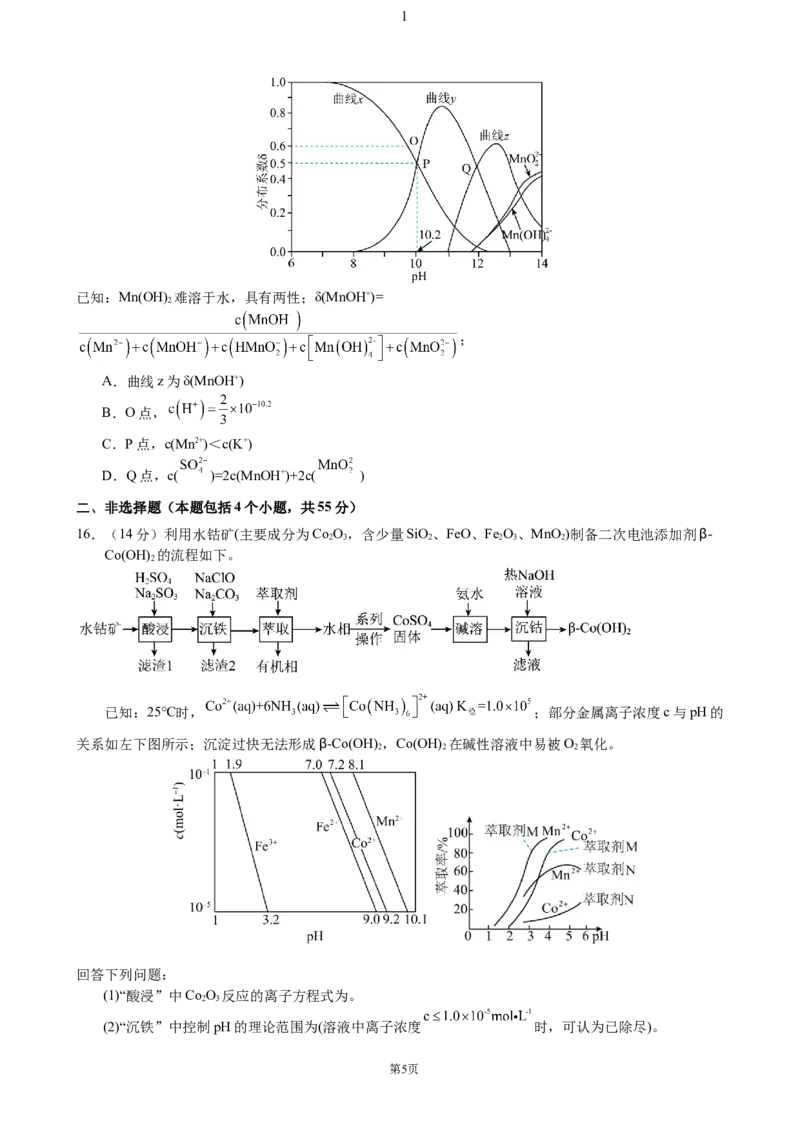
15.废弃电池中锰可通过浸取回收。某温度下,MnSO 在不同浓度的KOH水溶液中,若Mn(Ⅱ)的分布系
4
数δ与pH的关系如图。下列说法正确的是
第4页1
已知:Mn(OH) 难溶于水,具有两性;δ(MnOH+)=
2
;
A.曲线z为δ(MnOH+)
B.O点,
C.P点,c(Mn2+)<c(K+)
D.Q点,c( )=2c(MnOH+)+2c( )
二、非选择题(本题包括4个小题,共55分)
16.(14分)利用水钴矿(主要成分为Co O,含少量SiO、FeO、Fe O、MnO )制备二次电池添加剂β-
2 3 2 2 3 2
Co(OH) 的流程如下。
2
已知:25℃时, ;部分金属离子浓度c与pH的
关系如左下图所示;沉淀过快无法形成β-Co(OH) ,Co(OH) 在碱性溶液中易被O 氧化。
2 2 2
回答下列问题:
(1)“酸浸”中Co O 反应的离子方程式为。
2 3
(2)“沉铁”中控制pH的理论范围为(溶液中离子浓度 时,可认为已除尽)。
第5页1
(3)萃取剂对Co2+、Mn2+萃取率随pH的影响如右上图,应选择萃取剂(填“M”或“N”)。若萃取剂的量
一定时,(填“一次萃取”或“少量多次萃取”)的萃取效率更高。
(4)“沉钴”步骤中,发生反应的离子方程式为。
(5) 过程中,先加氨水再缓慢加NaOH溶液的理由是,“沉钴”
中使用热NaOH溶液的目的是。
17.(14分)三氯化铬(CrCl )为紫色单斜晶体,熔点为83℃,易潮解,易升华,溶于水但不易水解,高温
3
下能被氧气氧化,工业上主要用作媒染剂和催化剂。
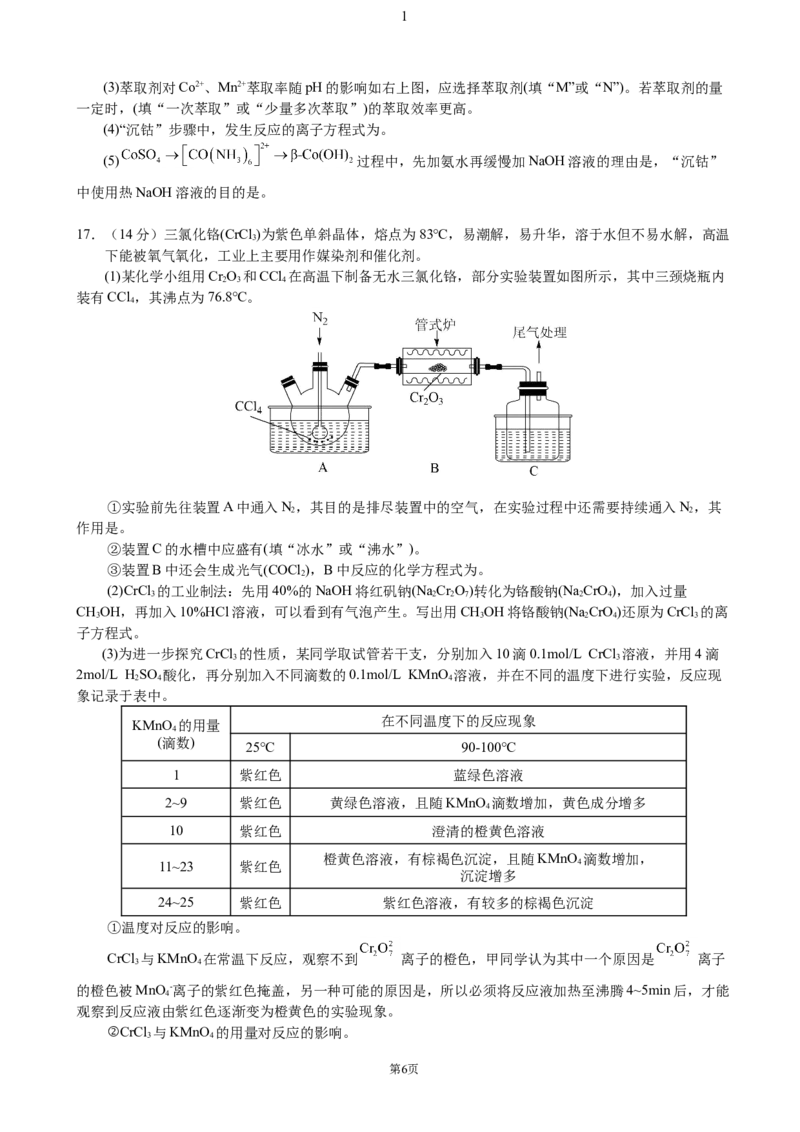
(1)某化学小组用Cr O 和CCl 在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶内
2 3 4
装有CCl ,其沸点为76.8℃。
4
①实验前先往装置A中通入N,其目的是排尽装置中的空气,在实验过程中还需要持续通入N,其
2 2
作用是。
②装置C的水槽中应盛有(填“冰水”或“沸水”)。
③装置B中还会生成光气(COCl ),B中反应的化学方程式为。
2
(2)CrCl 的工业制法:先用40%的NaOH将红矾钠(Na Cr O)转化为铬酸钠(Na CrO),加入过量
3 2 2 7 2 4
CHOH,再加入10%HCl溶液,可以看到有气泡产生。写出用CHOH将铬酸钠(Na CrO)还原为CrCl 的离
3 3 2 4 3
子方程式。
(3)为进一步探究CrCl 的性质,某同学取试管若干支,分别加入10滴0.1mol/L CrCl 溶液,并用4滴
3 3
2mol/L HSO 酸化,再分别加入不同滴数的0.1mol/L KMnO 溶液,并在不同的温度下进行实验,反应现
2 4 4
象记录于表中。
在不同温度下的反应现象
KMnO 的用量
4
(滴数)
25℃ 90-100℃
1 紫红色 蓝绿色溶液
2~9 紫红色 黄绿色溶液,且随KMnO 滴数增加,黄色成分增多
4
10 紫红色 澄清的橙黄色溶液
橙黄色溶液,有棕褐色沉淀,且随KMnO 滴数增加,
11~23 紫红色 4
沉淀增多
24~25 紫红色 紫红色溶液,有较多的棕褐色沉淀
①温度对反应的影响。
CrCl 与KMnO 在常温下反应,观察不到 离子的橙色,甲同学认为其中一个原因是 离子
3 4
的橙色被MnO -离子的紫红色掩盖,另一种可能的原因是,所以必须将反应液加热至沸腾4~5min后,才能
4
观察到反应液由紫红色逐渐变为橙黄色的实验现象。
②CrCl 与KMnO 的用量对反应的影响。
3 4
第6页1
对表中数据进行分析,在上述反应条件下,欲将 氧化为 ,CrCl 与KMnO 最佳用量比为。
3 4
这与由反应 所推断得到的用量比不符,你推测的原因是。
18.(14分)苯乙烯是生产塑料与合成橡胶的重要原料。CO 氧化乙苯脱氢制苯乙烯的反应为:
2
反应Ⅰ: +CO (g) + H O(g) +CO(g)
2 2
已知:反应Ⅱ: + H (g)
2
反应Ⅲ:
回答下列问题:
(1)反应Ⅰ的 。
(2)下列关于反应Ⅰ~Ⅲ的说法正确的是___________(填字母)。
A.及时分离出水蒸气,有利于提高平衡混合物中苯乙烯的含量
B.n(CO):n(CO)保持恒定时,说明反应Ⅰ达到化学平衡状态
2
C.其他条件相同,反应Ⅱ分别在恒容和恒压条件下进行,前者乙苯的平衡转化率更高
D.反应Ⅲ正反应的活化能小于逆反应的活化能
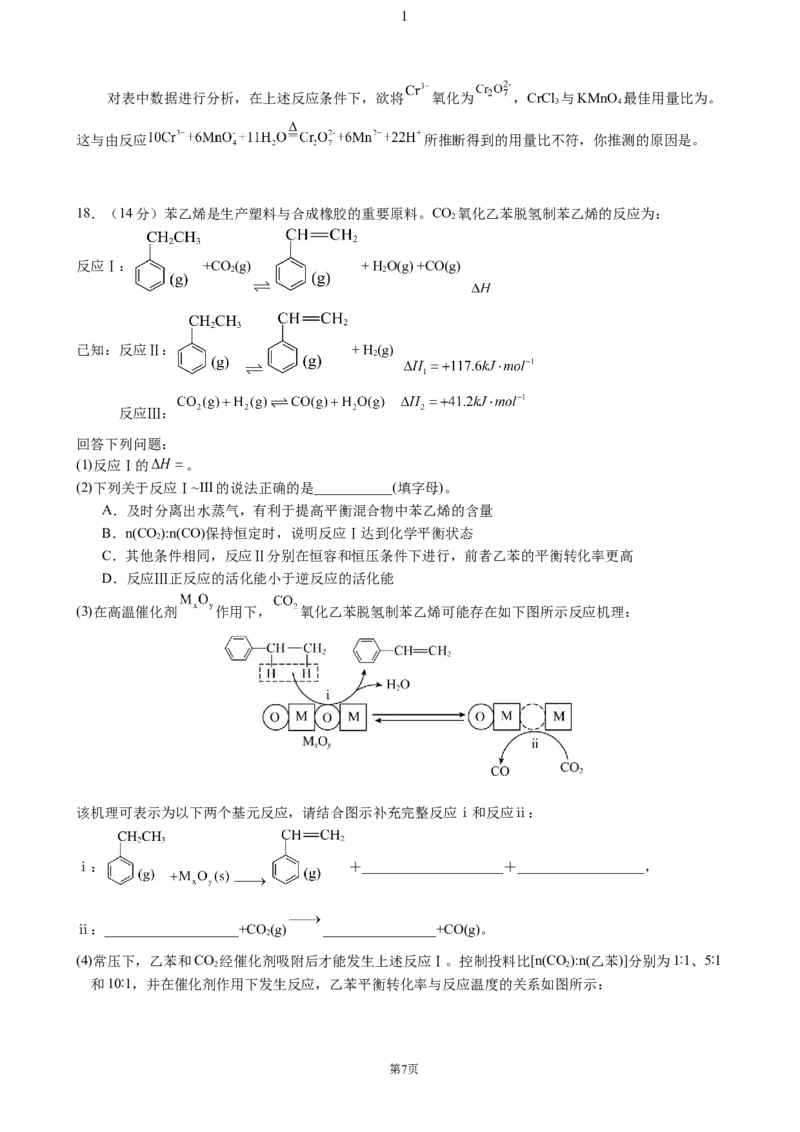
(3)在高温催化剂 作用下, 氧化乙苯脱氢制苯乙烯可能存在如下图所示反应机理:
该机理可表示为以下两个基元反应,请结合图示补充完整反应ⅰ和反应ⅱ:
ⅰ: +____________________+__________________,
ⅱ:___________________+CO (g) ________________+CO(g)。
2
(4)常压下,乙苯和CO 经催化剂吸附后才能发生上述反应Ⅰ。控制投料比[n(CO ):n(乙苯)]分别为1∶1、5∶1
2 2
和10∶1,并在催化剂作用下发生反应,乙苯平衡转化率与反应温度的关系如图所示:
第7页1
①曲线A的投料比为,Q点平衡常数P点平衡常数(填“>”、“<”或“=”)。
②相同温度下,投料比远大于10∶1时,乙苯的消耗速率明显下降,可能的原因是:
ⅰ.乙苯的浓度过低;
ⅱ.。
③850K时,若初始乙苯的物质的量为n mol,反应经t min达到图中P点所示状态,则
ν(苯乙烯)= 。
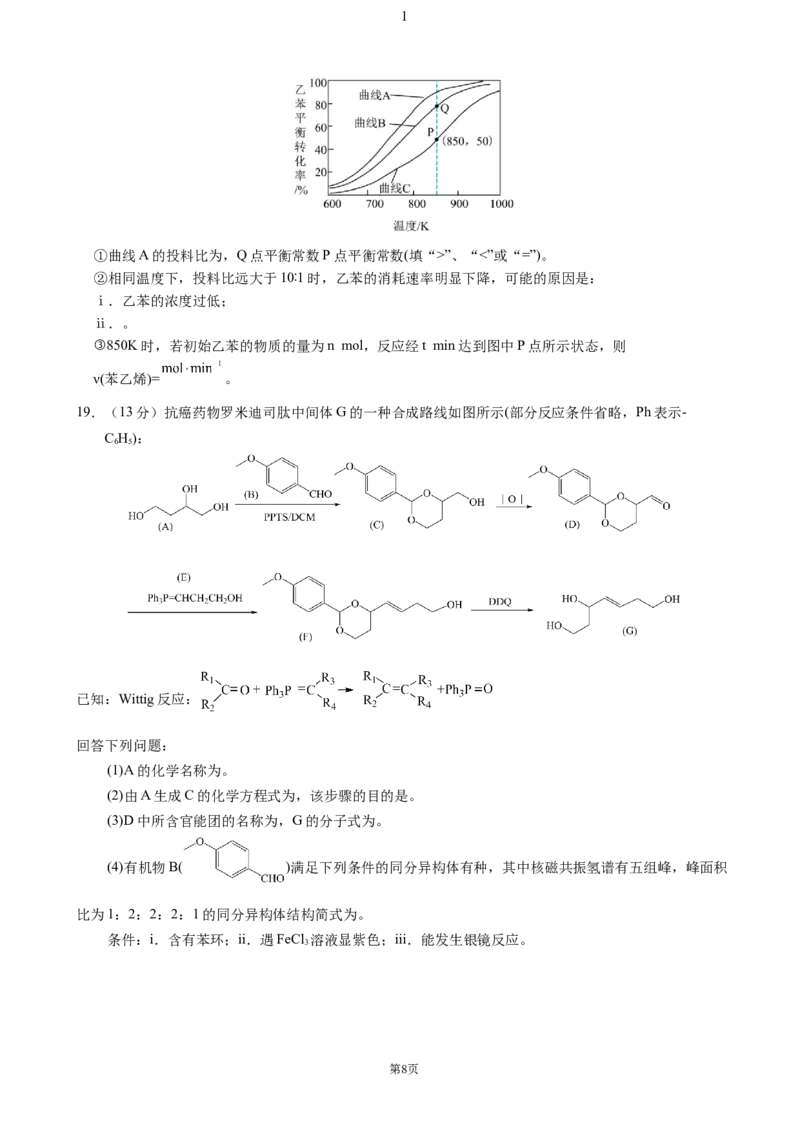
19.(13分)抗癌药物罗米迪司肽中间体G的一种合成路线如图所示(部分反应条件省略,Ph表示-
C H):
6 5
已知:Wittig反应:
回答下列问题:
(1)A的化学名称为。
(2)由A生成C的化学方程式为,该步骤的目的是。
(3)D中所含官能团的名称为,G的分子式为。
(4)有机物B( )满足下列条件的同分异构体有种,其中核磁共振氢谱有五组峰,峰面积
比为1:2:2:2:1的同分异构体结构简式为。
条件:i.含有苯环;ii.遇FeCl 溶液显紫色;iii.能发生银镜反应。
3
第8页1
高三年级 11 月月考化学答案
1-15 BCCDA AABBD CDDBC
16.(14分)
(1) (2)3.2≤pH<7.2
△
(3)N 少量多次萃取(4)
(5)“碱溶”形成的 在加入 “沉钴”时可缓释 利于晶体形成,缓慢加 溶液可
以防止沉淀过快无法形成
温度高利于减少溶解氧,形成 气氛隔绝空气,防止产物被氧化
17.(14分)
(1)将四氯化碳吹入管式炉中和 反应生成三氯化铬 冰水 (2)
(3)反应的活化能较高,需要较高温度反应才能进行 1:1
高锰酸根离子和溶液中氯离子发生了氧化还原反应,导致高锰酸钾溶液用量增加
18.(14分)
(1)
(2)AB
(3)
(4)10∶1 (1分) = (1分)
CO 过多地占据催化剂表面,导致催化剂对乙苯的吸附率降低
2
19.(13分)
(1)1,2,4−丁三醇
第9页1
(2) + +H O 保护羟基(1分)
2
(3)醚键、醛基 C H O
7 14 3
(4)13
第10页