文档内容
姓 名____________________
准考证号____________________
机密 启用前
★
2025 届新高考教学教研联盟高三第 次预热考试
一
化学试卷
长郡中学;衡阳市八中;永州市四中;岳阳县一中;湘潭县一中;湘西州民中;石门县一中;
由 澧县一中;益阳市一中;桃源县一中;株洲市二中;麓山国际;郴州市一中;岳阳市一中; 联合命题
娄底市一中;怀化市三中;邵东市一中;洞口县一中;宁乡市一中;浏阳市一中。
命题学校:长郡中学、邵东一中 审题学校:株洲市二中、湘潭县一中
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2 . 回答选择题,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干
净后,再选涂其他答案标号 。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
第 卷选择题 (共 42分)
Ⅰ
一、选择题(本大题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
硫的含氧酸根有很多,如SO2、S O2、S O2、S O2等,其中S O2可看作SO2中的一个O原子被S原子取代后的
4 2 3 2 5 2 8 2 3 4
产物,S O2内部含过氧键;焦亚硫酸钠(Na S O )在医药、橡胶、印染、食品等方面应用广泛,生产Na S O 通常是由
2 8 2 2 5 2 2 5
NaHSO 过饱和溶液经结晶脱水制得。利用烟道气中的SO 生产Na S O 的工艺如下。阅读材料,回答下列问题。
3 2 2 2 5
1
.上述过程中涉及或拓展的方程式中,错误的是
A Na S O 2NaHSO Na S O H O
.结晶脱水制 2 2 5的反应: 3 2 2 5 2
B I 2CO2SO H O2HCOSO2
. 中发生的反应: 3 2 2 3 3
C Na CO CO 2Na CO2CO H O2NaHCO
.向 2 3饱和溶液中通入 2: 3 2 2 3
D Na S O S O22I 3H O 2SO24I6H
.用碘标准液测定某葡萄酒中 2 2 5含量: 2 5 2 2 4
2
.下列有关说法正确的是
A S O2 S―S―OSO2 O―S―O
. 2 3 中的键角 4 中的键角
思思想政治
化学试题CJ 第1页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}B S O2 +7
. 2 8 中的硫元素的化合价为 价
C SO2
. 4 的立体结构图可表示为:
D (Na S O )
.焦亚硫酸钠 2 2 5 的水溶液呈中性
3 0.1molL1 FeNO CuNO HNO Zn
.向物质的量浓度均为 的 3 3、 3 2、 3的混合溶液中加入一定质量的 粉,充分反应后
A B
过滤,得到固体 和溶液 。下列说法正确的是
A B KSCN
.向溶液 中滴入几滴 溶液,溶液可能变为血红色
B A B H Cu2
.将固体 投入稀盐酸中,没有气泡生成,则溶液 中可能含有大量 和
C B A
.若溶液 呈蓝绿色,则固体 中一定不含铁元素
D B A Zn
.若溶液 无色透明,则固体 中一定含有 粉
4 FeCl
.下列化合物中,能与 3溶液发生颜色反应的是
A B C D
. . . .
5
.一种实现二氧化碳固定及再利用的反应如图所示。下列叙述正确的是
A 1
.化合物 存在顺反异构
B 1
.化合物 与乙烯互为同系物
C 2
.化合物 可以与乙二醇发生缩聚反应
D 2
.化合物 中含手性碳原子且所有碳原子一定共面
6 MgO SiO Fe O Al O ——
.某 粗品中含少量 2、 2 3和 2 3等杂质,以氧化镁粗品为原料制备耐火材料 轻质氧化镁的流程如下:
以下说法中,不正确的是
A SiO
.滤渣Ⅰ的主要成分是 2
B
AlOH
.步骤Ⅱ利用了 3是两性氢氧化物的特点将之分离
C c
NH
c
SO2
c
H
c
OH
.硫酸铵溶液中各离子浓度大小关系满足: 4 4
思思想政治
化学试题CJ 第2页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}D 2Mg22OHCO2 Mg OH CO
.步骤Ⅳ中发生反应的离子方程式为: 3 2 2 3
7 “ CO ”
.我国科学家研究成果 无细胞化学酶系统催化 2合成淀粉 取得重要进展,其中一步核心反应如下图所示。
下列说法错误的是
A 44gCO 6mol B MnO
.反应①中每消耗 2,转移 电子 .反应③中的催化剂,实验室中可用 2
C HCHO DHA 30g 2molO D
. 与 的混合物 中含有 .淀粉与纤维素,不互为同分异构体
8
.壳聚糖是最丰富的天然高分子多糖之一,可由甲壳素在碱性溶液中煮沸制得,其转化关系如图所示。
下列有关说法正确的是
A NOC
.电负性:
B >
.水溶性:壳聚糖 甲壳素
C
.壳聚糖均既有酸性又有碱性
D 1mol KOH(aq) KOH 3nN
. 甲壳素与足量浓 反应,消耗 的物质的量为 A
9 X Y Z W
.四种元素与锂组成的盐是一种新型锂离子电池的电解质,结构如图所示。 、 、 、 是同周期主族元素,四种元
W
素均是短周期元素, 元素形成的某种单质具有强氧化性,可用于杀菌消毒。下列说法正确的是
A W>X>Y>Z B Y +1
.电负性大小: .该阴离子中 元素的化合价为 价
C X>W D W 3
.最简单氢化物的沸点: .同周期中第一电离能比 大的有 种元素
10 (Ga) Ga I
.镓 常用作半导体的原料,能形成化合物 6 6,研究表明该物质由离子构成
Ga I 2 8
,其阴离子 2 6 中所有原子的价层均有 个电子。以下说法不正确的是
...
A p
.镓和碘均位于元素周期表的 区
B Ga I
.化合物 6 6中镓的化合价不止一种
C Ga I 2
. 2 6 的结构可以表示为
D Ga I 2 Ga sp3
. 2 6 中 原子的杂化方式为
11 1 3- 5- 。
.药物中间体 , 环己二酮可由 氧代己酸甲酯合成,转化步骤如下 下列说法或操作错误的是
思思想政治
化学试题CJ 第3页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}A
.反应须在通风棚中进行
B CH OH 5- DMF
.减压蒸馏去除 3 、 氧代己酸甲酯和
C
.减压蒸馏后趁热加入盐酸
D
.过滤后可用少量冰水洗涤产物
12
.根据下列实验目的设计实验方案,观察到相关现象。其中方案设计和结论都正确的是
选
实验目的 方案设计 现象 结论
项
23mL
探究钠在氧气中燃烧所得 取少量固体粉末,加入 蒸馏 钠在氧气中燃烧所得产物为
A
有气体生成
Na O
固体产物的成分 水 2 2
pH 1mol/L
常温下,用 计分别测定 同温下,不同浓度的
B 0.1mol/L CH COONH pH 7.0 CH COONH
比较水的电离程度 和 3 4溶液的 均为 3 4溶液中水的电
pH
离程度相同
CuH
2
O
4
2 +4Cl
2mL0.5mol/LCuCl
探究温度对化学平衡的影 取 2溶液于试管
C 溶液变绿 CuCl 4 2 +4H 2 O 温度升高
响 中,将试管加热
平衡逆向移动
FeCl (
定性证明配合物 4 溶液亮黄色
4mL FeCl
取 工业盐酸于试管中,滴加几 配合物 4 只有在高浓度
D 亮黄色 ) 只有在高浓度 Cl 的 褪去,变为
滴硝酸银饱和溶液
Cl
的条件下才是稳定的
很浅的黄色
条件下才是稳定的
13 (SCC) (NORR)
.南京理工大学朱卫华等人基于单簇催化剂 ,提出了一种一氧化氮还原反应 的新型结构~活性关系,经
研究发现主要反应如下:
( )2NOg2H gN g2H Og H0 ( )2NOg5H g2NH g2H Og H0
Ⅰ 2 2 2 Ⅱ 2 3 2
( )N g3H g2NH g H0
Ⅲ 2 2 3
T 100kPa 2molNO 6molH [ N
在 ℃、 反应条件下,向密闭容器中充入 和 2,发生上述反应,测得含氮元素占比 如 2的含氮元
nN 2
2 100%]
素占比nNOnNH nN 2 与时间的关系如图所示。
3 2
思思想政治
化学试题CJ 第4页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}K
已知:反应Ⅱ为快速平衡,可认为不受慢反应Ⅰ、Ⅲ的影响; x为用物质的量分数表示的平衡常数。下列有关说法正
确的是
A c
.曲线 表示的是氨气的含氮元素占比
B F E
.若选择对反应Ⅱ催化效果更好的催化剂,则 点将移向 点
C I 0 45min 1kPamin1
. 点时, ~ 内用氨气表示的平均反应速率约为
2
0.16
6.9
D 95min K
.若 时达到平衡,则反应Ⅲ的平衡常数 x的计算式为 3
0.86 3.88
6.9 6.9
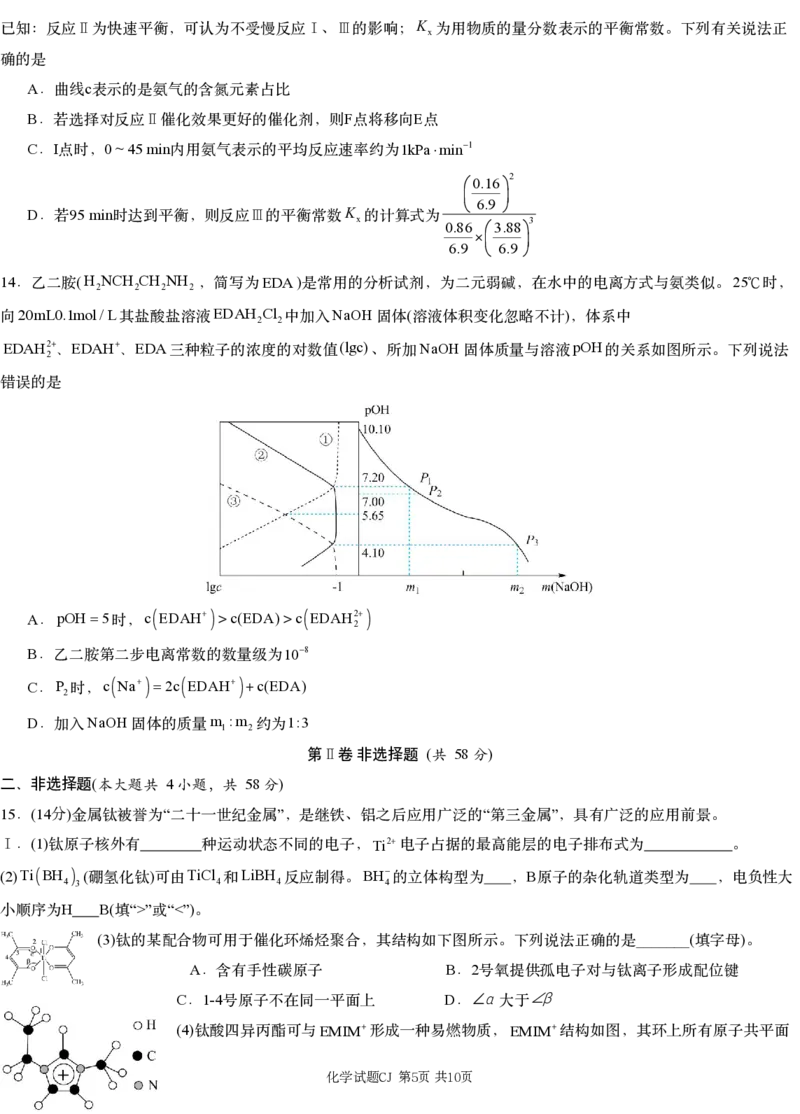
14 (H NCH CH NH EDA) 25℃
.乙二胺 2 2 2 2 ,简写为 是常用的分析试剂,为二元弱碱,在水中的电离方式与氨类似。 时,
20mL0.1mol/L EDAH Cl NaOH ( )
向 其盐酸盐溶液 2 2中加入 固体 溶液体积变化忽略不计 ,体系中
EDAH2、EDAH、EDA (lgc) NaOH pOH
2 三种粒子的浓度的对数值 、所加 固体质量与溶液 的关系如图所示。下列说法
错误的是
A pOH5 c
EDAH
c(EDA)c
EDAH2
. 时, 2
B 108
.乙二胺第二步电离常数的数量级为
C P c
Na
2c
EDAH
c(EDA)
. 2时,
D NaOH m :m 1:3
.加入 固体的质量 1 2约为
第 卷非选择题 (共 58分)
Ⅱ
二、非选择题(本大题共 4小题,共 58分)
15 (14分) “ ” “ ”
. 金属钛被誉为 二十一世纪金属 ,是继铁、铝之后应用广泛的 第三金属 ,具有广泛的应用前景。
(1) Ti2
Ⅰ. 钛原子核外有 种运动状态不同的电子, 电子占据的最高能层的电子排布式为 。
(2)TiBH ( ) TiCl LiBH BH B
4 3 硼氢化钛 可由 4和 4反应制得。 4的立体构型为 , 原子的杂化轨道类型为 ,电负性大
H B( “>” “<”)
小顺序为 填 或 。
(3) _______( )
钛的某配合物可用于催化环烯烃聚合,其结构如下图所示。下列说法正确的是 填字母 。
A B 2
.含有手性碳原子 . 号氧提供孤电子对与钛离子形成配位键
C 1-4 D
. 号原子不在同一平面上 . 大于
(4) EMIM EMIM
钛酸四异丙酯可与 形成一种易燃物质, 结构如图,其环上所有原子共平面
思思想政治
化学试题CJ 第5页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#} πn m n EMIM
。大 键可用符号 m表示,其中 表示参与形成大 键的原子数, 表示形成大 键的电子数。 中的大 键应表
EMIM N CH CH CH H
示为 。为使 以单个形式存在从而获得良好的溶解性,应避免与 原子相连的 3、 2 3被
原子替代,其原因是 。
II
TiO
( CaO Fe O
.钛白粉 2 作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿 含及少量的 、 2 3
SiO )
、 2 为原料生产钛白粉的工艺流程如图:
(5)“ ” 150 200 “ 1” TiOSO “ ” FeTiO
酸浸 是用硫酸在温度为 ~ ℃下溶煮钛铁矿, 滤液 的主要成分中含有 4,则 酸浸 时 3发生的化
学反应方程式为 。
(6)“ 1”
滤渣 的主要成分是 。
(7)“ ” ( )
还原 中加入过量铁屑的目的是 填离子方程式 。
(8)
硫酸亚铁晶体的溶解度如表所示:
/ 0 10 30 50 56.7 60 64 70 80 90
温度℃
/g 14.0 17.0 25.0 33.0 35.2 35.3 35.6 33.0 30.5 27
溶解度
FeSO 7H O FeSO 4H O FeSO H O
析出晶体 4 2 4 2 4 2
FeSO 7H O “ ”
其中绿矾 4 2 容易被氧化,则 分离 时的操作为真空加热浓缩、 、 、洗涤、干燥。
(9) TiCl
工业上将钛白粉与焦炭、氯气共热生成 4和一种可燃气体,反
应的化学方程式为 ,最后在氯气氛围和加热的
TiCl
条件下用金属镁还原 4制取性能优越的金属钛。
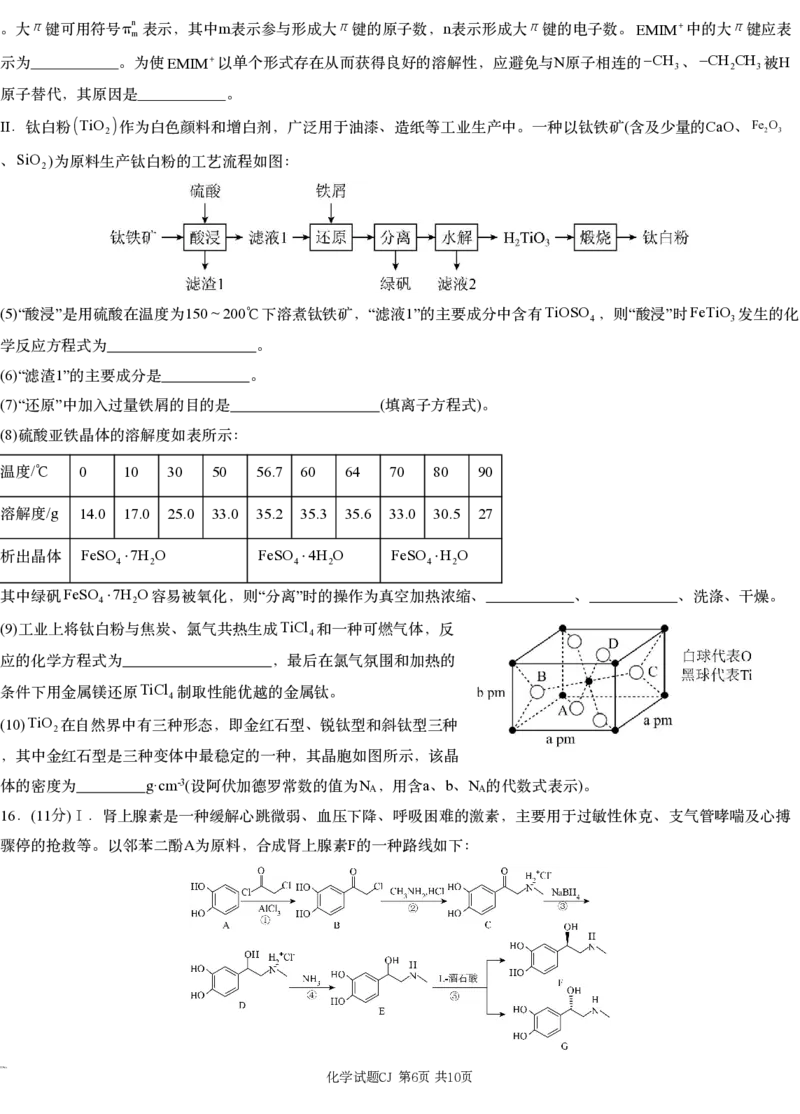
(10)TiO
2在自然界中有三种形态,即金红石型、锐钛型和斜钛型三种
,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶
g·cm-3( N a b N )
体的密度为 设阿伏加德罗常数的值为 A,用含 、 、 A的代数式表示 。
16 (11分)
. Ⅰ.肾上腺素是一种缓解心跳微弱、血压下降、呼吸困难的激素,主要用于过敏性休克、支气管哮喘及心搏
A F
骤停的抢救等。以邻苯二酚 为原料,合成肾上腺素 的一种路线如下:
思思想政治
化学试题CJ 第6页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}(1)A
最多有 个原子共平面。
(2)A H ( “ ” “ ” “
的一种芳香族同分异构体 满足下列谱图,此谱图的类型为 选填 核磁共振氢谱 、 红外光谱 、 质
”) H
谱 ; 的结构简式为 。
(3)
写出①的化学方程式 。
(4) ___________
③的反应类型是 。
A B C D
.取代反应 .消去反应 .氧化反应 .还原反应
(5) F (Na S O )
肾上腺素 的盐酸盐注射液中通常添加偏亚硫酸钠 2 2 5 ,可能的原因是 。
(6) E L- F G F G
经前四步反应得到的 为混合物,加入 酒石酸是为了分离去除与 具有不同药效的同分异构体 , 和 属于 。
A B C
.构造异构 .顺反异构 .对映异构
( )
Ⅱ.以酪氨酸 为起始原料,用纯生物法合成,经中间产物多巴胺,也可得肾上腺素。
(7) ___________
酪氨酸中不含有的官能团为 。
A B C D
.醛基 .羧基 .羟基 .氨基
(8) “*”
用 标出酪氨酸中的手性碳原子 。
(9)
酪氨酸二肽分子中,起到连接作用的官能团的结构简式为 。
(10) ( ) ( )
试设计以邻苯二酚 为原料,制备聚酯 的合成路线 。 无机试剂任选
i.O3
已知: ii.Zn/H2O
17 (10分)
. 学习结构化学,有助干洞悉物质内部奥秘。回答下列问题:
(1)Ti2+ Li Be B
电子占据的最高能层的电子排布式为 , 、 、 三种元素第二电离能由大到小的顺序为
( )
用元素符号表示 。
(2) BF 3 B-F B F
实验测得 3中 个 键长远比 和 的半径之和小,原因是 。
(3) ( ) 120
用质谱仪检测气态乙酸时,谱图中出现质荷比 相对分子质量 为 的峰,原因是 。
(4)2001 N H (SO )
SO2
N
H4
年德国专家从硫酸铵中检出一种组成为 4 4 4 2的物质,经测定该物质易溶于水,在水中以 4 和 4 4 两种
N H4 N sp3 N H4
离子的形式存在。 4 4 中 原子均为 杂化,请推测 4 4 的结构式 。
(5) (Ga) 4 A
金属镓 位于元素周期表中第 周期Ⅲ 族,其卤化物的熔点如下表:
思思想政治
化学试题CJ 第7页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}GaF GaCl GaBr
物质 3 3 3
>1000 77.75 122.3
熔点
GaF GaCl
3熔点比 3熔点高很多的原因是 。
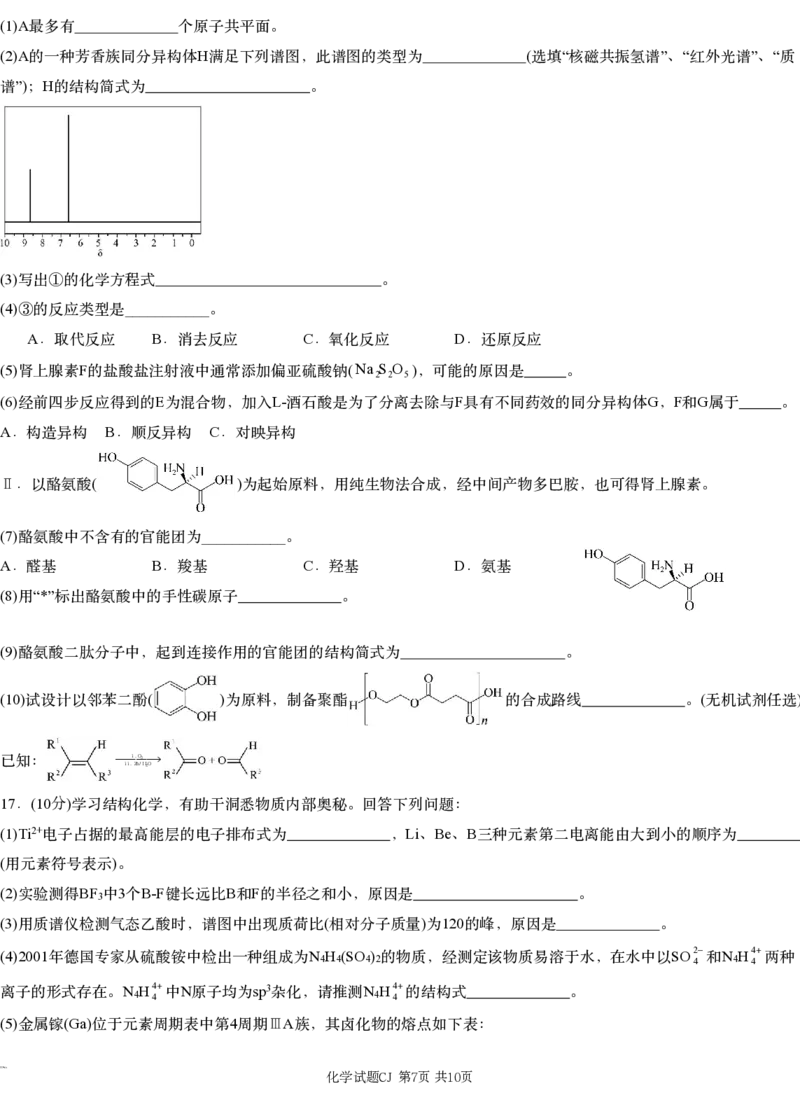
1 2 1
(6)Ni As As Ni As ( )
和 形成某种晶体的晶胞结构如图所示,距离 最近的 构成正三棱柱,下方 原子坐标为 3,3,4 ,晶体中
Ni N g/cm3( )
的配位数为 ; A为阿伏加德罗常数,则晶胞密度为 列出计算式即可 。
18 (10分) 1- (1-MN) (MTLs 1-MTL 5-MTL) (1-MD)
. 利用 甲基萘 制备四氢萘类物质 ,包括 和 。反应过程中伴有生成十氢萘
的副反应,涉及反应如图:
回答下列问题:
(1) R、R 、R ΔH、ΔH、ΔH R ( ΔH、ΔH、ΔH
已知一定条件下反应 1 2 3的焓变分别为 1 2 3,则反应 4的焓变为 用含 1 2 3的代数式表
)
示 。
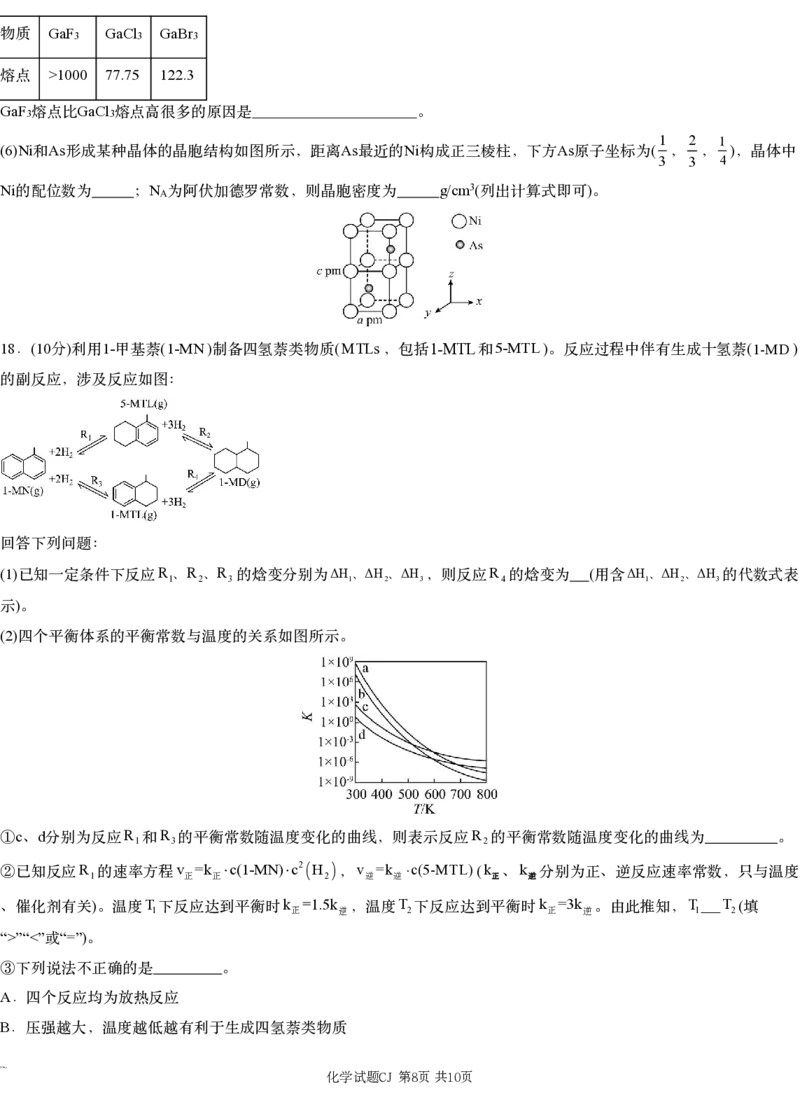
(2)
四个平衡体系的平衡常数与温度的关系如图所示。
c d R R R
① 、 分别为反应 1和 3的平衡常数随温度变化的曲线,则表示反应 2的平衡常数随温度变化的曲线为 。
R v =k c(1-MN)c2H v =k c(5-MTL)(k k
②已知反应 1的速率方程 正 正 2 , 逆 逆 正、 逆分别为正、逆反应速率常数,只与温度
) T k =1.5k T k =3k T T (
、催化剂有关 。温度 1下反应达到平衡时 正 逆,温度 2下反应达到平衡时 正 逆。由此推知, 1 2 填
“>”“<” “=”)
或 。
③下列说法不正确的是 。
A
.四个反应均为放热反应
B
.压强越大,温度越低越有利于生成四氢萘类物质
思思想政治
化学试题CJ 第8页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}C 400K R
.由上述信息可知, 时反应 4速率最快
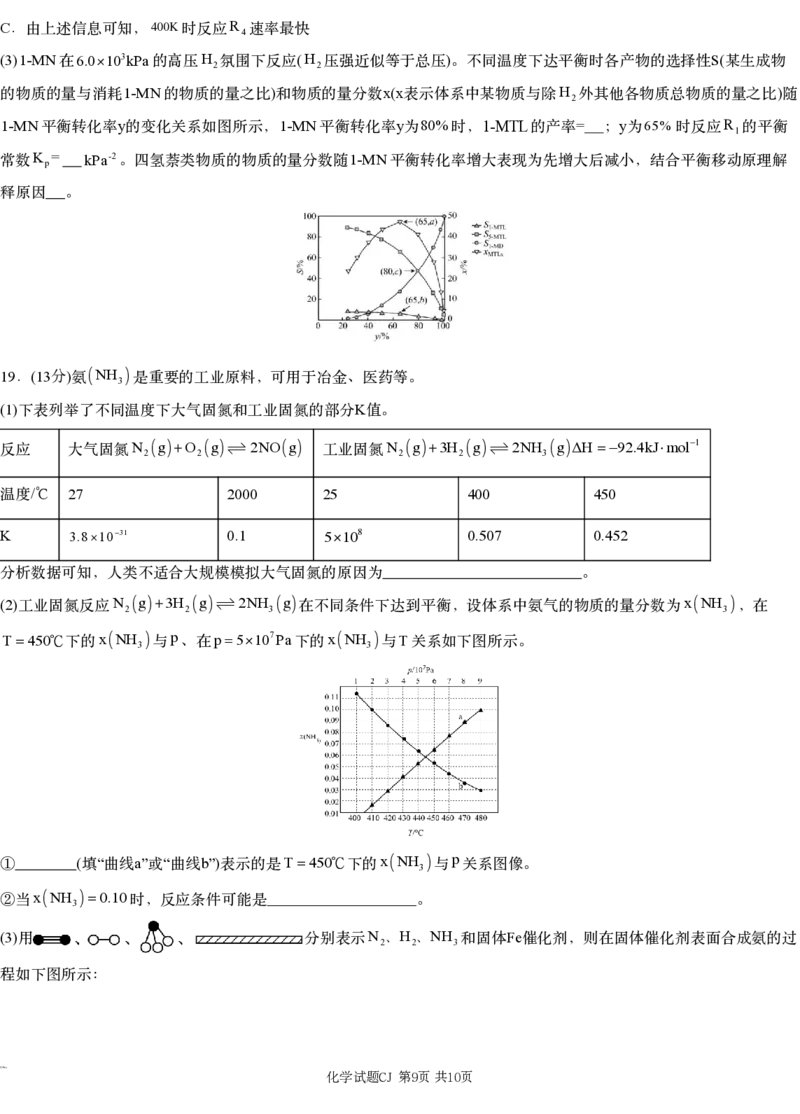
(3)1-MN 6.0103kPa H (H ) S(
在 的高压 2氛围下反应 2压强近似等于总压 。不同温度下达平衡时各产物的选择性 某生成物
1-MN ) x(x H )
的物质的量与消耗 的物质的量之比 和物质的量分数 表示体系中某物质与除 2外其他各物质总物质的量之比 随
1-MN y 1-MN y 80% 1-MTL = y 65% R
平衡转化率 的变化关系如图所示, 平衡转化率 为 时, 的产率 ; 为 时反应 1的平衡
K = kPa-2 1-MN
常数 p 。四氢萘类物质的物质的量分数随 平衡转化率增大表现为先增大后减小,结合平衡移动原理解
释原因 。
19 (13分)
NH
. 氨 3 是重要的工业原料,可用于冶金、医药等。
(1) K
下表列举了不同温度下大气固氮和工业固氮的部分 值。
N gO g2NOg N g3H g2NH gΔH92.4kJmol1
反应 大气固氮 2 2 工业固氮 2 2 3
/ 27 2000 25 400 450
温度℃
K 3.81031 0.1 5108 0.507 0.452
分析数据可知,人类不适合大规模模拟大气固氮的原因为 。
(2) N g3H g2NH g xNH
工业固氮反应 2 2 3 在不同条件下达到平衡,设体系中氨气的物质的量分数为 3 ,在
T450℃ xNH p p5107Pa xNH T
下的 3 与 、在 下的 3 与 关系如下图所示。
( “ a” “ b”) T450℃ xNH p
① 填 曲线 或 曲线 表示的是 下的 3 与 关系图像。
xNH 0.10
②当 3 时,反应条件可能是 。
(3) N 、H 、NH Fe
用 分别表示 2 2 3和固体 催化剂,则在固体催化剂表面合成氨的过
程如下图所示:
思思想政治
化学试题CJ 第9页共10页
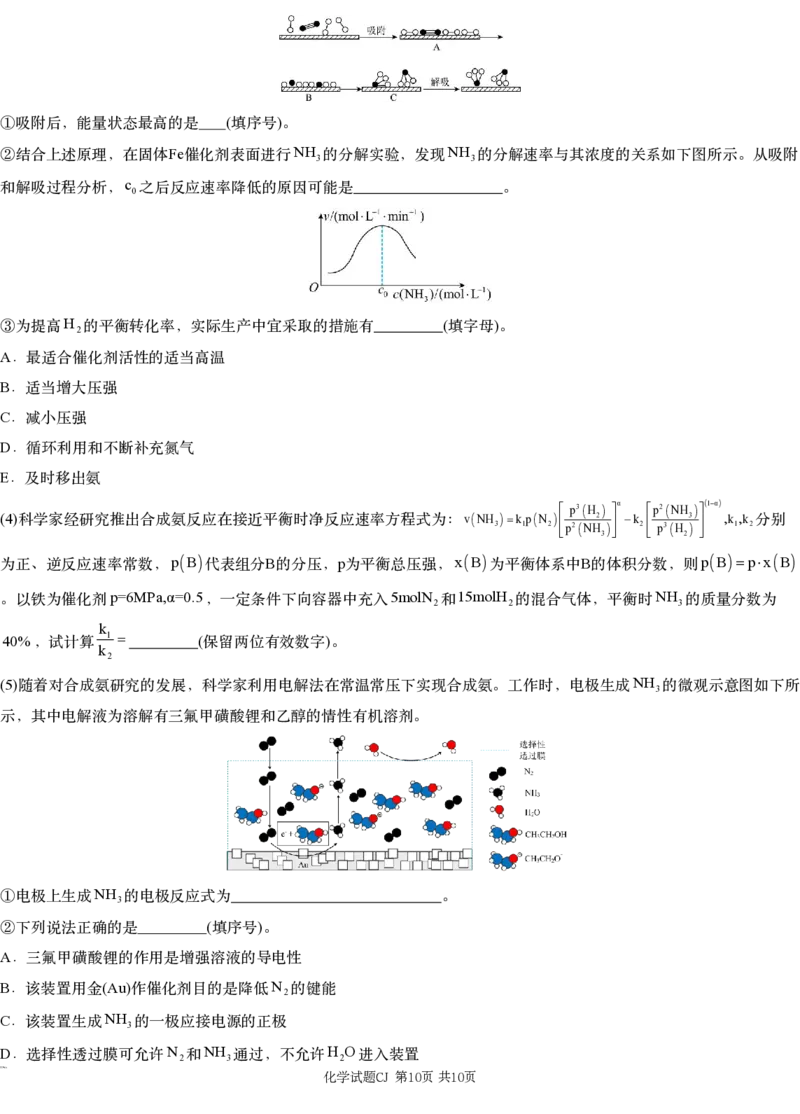
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}( )
①吸附后,能量状态最高的是 填序号 。
Fe NH NH
②结合上述原理,在固体 催化剂表面进行 3的分解实验,发现 3的分解速率与其浓度的关系如下图所示。从吸附
c
和解吸过程分析, 0之后反应速率降低的原因可能是 。
H ( )
③为提高 2的平衡转化率,实际生产中宜采取的措施有 填字母 。
A
.最适合催化剂活性的适当高温
B
.适当增大压强
C
.减小压强
D
.循环利用和不断补充氮气
E
.及时移出氨
p3H α p2NH 1α
(4) vNH kpN 2 k 3 ,k ,k
科学家经研究推出合成氨反应在接近平衡时净反应速率方程式为: 3 1 2 p2NH
3
2 p3H
2
1 2分别
pB
B p
xB
B
pBpxB
为正、逆反应速率常数, 代表组分 的分压, 为平衡总压强, 为平衡体系中 的体积分数,则
p=6MPa,α=0.5 5molN 15molH NH
。以铁为催化剂 ,一定条件下向容器中充入 2和 2的混合气体,平衡时 3的质量分数为
k
40% 1 ( )
,试计算k 保留两位有效数字 。
2
(5) NH
随着对合成氨研究的发展,科学家利用电解法在常温常压下实现合成氨。工作时,电极生成 3的微观示意图如下所
示,其中电解液为溶解有三氟甲磺酸锂和乙醇的情性有机溶剂。
NH
①电极上生成 3的电极反应式为 。
( )
②下列说法正确的是 填序号 。
A
.三氟甲磺酸锂的作用是增强溶液的导电性
B (Au) N
.该装置用金 作催化剂目的是降低 2的键能
C NH
.该装置生成 3的一极应接电源的正极
D N NH H O
.选择性透过膜可允许 2和 3通过,不允许 2 进入装置
思思想政治
化学试题CJ 第10页共10页
{#{QQABTQoEggAgABJAABhCUwUwCgIQkgGCAQgGQFAEsAAByQFABAA=}#}