文档内容
南阳一中高二年级 2025 年秋期第二次月考
化学试卷
可能用到的相对原子质量:H1 N14 O16 Na 23 Al27 S32 Cl35.5 Co59 Cu64 Ag108
一、选择题(每题只有一个正确选项,每题3分,共45分)
1.下列对化学反应的预测正确的是( )
选项 化学方程式 已知条件 预测
A A(s)===B(g)+C(s) ΔH>0 它一定是非自发反应
B A(g)+2B(g)===2C(g)+3D(g) 能自发反应 ΔH一定小于0
C M(s)+aN(g)===2Q(g) ΔH<0,自发反应 a可能等于1、2、3
D M(s)+N(g)===2Q(s) 常温下,自发进行 ΔH>0
2.下列说法错误的是
A.室温下, ,则稀 和稀 溶液反应生
成1mol 时,放出的热量是57.3 kJ
B . 已 知 、 条 件 下 : ,
,则可推出 比 稳定
C.等质量的硫蒸气和硫固体分别完全燃烧生成 ,前者放出的热量多
D.已知 、 下,将 和 置于密闭的容器中充分反应生成 ,当
的 转 化 率 为 时 , 放 热 , 则 热 化 学 方 程 式 为
3.(高二教材p49第9题变式)研究人员研制出一种可在一分钟内完成充电
的超常性能铝离子电池,该电池以金属铝和石墨为电极。用 、
和有机阳离子组成电解质溶液。其放电工作原理如图所示。下列说
法正确的是
A.放电时,电子由石墨电极经用电器流向铝电极
B.充电时,铝电极上发生氧化反应
C.充电时, 向铝电极方向移动
D.放电时,负极的电极反应为Al-3e-+7 =4AlCl
2 7
4.钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意
图。下列说法正确的是( )
A.工作时,Ⅰ室和Ⅱ室溶液的pH均增大
B.生成1 mol Co,Ⅰ室溶液质量理论上减少16 g
C.移除两交换膜后,石墨电极上发生的反应不变
D.电解总反应:2Co2++2HO=====2Co+O↑+4H+
2 2
5.某同学组装了如图所示的电化学装置,则下列说法正确的是
A.图中甲池为原电池装置,Cu电极发生还原反应
B.实验过程中,甲池左侧烧杯中 的浓度不变
C.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变
D.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某
盐溶液可能是足量 溶液
6.下列说法中可以证明反应H(g)+I(g) 2HI(g)已达平衡状态的是( )
2 2
①单位时间内生成n mol H 的同时生成n mol HI;②一个H—H断裂的同时有两
2
个H—I断裂;③百分含量w(HI)=w(I );④反应速率v(H )=v(I)=v(HI);⑤c(HI)∶c(H)∶c(I )=2∶1∶1;⑥温
2 2 2 2 2
度和体积一定时,生成物浓度不再变化;⑦温度和体积一定时,容器内的压强不再变化;⑧条件一定时,
混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体颜色不再变化;⑩温度和压强一
定时,混合气体的密度不再变化
A.①②③④ B.②⑥⑨ C.②⑥⑨⑩ D.③⑤⑥⑦⑧
7.(作业错题变式再练)下列事实不能用勒夏特列原理解释的是( )①工业合成氨,反应条件选择高温 ②实验室可以用排饱和食盐水的方法收集氯气 ③使用催化剂可加快
SO 转化为SO 的速率 ④硫酸工业中,增大O 的浓度有利于提高SO 的转化率⑤Fe(SCN) 溶液中加入固
2 3 2 2 3
体KSCN后颜色变深 ⑥向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 ⑦棕红色 NO 加压后颜色
2
先变深后变浅 ⑧由H(g)、I(g)和HI(g)组成的平衡体系加压后颜色变深 ⑨将混合气体中的氨液化有利
2 2
于合成氨反应
A.①②⑥⑧ B.①③⑤⑦ C.①③⑥⑧ D.②⑤⑦⑨
8.化学反应Ⅰ、Ⅱ、Ⅲ在不同温度时达到平衡,其平衡常数如下表:
温度
编号 化学方程式
979 K 1 173 K
Ⅰ Fe(s)+CO(g) FeO(s)+CO(g) 1.47 2.15
2
Ⅱ CO(g)+HO(g) CO(g)+H(g) 1.62 b
2 2 2
Ⅲ Fe(s)+HO(g) FeO(s)+H(g) a 1.68
2 2
根据以上信息判断,下列结论正确的是( )
A.将铁粉磨细可以使平衡Ⅰ向右移动 B.反应Ⅱ、Ⅲ均为放热反应
C.升高温度,反应Ⅲ平衡向正反应方向移动 D.a”“<”“=”)0;比较 的大小: ,若
初始时通入 为7.0MPa,则A点平衡常数
(用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量
分数,写出计算式即可)。
19.(14分)以节能减排为基础的低碳经济已成为实现人类可持续发展
的重要课题,“减排”的关键是减少CO 排放,而“减排” 的重要手
2
段是合理利用CO。回答下列问题:
2
Ⅰ.利用 合成 ,实现资源的再利用。已知:在 、 下,由最稳定的单质生成 物质的
反应焓变,叫作该物质的标准摩尔生成焓,规定稳定单质的标准摩尔生成焓为0。下表为几种常见物质的
标准摩尔生成焓的数值。
物质
标准摩尔生成焓/
反应 ,为了让该反应自发进行,最好选用的
条件是 (填“低”或“高”)温。
Ⅱ.CO与 反应合成可再生能源甲醇,反应为 。在一个容积可变的密闭
容器中充入 和 ,在催化剂作用下发生反应,CO的平衡转化率( )与温度(T)、压强(p)的关
系如图所示。回答下列问题:
(1)A点的正反应速率 (填“ ”或“ ”)C点的逆反应速率。
(2)若达到平衡状态A时,容器的容积为5L,则在平衡状态B时容器的容积为 L。
Ⅲ.(2025云南高考真题)我国科学家研发出一种乙醇(沸点78.5℃)绿色制氢新途径,并实现高附加值乙酸
(沸点118℃)的生产,主要反应为:
Ⅰ.
Ⅱ.
恒压100kPa下,向密闭容器中按 投料,产氢速率和产物的选择性随温度变化关
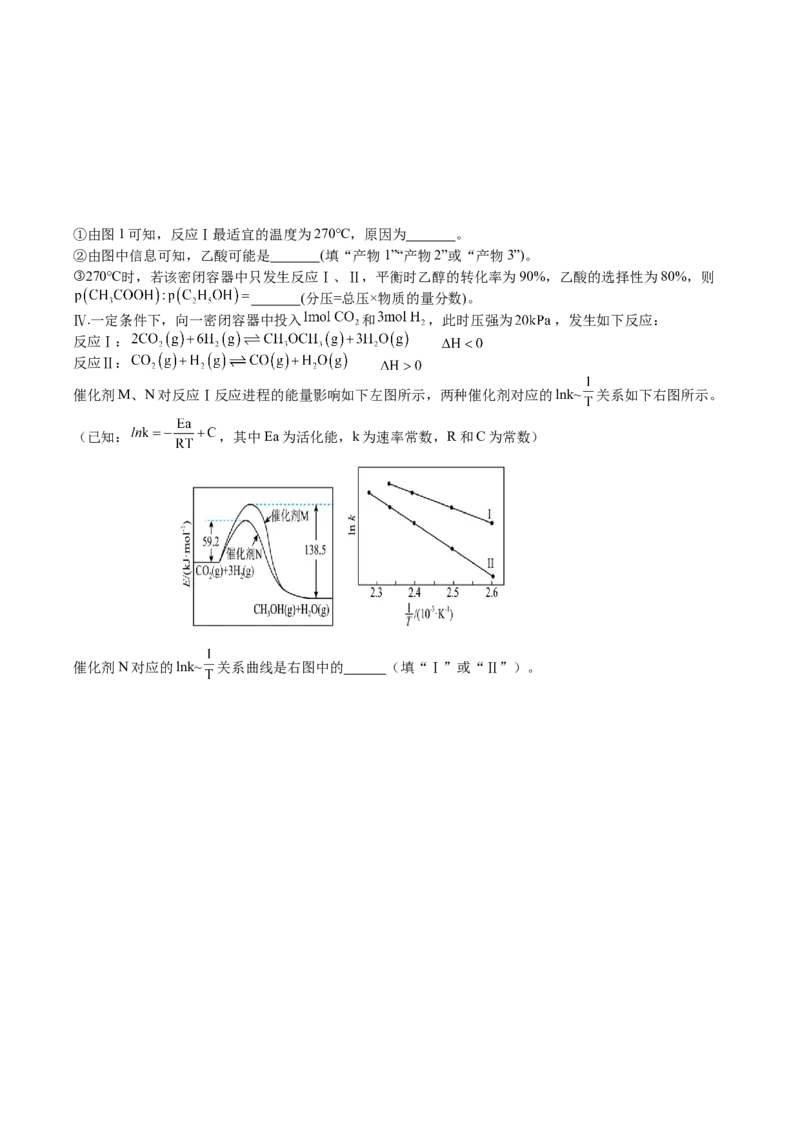
系如图1,关键步骤中间体的能量变化如图2。[比如:乙酸选择性 ]①由图1可知,反应Ⅰ最适宜的温度为270℃,原因为 。
②由图中信息可知,乙酸可能是 (填“产物1”“产物2”或“产物3”)。
③270℃时,若该密闭容器中只发生反应Ⅰ、Ⅱ,平衡时乙醇的转化率为90%,乙酸的选择性为80%,则
(分压=总压×物质的量分数)。
Ⅳ.一定条件下,向一密闭容器中投入 和 ,此时压强为 ,发生如下反应:
反应Ⅰ:
反应Ⅱ:
催化剂M、N对反应Ⅰ反应进程的能量影响如下左图所示,两种催化剂对应的lnk~ 关系如下右图所示。
(已知: ,其中Ea为活化能,k为速率常数,R和C为常数)
催化剂N对应的lnk~ 关系曲线是右图中的 (填“Ⅰ”或“Ⅱ”)。南阳一中高二年级2025年秋期化学第二次月考参考答案
1C 2A 3D 4D 5C 6B 7C 8B 9D 10C 11B 12D 13C 14C 15D
二、填空题(共55分)
16(除标注外,每空2分,共14分)
Ⅰ(1)CHCHOH+16OH--12e-=2CO 2-+11H O
3 2 3 2
(2) D(1分)外加电流阴极保护法或者阴极电保护法(1分) (3) 336(1分)
Ⅱ 1∶4
Ⅲ NH - 4e= N+4H+ 阳离子(1分) 62g
2 4 2
17(每空2分,共12分)
(1) 探究 浓度(或者反应物浓度)对反应速率的影响 (2)5:2
(3)保证①②中溶液总体积相等 (4)0.0041mol·L-1·min-1
(5) 溶液褪色所需时间小于3.7min
18 (除标注外,每空2分,共15分)
(1)
(2) 不变 ab 升高温度(1分) 加入催化剂(1分)
(3)0.05mol·L-1·min-1(无单位或者单位错不给分)
(4) <(1分)
19(除标注外,每空2分,共14分)
Ⅰ 低 (1分)
Ⅱ <(1分) 1
Ⅲ ①乙酸选择性最大且产氢反应速率较快 ②产物1 ③ 36:5