文档内容
扶沟县高级中学2025-2026学年高二上学期快班10月月考化学A卷
一、单选题
1.化学与生产、生活密切相关。下列事实与化学反应速率无关的
A.食品、蔬菜贮存在冰箱和冰柜里,能延长保鲜时间
B.家用铁锅、铁铲等餐具保持干燥,能减缓生锈
C.制造蜂窝煤时加入生石灰,减少SO 排放
2
D.向过氧化氢溶液中加二氧化锰固体制氧气
2.科学家最近设计出生产氢气的人造树叶,原理为 。则有关该反应自
发进行的条件判断正确的是
A.低温 B.高温
C.任何温度下都能自发进行 D.一定非自发
3.下列叙述中,能说明该物质是弱电解质的是
A.熔化时不导电 B.不是离子化合物,而是共价化合物
C.水溶液的导电能力很差 D.溶液中溶质分子和电离出的离子共存
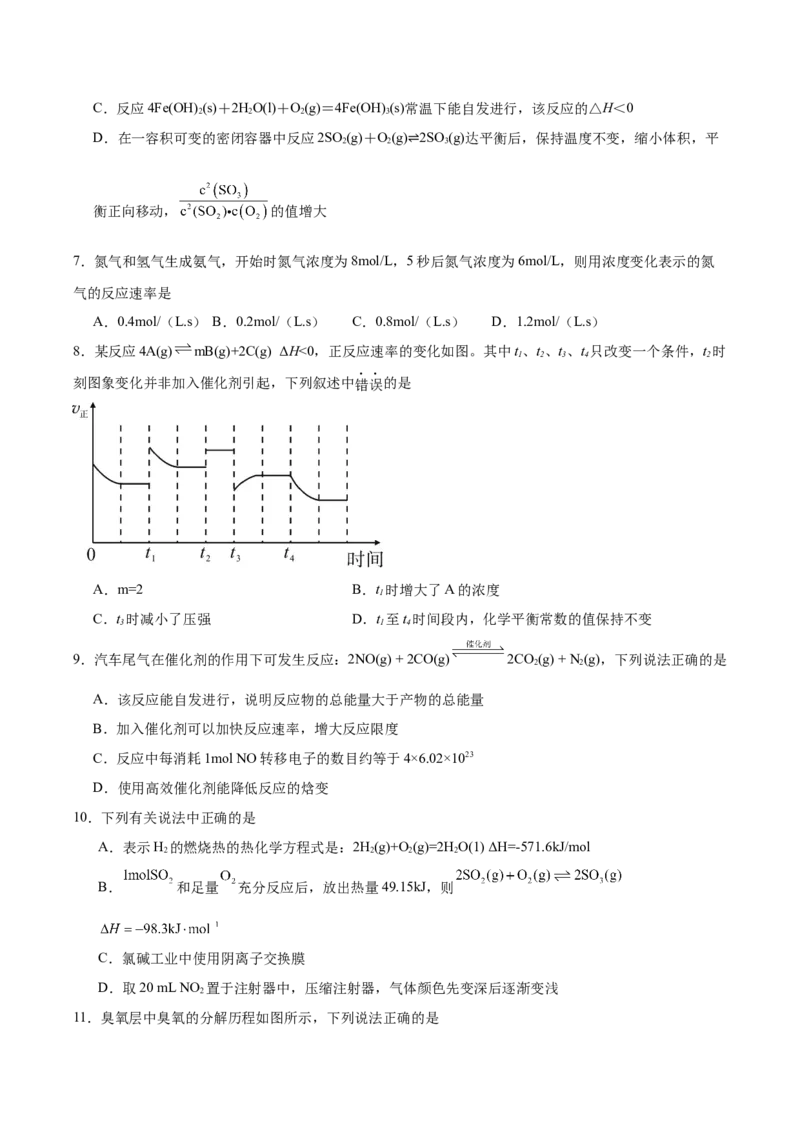
4.某反应由两步反应A→B→C构成,它的反应过程中能量变化曲线如下图所示(E 、E、E、E 表示活化
1 2 3 4
能)。下列有关叙述正确的是
A.两步反应均为吸热反应 B.加入催化剂会改变反应的焓变
C.三种物质中C最稳定 D.A→C反应中ΔH=E-E
1 2
5.下列溶液中,导电能力最强的是
A.1L0.1mol·L-1醋酸 B.1L0.1mol·L-1HSO 溶液
2 4
C.0.5L0.1mol·L-1盐酸 D.2L0.1mol·L-1HPO 溶液
3 4
6.下列叙述正确的是
A.合成氨反应放热,采用低温可以提高氨的生成速率
B.常温下,等物质的量浓度的CHCOOH溶液和HCl溶液中,水的电离程度相同
3C.反应4Fe(OH) (s)+2HO(l)+O(g)=4Fe(OH) (s)常温下能自发进行,该反应的△H<0
2 2 2 3
D.在一容积可变的密闭容器中反应2SO (g)+O(g) 2SO (g)达平衡后,保持温度不变,缩小体积,平
2 2 3
⇌
衡正向移动, 的值增大
7.氮气和氢气生成氨气,开始时氮气浓度为8mol/L,5秒后氮气浓度为6mol/L,则用浓度变化表示的氮
气的反应速率是
A.0.4mol/(L.s) B.0.2mol/(L.s) C.0.8mol/(L.s) D.1.2mol/(L.s)
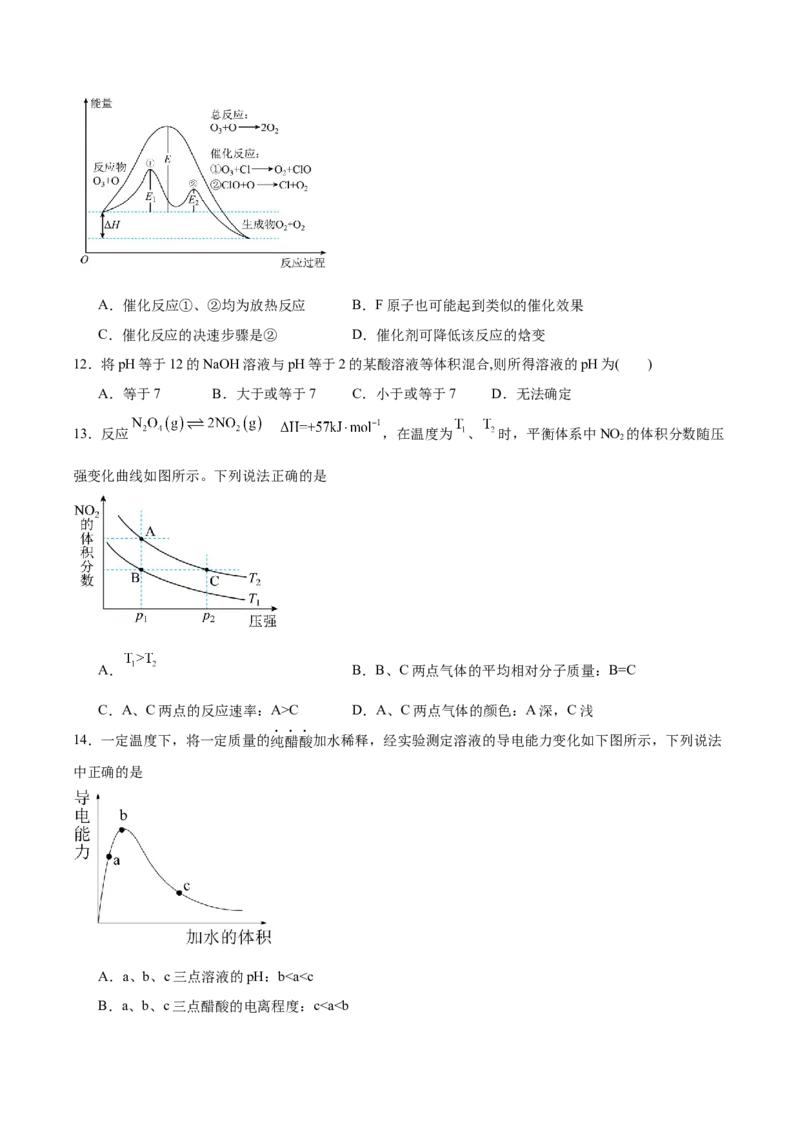
8.某反应4A(g) mB(g)+2C(g) ΔH<0,正反应速率的变化如图。其中t、t、t、t 只改变一个条件,t 时
1 2 3 4 2
刻图象变化并非加入催化剂引起,下列叙述中错误的是
A.m=2 B.t 时增大了A的浓度
1
C.t 时减小了压强 D.t 至t 时间段内,化学平衡常数的值保持不变
3 1 4
9.汽车尾气在催化剂的作用下可发生反应:2NO(g) + 2CO(g) 2CO(g) + N(g),下列说法正确的是
2 2
A.该反应能自发进行,说明反应物的总能量大于产物的总能量
B.加入催化剂可以加快反应速率,增大反应限度
C.反应中每消耗1mol NO转移电子的数目约等于4×6.02×1023
D.使用高效催化剂能降低反应的焓变
10.下列有关说法中正确的是
A.表示H 的燃烧热的热化学方程式是:2H(g)+O(g)=2HO(1) ΔH=-571.6kJ/mol
2 2 2 2
B. 和足量 充分反应后,放出热量49.15kJ,则
C.氯碱工业中使用阴离子交换膜
D.取20 mL NO 置于注射器中,压缩注射器,气体颜色先变深后逐渐变浅
2
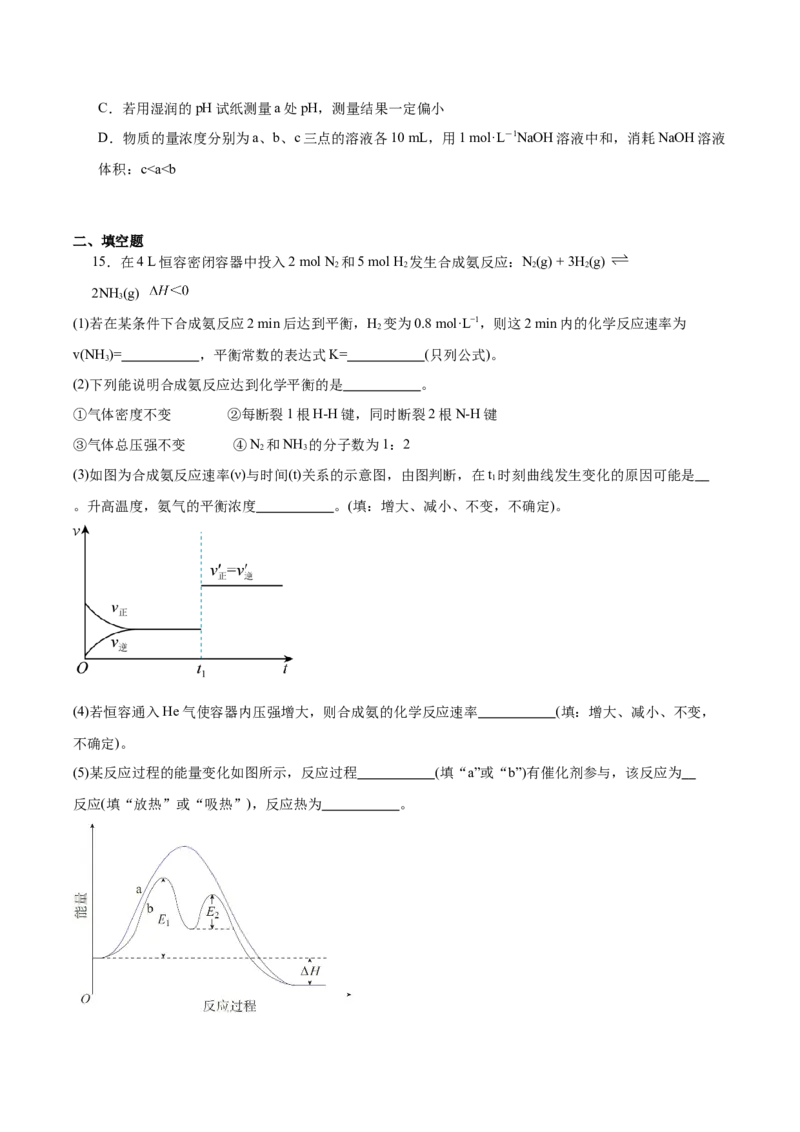
11.臭氧层中臭氧的分解历程如图所示,下列说法正确的是A.催化反应①、②均为放热反应 B.F原子也可能起到类似的催化效果
C.催化反应的决速步骤是② D.催化剂可降低该反应的焓变
12.将pH等于12的NaOH溶液与pH等于2的某酸溶液等体积混合,则所得溶液的pH为( )
A.等于7 B.大于或等于7 C.小于或等于7 D.无法确定
13.反应 ,在温度为 、 时,平衡体系中NO 的体积分数随压
2
强变化曲线如图所示。下列说法正确的是
A. B.B、C两点气体的平均相对分子质量:B=C
C.A、C两点的反应速率:A>C D.A、C两点气体的颜色:A深,C浅
14.一定温度下,将一定质量的纯醋酸加水稀释,经实验测定溶液的导电能力变化如下图所示,下列说法
中正确的是
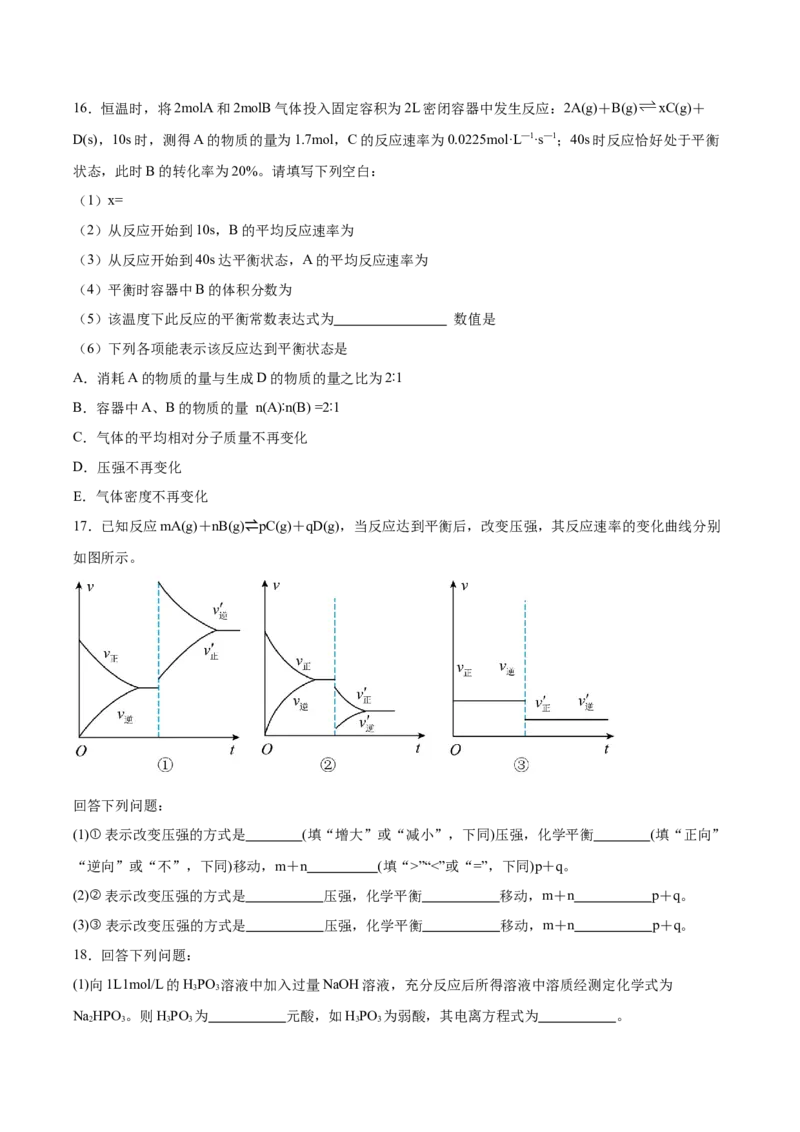
A.a、b、c三点溶液的pH:b”“<”或“=”,下同)p+q。
(2)②表示改变压强的方式是 压强,化学平衡 移动,m+n p+q。
(3)③表示改变压强的方式是 压强,化学平衡 移动,m+n p+q。
18.回答下列问题:
(1)向1L1mol/L的HPO 溶液中加入过量NaOH溶液,充分反应后所得溶液中溶质经测定化学式为
3 3
NaHPO 。则HPO 为 元酸,如HPO 为弱酸,其电离方程式为 。
2 3 3 3 3 3(2)向NaClO溶液中通入少量CO 的离子方程式(已知K(HClO)=3.0×10-8,K (H CO)=4.3×10-7,
2 a1 2 3
K (H CO)=5.6×10-11) 。
a2 2 3
(3)使Cl 和HO(g)通过灼热的炭层,生成HCl(g)和CO,当有35.5gCl 参与反应时释放出72.5kJ热量,写
2 2 2 2
出该反应的热化学方程式 。1.C
2.B
3.D
4.C
5.B
6.C
7.A
8.C
9.A
10.D
11.B
12.C
13.B
14.A
15.(1) 0.15
(2)②③
(3) 加入催化剂 减小
(4)不变
(5) b 放热 △H
16. 3 0.0075mol/(L·s) 0.01mol•(L·s)—1 40% 0.75 CE
17.(1) 增大 逆向 <
(2) 减小 正向 <
(3) 减小 不 =
18.(1) 二 HPO H++ 、 H++
3 3
(2)ClO-+CO +H O=HClO+
2 2
(3)2Cl (g)+2HO(g)+C(s)=4HCl(g)+CO (g) ΔH=-290kJ/mol(热方程式系数减半,焓变减半也可)
2 2 2