文档内容
2025 年秋季学期高二年级校联体第一次联考
化学 参考答案
题号 1 2 3 4 5 6 7
答案 D C D A B D C
题号 8 9 10 11 12 13 14
答案 A C A B C B D
1.D
【详解】金属的腐蚀、食物的腐败、塑料的老化都是对人类有害的;正确选项D。
2.C
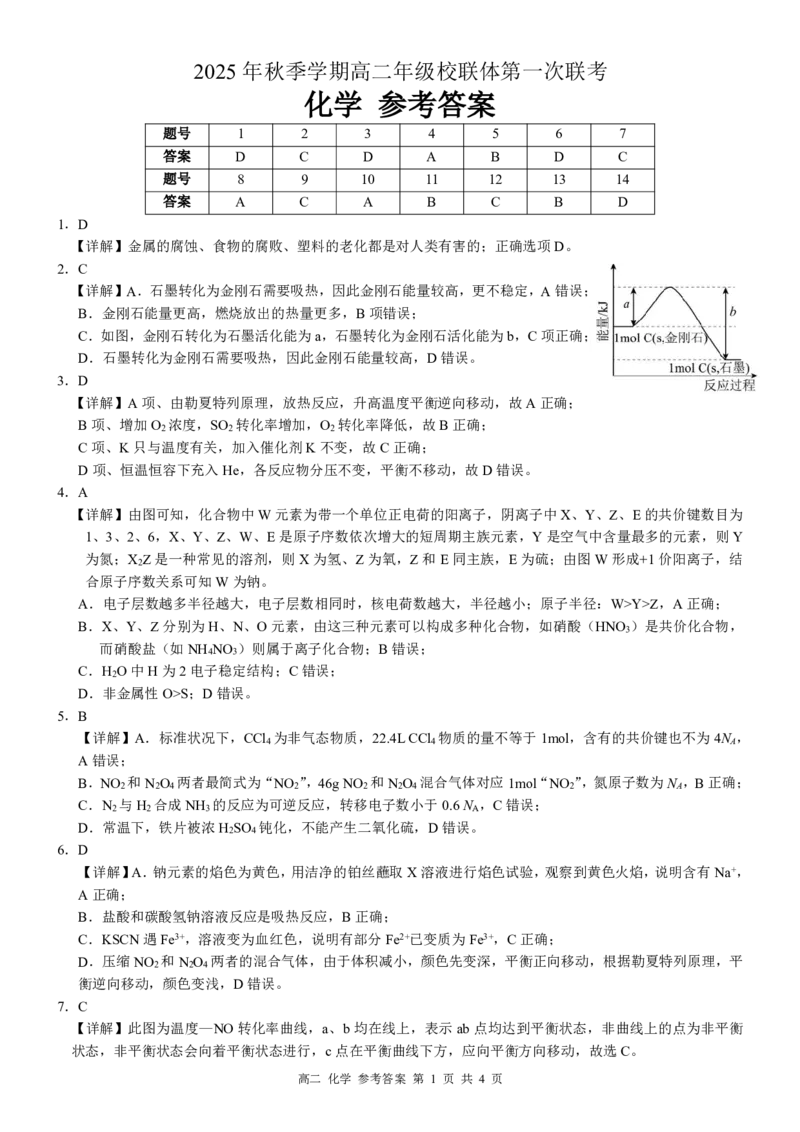
【详解】A.石墨转化为金刚石需要吸热,因此金刚石能量较高,更不稳定,A错误;
B.金刚石能量更高,燃烧放出的热量更多,B项错误;
C.如图,金刚石转化为石墨活化能为a,石墨转化为金刚石活化能为b,C项正确;
D.石墨转化为金刚石需要吸热,因此金刚石能量较高,D错误。
3.D
【详解】A项、由勒夏特列原理,放热反应,升高温度平衡逆向移动,故A正确;
B项、增加O 浓度,SO 转化率增加,O 转化率降低,故B正确;
2 2 2
C项、K只与温度有关,加入催化剂K不变,故C正确;
D项、恒温恒容下充入He,各反应物分压不变,平衡不移动,故D错误。
4.A
【详解】由图可知,化合物中W元素为带一个单位正电荷的阳离子,阴离子中X、Y、Z、E的共价键数目为
1、3、2、6,X、Y、Z、W、E是原子序数依次增大的短周期主族元素,Y是空气中含量最多的元素,则Y
为氮;X Z是一种常见的溶剂,则X为氢、Z为氧,Z和E同主族,E为硫;由图W形成+1价阳离子,结
2
合原子序数关系可知W为钠。
A.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;原子半径:W>Y>Z,A正确;
B.X、Y、Z分别为H、N、O元素,由这三种元素可以构成多种化合物,如硝酸(HNO )是共价化合物,
3
而硝酸盐(如NH NO )则属于离子化合物;B错误;
4 3
C.H O中H为2电子稳定结构;C错误;
2
D.非金属性O>S;D错误。
5.B
【详解】A.标准状况下,CCl 为非气态物质,22.4LCCl 物质的量不等于1mol,含有的共价键也不为4N ,
4 4 A
A错误;
B.NO 和N O 两者最简式为“NO ”,46gNO 和N O 混合气体对应1mol“NO ”,氮原子数为N ,B正确;
2 2 4 2 2 2 4 2 A
C.N 与H 合成NH 的反应为可逆反应,转移电子数小于0.6N ,C错误;
2 2 3 A
D.常温下,铁片被浓H SO 钝化,不能产生二氧化硫,D错误。
2 4
6.D
【详解】A.钠元素的焰色为黄色,用洁净的铂丝蘸取X溶液进行焰色试验,观察到黄色火焰,说明含有Na+,
A正确;
B.盐酸和碳酸氢钠溶液反应是吸热反应,B正确;
C.KSCN遇Fe3+,溶液变为血红色,说明有部分Fe2+已变质为Fe3+,C正确;
D.压缩NO 和N O 两者的混合气体,由于体积减小,颜色先变深,平衡正向移动,根据勒夏特列原理,平
2 2 4
衡逆向移动,颜色变浅,D错误。
7.C
【详解】此图为温度—NO转化率曲线,a、b均在线上,表示ab点均达到平衡状态,非曲线上的点为非平衡
状态,非平衡状态会向着平衡状态进行,c点在平衡曲线下方,应向平衡方向移动,故选C。
高二 化学 参考答案 第 1 页 共 4 页
{#{QQABCQSQoggAAoBAAAgCAQ2wCAEYkBCAACgGgBAUMAIBwQNABAA=}#}8.A
【详解】A.催化剂通过改变反应历程改变活化能,A正确;
B.CO +CH =CH COOH,反应的原子利用率为100%,B错误;
2 4 3
C.反应I存在C-H键的断裂,反应II不存在C-H键的断裂,C错误;
D.催化剂不改变反应的焓变,D错误。
9.C
【详解】该反应的特点是正反应为放热反应,反应后气体分子总数减小。
A.平衡常数仅与温度有关,升高温度,该反应平衡左移,平衡常数减小,A错误;
B.升高温度,该反应平衡左移,CO转化率减小,B错误;
C.平衡常数仅与温度有关,NO的物质的量增加,平衡常数不变,C正确;
D.增加氮气的物质的量,平衡左移,NO的转化率减小,D错误。
10.A
【详解】A.对于气体反应,增大压强,反应物浓度增大,单位体积内活化分子的数目增大,反应速率增大,
故A正确;
B.升高温度,更多分子吸收能量成为活化分子,但反应所需活化能不变,分子动能增加,分子运动加快,
有效碰撞频率增加,反应速率增大,故B错误;
C.选用适当的催化剂,降低反应的活化能,使更多分子成为活化分子,但不能使分子运动加快,活化分子
的数目和百分数增加,有效碰撞频率增加,反应速率增大,故C错误;
D.向反应体系中加入相同浓度的反应物,活化分子百分数不变,单位体积内活化分子数不变,有效碰撞速
率不变,D错误。
11.B
【详解】 3A(g) +B(g) 2C(g) +xD(g)
起始物质的量浓度(mol/L) 1.5 1.5 0 0
转化物质的量浓度(mol/L) 0.75 0.25 0.5 0.25x=1
平衡物质的量浓度(mol/L) 0.75 1.25 0.5 1
则x=4;B的转化率为0.25/1.5×100%=16.7%;平衡时A的浓度为0.75mol/L;因为反应后气体分子总
数增加,则达到平衡时,在相同温度下容器内混合气体的压强是更大的,故选B。
12.C
1
【详解】当c(X)=0.3mol/L,将容器容积缩小到原来的 时,若平衡不移动,则c(X)=0.6mol/L>0.5mol/L,
2
1
所以容器容积缩小到原来的 时,平衡向右移动。若Y为非气体,m<2m,缩小容积平衡应向左移动,所以
2
Y一定为气体,且m+n>2m,所以n>m。
13.B
【详解】KOH与CO 反应生成正盐KCO 的方程式为2KOH+CO=KCO+HO。KOH的物质的量为5mol·L-1×0.1L=0.5mol,
2 2 3 2 2 3 2
0.25
与其生成正盐的CO 为0.25mol。根据方程式C H (g)+ 13 O (g)=4CO (g)+5H O(l),生成0.25molCO ,消耗 molC H ,
2 4 10
2
2 2 2 2
4
4 10
放出的热量为QkJ。故1molC H 完全燃烧放出的热量为16QkJ,B符合题意。
4 10
14.D
【详解】A.由图象可知,随着温度升高,①的pK增大,则①的K减小,②的pK减小,则②的K增大,所
以①为放热反应,②为吸热反应,故A错误;
B.②为吸热反应,升高温度,平衡正向移动,故B错误;
C.a点反应①和②的K相等,N 浓度不一定相等,C 错误;
2
D.0℃时,①的pK=-10,①的K=1010,,一个反应的K>105 可认为反应进行得基本完全了,故D正确。
高二 化学 参考答案 第 2 页 共 4 页
{#{QQABCQSQoggAAoBAAAgCAQ2wCAEYkBCAACgGgBAUMAIBwQNABAA=}#}二、非选择题
15.(1)不能 Cu传热快,热量损失大
(2)-57.1kJ·mol-1
(3)大于 更多 相等
(4)AD
【详解】(1)不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体,导热快,热量损失多。
(2)第1次实验盐酸和NaOH溶液起始平均温度为20.25℃,反应前后温度差为:3.45℃;第2次实验
盐酸和NaOH溶液起始平均温度为20.40℃,反应前后温度差为:3.40℃;第3次实验盐酸和NaOH
溶液起始平均温度为21.55℃,反应前后温度差为:3.35℃;第4次实验盐酸和NaOH溶液起始平
均温度为20.20℃,反应前后温度差为:4.5℃,与前三次偏差过大,舍去。三次温度差的平均值为
3.40℃,50mL0.50 molL−1盐酸、50mL0.55molL−1NaOH 溶液的质量 m=100mL×1g/mL=100g,
c=4.2J/(g℃),代入公式Q=cm T得生成0.025mol的水放出热量Q=4.2J/(g ℃)×100g×3.40℃=1.428kJ,
⋅ ⋅
1mol
即生成0.⋅025mol的水放出热量△1.428kJ,所以生成1mol的水放出热量为1.⋅428kJ× =57.1kJ,
0.025mol
即该实验测得的中和热 H=−57.1kJ/mol;
(3)氨水为弱电解质,电离过程需要吸收能量,反应放出的热量相对应低一些,故所求出的热量Q偏
△
低,导致 H 大于 H;反应放出的热量和所用酸以及碱的量的多少有关,改用60mL0.50mol/L盐
1
酸跟50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,
△ △
但是中和热均是强酸和强碱反应生成1mol水时放出的热,中和热相等;
(4)A、测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度
计示数变化值减小,所以导致实验测得放热的数值偏小,故A正确;
B、若将0.5mol·L-1硫酸当成0.5mol·L-1盐酸,H+的物质的量增加,生成水的物质的量增加,放
出的热量偏高,故B错误;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、在量取盐酸时俯视计数,会使得实际量取体积低于所要量的体积,酸不足,无法完全反应,导
致实验测得放热的数值偏小,故D正确;故选AD。
16.(1)放热 307
(2)AC
(3)C
(4)-1160kJ·mol-1
(5)正 N H 2O2 4e N 2H O
2 4 2 2
【详解】(1)反应焓变为负值,放热反应。ΔH=2×799+3×436-2×467-3×414-x-472=-49kJ/mol,解得
x=307
(2)NO 是引起光化学烟雾的主要原因之一,A正确;
x
B.第一步反应速率最慢,对总反应速率起决定作用,B错误;
C.第一步反应速率比第二步慢,说明活化能比第二步大,C正确;
D.NO 为反应的中间产物,不是催化剂,D错误;
3
故选AC。
(3)天然气、煤、石油属于化石能源,核能、太阳能、生物质能、风能、氢能属于新能源,故选C
(4)已知反应①CH (g)+4NO (g)=4NO(g)+CO (g)+2H O(g) ΔH =-574kJ·mol-1
4 2 2 2 1
反应②CH (g)+2NO (g)=CO (g)+2H O(g)+N (g) ΔH =-867kJ·mol-1
4 2 2 2 2 2
根据盖斯定律,2×②-①得到CH +4NO=CO +2N +2H O(g),则ΔH=2×(-867kJ·mol-1)-(-574
4 2 2 2
kJ·mol-1)=-1160kJ·mol-1
(5)氧气在正极反应得电子,液态肼为负极反应,根据图示,负极电极反应式为
N H 2O2 4e N 2H O。
2 4 2 2
17.(1)
(2)abc
(3)能
(4)高 低
高二 化学 参考答案 第 3 页 共 4 页
{#{QQABCQSQoggAAoBAAAgCAQ2wCAEYkBCAACgGgBAUMAIBwQNABAA=}#}(5)a
(6)-1
【详解】(1)H S是共价化合物电子式为
2
(2)升高温度,反应速率增大,故a符合;b.增大水蒸气浓度,反应速率增大,故b符合;c.加入催
化剂,反应速率增大,故c符合;d.降低压强,反应速率减小,故d不符合;故选abc;
(3)合成氨反应气体体积减小,体系混乱度减小∆S<0,由∆H<0,自发进行的综合判据∆G=∆H-T∆S<0,
反应在低温下能自发;
(4)升高温度,反应速率加快,则高温有利于提高反应速率,合成氨是放热反应,降低温度平衡正向移
动,低温有利于提高平衡转化率;
(5)a.由题图可知,300℃时,复合催化剂催化时合成氨反应的反应速率比单一催化剂催化时大很多,
说明300℃时复合催化剂比单一催化剂效率更高,a正确;b.350℃时,采用Fe-LiH催化剂效率
更高,而不是Mn-LiH,b错误;c.温度过高,复合催化剂可能会失去活性,催化效率反而降低,
c错误;故选a;
(6)将实验1、3中数据分别代入合成氨的速率方程可得:①q=k·mα·nβ·pγ,③10q=k·mα·nβ·(0.1p)γ,可得
γ=-1,
18.(1)ABC
0.00840.002
(2)L >
1
0.04860.0162
(3)①反应I
②不是 图中P点甲烷产率不是最大,所以反应还没有达到平衡,P点不是处于平衡状态
③(可能原因1)该反应是放热反应,达到平衡后升高温度,平衡逆向移动;(原因2)也可能是未平衡,温
度升高催化剂活性降低导致速率下降,产率下降
【详解】(1)由化学平衡特点可知,体系压强随反应进行发生变化,若压强不变时,即为平衡,A正确;气体的
平均摩尔质量随反应进行发生变化,若平均摩尔质量不变时,能说明到达平衡,B正确;CO 的体
2
积分数随反应进行发生变化,保持不变时,即为平衡,C正确;v (CO )=3v (H )时,正逆反应不
正 2 逆 2
相等,不平衡,D错误;气体的密度随反应进行没有变化,不能说明到达平衡,E错误;
(2)CO 物质的量越大,CO 的平衡转化率越低,H 的平衡转化率越高,所以其中H 的转化率随n的
2 2 2 2
变化的曲线为L ;由图甲可知,CO 和H 的平衡转化率都为20%,计算反应I的平衡常数需列如
1 2 2
2CO 6H CH 4HO
2 2 2 4 2
起始/mol n 0.3 0 0
下三段式: 1
转变/mol 0.02 0.06 0.01 0.04
平衡/mol n10.02 0.24 0.01 0.04
0.02 mol
列CO 的平衡转化率 100%20%,解得n =0.1,所以CO 平衡时物质的量为0.08mol,
2 1 2
n1 mol
0.00840.002
刚性密闭容器的体积为5L,该温度下反应I的平衡常数K L3mol3;若改为初始
0.04860.0162
容积为5L的恒压密闭容器,对于气体分子数目减少的反应,恒容换成恒压相当于增大平衡时压强,
平衡正向移动,转化率提高,平衡时CO 的转化率a(CO )>20%;
2 2
(3)①由图中存在的物质可知,840℃时主要存在乙烯,故催化剂主要选择生成乙烯的反应;
②从图中可知P点甲烷产率不是最大,所以反应还没有达到平衡,P点不是处于平衡状态;
③(可能原因1)该反应是放热反应,达到平衡后升高温度,平衡逆向移动;(原因2)也可能是未平衡,
温度升高催化剂活性降低导致速率下降,产率下降。
高二 化学 参考答案 第 4 页 共 4 页
{#{QQABCQSQoggAAoBAAAgCAQ2wCAEYkBCAACgGgBAUMAIBwQNABAA=}#}