文档内容
2025—2026 学年度上学期 2024 级
10 月月考化学试卷
命题人:李昌坤 审题人:刘安源
时间:75分钟 分数:100分
可能用到的相对原子质量:H 1 C 12 N 16 O 16 Na 23 S 32 Cl 35.5 Ca 40 Fe 56
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.下列有关说法错误的是
A.稀土是我国反制美国霸权的重要资源,稀土元素都是金属元素
B.人工智能依赖于硅基芯片,硅及部分其他元素的单质具有半导体的特性
C.我国的固态电池研发取得突破性成就,与传统锂离子电池相比,固态电池是指电极材料
是固体。
D.出土于荆州的虎座鸟架鼓是东周时期的漆器,其上面使用的生漆是天然高分子材料
2.下列说法错误的是
A.101kPa时,1molN H 完全燃烧生成液态水和二氧化氮气体放出的热量是肼的燃烧热
2 4
B.等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
C.在等温条件下,化学反应体系向环境释放或从环境吸收的热量是反应热
D.焓是与内能有关的物理量,等压条件下进行的化学反应其反应热等于焓变。
3.下列关于可逆反应的叙述正确的是( )
A.放热反应一定可以自发进行
B.只有绝热体系的自发过程才向着熵增的方向进行
C.外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
D.等温等压条件下的反应体系中可用自由能变化来判断反应的方向
4.下列关于反应焓变计算的方法正确的是( )
A.反应物的焓减生成物的焓 B.正反应的活化能减逆反应的活化能
C.生成物键能之和减反应物键能之和 D.反应物能量减生成物能量
5.根据能量变化示意图(其中a、b、c均大于0),下列说法正确的是( )
1
学科网(北京)股份有限公司A.断开1 mol HCl(g)中的H−Cl键需要吸收b kJ能量
B.反应H(g)+Cl (g)=2HCl(g),反应物的总能量小于生成物的总能量
2 2
C.H(g)+Cl (g)=2HCl(g) ΔH=−(a−b)kJ∙mol−1
2 2
D.由题可知b>c
6.工业合成氨是对解决人类粮食问题做出了突出性的贡献,下列有关说法不正确的是
A.工业合成氨的基础原料是煤炭和空气,CO 是其副产品
2
B.工业合成氨中未转化的合成气循环利用,可以提高反应物的转化率
C.一般选择400-500℃的条件是从反应速率、催化剂活性、设备及成本等多方面考量的结果
D.将生成的氨气及时液化分离,可促进平衡正向移动,加快反应速率
7.通过在隧道的路面涂上一种光催化剂涂料,可将汽车尾气中的NO和CO转化成N 和CO,发
2 2
生的反应为2NO(g)+2CO(g) N(g)+2CO (g) ΔH=x(x<0)kJ·mol-1,向某恒温恒容密闭容器中
2 2
通入1 mol NO(g)和1 mol CO(g)发生上述反应,下列说法正确的是( )
A.反应中4种物质含有的共价键均为极性共价键
B.使用光催化剂能增大该反应的活化能,从而增大有效碰撞频率,加快化学反应速率
C.当混合气体的密度不再变化时,说明该反应达到平衡状态
D.反应达到平衡后,升高温度,再次达到平衡时NO的体积分数增大
8.下列实验操作及现象得出的相应结论正确的是
选项 实验及现象 结论
向1mL0.1mol/LK CrO 溶液中加入 c(H+)增大,平衡
2 4
A
10mL1.0mol/LHI溶液,黄色溶液变橙色 2CrO
4
2-+2H+ Cr
2
O
7
2-+H
2
O正向进行
B 对CuCl 2 溶液加热,溶液颜色由蓝色变为 [Cu(H 2 O) 4 ]2+ +4Cl- [CuCl 4 ]2- + 4H 2 O
黄色 反应正向吸热
向水溶液平衡体系
C FeCl +3KSCN Fe(SCN) +3KCl 中加入 平衡逆向移动,溶液的颜色加深
3 3
适量KCl固体
分别向两支装有2mL0.05mol/L的KMnO
4
D 溶液的试管中滴加 2mL0.05mol/L 和 验证浓度对反应速率的影响
2mL0.02mol/L的草酸溶液,前者褪色更快
2
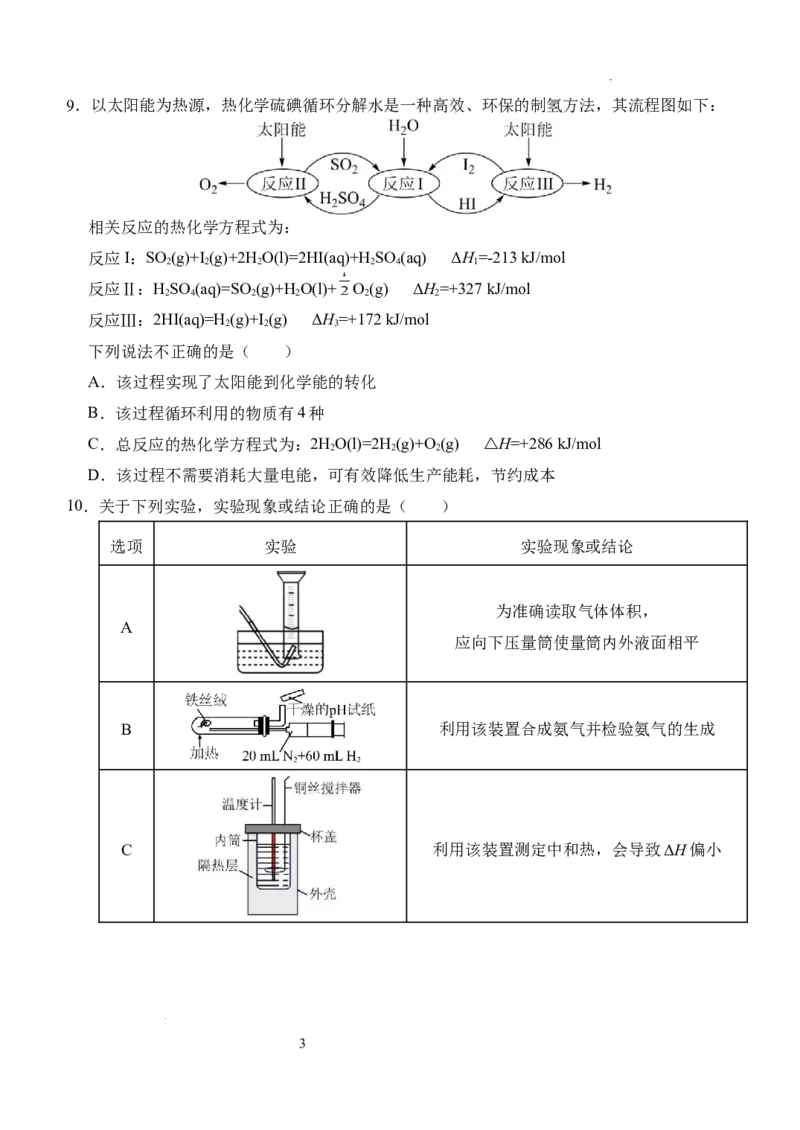
学科网(北京)股份有限公司9.以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
相关反应的热化学方程式为:
反应I:SO (g)+I (g)+2HO(l)=2HI(aq)+H SO (aq) ΔH=-213 kJ/mol
2 2 2 2 4 1
反应Ⅱ:HSO (aq)=SO(g)+HO(l)+ O(g) ΔH=+327 kJ/mol
2 4 2 2 2 2
反应Ⅲ:2HI(aq)=H(g)+I (g) ΔH=+172 kJ/mol
2 2 3
下列说法不正确的是( )
A.该过程实现了太阳能到化学能的转化
B.该过程循环利用的物质有4种
C.总反应的热化学方程式为:2HO(l)=2H(g)+O(g) △H=+286 kJ/mol
2 2 2
D.该过程不需要消耗大量电能,可有效降低生产能耗,节约成本
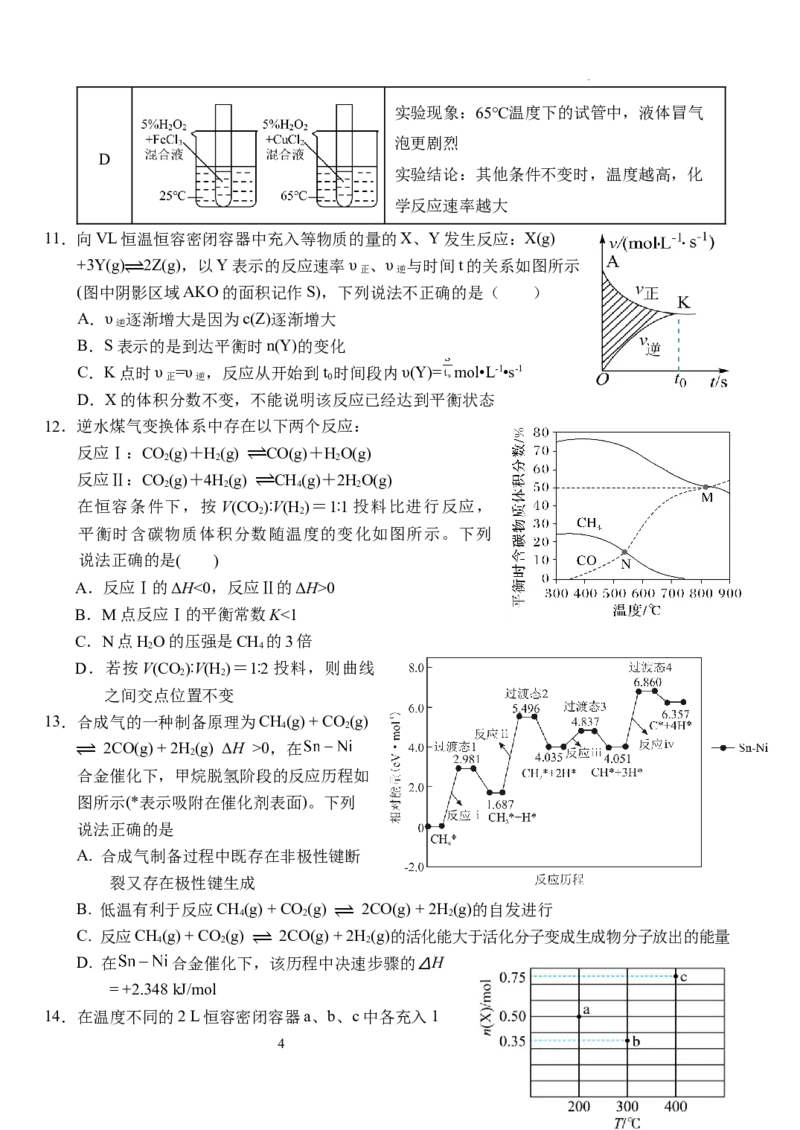
10.关于下列实验,实验现象或结论正确的是( )
选项 实验 实验现象或结论
为准确读取气体体积,
A
应向下压量筒使量筒内外液面相平
B 利用该装置合成氨气并检验氨气的生成
C 利用该装置测定中和热,会导致ΔH偏小
3
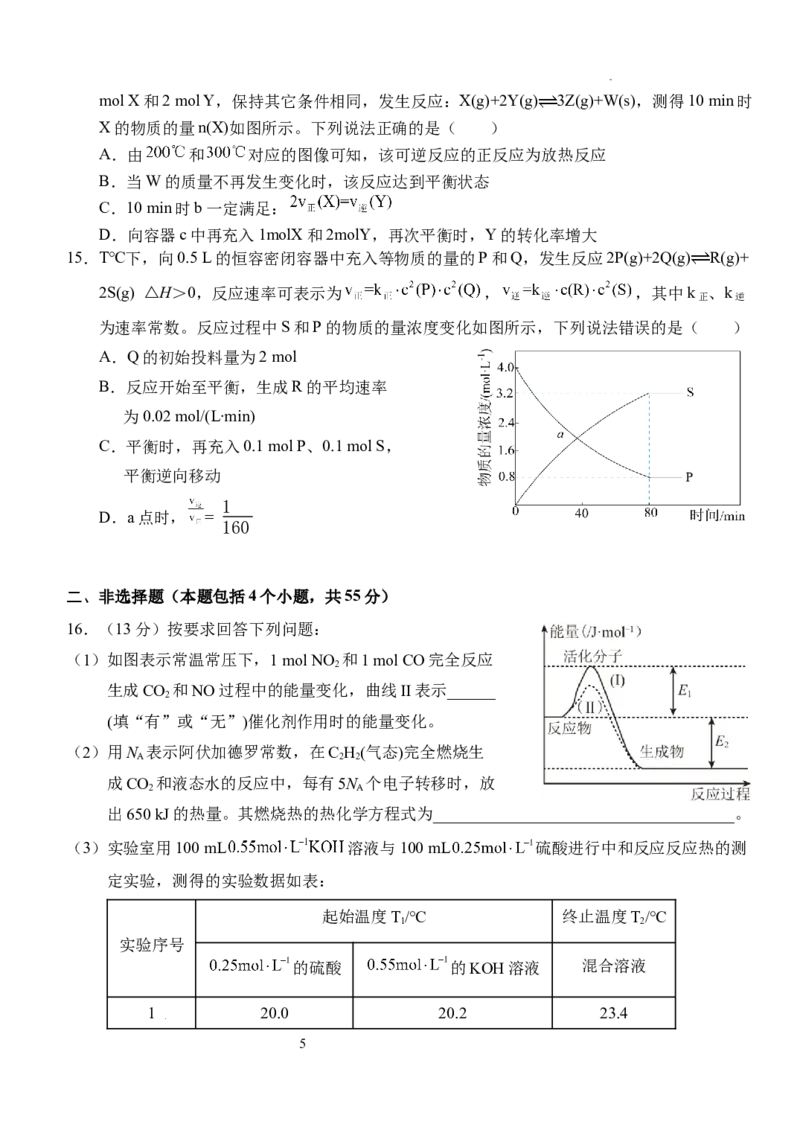
学科网(北京)股份有限公司实验现象:65℃温度下的试管中,液体冒气
泡更剧烈
D
实验结论:其他条件不变时,温度越高,化
学反应速率越大
11.向VL恒温恒容密闭容器中充入等物质的量的X、Y发生反应:X(g)
+3Y(g) 2Z(g),以Y表示的反应速率υ 、υ 与时间t的关系如图所示
正 逆
(图中阴影区域AKO的面积记作S),下列说法不正确的是( )
A.υ 逐渐增大是因为c(Z)逐渐增大
逆
B.S表示的是到达平衡时n(Y)的变化
C.K点时υ =υ ,反应从开始到t 时间段内υ(Y)= mol•L-1•s-1
正 逆 0
D.X的体积分数不变,不能说明该反应已经达到平衡状态
12.逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g)
2 2 2
反应Ⅱ:CO(g)+4H(g) CH(g)+2HO(g)
2 2 4 2
在恒容条件下,按 V(CO)∶V(H )=1∶1投料比进行反应,
2 2
平衡时含碳物质体积分数随温度的变化如图所示。下列
说法正确的是( )
A.反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0
B.M点反应Ⅰ的平衡常数K<1
C.N点HO的压强是CH 的3倍
2 4
D.若按V(CO)∶V(H )=1∶2投料,则曲线
2 2
之间交点位置不变
13.合成气的一种制备原理为CH(g) + CO (g)
4 2
2CO(g) + 2H (g) ∆H >0,在
2
合金催化下,甲烷脱氢阶段的反应历程如
图所示(*表示吸附在催化剂表面)。下列
说法正确的是
A. 合成气制备过程中既存在非极性键断
裂又存在极性键生成
B. 低温有利于反应CH(g) + CO (g) 2CO(g) + 2H (g)的自发进行
4 2 2
C. 反应CH(g) + CO (g) 2CO(g) + 2H (g)的活化能大于活化分子变成生成物分子放出的能量
4 2 2
D. 在 合金催化下,该历程中决速步骤的∆H
= +2.348 kJ/mol
14.在温度不同的2 L恒容密闭容器a、b、c中各充入1
4
学科网(北京)股份有限公司mol X和2 mol Y,保持其它条件相同,发生反应:X(g)+2Y(g) 3Z(g)+W(s),测得10 min时
X的物质的量n(X)如图所示。下列说法正确的是( )
A.由 和 对应的图像可知,该可逆反应的正反应为放热反应
B.当W的质量不再发生变化时,该反应达到平衡状态
C.10 min时b一定满足:
D.向容器c中再充入1molX和2molY,再次平衡时,Y的转化率增大
15.T℃下,向0.5 L的恒容密闭容器中充入等物质的量的P和Q,发生反应2P(g)+2Q(g) R(g)+
2S(g) △H>0,反应速率可表示为 , ,其中k 、k
正 逆
为速率常数。反应过程中S和P的物质的量浓度变化如图所示,下列说法错误的是( )
A.Q的初始投料量为2 mol
B.反应开始至平衡,生成R的平均速率
为0.02 mol/(L∙min)
C.平衡时,再充入0.1 mol P、0.1 mol S,
平衡逆向移动
1
D.a点时, =
160
二、非选择题(本题包括4个小题,共55分)
16.(13分)按要求回答下列问题:
(1)如图表示常温常压下,1 mol NO 和1 mol CO完全反应
2
生成CO 和NO过程中的能量变化,曲线II表示______
2
(填“有”或“无”)催化剂作用时的能量变化。
(2)用N 表示阿伏加德罗常数,在C H(气态)完全燃烧生
A 2 2
成CO 和液态水的反应中,每有5N 个电子转移时,放
2 A
出650 kJ的热量。其燃烧热的热化学方程式为_____________________________________。
(3)实验室用100 mL 溶液与100 mL 硫酸进行中和反应反应热的测
定实验,测得的实验数据如表:
起始温度T/℃ 终止温度T/℃
1 2
实验序号
的硫酸 的KOH溶液 混合溶液
1 20.0 20.2 23.4
5
学科网(北京)股份有限公司2 20.3 20.7 25.4
3 20.4 20.6 23.9
4 20.2 20.4 23.5
①已知:在稀溶液中,可近似认为 的KOH溶液和 的硫酸的密度都
是 ,反应后生成溶液的比热容 。据该学生的实验数据计算,该实
验测得的中和反应反应热ΔH=________(结果保留三位有效数字) 。
②分析下列因素会导致测得的中和反应反应热的数值变化情况(填“偏大”、“偏小”或
“无影响”)
a.量取硫酸时仰视读数:________;
b.测定KOH溶液温度的温度计未洗涤直接用于测定硫酸的温度:________。
(4)已知弱酸、弱碱的电离过程为吸热过程。若某化学兴趣小组用100 mL 醋酸代替
100 mL 硫酸进行上述实验,所测得的中和反应反应热(ΔH)偏 (“大”或者
“小”),
17.(14分)甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:NaSO+H SO =Na SO +SO↑+S↓+H O,反应过程中溶液出现乳白色浑浊和
2 2 3 2 4 2 4 2 2
有刺激性气味的气体。
【实验用品】0.1 mol/L Na SO 溶液、0.1 mol/L H SO 溶液、蒸馏水,试管、烧杯、量筒、胶头
2 2 3 2 4
滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
(1)为保证实验的准确性和可靠性,利用该装置进行实验前应先
进行的操作是________________。除如图所示的实验用品外,
还需要的实验仪器是__________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出在2 min内的反应速率
υ(H+)=0.02 mol/(L·min),而该速率值比实际值偏小,其原因是
_________________________。
实验二:乙同学得到各组实验数据如下表。
实验 NaSO 溶液 HSO 溶液 蒸馏水 温度/℃
2 2 3 2 4
6
学科网(北京)股份有限公司编号
浓度/(mol/L) 体积/mL 浓度/(mol/L) 体积/mL 体积/mL
Ⅰ 0.1 1.5 0.1 1.5 V 20
Ⅱ 0.1 2.5 0.1 1.5 8 a
Ⅲ 0.1 2.5 0.1 1.5 8 30
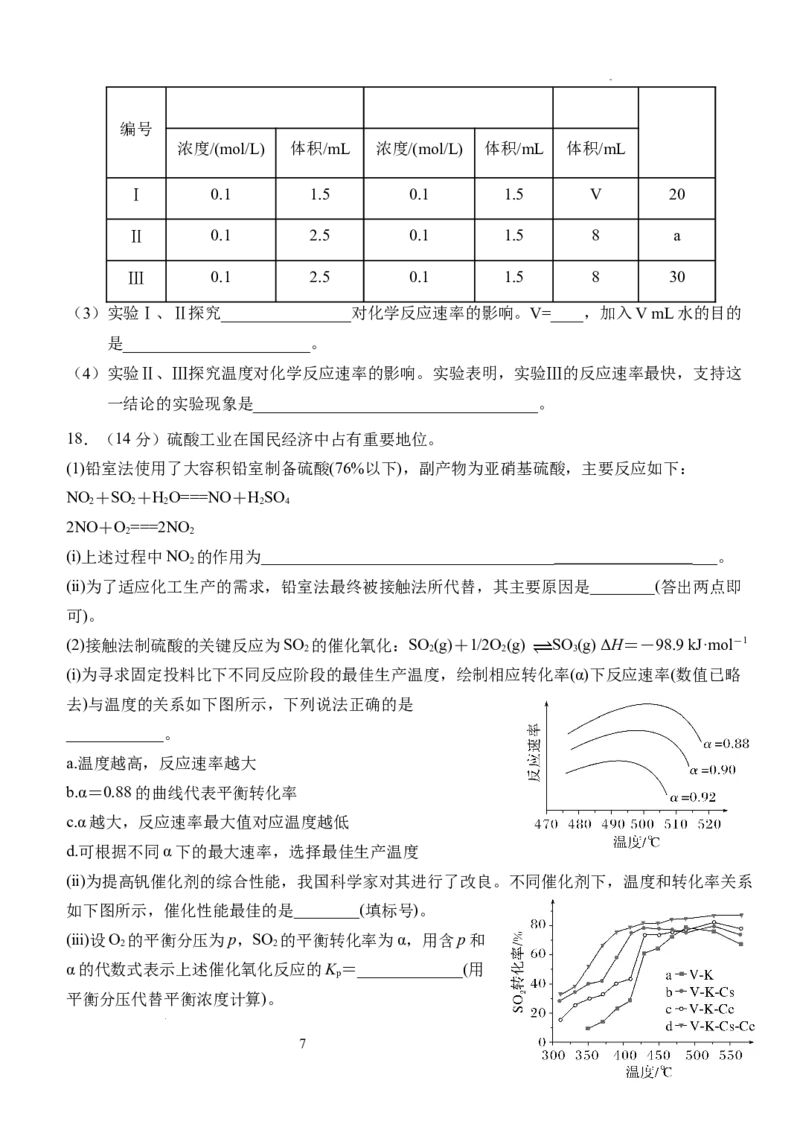
(3)实验Ⅰ、Ⅱ探究________________对化学反应速率的影响。V=____,加入V mL水的目的
是_______________________。
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这
一结论的实验现象是___________________________________。
18.(14分)硫酸工业在国民经济中占有重要地位。
(1)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO +HO===NO+HSO
2 2 2 2 4
2NO+O===2NO
2 2
(ⅰ)上述过程中NO 的作用为____________________________________ ___。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是________(答出两点即
可)。
(2)接触法制硫酸的关键反应为SO 的催化氧化:SO (g)+1/2O (g) SO (g) ΔH=-98.9 kJ·mol-1
2 2 2 3
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略
去)与温度的关系如下图所示,下列说法正确的是
____________。
a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系
如下图所示,催化性能最佳的是________(填标号)。
(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α,用含p和
2 2
α的代数式表示上述催化氧化反应的K =_____________(用
p
平衡分压代替平衡浓度计算)。
7
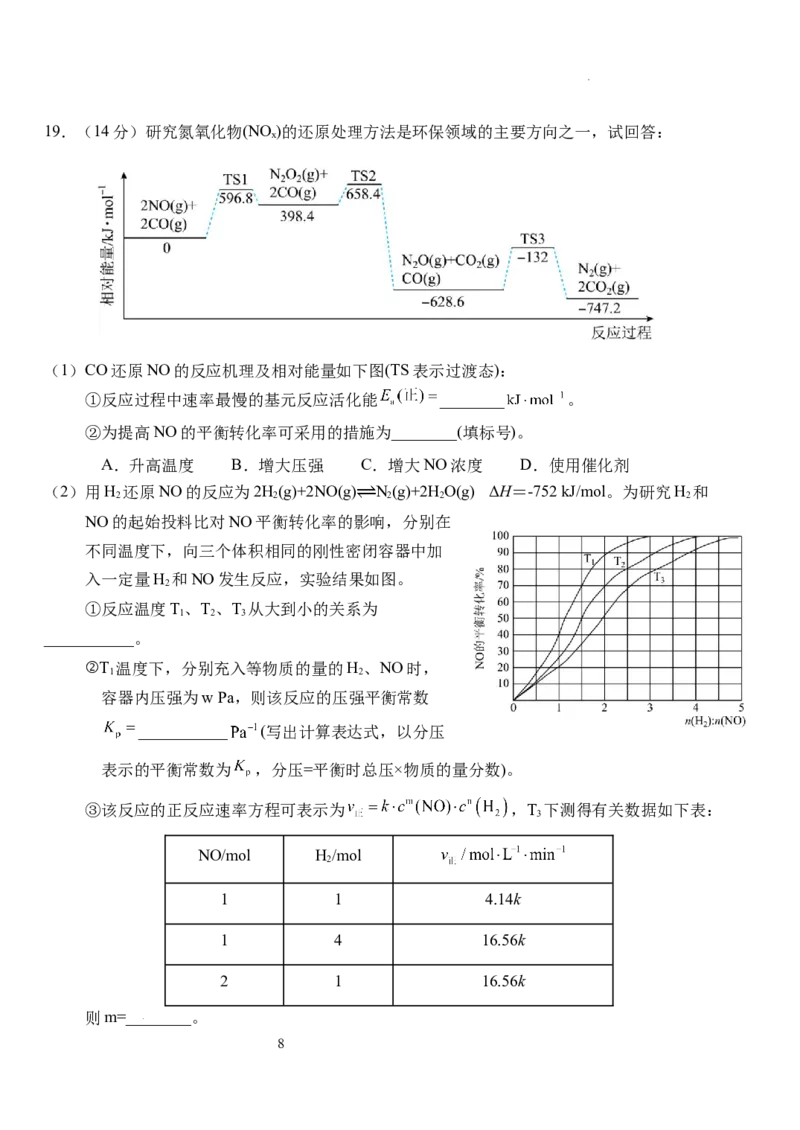
学科网(北京)股份有限公司19.(14分)研究氮氧化物(NO )的还原处理方法是环保领域的主要方向之一,试回答:
x
(1)CO还原NO的反应机理及相对能量如下图(TS表示过渡态):
①反应过程中速率最慢的基元反应活化能 ________ 。
②为提高NO的平衡转化率可采用的措施为________(填标号)。
A.升高温度 B.增大压强 C.增大NO浓度 D.使用催化剂
(2)用H 还原NO的反应为2H(g)+2NO(g) N(g)+2HO(g) ΔH=-752 kJ/mol。为研究H 和
2 2 2 2 2
NO的起始投料比对NO平衡转化率的影响,分别在
不同温度下,向三个体积相同的刚性密闭容器中加
入一定量H 和NO发生反应,实验结果如图。
2
①反应温度T、T、T 从大到小的关系为
1 2 3
___________。
②T 温度下,分别充入等物质的量的H、NO时,
1 2
容器内压强为w Pa,则该反应的压强平衡常数
___________ (写出计算表达式,以分压
表示的平衡常数为 ,分压=平衡时总压×物质的量分数)。
③该反应的正反应速率方程可表示为 ,T 下测得有关数据如下表:
3
NO/mol H/mol
2
1 1 4.14k
1 4 16.56k
2 1 16.56k
则m=________。
8
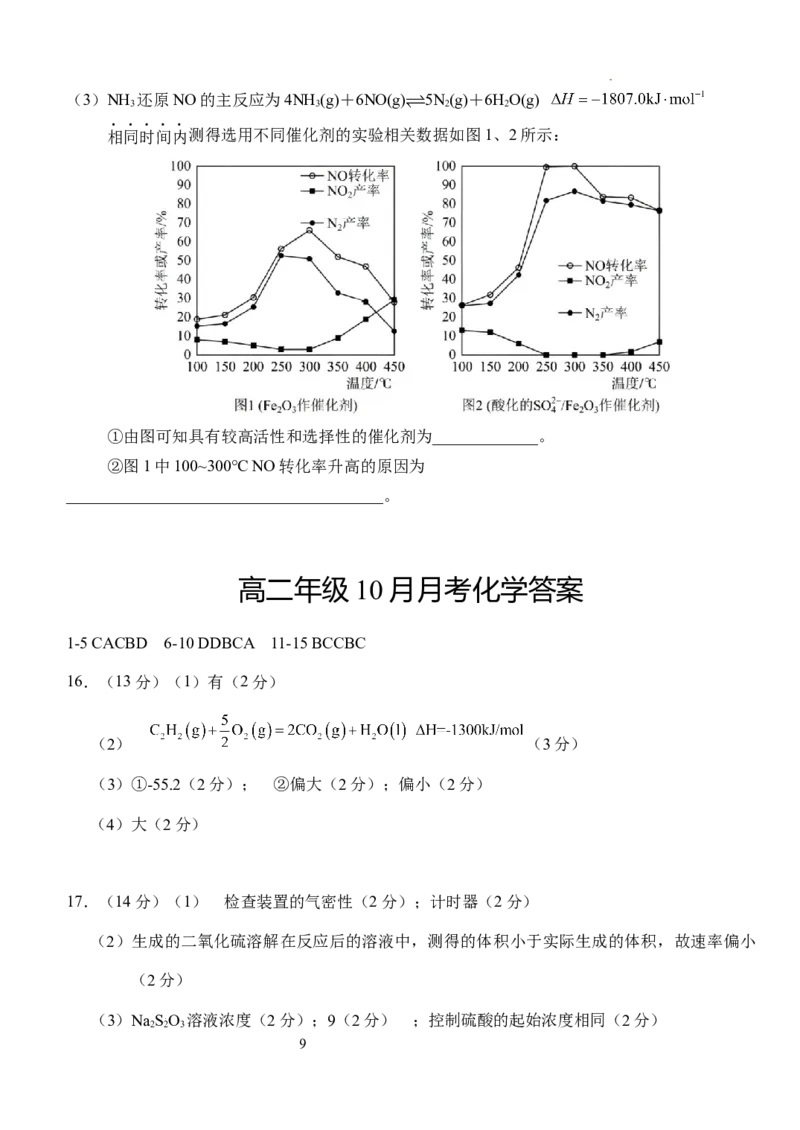
学科网(北京)股份有限公司(3)NH 还原NO的主反应为4NH (g)+6NO(g) 5N(g)+6HO(g)
3 3 2 2
相同时间内测得选用不同催化剂的实验相关数据如图1、2所示:
①由图可知具有较高活性和选择性的催化剂为_____________。
②图1中100~300℃ NO转化率升高的原因为
_______________________________________。
高二年级 10 月月考化学答案
1-5 CACBD 6-10 DDBCA 11-15 BCCBC
16.(13分)(1)有(2分)
(2) (3分)
(3)①-55.2(2分); ②偏大(2分);偏小(2分)
(4)大(2分)
17.(14分)(1) 检查装置的气密性(2分);计时器(2分)
(2)生成的二氧化硫溶解在反应后的溶液中,测得的体积小于实际生成的体积,故速率偏小
(2分)
(3)NaSO 溶液浓度(2分);9(2分) ;控制硫酸的起始浓度相同(2分)
2 2 3
9
学科网(北京)股份有限公司(4)实验III观察到出现浑浊所需的时间更短(2分)
18.(1)(ⅰ)催化剂(2分) (ⅱ)铅室法制得的产品中存在亚硝基硫酸杂质、铅室法生产硫酸过程中
需使用有毒物质氮氧化物(2分)
(2)(ⅰ)cd(4分) (ⅱ)d(2分) (ⅲ) α/(1-α)p1/2 (4分)
19.(14分)(1)596.8(2分);B(2分)
(2)T>T>T(2分); 或 (2分);2(2分)
3 2 1
(3)①酸化的 (2分);
②图1中100℃至300℃,反应未达到平衡状态,温度越高,反应速率越大,NO转化率
升高(2分)
10
学科网(北京)股份有限公司