文档内容
高二联考化学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号,考场号,座位号填写在答题卡上。2.回答选择题
时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版选择性必修1第一章至第三章第三节。
5.可能用到的相对原子质量:H-1 C-12 O-16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与生产,生活密切相关,下列事实与盐类的水解无关的是
A.用热的纯碱溶液洗涤餐具上的油污 B.用可溶性的铁盐作净水剂
C.草木灰与铵态氮肥不能混合使用 D.侯氏制碱法制碳酸氢钠
2.下列描述涉及的主要化学反应中反应物的总能量小于生成物的总能量的是
A.碳酸钙的分解 B.煤炭的燃烧
C.稀释浓硫酸 D.工业上合成氨反应
3.下列物质属于强电解质的是
A.Cu B.CO C.CHCOOH D.NaCO
3 2 3
4.下列属于水解方程式且书写正确的是
A. +H O HSO +OH- B.OH-+ +H O
2 2 3 2
C.HO+HO HO++ OH- D. +2H O HCO+OH-
2 2 3 2 2 3
5.废碳再生的“绿色甲醇”作为燃料可实现碳循环内的零排放。下列表示甲醇燃烧热的热化学方程式正确
的是(已知1g甲醇完全燃烧时放出22.68kJ热量)
A.2CHOH(l)+3O (g)=2CO (g)+4HO(l) H=-l451.52kJ/mol
3 2 2 2
△
B.CHOH(1)+ O(g)=CO (g)+2HO(g) H=-22.68kJ/mol
3 2 2 2
△
C. CHOH(1)+ O(g)=CO (g)+2HO(l) H=-725.76kJ/mol
3 2 2 2
△
D. CHOH(1)+ O(g)=CO(g)+2HO(l) H=-725.76kJ/mol
3 2 2
△
6.向CHCOOH溶液中滴入过量NaOH溶液,溶液中水电离出的H+的物质的量浓度c(H+)随加入NaOH溶液
3
的体积(V)的变化曲线正确的是A. B.
C. D.
7.下列说法正确的是
A.化学反应一定伴随能量变化,有能量变化的未必是化学反应
B.催化剂不仅能改变反应速率,还能改变烩变和嫡变
C.对于有气体参与的反应,反应物分子的每一次碰撞都为有效碰撞
D.加热才能发生的反应为吸热反应,不需要加热就能发生的反应为放热反应
8.常温下,将0.lmol/L的(NH )SO 溶液加水稀释至0.01mol/L的过程中,下列说法错误的是
4 2 4
A.c( )>c( ) B.c(H+)>c(OH-)
C.n( )保持不变 D.溶液中一直存在2c(NH ·H O)=c(H+)-c(OH-)
3 2
9.一定条件下,在5L恒容密闭容器中进行反应4NH (g)+5O(g) 4NO(g)+6H O(g) H<0,在0~2min内,
3 2 2
△
NO的物质的量增加了0.6mol。下列说法错误的是
A.在0~lmin内,用NO表示的平均速率v(NO)>0.06mol/(L·min)
B.在0~2min内,用NH 表示的平均速率v(NH )=0.00lmol/(L·s)
3 3
C.其他条件不变,降低温度,v(正)增大,v(逆)减小
D.其他条件不变,升高温度,v(正)、v(逆)均增大
10.室温下,向20ml,0.lmol/LHA(一元弱酸)溶液中逐滴加入0.lmol/L的NaOH溶液[忽略溶液体积和温度的
变化,Ka(HA)=1×10-a(a>0)]。下列有关说法错误的是
A.室温下,A-的水解常数Ka(HA)=l×10a-14
B.当滴入NaOH溶液的体积为5mL时,c(HA)+c(A-)=4c(Na+)
C.当混合溶液的pH=7时,溶液中各离子浓度之间的大小关系为c(A-)=c(Na+)>c(OH-)=c(H+)
D.当滴入NaOH溶液的体积为20mL时,c(OH-)+c(HA)= c(H+)
l1.反应C H(g)+3O(g)=2CO (g)+2HO(g) H=-1323.0kJ/mol,在2L密闭容器中充入lmol C H 和4molO ,
2 4 2 2 2 2 4 2
5min后反应达到平衡状态,此时CO 的物质的量增加了1.2mol。下列说法错误的是
2 △
A.0~5min内,v(H O)=0.12mol/(L·min) B.2.5min时,c(CO2)=0.6mol·L-1
2
C.该条件下,O 的平衡转化率为45% D.0~5min内,该反应共放出793.8kJ热量
2
12.下列实验操作正确且能达到预期实验目的的是选 实验操作 实验目的
项
A 用蒸馏水润湿的pH试纸测同浓度的HCl溶液、 测两溶液的pH并比较Ka(HCl)、
CHCOOH溶液的pH K(CHCOOH)的相对大小
a 3
B 向MgCl 、FeCl 混合溶液中加入过量的氨水,充分 除去MgCl 溶液中的杂质FeCl
2 3 2 3
搅拌,反应后过滤
C 直接蒸干Fe (SO ) 溶液 制备Fe (SO ) 固体
2 4 3 2 4 3
D 将硫化氢气体通入硫酸铜溶液中 比较HS、HSO 酸性的强弱
2 2 4
13.常温下,用0.1000mol/L的NaOH溶液分别滴定20.00mL,浓度均为0.1000mol/L的CHCOOH溶液和
3
HCN溶液,所得滴定曲线如图。下列说法错误的是
A.常温下,CHCOOH的电离常数K≈1×10-5
3 a
B.含有等物质的量的HCN和NaCN的混合溶液中:c(CN-)>c(Na+)>c(H+)>c(OH-)
C.②对应溶液中存在:2c(H+)+c(CH COOH)=2c(OH-)+c(CH COO-)
3 3
D.将④和⑤对应溶液混合,混合后的溶液中存在:c(CHCOO-)-c(CN-)=c(HCN)-
c(CHCOOH)
3
14.CO 氧化C H 制备C H 发生的主要反应为C H(g)+CO (g) C H(g)+CO(g)+HO(g) H>0,向容积为
2 2 6 2 4 2 6 2 2 4 2
△
2L的恒容密闭容器中投入2mol C H (g)和2molCO (g)不同温度下,测得5min时(反应均未达到平衡,其他
2 6 2
副反应均不消耗和生成乙烯)的相关数据见下表,下列说法正确的是
温度/℃ T T T
1 2 3
乙烷转化率/% 2 9 18
乙烯选择性/% 93 80 62
注:乙烯选择性= ×100%。
A.T℃,5min时,容器内C H 的物质的量为0.04mol
1 2 4
B.T℃,0~5min内,平均速率v(C H)=0.0144mol/(L·min)
2 2 4
C.反应达到平衡后,其他条件不变,仅升高温度,平衡向逆反应方向移动
D.该反应仅在低温条件下能正向自发进行
二、非选择题:本题共4小题,共58分。
15.(14分)根据所学知识回答下列问题:
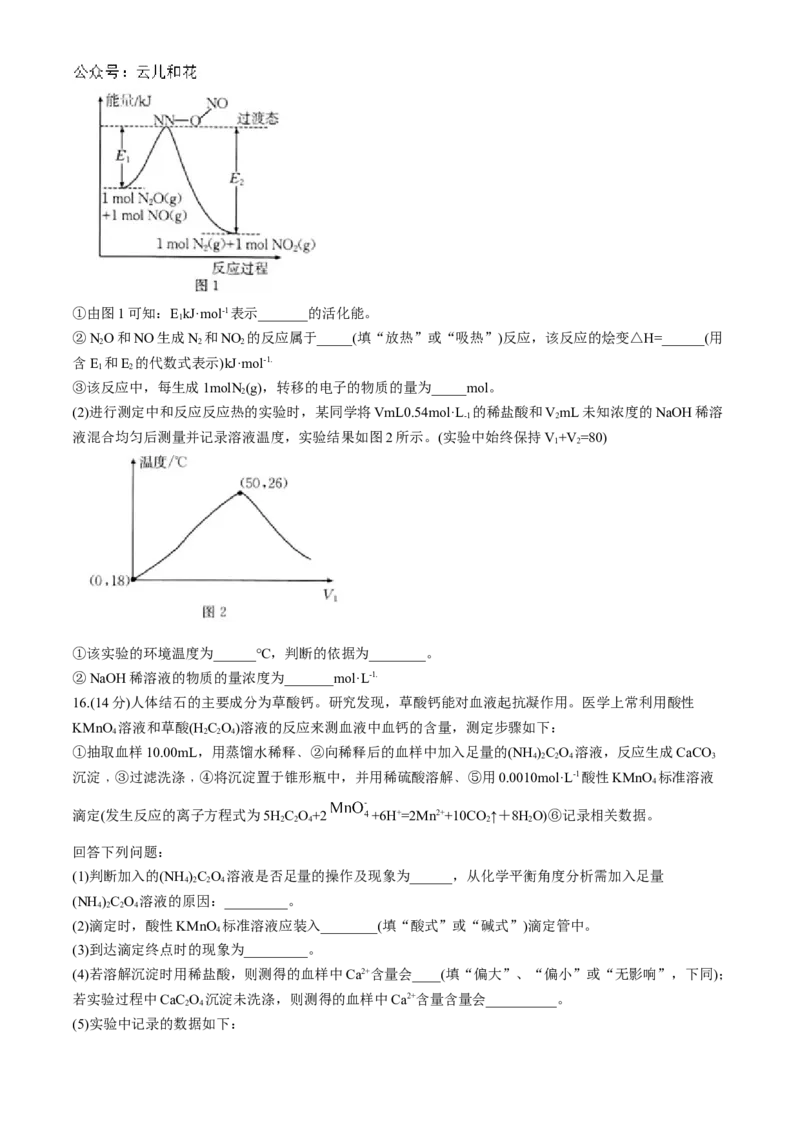
(1)由NO和NO反应生成N 和NO 的能量变化如图1所示。
2 2 2①由图1可知:EkJ·mol-1表示_______的活化能。
1
②NО和NO生成N 和NO 的反应属于_____(填“放热”或“吸热”)反应,该反应的烩变△H=______(用
2 2 2
含E 和E 的代数式表示)kJ·mol-1.
1 2
③该反应中,每生成1molN (g),转移的电子的物质的量为_____mol。
2
(2)进行测定中和反应反应热的实验时,某同学将VmL0.54mol·L 的稀盐酸和VmL未知浓度的NaOH稀溶
-1 2
液混合均匀后测量并记录溶液温度,实验结果如图2所示。(实验中始终保持V+V =80)
1 2
①该实验的环境温度为______℃,判断的依据为________。
②NaOH稀溶液的物质的量浓度为_______mol·L-1.
16.(14分)人体结石的主要成分为草酸钙。研究发现,草酸钙能对血液起抗凝作用。医学上常利用酸性
KMnO 溶液和草酸(H C O)溶液的反应来测血液中血钙的含量,测定步骤如下:
4 2 2 4
①抽取血样10.00mL,用蒸馏水稀释﹑②向稀释后的血样中加入足量的(NH )C O 溶液,反应生成CaCO
4 2 2 4 3
沉淀﹐③过滤洗涤﹐④将沉淀置于锥形瓶中,并用稀硫酸溶解﹑⑤用0.0010mol·L-1酸性KMnO 标准溶液
4
滴定(发生反应的离子方程式为5HC O+2 +6H+=2Mn2++10CO ↑+8HO)⑥记录相关数据。
2 2 4 2 2
回答下列问题:
(1)判断加入的(NH )C O 溶液是否足量的操作及现象为______,从化学平衡角度分析需加入足量
4 2 2 4
(NH )C O 溶液的原因:_________。
4 2 2 4
(2)滴定时,酸性KMnO 标准溶液应装入________(填“酸式”或“碱式”)滴定管中。
4
(3)到达滴定终点时的现象为_________。
(4)若溶解沉淀时用稀盐酸,则测得的血样中Ca2+含量会____(填“偏大”、“偏小”或“无影响”,下同);
若实验过程中CaC O 沉淀未洗涤,则测得的血样中Ca2+含量含量会__________。
2 4
(5)实验中记录的数据如下:滴定次数 血样的体积/mL 0.0010mol/L酸性KMnO 溶液
4
滴定前的刻度/mL 滴定后的刻度/mL 消耗溶液体积/mL
1 10.00 0.15 10.45 10.30
2 10.00 0.36 13.06 12.70
3 10.00 0.00 10.10 10.10
4 10.00 0.10 10.30 10.20
经计算,该血样中Ca2+含量约为______mol·L-1.
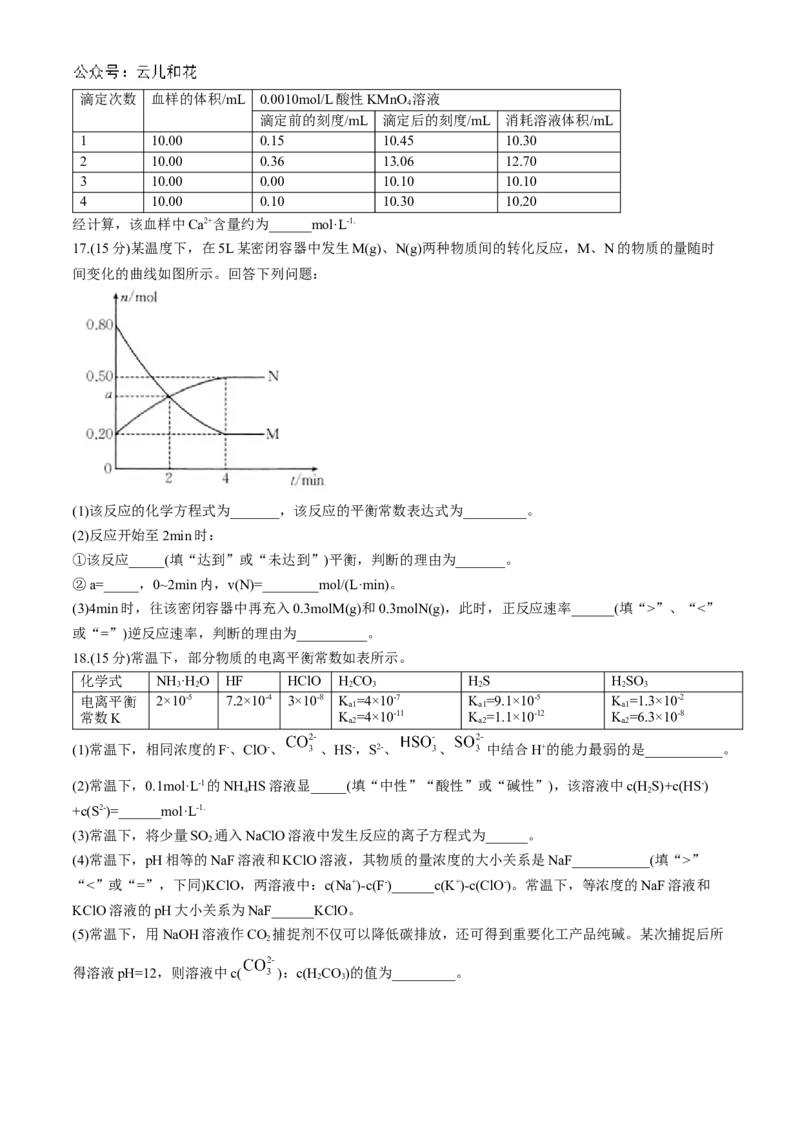
17.(15分)某温度下,在5L某密闭容器中发生M(g)、N(g)两种物质间的转化反应,M、N的物质的量随时
间变化的曲线如图所示。回答下列问题:
(1)该反应的化学方程式为_______,该反应的平衡常数表达式为_________。
(2)反应开始至2min时:
①该反应_____(填“达到”或“未达到”)平衡,判断的理由为_______。
②a=_____,0~2min内,v(N)=________mol/(L·min)。
(3)4min时,往该密闭容器中再充入0.3molM(g)和0.3molN(g),此时,正反应速率______(填“>”、“<”
或“=”)逆反应速率,判断的理由为__________。
18.(15分)常温下,部分物质的电离平衡常数如表所示。
化学式 NH ·H O HF HClO HCO HS HSO
3 2 2 3 2 2 3
电离平衡 2×10-5 7.2×10-4 3×10-8 K =4×10-7 K =9.1×10-5 K =1.3×10-2
a1 a1 a1
常数K K =4×10-11 K =1.1×10-12 K =6.3×10-8
a2 a2 a2
(1)常温下,相同浓度的F-、ClO-、 、HS-,S2-、 、 中结合H+的能力最弱的是___________。
(2)常温下,0.1mol·L-1的NH HS溶液显_____(填“中性”“酸性”或“碱性”),该溶液中c(HS)+c(HS-)
4 2
+c(S2-)=______mol·L-1.
(3)常温下,将少量SO 通入NaClO溶液中发生反应的离子方程式为______。
2
(4)常温下,pH相等的NaF溶液和KClO溶液,其物质的量浓度的大小关系是NaF___________(填“>”
“<”或“=”,下同)KClO,两溶液中:c(Na+)-c(F-)______c(K+)-c(ClO-)。常温下,等浓度的NaF溶液和
KClO溶液的pH大小关系为NaF______KClO。
(5)常温下,用NaOH溶液作CO 捕捉剂不仅可以降低碳排放,还可得到重要化工产品纯碱。某次捕捉后所
2
得溶液pH=12,则溶液中c( ):c(HCO)的值为_________。
2 3高二联考化学参考答案
l。D
【解析】侯氏制碱法的原理是利用溶解度大的物质制取溶解度相对小的物质,D项符合题意。
2.A
【解析】煤炭的燃烧为放热反应,反应物的总能量大于生成物的总能量,B项不符合题意;稀释浓硫酸的
过程未涉及化学反应,C项不符合题意;工业上合成氨的反应为放热反应,反应物的总能量大于生成物的
总能量,D项不符合题意。
3.D
【解析】铜为单质,A项不符合题意;CO为非电解质,B项不符合题意;醋酸为弱电解质,C项不符合题
意。
4.A
【解析】该方程式为离子方程式,B项错误;该方程式为水的电离方程式,C项错误;弱酸阴离子的水解
是分步进行的,D项错误。
5.C
【解析】依据燃烧热的定义,可知C项正确。
6.C
【解析】向CHCOOH溶液中滴入过量NaOH溶液的过程中,溶液中c(H+)先增大后减小,C项正确。
3
7.A
【解析】催化剂不能改变化学反应的嫦变和嫡变,B项错误;活化分子间才能发生有效碰撞,C项错误;
不需要加热的反应也可能为吸热反应,如氯化铵晶体与八水合氢氧化钡间的反应,D项错误。
8.D
【解析】依据电荷守恒和原子守恒可知c(NH ·H O)=c(H+)-c(OH-),D项错误。9.C
3 2
【解析】降低温度,正反应、逆反应的速率均减小,C项错误。
10.D
【解析】此时HA恰好完全反应,溶液可看作为NaA溶液,依据质子守恒,可得c(OH-)=c(H+)+c(HA),D
项错误。
11.B
【解析】5min时,二氧化碳的物质的量浓度为0.6mol·L-1,B项错误。
12C
【解析】测定溶液的pH时,不能使用湿润的pH试纸,A项不符合题意;镁离子会转化为氢氧化镁沉淀,
B项不符合题意;生成的是不溶于硫酸的硫化铜沉淀和硫酸,不符合强酸制弱酸,D项不符合题意。
l3.B
【解析】常温下,HCN的电离平衡常数约为1×10-11,由此可知,常温下,CN-的水解程度大于HCN的电离
程度﹐故含等物质的量的HCN和NaCN的混合溶液呈碱性,B项错误。
14.B
【解析】5min时容器内乙烯的物质的量为2×2%×93%=0.0372(mol),A项错误;正向反应为吸热反应,温
度升高,平衡向正反应方向移动,C项错误;△H>0、△S>0的反应在高温下能正向自发进行,D项错误。15.(1)①正反应(2分)
②放热(2分);E-E 或-(E -E )(2分)
1 2 2 1
③2(2分)
(2)①18(2分);由图可知,未加入稀盐酸时,起始温度为18℃(2分)
②0.90(2分)
【解析】(2)②由50×10-3L×0.54mol·L-1=30×1073L×c(NaOH),可得c(NaOH)=0.90mol·L-1.
16.(1)向过滤得到的滤液中继续滴加(NH )CO 溶液,若不产生沉淀,则(NH )C O 足量;若产生沉淀则
4 2 3 4 2 2 4
(NH )C O 量不足(2分);使Ca2+沉淀完全(2分)
4 2 2 4
(2)酸式(2分)
(3)滴入最后半滴酸性KMnO 溶液时,溶液由无色变为淡红色且半分钟内不褪色(2分)
4
(4)偏大(2分);偏大(2分)
(5)2.55×10-3(2分)
【解析】(5)依据5Ca2+~5H C O~2 ,可得,c(Ca2+)= =2.55×10-3(mol·L-1)。
2 2 4
17.(1)2M(g) N(g)或2M N(2分);K= (2分)
(2)①未达到(1分);M和N的物质的量还在发生变化(或其他合理答案,2分)
②0.40(2分);0.02(2分)
(3)>(2分);K=62.5>Q=16,化学平衡向正反应方向移动,则正反应速率大于逆反应速率(2分)
【解析】(3)K= =62.5,同理算得Q=16,K>Q,化学平衡向正反应方向移动,则正反应速
率大于逆反应速率。
18.(1) (1分)
(2)碱性(2分);0.1(2分)
(3)3ClO-+SO+H O= +Cl-+2HClO(2分)
2 2
(4)>(2分);=(2分);<(2分)
(5)1.6×107(2分)
【解析】2常温下,HS-的水解(使溶液呈碱性)程度大于电离程度,其水解平衡常数约为1×10-7, 的水
解(使溶液呈酸性)平衡常数为5×10-10,故NH HS溶液呈碱性。
4
(4)由已知数据可知,常温下,氟离子的水解程度小于次氯酸根离子的水解程度,故等pH的两溶液中,
NaF的物质的量浓度更大;NaF溶液中存在c(Na+)+c(H+)=c(OH-)+c(F-),KClO溶液中存在c(K+)
+c(H+)=c(OH-)+c(ClO-),故等pH的两溶液中c(Na+)- c(F-)=c(K+)-c(ClO-)。(5)依据碳酸的K ×K = ,代人数据可求得c( ):c( )=1.6×107.
a1 a2